Introducción
El carcinoma basocelular (CBC) es un tumor de invasión local, de crecimiento lento, que rara vez produce metástasis; se origina en las células epidérmicas de los folículos pilosos o las células basales de la epidermis, el factor más importante entre los involucrados en su génesis es la exposición a las radiaciones solares de forma crónica junto al envejecimiento poblacional. Pueden ser causa de morbilidad debido a la destrucción, deformidad y mutilaciones que ocasiona al ser más frecuente en la cara y cuello (hasta el 80 % del total de los CBC).1,2
Separando las regiones anatómicas por el riesgo de recidivar los tumores, se han definido tres áreas fundamentales donde el CBC se localiza: área de riesgo bajo (Low-Risk), llamada área L, constituida por el tronco y las extremidades, área de riesgo medio (Medium-Risk), llamada área M, formada por las regiones genianas y frontal de cara, cuello y cuero cabelludo y la zona de riesgo alto (High-Risk) llamada área H, que incluye área central de la cara, la nariz y surco nasogeniano, regiones perioculares, peribucal, pre y retroauriculares, pabellón auricular, regiones temporales, genitales, manos, pies, pezones y areola, estas zonas anatómicas poseen varios planos de fusión embriológica y de clivaje naturales con un mayor índice de recurrencia tumoral y de posibilidad de invasión a estructuras adyacentes y subyacentes.3,4,5
La resección quirúrgica es el tratamiento de elección del CBC; cuando se realiza respetando el margen oncológico a nivel de la zona H puede implicar la extirpación de amplias áreas de piel y, por razones cosméticas, existe la tendencia a que la cirugía en la cara elimine la menor cantidad de tejido posible y los bordes tumorales no sean bien eliminados completamente, lo que aumenta el riesgo de recidivas.6,7
El tratamiento conservador del CBC es una valiosa herramienta y, dentro de la inmunoterapia, el uso del HeberFERON, mezcla de interferones (IFNs) alpha-2b y gamma con propiedades antiproliferativa, antiangiogénica e inmunomoduladora. La acción antitumoral de los IFNs está dada por la inhibición del crecimiento de las células tumorales y por la inducción de la apoptosis de estas (muerte celular programada), al ser dos interferones, se produce un incremento y prolongación de la actividad farmacológica sin toxicidad adicional, con un efecto más rápido y prolongado en comparación con los interferones individuales, disminución en la frecuencia de inyecciones, excelentes resultados cosméticos y mayor calidad de vida del paciente.8,9,10
No se conoce cuáles son los resultados de la aplicación del HeberFERON en el CBC en zonas de alto riesgo en la práctica médica habitual y no existen publicaciones al respecto que describan los efectos beneficiosos o perjudiciales de la combinación de estos interferones, por lo que es necesario evidencia que aporte elementos que permita la aplicación oportuna del tratamiento para evitar mutilaciones, deformidades y recidivas en la atención primaria de salud.
Se realizó la investigación con el objetivo de evaluar los resultados de la aplicación del HeberFERON en pacientes con carcinoma basocelular en zona de alto riesgo.
Métodos
Se realizó un estudio observacional, descriptivo y prospectivo en pacientes con diagnóstico clínico, dermatoscópico e histopatológico de CBC en zona de alto riesgo, tratados con HeberFERON. Los sujetos procedían de la consulta del Policlínico Centro de Sancti Spíritus, desde el 12 de enero de 2016 hasta el 25 de marzo de 2022.
El grupo de estudio estuvo conformado por todos los pacientes con diagnóstico clínico, dermatoscópico e histológico de carcinoma basocelular en zona de alto riesgo que acudieron a la consulta de dermatología en el lugar y período antes mencionado (179 pacientes). La muestra quedó conformada por 61 pacientes con diagnóstico clínico, dermatoscópico e histológico de carcinoma basocelular en zona de alto riesgo que rechazaron la cirugía, con alguna enfermedad que impidió el proceder quirúrgico o uso de anestesia, que el tumor o el proceder para su eliminación fuese causa de mutilación, deformidad o afectación de algún órgano de la zona H y recibieron tratamiento con HeberFERON, con buen estado mental, con lesión recidivante o no, de cualquier tamaño, subtipo clínico, fototipo de piel, que no tuvieran hipersensibilidad a interferón o preparaciones utilizadas en el producto, embarazo, puerperio o mujeres lactando; y enfermedad crónica descompensada comprobada mediante el examen clínico (insuficiencia cardíaca respiratoria, o arterial crónica, isquemias cerebrales transitorias, convulsiones intratables médicamente, signos de afectación medular, trastornos serios de la coagulación, sicklemia o anemia drepanocítica, estado general muy comprometido y trastorno psiquiátrico severo u otra limitación que impida al paciente su evaluación).
La evaluación inicial incluyó la historia clínica, los datos demográficos y clínicos y el examen físico. Se realizó fotografía inicial, dermatoscopia y toma de muestra para biopsia de la lesión por ponche de 3 mm para estudio histopatológico. Se indicaron complementarios. La intervención terapéutica se realizó en régimen ambulatorio en la consulta del Policlínico Centro, la dosis de HeberFERON fue de 10,5 ( 106 UI/ml, perilesional e intradérmico, 3 veces por semana, por 3 semanas, hasta completar 9 dosis. La evaluación final se realizó a las 16 semanas de tratamiento con los mismos parámetros que la inicial para medir la respuesta a la terapéutica. Las principales variables estudiadas fueron la respuesta al tratamiento y la presencia o no de eventos adversos.
La respuesta clínica al tratamiento en la serie de casos se realizó teniendo en cuenta los siguientes criterios:
Respuesta completa (RC): cuando la desaparición de la lesión fue total.
Respuesta parcial (RP): la reducción de al menos el 30 % de la suma de los diámetros mayores donde se tomó como referencia la suma de los diámetros mayores de base.
Enfermedad estable (EE) reducción no suficiente para calificar como respuesta parcial o incremento insuficiente para calificar como enfermedad progresiva tomando como referencia la suma más pequeña de diámetros mayores desde el inicio del tratamiento.
La respuesta dermatoscópica se realizó utilizando el dermatoscopio DermLITE DL100 para evaluar las estructuras dermatoscópicas características del CBC y mediante la comparación de la imagen inicial y final de la lesión se clasificó en:
Ausencia de tumor: sin evidencia de células neoplásicas al finalizar el tratamiento.
Presencia de tumor: evidencia de células neoplásicas al finalizar el tratamiento.
La respuesta histopatológica: se tomó muestra para biopsia de 3 mm de la lesión al inicio y al final del tratamiento y se clasificó en:
Evento adverso: cualquier manifestación médica indeseable y no intencionada que ocurre en un paciente que se le ha administrado HeberFERON, independientemente que esté o no relacionado con este tratamiento. De este modo, puede ser cualquier signo (incluyendo datos de laboratorio anormales), síntomas o enfermedad asociada temporalmente con el uso de un producto farmacéutico, exista o no una relación con el fármaco.
Tipo de evento adverso (fiebre, escalofrío, cefalea, artralgia, mialgia, dolor y ardor en el sitio de inyección, edema y eritema perilesional, náuseas, vómitos, mal estar general, taquicardia, bradicardia)
Intensidad del evento:
Grado 1: Leve, evento adverso (EA) que el sujeto tolera bien, no interfiere con las actividades cotidianas. No requiere tratamiento y no interrumpe la administración.
Grado 2: Moderado, EA que interfiere en las actividades cotidianas. Requiere tratamiento y no necesariamente requiere la suspensión del medicamento causante.
Grado 3: Severo, EA que impide las actividades cotidianas. Requieren la suspensión del fármaco y la administración de un tratamiento específico.
Grado 4: Evento adverso grave con peligro para la vida o discapacidad.
Grado 5: Muerte relacionada con el evento adverso.
Gravedad del evento
Los datos se recogieron en la historia clínica y fueron registrados con los programas Microsoft Excel y SPSS. Los resultados se procesaron por cálculo porcentual y se presentaron en tablas e incluyó números absolutos y relativos. En el caso de la edad, se presentó su media y recorrido de valores (mínimo y máximo).
La investigación se realizó con la aprobación del Consejo Científico y Comité de Ética del Policlínico Centro. Se contó con el consentimiento informado de los participantes.
Resultados
Las características epidemiológicas de los pacientes incluidos en la serie de caso se muestran en la tabla 1. Del total de pacientes incluidos el 69,3 % fueron del sexo masculino, con ligero predominio del fototipo cutáneo tipo III (54,8 %) y el rango de edad entre los 42 y 86 años, el 51,6 % de los casos fueron del área rural y solo un 11,3 % presentaron más de tres lesiones de CBC.
Tabla 1 Características epidemiológicas de los pacientes con carcinoma basocelular en zona de alto riego tratados con HeberFERON N = 62 (100 %)
| Características epidemiológicas de los pacientes | No. (%) | |
|---|---|---|
| Sexo | Femenino | 19 (30,6) |
| Masculino | 43 (69,3) | |
| Procedencia | Urbana | 30 (48,4) |
| Rural | 32 (51,6) | |
| Edad | Media | Máx ( 86 |
| Mín ( 42 | ||
| Fototipo cutáneo | II | 26 (41,9) |
| III | 34 (54,8) | |
| IV | 2 (3,2) | |
| Pacientes con CBC múltiples | ( 3 lesiones | 55 (88,7) |
| ( 3 lesiones | 7 (11,3) | |
Fuente: Historia clínica.
En la tabla 2 se muestran las características de CBC en zona de alto riesgo tratado con HeberFERON. La localización más frecuente del tumor fue la nariz (45,1 %), seguido de la región periocular (27,4 %), el subtipo histológico que predominó fue el nodular o sólido (83,9 %), al igual que el subtipo clínico (77,4 %), solo un 16,1 % de los casos recibieron tratamiento previo, la cirugía fue el proceder más frecuente y la mayoría de las lesiones fueron menores de 2 cm (66,1 %).
Tabla 2 Características clínicas de las lesiones de carcinoma basocelular en zona de alto riego tratados con HeberFERON N = 62 (100 %)
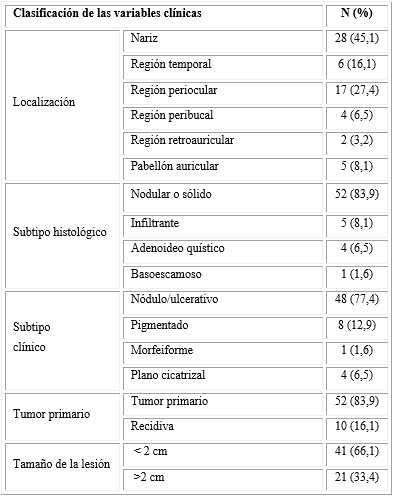
Fuente: Historia clínica.
La respuesta al tratamiento se evaluó a través de la clínica, la dermatoscopia e histopatología. Dos pacientes no culminaron el tratamiento por los eventos adversos y no fueron evaluados. El 70 % de los casos tuvo una respuesta clínica y dermatoscópica completa por no estar presente el tumor con una respuesta objetiva en 98,3 % y una enfermedad estable en el 100 % de los pacientes (figuras 1y2). Desde el punto de vista histológico, en el 81,4 % no estuvo presente el tumor. Solo 27 pacientes aceptaron realizar biopsia en la evaluación final a las 16 semanas y el 100 % con control de la enfermedad (tabla 3).
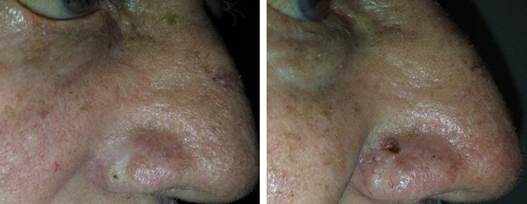
Fig. 1 Paciente con CBC nodular, en la figura izquierda se observa lesión tumoral en el ala nasal derecha.

Fig. 2 Paciente con CBC nódulo ulcerado, en la figura izquierda se observa lesión tumoral en parpado inferior derecho.
Tabla 3 Respuesta al tratamiento con HeberFERON en carcinoma basocelular en zona de alto riesgo a las 16 semanas

Fuente: Historia clínica.
Los eventos adversos más frecuentemente observados durante la administración del HeberFERON fueron el dolor y el ardor en el sitio de inyección (100 %), el edema y eritema perilesional (73,3 %) y la fiebre (55 %), todos sin peligro para la vida y cuya intensidad estuvo entre 1 y 2 al ser bien tolerado por el paciente, no interfirieron con las actividades cotidianas, se necesitó de tratamiento sintomático, pero sin interrumpir la administración del producto como se observa en la tabla 4.
Discusión
El CBC en zona de alto riesgo continúa siendo frecuente en la lista de cáncer de piel no melanoma a escala mundial. Es un tumor que aparece después de los 40 años de edad, que predomina en el sexo masculino, con fototipocutáneo bajo según Fitzpatrick y el principal factor de riesgo es la exposición crónica y prolongada a las radiaciones solares, por lo que es común en personas cuyo trabajo lo realizan al aire libre, muchas veces en áreas urbanas, relacionado con el estilo de vida de la ciudad, prácticas de deportes, exposiciones frecuentes al sol y otras actividades donde no se usan los medios de protección. Un 40 % de los pacientes que desarrollan el primer CBC desarrollarán al menos un tumor adicional dentro de 2 años del diagnóstico, independientemente de la adopción de medidas preventivas se considera como una enfermedad crónica. Estos datos son coincidentes con los resultados del estudio, con un predominio del sexo masculino, del área urbana, mayores de 40 años y la minoría con más de un CBC. En cuanto al fototipocutáneo fue más frecuente el tipo III, que son aquellos que se queman de forma moderada, pocas pecas, cabello rubio o castaño, ojos marrón a miel, enrojecimiento con el sol, suele ser la raza caucásica europea de piel blanca, con sensibilidad normal a la luz solar, lo cual no concuerda con algunos autores en este aspecto.11,12,13
El 80 % de los CBC aparecen en la cara y el cuello, aunque existen diferencias con respecto a su ubicación por sexo, en las mujeres se observa más en área frontal y región periorbitaria y en los hombres en el pabellón auricular, área geniana y cuello, en ambos sexos la zona más afectada es la nariz y los surcos nasogenianos con un 25,5 %, varios autores coinciden en que son frecuentes en los sitios más sobresalientes de la piel y en la zona periocular es el tumor maligno más frecuente con un 80-95 %.14
Investigaciones actuales refieren que el patrón histológico del CBC es importante para establecer los factores de riesgo de agresividad, la recurrencia y la mejor opción terapéutica. El CBC nodular o sólido es el más frecuente, representando el 70 % de todos los casos, es circunscrito, su pronóstico es bueno, porque no invade en profundidad y desde el punto de vista clínico el nodular, que puede ser ulcerado y nódulo ulcerativo es el más común, se presenta como un tumor de bordes bien definidos, ulcerado o no, con telangiectasias alrededor. El tamaño de la lesión es importante y se considera de mejor pronóstico los que tienen menor tamaño, por su extensión y el tiempo de evolución. Las recidivas son comunes en la cara; por razones cosméticas, la cirugía en la región facial tiende a eliminar la menor cantidad de tejido posible y los bordes de los tumores no son bien eliminados, lo que aumenta considerablemente el riesgo de recurrencia.11,12,13 El presente trabajo coincide en algunos puntos con lo comentando anteriormente, fue más común la localización de la nariz y periocular, el tamaño menor de 2 cm, el subtipo histológico y nodular. Esta investigación no concuerda con algunos investigadores que plantean que la mayoría de las lesiones fueron tratadas con criocirugía o efudit, ya que un porciento menor presentó un tumor recidivante y el proceder más usado fue la cirugía.12
El tratamiento del CBC en zona de alto riesgo depende de varios factores relacionados con el paciente y con las características del tumor. La resección quirúrgica continúa siendo el principal pilar del tratamiento; sin embargo, en algunas condiciones se convierte en una opción a evaluar, porque en estas zonas existen mayor densidad de nervios y de glándulas sebáceas y la dermis se encuentra más cercana al pericondrio, al periostio y al músculo, lo cual favorece que el tumor desarrolle extensiones laterales y profundas con un mayor índice de recurrencia tumoral y de posibilidad de invasión a estructuras adyacentes y subyacentes, unido a esto las complicaciones estéticas y funcionales, con riesgo de mutilación inminente y el tratar un tumor recurrente que se hace mas resistente a cualquier terapeutica.13-15 Algunos investigadores en sus resultados muestran que el HeberFERON es una opción no quirúrgica con el cual se han obtenido respuestas completas, al desaparecer el tumor completamente, o parciales, al reducir el tamaño de la lesión para luego intervenir quirurgicamente con excelentes resultados estéticos, evitando las mutilaciones, en la localización periocular tiene una respuesta más rápida y prolongada y buen resultado funcional, evita complicaciones quirúrgicas como la infección, sangrado, dehiscencias de sutura y queloides.16,17,18,19 Este trabajo presenta similitud con los mencionados anteriormente, porque la mayoría de los pacientes tratados con la mezcla de interferones tuvo una respuesta completa clínica y dermatoscópicamente, por no existir evidencia del tumor, y la respuesta parcial permitió la cirugía con los bordes establecidos, teniendo en cuenta que esta región anatómica es de riesgo de recidiva por la importancia de los planos de fusión embriológica con la progresión tumoral.
Los eventos adversos ocasionados por el uso del HeberFERON se caracterizan por ser grado I-II, dados por un síndrome pseudogripal (fiebre, cefalea, escalofríos, mialgia, astenia, artralgia, y malestar general), son frecuentes, transitorias, dosis-dependientes, reversibles al cesar el tratamiento y se reducen con antinflamatorios no esteroideo.16,17,18
Las reacciones adversas que presentaron los pacientes son las descritas por el uso de los interferones, de intensidad leve a moderada y responden bien al tratamiento sintomático, sin abandonar el esquema terapéutico. No se presentaron cambios en exámenes hematológicos ni bioquímicos. Estos resultados coinciden con otros trabajos donde todos los pacientes tratados presentaron reacciones secundarias a la administración del HeberFERON.16,17,18,19
El HeberFERON alcanza un perfil de seguridad que admite su uso en pacientes adultos mayores o con alteraciones de la cicatrización, por lo que es un medicamento seguro, que permite la conservación de la integridad de la piel, por lo que es una opción en pacientes con CBC en zona de alto riesgo.
En conclusión, el HeberFERON resultó de gran utilidad en los pacientes con carcinoma basocelular en zona de alto riesgo, porque se obtuvo una respuesta completa en la mayoría de los pacientes y los eventos adversos fueron los descritos en la literatura causados por el uso de los interferones, sin cambio en la actitud farmacológica.
Aporte científico
Se reporta por primera vez un estudio del carcinoma basocelular en zona de alto riesgo en la atención primaria de salud tratados con HeberFERON y las evidencias obtenidas sirven para la toma de decisiones en este cáncer de piel cada vez más común en la población cubana.