Introducción
Nailing es el anglicismo aceptado para describir el enclavijamiento intramedular con clavos rígidos, rectos, canalados, que penetran el canal medular y mantienen la reducción de la fractura a cielo cerrado. Los clavos ocupan el canal en la mayor extensión posible. Según su grosor, son bloqueados mediante tornillos que lo unen al hueso en ambos extremos para garantizar su estabilidad y evitar desplazamientos interfragmentarios.
El uso de clavos rígidos en la osteosíntesis intramedular se relaciona con acontecimientos sociales de carácter histórico y con el incremento de las innovaciones tecnológicas, organizadas en tres etapas o generaciones. La primera generación o iniciadora de la osteosíntesis intramedular con clavos rígidos coincide con el comienzo de la Segunda Guerra Mundial en 1939 y se desarrolla a la par del conflicto bélico.
La segunda generación continúa el trabajo de su antecesora, pero introduce nuevas técnicas. Aunque inicia a finales de los años ´40, su máximo esplendor lo alcanza a mediados de la década del ´50 y se conoce como la década brillante de la traumatología (1955-1965) porque extiende la consolidación por compresión dinámica-interfragmentaria, el fresado del canal y el cerrojo metal-hueso, como estabilizadores del sistema.
Por su parte, la tercera generación surge a finales del siglo pasado y se afianza a principios del siglo xxi gracias al incremento de las innovaciones tecnológicas en la medicina. Ha introducido modificaciones en la conformación anatómica del implante, la reducción funcional cerrada de la fractura y el acerrojado o bloqueo del implante en el canal; estos procedimientos se encuentran en fase de generalización y evaluación de sus resultados. Por consiguiente, el objetivo del presente trabajo fue caracterizar las diferentes generaciones que desarrollaron la osteosíntesis intramedular con clavos rígidos y con ello establecer un punto de referencia y consulta para los ortopédicos y traumatólogos.
Primera generación de osteosíntesis intramedular con clavos rígidos
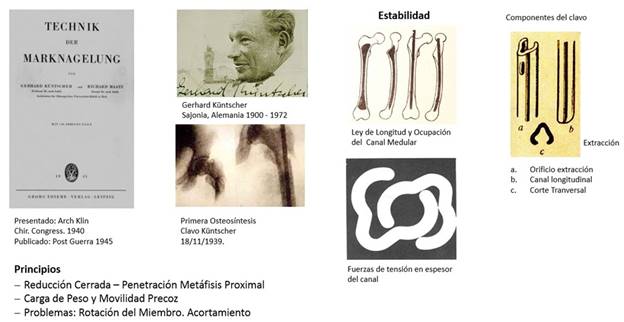
El periodo comprendido entre 1937-1940 se considera la primera generación de la osteosíntesis intramedular.1Gerhard Küntscher cambió la traumatología mundial cuando el 18 noviembre de 1939 implantó el primer clavo rígido intramedular a un paciente con fractura de la diáfisis del fémur 5 cm por debajo del trocánter menor.
Meses después, en mayo de 1940, presentó en la Academia Alemana de Cirugía en Berlín sus primeras experiencias con el clavo rígido en 13 fracturas de diáfisis de huesos largos (fémur 11, húmero 1 y cúbito 1) y mostró la descripción del procedimiento quirúrgico que posteriormente se indicaría en fracturas diafisarias transversales, oblicuas y espirales cortas.
En sus conferencias introductorias sobre el clavo rígido, Küntscher reconoció la idea de seguir en las diáfisis los conceptos de Smith Petersen en las fracturas intracapsulares del cuello del fémur, al aplicar como implante un grueso clavo rígido trilaminar de acero inoxidable en la osteosíntesis intramedular.
Para afianzar sus ideas, en 1939 presentó en la Academia de Cirugía un trabajo con 37 pacientes operados de fracturas de cadera con esa técnica. Küntscher junto con Richard Matz escribió “La técnica de enclavado intramedular” en 1942, libro que no sería publicado hasta 1945 por las condiciones de la guerra. En 1950 publicó un segundo libro para divulgar el procedimiento en varios idiomas y darle una visión internacional.
En 1962 publicó un tercer libro, “Uso clínico de los clavos intramedulares”, traducido al español en 1965. Ese mismo año presentó una sierra circular, que cortaba desde dentro del canal medular hacia afuera sin exponer el hueso, para realizar osteotomías correctoras de deformidades.
Su último libro (1970) abordó las diferencias científicas con el callo óseo por compresión que preconizaba la Arbaiten Orthopaedics (AO); abogó por los resultados del enclavijamiento con bloqueo del clavo y lo señaló como el procedimiento de elección para el tratamiento de las fracturas de huesos largos.2
Esta primera generación se caracterizó por la reducción cerrada de la fractura con la ayuda de sistemas de poleas o tracción podálica para mantener la longitud del miembro y el alineamiento del sitio de fractura bajo control radiográfico. En las fracturas femorales, se introducía el clavo a cierta distancia de la fractura mediante una pequeña incisión en el vértice del trocánter mayor para abordar la fosita del piriforme situada en su base; se perforaba el cortical y se ponía el clavo en el canal medular del fragmento proximal para que llegara hasta el foco de fractura a presión manual o golpe de martillo.
Se realizaba la osteosíntesis, se mantenían ambos extremos afrontados para atravesar el foco de la fractura y continuar la penetración en el fragmento distal hasta impactar la punta del clavo en la esponjosa de la metafisis distal.
El clavo se caracterizaba por ser de cuerpo cilíndrico, macizo en sus primeras experiencias, configuración que variaría Küntscher al trabajar junto a Ernet Pohl, un fabricante de herramientas. Pasó primero a ser acanalado en forma de letra V en toda su longitud y terminó por adoptar, en su estructura transversal, la forma de una hoja de trébol (clover leaf) de tres convexidades en su periferia.
Con esta estructura se incrementaba la estabilidad del montaje gracias a los diferentes diámetros, entre 9 y 15 mm, que ocupaban el canal medular y el adosamiento del clavo a las paredes internas. Concluida la osteosíntesis, se dejaban libres 2 o 3 cm del extremo proximal del clavo en la región glútea para su abordaje y extracción ulterior, por ello disponía de un orificio ovalado, labrado en la cara lateral de su extremo superior. En el seguimiento de los pacientes, ayudaba a la movilidad y a la marcha precoz.3
La técnica de Küntscher fue opacada en Occidente por la guerra y las falsas interpretaciones sobre los resultados de los pacientes tratados. Su valor fue reconocido tardíamente por la comunidad científica. Este procedimiento fue puesto en duda, e incluso criticado por la prensa, hasta que en 1942 fue reconocido como ingenioso y satisfactorio por la Revista Time Magazine en un artículo sobre los clavos intramedulares de fémur. Esto aportó valor científico a dicha innovación que muchos catalogaban como proceder de tortura.
No fue hasta después de terminada la guerra cuando se publicaría la primera osteosíntesis por clavos rígidos realizada en América con el trabajo de Mac Ausland en la Revista Surgical Ginecology and Obstetric (1947;84:85-89).4
El uso del proceder se extendió en 1951, cuando se introdujo el clavo de Street-Hansen con forma romboidal en su corte transversal para evitar la rotación del fragmento distal que ocurría con los clavos cilíndricos. Este clavo presentaba prominencias roscadas en sus extremos para adaptarse a la guía de penetración en osteosíntesis para técnicas ascendentes y descendentes.5
Küntscher incluye, en su técnica quirúrgica, el perforador manual de punta fina y estructura triangular para la perforación de la cortical fina de las metáfisis y la esponjosa, lo que propicia la penetración del clavo en el canal medular. Asimismo, incorpora las barrenas flexibles con estrías en su extremo para ensanchar la esponjosa del canal por fresado o rimado y darle mayor diámetro. También diseña un sistema de reducción portátil de la fractura para mantener la distracción y el alineamiento durante reducciones cerradas en mesas quirúrgicas lisas, carentes de sistemas de tracción.
A principios de los años '50 Lottes crea un clavo intramedular para fracturas de tibia que tenía forma triangular en su diámetro transversal, con angulaciones en su tercio superior e inferior, para adaptarse a la anatomía del canal medular de la tibia. Este clavo se introducía por la meseta tibial en un orificio hecho en la superficie interna de la tuberosidad anterior; bajo control radiográfico y con la rodilla en una posición de 90º, se guiaba el clavo en sentido longitudinal a medida que avanzaba. Fue muy usado en Cuba en la segunda mitad del pasado siglo para fracturas transversales u oblicuas de la diáfisis tibial.6,7
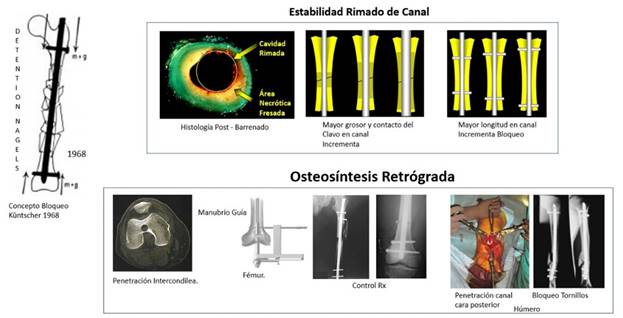
En 1968 Küntscher presentó en la Academia de Cirugía de Münich el Sistema Detentions Nagel. Basado en sus principios sobre la estabilidad de los implantes, el objetivo era fijar el clavo al hueso en sus dos extremos, mediante tornillos o pernos transversales u oblicuos, y con ello evitar la rotación interfragmentaria o la migración del clavo en sentido proximal por inestabilidad o aflojamiento del montaje. Este método luego fue conocido como “clavo con cerrojo”.
El bloqueo del clavo sería desarrollado por los estudios de Carr en sus análisis sobre la biomecánica de los implantes rígidos en el espesor del canal, procedimiento que se continuó modificando y en la actualidad presenta varias innovaciones.8) Küntscher afirmaba que la técnica de bloqueo del clavo brinda mayor estabilidad que la de compresión dinámica interfragmentaria, la cual había tomado prestigio con los trabajos del Grupo AO en 1954 y las llamadas Locking Compression Plates (placas de compresión y bloqueo).
Küntscher refería que la irrigación sanguínea del hueso para consolidar se lograba cuando el sistema vascular del periostio y de las masas musculares vecinas no eran separados de la cortical externa del hueso durante la introducción del clavo a cielo cerrado, es decir, sin decolar los músculos ni desperiostizar como ocurre en determinados procedimientos quirúrgicos para colocar los implantes del sistema de compresión por placas y tornillos. Posteriormente, José Tuerta ratificaría esta afirmación en sus estudios sobre la vascularización ósea de la osteogénesis.9
Aunque Küntscher fue jubilado en 1965, continuó su labor investigativa: reunió los criterios y referencias sobre los resultados de la primera generación de clavos rígidos y del procedimiento de bloqueo. Murió el 17 de diciembre de 1972.
La variante quirúrgica utilizada por esta primera generación fue la osteosíntesis abierta o expuesta de fracturas de la diáfisis del fémur. A partir de los años 50, este procedimiento fue muy utilizado en países de limitados recursos que no contaban con suficientes mesas ortopédicas, equipos fundamentales en la osteosíntesis cerrada, y solo disponían de aparatos de rayos X en forma de equipos portátiles que se adaptaban en el salón de operaciones.
Este método se describe de la siguiente manera: se expone el foco de la fractura, con el paciente en decúbito lateral en una mesa plana de cirugía; se hace una incisión longitudinal lateral externa para el abordaje por el espacio intermuscular externo del muslo, se separa el cuádriceps al plano anterior y los isquio-tibiales al posterior; se liberan los tejidos del foco de la fractura y se procura conservar el periostio.
Se barrena el canal del fragmento proximal en sentido retrógrado hasta exteriorizar su punta en la región glútea; se realiza una pequeña incisión de piel en la prominencia de salida para retirar el barreno e introducir el clavo en sentido distal hasta el foco de la fractura; después se barrena la esponjosa del canal medular con el mismo diámetro hasta el área de los cóndilos. Para concluir, se mantiene la reducción con uno o dos ayudantes y se coloca el clavo en el fragmento distal hasta la metafisis supracondilea.
Los clavos de Küntscher se conformaban de aleaciones de acero inoxidable 316L (hierro, níquel, cromo, molibdeno, carbono). También se usó el Vitalio, aleación de cromo, cobalto y molibdeno. Entre los biomateriales conocidos, el acero inoxidable demostró ser el de mayor biocompatibilidad y resistencia a la corrosión.10
La consolidación dependía de los principios que regían el proceder y eran fundamentales el tiempo transcurrido entre el momento de la fractura y la osteosíntesis, las características del implante, el acceso, la reducción y la penetración del clavo. Al respecto debemos señalar que en los primeros años de la técnica de Küntscher se debían esperar 5 y 14 días, según el estado físico del paciente, para realizar la osteosíntesis; o sea, no se corría el riesgo de practicar osteosíntesis de urgencia. En fracturas cerradas se debía esperar a que se organizara el hematoma fracturario para no perder sus elementos constituyentes en la creación del callo óseo.
Al preservar el hematoma fracturario, se crea un medio ambiente propicio a la invasión fibroso-celular y al depósito de minerales en el desarrollo del callo primario. Al no desperiostizar, se produce la formación de callo con el aporte de células osteoprogenitoras y tejido condral.
Küntscher aseveraba que la forma en hoja de trébol del clavo incrementaba la estabilidad y permitía el crecimiento de células del callo medular a su alrededor y en su interior por ser acanalado. Además este se beneficiaba con la dinámica de las fuerzas tensionales que aumentan gracias a la movilidad y la carga de peso precoz.
El callo óseo rellena el foco en forma de capas laminares con calcificación, pero con lentitud en el proceso de remodelación y la osificación ulterior, por lo que en ocasiones la imagen radiográfica provoca confusión y discrepancias en relación con el tiempo que debe mantenerse el clavo para garantizar la consolidación.
En caso de ser retirado erróneamente, antes de una consolidación ósea estable con procesos de remodelación visibles, se provocan refracturas espontáneas o por traumas mínimos. En la actualidad muchos autores recomiendan la permanencia del clavo hasta 18 meses como mínimo para que la fractura esté consolidada.11,12
Segunda generación de osteosíntesis intramedular con clavos rígidos
La segunda generación de osteosíntesis intramedular con clavos rígidos se inicia después de la Segunda Guerra Mundial y se corresponde con la generalización de los cambios introducidos por el Grupo de Trabajo Arbaiten Orthopaedics (AO) creado en Suiza en 1954. Este periodo se caracterizó por numerosas innovaciones tecnológicas en todas las esferas de la ciencia, en el diseño de los implantes, los biomateriales y los procedimientos quirúrgicos en el tratamiento de las fracturas. Aquí nació el sistema de osteosíntesis por compresión.
La compresión interfragmentaria se aplica en la osteosíntesis con exposición del foco de fractura y en la fijación de los fragmentos mediante el bloqueo por placas con orificios roscados y tornillos de cabeza cónica con estrías. Tiene como objetivo lograr la consolidación endomedular por reducción del espacio entre los extremos de los fragmentos mayores, lo que permite el paso directo, a través de la interlínea de fractura, de las masas del tejido óseo en formación (osteonas), pero con escasa formación de callo perióstico; esta consolidación se conoce como callo Per-Priman.
Paralelamente se continuaba desarrollando la osteosíntesis por clavos endomedulares rígidos de Küntscher: se mantenía la técnica cerrada, se preservaban las partes blandas, se empleaban clavos rígidos acanalados de mayor grosor, con distintas formas en su diámetro transversal, para conseguir la estabilidad de la fractura.13
La estabilidad de la osteosíntesis constituye el elemento fundamental para reducir la fractura hasta su consolidación. Puede ser absoluta o relativa. Los investigadores aseguran que esto depende de la adherencia del implante entre ambos fragmentos según el tipo de fractura. La estabilidad absoluta por compresión se refiere a la coaptación anatómica asociada a la fijación estable con osteosíntesis por placas y tornillos.14) Y la relativa, también llamada funcional, es provocada por la fijación intramedular alineada, sin rotación ni asimetría de los miembros, preferiblemente sin exposición del foco de fractura; permite micro-movimientos dinámicos a nivel del área lesionada de manera que la dirección de sus fuerzas sean positivas a la formación del callo óseo y garanticen la nutrición del hueso y de las partes blandas gracias a la conservación del periostio y de la irrigación sanguínea de los tejidos vecinos.15
Para garantizar la estabilidad del foco de fractura en la osteosíntesis funcional fueron introducidos dos procedimientos quirúrgicos que van a caracterizar a la segunda generación de osteosíntesis intramedular, ellos fueron el fresado del canal medular y el acerrojado o bloqueo clavo-hueso.16
1. Fresado o legrado del canal medular
Consiste en barrenar el interior del canal, con extracción parcial de la médula ósea, fragmentos de hueso esponjoso y de cortical interna, para ampliar su diámetro básicamente a nivel del foco fracturario, en las áreas más estrechas del istmo femoral, en el canal de torsión en el tercio medio del húmero y en la diáfisis de la tibia. Incrementar el diámetro permitía usar clavos más gruesos y cumplía con la Ley de trabajo del clavo en el interior del canal que precisaba que a mayor espacio y longitud del implante, mayor sería la estabilidad.17
Los autores que se oponen a este procedimiento argumentan que el hueso de la cara interna del canal medular y el tejido esponjoso quedan como una papilla de mayor o menor densidad y estructura. Esta resultante del fresado puede permanecer in-situ o drenarse parcialmente a las partes blandas e incluso provocar trombos que afectan los aparatos respiratorios y vasculares. Se ha demostrado histológicamente que esta técnica perjudica la estructura ósea medular y su irrigación vascular endógena porque la rotación del barreno disminuye el volumen de perfusión sanguínea necesaria para la consolidación de la fractura y esto provoca necrosis térmica.18
Desde los inicios de la Traumatología había referencias de que al fracturarse el hueso, la grasa del canal medular podía invadir las partes blandas, e incluso las masas de tejido de medula ósea podían llegar al hematoma; esto constituye una complicación letal porque participa en la etiología de afecciones como la embolia grasa y lesiones traumáticas severas de partes blandas como el derrame seroso de Morell Lavallee.19,20 Por ello en la osteosíntesis intramedular, el fresado del canal conlleva a la discusión de fresar contra no fresar.
Diversos estudios han demostrado que la presión de la circulación sanguínea endógena disminuye al retirarse el hueso esponjoso y la medula ósea, y también cuando se destruyen las conexiones vasculares capilares en el canal medular.
El fresado del canal para la osteosíntesis y el implante del clavo rígido de mayor diámetro con adosamiento a sus paredes demostró que la perfusión se reduce a 1,18 ml/100 gr/min (valor normal 6,11 ml/100 gr/min). En comparación con las fracturas tratadas por fijación externa, la perfusión se reduce a unos 2,3 ml/100 gr/min debido a la presencia de alambres o clavos transversales en el canal.21) Otro experimento demostró que el rimado o fresado incrementa la presión normal de la médula ósea en aproximadamente unos 30 mm de Hg y puede alcanzar hasta 140 mm de Hg, con el consiguiente daño a la base capilar.
Por estas razones, más la presencia de zonas necróticas provocadas por el déficit irrigatorio y su incidencia negativa en la formación del callo óseo, los detractores del fresado proponen eliminarlo del canal. En cambio, sus defensores destacan que ofrece mejor resistencia a los movimientos intempestivos y a las fuerzas de cizallamiento que actúan sobre el foco de la fractura gracias al uso de clavos de mayor grosor. También señalan que el fresado, junto con el aumento de la “longitud de la zona de trabajo del clavo”, crea un espacio a ambos lados del istmo hasta las metafisis que incrementa la estabilidad del clavo, sobre todo cuando se asocia con el procedimiento de cerrojo o bloqueo del implante.22
Al evaluar su aplicación, se deben valorar las siguientes desventajas: la disminución temporal de la circulación endóstica, la necrosis térmica del hueso esponjoso por fricción al usar barrenos eléctricos y el riesgo de embolismo graso o de médula ósea como complicación sistémica. A pesar de estos contratiempos, el fresado permite la inserción de clavos de mayor diámetro, más resistentes y estables; aumenta la superficie de contacto clavo-canal medular con distribución de esfuerzos en el istmo femoral y los extremos; favorece que los restos del tejido óseo medular puedan actuar como injertos autólogos de tejido esponjoso; beneficia la estabilidad temprana de la fractura y permite iniciar la movilidad y la carga de peso; por tanto, constituye un procedimiento de elección en fracturas inestables.
En la actualidad se recomienda limitar el fresado para incrementar el diámetro del canal y del clavo, autores de habla inglesa lo llaman ream to fit, es decir, fresar hasta cierta medida para fijar el clavo. Küntscher siempre se preocupó por la médula ósea y la penetración del clavo en el canal, por ello dejó el siguiente consejo quirúrgico:
“Al introducir el clavo hágalo despacio, que avance con la presión de su mano, y haga pausas después de varios golpes de martillo, lo que permitirá el drenaje de la médula ósea y evitará la obstrucción del canal y el encarcelamiento del avance del clavo, complicación intraoperatoria causante del fracaso de la osteosíntesis.”
Küntscher también recomendó irrigar y aspirar el área de fresado para arrastrar la mayor cantidad de tejido graso y de médula. Este concepto de ensanchar el espacio por el que avanzará el clavo y de eliminar el tejido medular y grasa del canal, permitió mantener el fresado en un diámetro que garantizara un enclavado intramedular de mayor grosor para mejorar la estabilidad de la osteosíntesis, según las necesidades del paciente.
2. Cerrojo o bloqueo de la unión clavo-hueso
Durante el Congreso de la Sociedad de Cirugía en Münich (1962), Küntscher presentó el primer intento de bloqueo o cerrojo del clavo en el canal medular del fémur, lo fijó mediante un tornillo transversal proximal y otro distal, que lo comprimían a una de sus corticales. Aseguró que sus resultados serían superiores a los de la compresión interfragmentaria por placas metálicas y tornillos.
Los ulteriores trabajos de Kleman en Frankfurt, junto a Grosse y Kempf en Estrasburgo, desarrollarían el sistema y su aplicación. Aseguraban que si estaba fijo uno de los extremos por bloqueo y el opuesto se encontraba libre, se lograba una dinamización que deslizaría las fuerzas de un fragmento a otro, como un mecanismo de pistón, y con ello se alcanzaba una controlada cantidad de stress en ambos extremos al producirse la carga de peso funcional.23
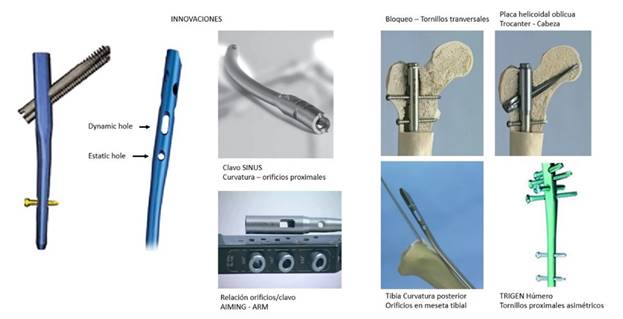
Para esto se crearon clavos con orificios labrados en los extremos diafisarios proximal y distal. El procedimiento quirúrgico de bloqueo consistía en la unión mediante tornillos implantados en las corticales que atravesaban estos orificios y creaban un paralelogramo de líneas de fuerzas que evitaban la rotación de los extremos y la migración del clavo. Inicialmente hubo dos tipos de orificios, los llamados estáticos (redondeados), perforados con el fin de bloquear la movilidad, y los dinámicos (ovalados), para estabilizar el foco y permitir realizar movimientos en sentido longitudinal.24
Con la incorporación del procedimiento de bloqueo o cerrojo, se incrementaron las indicaciones de este tipo de osteosíntesis, se trataron fracturas conminutas con fragmento libre interpuesto, fracturas de diáfisis con fragmento distal corto, las de trazos espiroideos y las oblicuas largas con fragmentos lineales. En relación con la estabilidad, el bloqueo evita el colapso por telescopage (penetración de un fragmento en otro) del foco fracturario y el acortamiento del hueso. La literatura anglosajona actual considera la incorporación de estos dos procedimientos como el “Gold Standard” de la osteosíntesis intramedular y lo llamaron “Locking Nailing”.25
Las principales técnicas quirúrgicas de bloqueo desarrolladas han sido las siguientes:
A. El cerrojo o bloqueo proximal se realiza a nivel de la metáfisis del sitio de penetración. Para ello fue diseñado el manipulador guía del clavo, dispositivo en forma de U invertida cuya rama horizontal sirve para sostener y dirigir la penetración del clavo y su bloqueo. Es condición indispensable que el implante haya penetrado totalmente, así no se pierde la orientación de la guía con el agujero del clavo y se evita que nuevos golpes del martillo aflojen la unión del tornillo de bloqueo o provoquen su ruptura.26
El mando guía y el tornillo de cerrojo deben mantenerse horizontales y paralelos con el plano del piso para que los orificios del clavo queden en el plano coronal. Cuando se introduce el extremo proximal del clavo, se mantiene con una presión manual hacia la cara interna en el fémur y hacia afuera cuando sea en la tibia para mantenerlo centrado en el canal hasta que atraviese el foco de la fractura y se impacte en la esponjosa distal.
Se puede aflojar la tracción del miembro para que se impacte el foco o, como hacen algunos cirujanos ortopédicos, golpear con firmeza en sentido longitudinal por la planta del talón. Hay que ser cuidadosos con las partes blandas periféricas, ya que de ser globulosas pueden elevar el mando guía y si este pierde su horizontalidad provoca molestias por la prominencia del extremo proximal del clavo.
Antes de iniciar la penetración del tornillo de bloqueo bajo control del fluoroscopio televisado o intensificador de imagen, se debe precisar que los orificios estáticos y dinámicos del clavo se vean en forma de círculo y de agujero oval respectivamente, señal de que están bien ubicados para continuar la fijación. El paso de la barrena de perforación y del tornillo a través de las partes blandas se hará dentro de una vaina metálica para evitar lesionarlas.
Algunos autores utilizan un alambre Kirschner para localizar el centro del orificio del clavo, o sea, actúa como guía en el barrenado y atornillado de implantes acanalados. Existen pernos y tornillos de cabezas cónicas con rosca en su superficie para ser fijadas a la cortical de penetración y garantizar la estabilidad transversal.27,28
B. Para realizar la técnica de cerrojo o bloqueo distal clavo-tornillo-hueso, se hace un corte de 2 cm en la cara lateral externa del miembro, una disección roma hasta llegar a la cortical; con control de imagen se introduce un alambre Kirschner para localizar el centro del agujero distal del clavo, y se crea una guía para facilitar la perforación y la fijación del tornillo. Debe medirse la longitud del tornillo que vaya a usarse para evitar la extrusión de su extremo cuando atraviesa la cortical interna del canal. Se barrena e introduce el tornillo, preferiblemente con destornillador manual.
Se indican 2 tornillos en pacientes con osteoporosis y fracturas conminutas, pero muchos autores indican su uso en todas las fracturas.29,30) Existen varios procedimientos para localizar los “puntos dianas” de los orificios distales del clavo para su bloqueo. En la actualidad es de mayor uso el alambre guía. El orificio estático se verá como un círculo perfecto, si se ve elíptico indica un mal alineamiento y debe corregirse antes de continuar el cerrojo.
Otra innovación de este grupo fue la osteosíntesis retrógrada, llamada así porque el clavo se introduce por el extremo distal del canal medular en las fracturas de fémur, húmero, tibia y radio y avanza en dirección proximal o retrógrada para realizar la osteosíntesis (fig. 2).
Se indica en el fémur para las fracturas supracondíleas, para las diafisarias proximales que disten 5 cm del trocánter menor, en las que concomitan con fracturas del cuello femoral o lesiones del acetábulo ipsilateral, en pacientes con hipertrofia de las masas glúteas bilaterales (esteatopigia) y en parapléjicos con fracturas femorales.
Se recomienda especialmente para las fracturas que provocan rodilla flotante (tercio inferior de fémur y superior de tibia) porque fija en un mismo acto operatorio y mediante una sola incisión de la rotuliana interna. La fractura del fémur se aborda por vía retrógrada, por el espacio intercondíleo, y en la tibia por vía anterógrada, por la meseta tibial.31
La osteosíntesis retrógrada del fémur se realiza de la siguiente manera: se coloca al paciente en supino sobre mesa plana y con soportes para mantener la rodilla en flexión. Se hace una incisión paralela medial al tendón rotuliano, se abre la cápsula articular y se separa hasta el espacio intercondíleo donde inicia el orificio de penetración por barrenado que sigue la línea eje en la esponjosa de la metafisis distal.
Al perforar con el barreno, se debe tener precaución con el ligamento cruzado y avanzar por el eje central del hueso en sentido proximal hasta llegar al canal medular. El clavo debe introducirse a presión o a golpes de martillo por el eje del fémur y debe centrarse guiado por imagen anteroposterior (AP) y lateral. Para concluir la síntesis, el clavo se coloca en el fragmento opuesto hasta la región intertrocantérea.
El extremo libre del clavo se introducirá en la metafisis unos 5 mm de la superficie articular para no chocar con la rótula a los movimientos de lexo-extensión. El bloqueo del clavo se realiza con la guía de mando; el tornillo atraviesa el cóndilo externo y el orificio estático del extremo proximal del clavo en sentido transversal para fijarse en la cortical interna del canal del lado opuesto. Para el bloqueo en el fragmento distal, se recomienda usar el sistema de control manual bajo imagen radiográfica.32,33
En el húmero, como el canal medular termina al inicio de la metafisis distal o paleta humeral por encima de la cavidad olecraneana, la vía de penetración del clavo varía en relación con lo descrito para el fémur. El paciente se coloca en decúbito prono, el tórax se levanta del plano de la mesa y se estabiliza el hombro con soportes para evitar complicaciones respiratorias durante la intervención.
Se realiza una incisión longitudinal que inicia a 2 o 3 cm de la fosa olecraneana en la cara posterior del brazo, se abre la fascia y el músculo tríceps hasta exponer el hueso (en este procedimiento siempre debe cuidarse el nervio radial). Se hace un orificio oval en la cortical posterior para acceder al canal medular y se introduce un barreno flexible para retirar el tejido esponjoso del canal en ambos fragmentos. Se ejecuta la reducción manual y la osteosíntesis mediante la introducción del clavo, manualmente o a golpe de martillo, junto con discretos movimientos rotatorios, para que avance por el eje de la diáfisis hasta la base del troquiter.
Con imagen en vista AP y lateral, se controla la reducción para evitar la diastasis y la rotación de la fractura. El bloqueo distal del clavo, en la metafisis proximal, se realiza con la guía de mando y bajo control de imagen, para corregir su ubicación y situar el agujero que fijará el tornillo de bloqueo.34
Otros procedimientos innovadores de la segunda generación fueron la penetración del clavo femoral por el vértice del trocánter mayor y no por la fosita del piramidal debido a que permitía el acceso vertical del clavo al canal medular y evitaba que se lesionara la base del cuello femoral en la unión cérvico diafisaria; si se fresaba el canal medular, en la tibia no debía usarse torniquete porque podían quedar atrapadas masas de medula ósea y tejido esponjoso lo cual favorecía la formación de trombos; y, por último, realizar el cerrojo una vez concluido el enclavijado.35
Estas innovaciones garantizaban la estabilidad del clavo y permitían usarlos con mayor grosor al aumentar el área de contacto en la cara interna del canal medular. Esto evitaba la rotación del fragmento distal de la fractura, ayudaba al alineamiento de la reducción y a la simetría de la osteosíntesis durante más tiempo; a la vez desarrollaba el callo óseo con tejido haversiano que permitía un retorno más rápido del paciente a las actividades de la vida diaria.
La evolución fisiológica de la relación osteoclastos-osteoblastos era señal de un hueso normal en su estructura y función. En lo relacionado con la visibilidad radiográfica del callo, debía mostrar mayor densidad tanto en la periferia de la cortical como en el área de contacto de ambos extremos fragmentarios, lo que permitía una evaluación más acertada del grado de consolidación en los estudios imagenológicos evolutivos.37,38
En esta segunda generación se mantuvieron las aleaciones de acero inoxidable AISI 316 LVM ASTM F138 para la confección de los implantes debido a que los electrolitos que circulan en el cuerpo humano no las desgastaban.36
Tercera generación de osteosíntesis intramedular con clavos rígidos
Se inició a finales del siglo XX y en la actualidad se encuentran en fase de generalización y evaluación sus procedimientos y resultados. Su desarrollo se vincula con la incorporación de las innovaciones tecnológicas de los últimos años. La tecnología enriqueció los métodos introducidos por la segunda generación y obligó a modificar el soporte teórico de sus procedimientos y la curva de aprendizaje.39
Los principios básicos de esta generación pueden detallarse de la siguiente manera:
- la certeza cuándo se elige la técnica a aplicar;
- en la fase preoperatoria, a partir de imágenes radiográficas, se mide (longitud, diámetro) el nuevo tipo de implante, ahora con forma curveada, para evitar complicaciones durante el acto quirúrgico.
- Se efectúa la reducción cerrada para no tener obstáculos en la visualización radiográfica. Se sigue el concepto de reducción funcional anatómica con el alineamiento y simetría de ambos miembros, sin rotaciones, ni angulaciones, durante el tiempo operatorio.
- Algunos autores recomiendan colocar un sistema de fijación externa lineal en la zona fracturada, como complemento transitorio de la estabilidad del foco durante la osteosíntesis.
Dentro de las innovaciones en el implante40) encontramos que el clavo rígido acanalado deja de ser recto para adaptarse a la anatomía del hueso y al lado del cuerpo que corresponda. Se divide en tres secciones con características diferentes según su función. El extremo proximal es recto y se ensancha de forma hexagonal o trapezoidal, en esa zona están los orificios transversales y el orificio dinámico oval para la fijación de los implantes de hojas helicoidales o los tornillos de refuerzo. En el extremo distal están situados los orificios estáticos para el cerrojo y algunos fabricantes incluyen un orificio dinámico. La junta tiene forma de diamante o se presenta hendida en dos mitades para su impacto y fijación en la esponjosa de la metafisis distal.
El manubrio o guía de penetración mantiene su forma de U invertida, pero modifica sus ramas verticales. La rama interna toma forma de cilindro rectilíneo y sirve para introducir el alambre guía, los barrenos flexibles para el fresado del canal y el impactador del clavo.
A la rama vertical externa se le añadieron orificios que la atraviesan en sentido transversal u oblicuo y coinciden con los orificios estáticos y dinámicos de la zona hexagonal del tercio proximal del clavo para realizar el cerrojo en la zona metafiso-epifisaria de penetración.41 Esta rama, además, se hizo removible. Se desmonta del manubrio al momento de ejecutar el bloqueo proximal y es sustituida por un dispositivo llamado Aiming Arm o brazo de puntería que tiene forma cuadrilátera longitudinal.
El extremo distal del brazo de puntería tiene un orifico oblicuo para un tornillo de bloqueo que recorre el dispositivo en sentido vertical ascendente y mantiene una angulación de 130º en relación al eje longitudinal del hueso. Esto fue diseñado para implantar clavos roscados especiales de hasta 7 mm de diámetro y realizar osteosíntesis de fracturas de cuello de fémur asociadas a fracturas de su diáfisis.
La reducción cerrada requiere de una mesa ortopédica modificada que permita el trabajo del arco en C durante el procedimiento quirúrgico. El paciente y los cirujanos deben estar en distintas posiciones según el hueso fracturado. Pongamos por caso, si es el fémur, el paciente debe estar en supinación o en posición lateral, la tracción debe ser simultánea y simétrica en ambos miembros para evitar la rotación de la cadera sobre el poste perineal; si fuese la tibia se debe mantener la rodilla en flexión de 90º para tener libertad de acción en la reducción manual y cuando es el húmero, el paciente debe mantenerse en posición de silla de playa con la mesa a la altura necesaria.42
En ausencia de una mesa ortopédica adecuada, así como en el tratamiento de fracturas conminutas o inestables, especialmente en politraumatizados con lesiones de cavidades, se recomienda mantener la reducción con un montaje de fijación externa lineal, de carácter transitorio, que incluya el hueso lesionado y deje libres las articulaciones vecinas.43
El montaje se realiza fijando clavos roscados tipo Shantz, con estrías de 6 o 7 mm de grosor, en ambas metafisis, proximal y distal, para una estabilización adecuada. En la proximal se fija con rosca manual, en la cara externa del trocánter mayor, con la cortical y la esponjosa, sin penetrar en el canal medular. En la distal se implanta, en la cara externa del cóndilo, con transfixión transversal bilateral en los cóndilos femorales con alambre liso de 3,5 mm a una distancia de 2,5 cm de la superficie articular.
Ambos sistemas de clavos se unen a la barra lineal del fijador por medio de adaptadores o clamps, según el tipo del fijador seleccionado (Orthofix, A.O. Hoffman-Vidal). Las barras o ejes de unión deben ser roscados. Se colocan en el plano lateral para mantener la tracción y el alineamiento sin rotación interfragmentaria, permitir la corrección de desplazamientos por el método de compresión o distracción longitudinal y dejar libre el área lesionada para el trabajo de los cirujanos y del sistema de imágenes.
Existen discrepancias sobre el origen y empleo de esta innovación. TM Scale, en el Journal of Trauma del año 2000, refirió que la fijación externa sería un puente para la estabilidad de las fracturas durante el acto operatorio debido a su corto tiempo de aplicación (25-30 min) y a los beneficios que brindaba a pacientes con lesiones de cavidades que requerían atención inmediata y estuvieran asociadas a trastornos metabólicos sistémicos tales como acidosis, coagulopatía e inestabilidad hemodinámica con compromiso letal.44
En la actualidad se le reconoce como el procedimiento de estabilidad primario de la fractura, aplicable en el tratamiento del llamado Damage Control Orthopedic Surgery, denominación que lo relaciona con el sistema de tratamiento descrito por Rotondo y Schwab: Damage Control Surgery o Cirugía del control de daños para el tratamiento primario de lesiones abdominales en pacientes politraumatizados con lesiones severas de cavidades y de los miembros.
Como tratamiento adjunto a la osteosíntesis intramedular, la fijación externa da la oportunidad al cirujano de analizar la conducta a seguir basado en el principio de aplicación primaria de tratamiento total (Early Total Care), o sea, realizar el tratamiento de cavidades y de fracturas de los miembros mientras se mantiene la estabilidad biomecánica entre 24 y 36 h, tiempo llamado óptimo, si el paciente se encuentra en condiciones biológicas compensadas sin trastornos inmunológicos asociados.
También se puede tomar la decisión de mantener inmovilizada la fractura hasta una segunda operación de osteosíntesis definitiva de acuerdo con el cuadro evolutivo del paciente. Incluso en los casos de evolución tórpida, con complicaciones que obliguen a postergar el tratamiento, se puede esperar el tiempo que sea necesario para una osteosíntesis secundaria definitiva tardía.45
Cualquier corrección de la osteosíntesis se hará antes de iniciar el bloqueo.46 Una vez acoplado el brazo de puntería, se precisa la posición en que han quedado los orificios del clavo mediante el intensificador de imagen. Los estáticos se visualizan como una circunferencia y los dinámicos de forma oval transversal. Se inserta un alambre Kirschner en uno de sus orificios para fijación estática y se comprueba bajo visión, que coincida con el orificio del clavo y se deja al alambre como guía.
Se hace una pequeña incisión longitudinal de piel para exponer los bordes del alambre, decolar los tejidos e introducir la vaina protectora de partes blandas. Guiado por el alambre Kirschner, se introduce el barreno para perforar ambas corticales de los orificios estáticos, medir la longitud del tornillo de bloqueo (acanalado con grosor de 3,2 a 4 mm) y fijarlo, de forma manual o eléctrica, en ambas corticales. De igual manera se procederá con los demás tornillos a implantar.47,48
El número de tornillos a usar varía según el área de utilización. En el fémur se implantarán dos tornillos transversales, uno proximal a nivel del trocánter menor, fijo en el calcar femoral (área de densidad ósea que garantiza la estabilidad) y otro distal al trocánter menor, que toma ambas corticales de la diáfisis. En la meseta tibial, se implanta un tornillo transversal que toma ambas corticales en el espesor de la esponjosa supratuberositaria anterior y otro por debajo de la inserción el tendón rotuliano en la cara anterior de la meseta. En el húmero los clavos disponen de orificios diseñados para implantar tornillos de bloqueo oblicuos en direcciones convergentes o divergentes y evitar su aflojamiento, debido a la estructura osteoporótica de esta zona.
El bloqueo proximal con lámina helicoidal o espiroidea es un implante tipo hélice de avión aplanada entre 35 y 120 mm. Las planchas son acanaladas con una inclinación de 100 a 120º. Su espesor es variable según el sitio de implantación y habitualmente se emplean en áreas osteoporóticas de las metafisis.
Su indicación como material de osteosíntesis y sus medidas deben evaluarse previamente para evitar complicaciones durante su implantación. Algunos autores señalan que puede emplearse en las fracturas intracapsulares del cuello femoral (ipsilaterales), lo que se realiza por medio de láminas helicoidales largas, penetradas por el orifico oblicuo situado en la base del brazo de puntería y a partir de los mismos principios de la técnica quirúrgica descrita para los tornillos.49
Indicado en osteosíntesis de cuello femoral en fracturas ipsilaterales, el dispositivo anexo de forma cuadrilátera constituye una las últimas innovaciones. Se trata de un pequeño bloque cuadrilátero, como una pequeña caja con perforaciones, que se anexa a la superficie del Aiming-Arm, al cual se fija por medio de un tornillo en el plano anteroposterior del brazo de puntería. Es capaz de girar sobre ese plano para orientarlo y seguir el eje del cuello del fémur.
El bloque en sus dos extremos presenta orificios con estrías labradas para colocar tornillos roscados tipo Lag Screw. Estos se introducen en la cortical libre del trocánter y avanzan bajo control radiográfico a lo largo del cuello hasta la esponjosa de la cabeza femoral.
De acuerdo con el trazo de la fractura, la fijación de los tornillos se realiza con el dispositivo colocado en la cara anterior o posterior del cuello del fémur. Tienen como función aumentar la estabilidad de los fragmentos y reforzar la osteosíntesis ya que actúan como elementos secundarios de compresión del foco de fractura.50
Los clavos de la tercera generación disponen de dos orificios estáticos (circulares) de dirección transversal situados en su tercio distal. Están separados unos 3 cm en su eje longitudinal y con ellos se realiza el cerrojo distal por tornillos o pernos transversales, acanalados, con estrías que lo fijan a ambas corticales. Se introducen manualmente bajo imagen radiográfica. Se utiliza un alambre Kirschner para la localizar el centro del agujero estático donde será fijado, guiar la perforación con el barreno y medir la longitud del tornillo que se colocará de la manera habitual. Hay tipos de clavos que sustituyen los orificios estáticos de bloqueo por un orificio dinámico oval para la formación del callo, mediante un mecanismo de pistón en sentido longitudinal.51
Concluida la osteosíntesis, se expone la incisión hecha sobre el vértice del trocánter mayor, se decolan las partes blandas hasta unir el impactador con el orificio proximal del clavo que se desconecta y en su lugar se coloca un tapón roscado que forma parte del montaje para ocluir el canal y evitar que salgan virutas de tejidos de la esponjosa y médula ósea a las partes blandas vecinas. El cierre del orificio de conexión del clavo con el tapón metálico impide que se forme una masa de tejido calcificado extraóseo que en ocasiones se inflama o infecta y necesita ser extraído.
En la actualidad la aleación más utilizada en la confección de clavos y tornillos de bloqueo es la de acero inoxidable AISI 136 LVM ASTM F138 con suficiente rigidez y buen nivel de aceptación por parte del organismo. También se han obtenido buenos resultados con la combinación de acero inoxidable y aleaciones de titanio en su fórmula Ti 6A 14V. Esta aleación, compuesta por alúmina (5,5 - 6,5 %) y vanadio (3,5 - 6,5 %), tiene la propiedad de pasivación de la superficie del metal para disminuir su rechazo por la corrosión e incrementar su resistencia frente a los esfuerzos y durabilidad del implante.
El futuro de los biomateriales se avizora como implantes que mejoren la regeneración natural de los tejidos y participen en sus funciones metabólicas, bioquímicas, biomecánicas y a la vez se integren a la estructura ósea. Además, debe generalizarse la combinación con nuevos polímeros de mayor resistencia al desgaste del metal.
A la osteosíntesis se han incorporado factores de crecimiento óseo y elementos de Medicina Regenerativa para mejorar la formación del callo, garantizar la estabilidad y la unión precoz de las fracturas conminutas, también favorecer el relleno de lesiones con pérdida de tejido y sustancia ósea.52
El proceso de formación del callo óseo ha sido el reto principal de las innovaciones. Se basa en la compatibilidad e integración de los materiales que estabilizan la fractura y permiten la regeneración natural de los tejidos en su estructura y metabolismo bioquímico y biomecánico. En la osteosíntesis con clavos anatómicos rígidos, han prevalecido el incremento del diámetro del canal para clavos de mayor grosor y estabilidad, junto al bloqueo proximal y distal, y la dinamización de las fuerzas por la movilidad y el apoyo precoz que ayudan a la formación de un callo óseo sólido con remodelación fisiológica capaz de adaptar la tensión y la compresión a su estructura.
Para reincoporar al paciente a sus actividades cotidianas, el futuro de la consolidación se basa en la supervivencia de los implantes (evitar el desgaste y prolongar la duración), junto con el estímulo de factores de crecimiento y proteínas morfogenéticas específicas, por consiguiente, la biociencia y la regeneración tisular para la reparación de las lesiones formarán parte fundamental de la Ortopedia y la Traumatología.53,54,55
Consideraciones finales
La revisión bibliográfica de la osteosíntesis intramedular identificó dos tipos de implantes intramedulares, en este caso los clavos rígidos. El análisis de los resultados de las variables seleccionadas para el estudio del sistema permitió individualizarlo y organizarlo por generaciones, de forma que el lector pueda ubicar en el tiempo su contribución a la optimización de los recursos y conocimientos para devolver al paciente a su vida activa.
El trabajo demuestra los avances en la técnica quirúrgica y la consolidación ósea. Los problemas de las fracturas van quedando prácticamente solucionados. El conocimiento es la mejor herramienta para impulsar las nuevas tecnologías y mejorar la calidad asistencial de la Traumatología y Ortopedia cubana.