Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Oftalmología
versión On-line ISSN 1561-3070
Rev Cubana Oftalmol v.13 n.1 Ciudad de la Habana ene.-jun. 2000
Hospital Oftalmológico Docente "Ramón Pando Ferrer"
Inductores de lágrimas: andrógenos y gammaglobulinas humanas
Dra. María Nila Santos Lagresa,1 Dra. Nereyda Martínez Suárez,2 Dra. Deysi Vilches Lescaille3 y Dra. Caridad Marisela Santos Lagresa4RESUMEN
Se comparan las respuestas terapéuticas en pacientes con diagnóstico de Síndrome de Sjögren que padecen de queratoconjuntivitis seca resistentes a los tratamientos tradicionales de lágrimas artificiales, lentes y otros, en dos grupos de pacientes de 18 y 32 casos con tratamientos de gammaglobulina humana: intacglobín (100 mg por kilo de peso cada 15 días por vía subcutánea interescapular por 3 meses) y andrógenos de depósito (100 mg cada 15 días por vía im durante 3 meses). Se evaluaron los niveles de inmunoglobulinas IgG, IgA, IgM e IgE, recuento de células sanguíneas factor reumatoideo, proteína C reactiva y estudio microbiológico. Ambas terapéuticas muestran una mejoría estadísticamente significativa p < 0,001 en los resultados obtenidos en la prueba de Shirmer I y en la negativización de las lesiones corneales valoradas en lámpara de hendidura después de tinción con fluorescencia. Se plantea las ventajas del uso de gammaglobulinas a causa de las contraindicaciones en el uso de andrógenos.Descriptores DeCS: SINDROME DE SJOGREN; QUERATOCONJUNTIVITIS/terapia.
El síndrome de Sjögren (SS) es una enfermedad crónica caracterizada por sequedad de boca, ojos y vagina y es considerada la enfermedad autoinmune más frecuente en todo el mundo. En esta entidad ocurre una invasión linfocítica de las glándulas exocrinas, produciendo una extensa inflamación y disfunción de las glándulas lagrimales y de otras glándulas asociadas a otras mucosas como la bucal y la vaginal. El SS afecta sobre todo a las mujeres (90 %) entre la cuarta y quinta décadas de la vida, aunque puede encontrarse en todas las edades y es una de las mayores causas del Síndrome de Ojo Seco en el mundo.1,2 La deficiencia acuosa de las lágrimas da lugar a enfermedad de la superficie ocular denominada queratoconjuntivitis seca (QCS), ésta resulta de una forma anormal de diferenciación terminal del epitelio de la superficie ocular y se asocia con una marcada reducción en la producción de mucina por estas células. Todos estos trastornos pueden dar lugar, aparte de los síntomas de sequedad de las mucosas y cutánea, a los daños oftalmológicos propios de la queratoconjuntivitis seca, cuyo tratamiento en formas leves consiste en el uso de lágrimas artificiales, lentes de contacto y en casos graves, pueden necesitar llegar al trasplante de córnea.3
Como el conocimiento de la patogenia y de la historia natural del ojo seco han aumentado, se buscan nuevos productos farmacéuticos que actúen tempranamente y en puntos cruciales en el proceso de esta enfermedad. Estamos entrando en una nueva era en el tratamiento del ojo seco con la introducción del primer agente que puede revertir los eventos básicos de las enfermedades del ojo seco; uno de los más prometedores y novedosos tratamientos para el ojo seco es la inmunoterapia, la cual ofrece la posibilidad de tratar la patogenia de base. En la actualidad se han realizado considerables investigaciones para entender los defectos locales y sistémicos del sistema inmune en el nivel molecular en estos pacientes, Sullivan ha demostrado que el tratamiento de ratas con andrógenos de depósito causa una supresión significativa de las lesiones inmunopatológicas a causa de que estos productos producen un aumento significativo de la producción de IgA secretora local así como un incremento en general de la síntesis de proteínas, lográndose con estos cambios una mejoría considerable en las lesiones del ojo seco.4
Por otra parte se ha comprobado que enfermedades que cursan con la formación de autoanticuerpos, la administración exógena de gammaglobulina humana normal (GGH) a dosis elevadas es capaz de suprimir la formación de autoanticuerpos patológicos como por ejemplo la inhibición que se produce en la formación de anticuerpos antiplaquetarios en la púrpura trombocitopénica idiopática después de la administración de altas dosis de GGH.5 Se señala que la administración de altas dosis de GGH es capaz de actuar como estimuladora de los monocitos que producen antagonistas del receptor de la interleucina I (arILI),6 otra posibilidad de acción de las GGH en estos casos es que actúen como terapia antiidiotípica, ya que estas proteínas usadas por vía endovenosa son capaces de modular la red idiotípica.7,8
Nosotros creemos que la combinación de las terapéuticas tradicionales con la inmunoterapia van a beneficiar, de forma dramática, los padecimientos crónicos que sufren los pacientes con ojo seco, por lo que teniendo en cuenta los aspectos que se relacionarán a continuación realizamos un ensayo terapéutico en el que comparamos el uso de andrógenos de depósito con el uso de gammaglobulinas humanas, en 2 grupos de pacientes con queratoconjuntivitis seca que presentaban lesiones desde hacía más de 3 meses y los cuales no habían mejorado con los tratamientos tradicionales por más de 3 meses.
Aspectos de importancia que motivaron la selección del presente problema de investigación:
- El cuadro grave ocular que padecen estos pacientes y que pueden llegar a la invalidez visual.
- Las dificultades actuales en el tratamiento tradicional de estos pacientes en el nivel mundial que incluye alergia y daño de las células corneales por los preservos de los colirios.
- Los colirios que se ofertan no aportan en ninguna medida los componentes naturales de las lágrimas que participan en la inmunidad de la conjuntiva, lo que posee una mayor importancia en países tropicales, si se tienen en cuenta el clima y las condiciones de temperatura y humedad relativa que favorecen el crecimiento de gérmenes patógenos, con mayor severidad en estos casos y desprovistos de inmunidad local.
- Los costos económicos ya que las terapéuticas tradicionales son de un alto costo.
- El incremento en la incidencia de la entidad en el nivel mundial motivado, fundamentalmente, por el envejecimiento de la población y el aumento de en las enfermedades de origen infeccioso.
Objetivos generales
- Comparar los resultados obtenidos en el tratamiento con andrógenos de depósitos con los resultados obtenidos con gammaglobulina humana (GGH) por vía subcutánea interescapular en pacientes con queratoconjuntivitis seca (QCS) resistentes por más de 3 meses al tratamiento tradicional.
Objetivos específicos
- Verificar el comportamiento del rango de edades, sexo, niveles de inmunoglobulinas, eritrosedimentación, proteína C reactiva (PCR), factor reumatoideo (FR), recuento globular y estudio de la presencia de gérmenes conjuntivales asociados al cuadro de queratoconjuntivitis seca que padecen estos pacientes.
- Comparar la producción de lágrimas en los pacientes antes y después de 3 meses de tratamiento con andrógenos de depósito y gammaglobulina humana utilizando como parámetro de la producción de lágrimas los resultados obtenidos en la prueba de Shirmer I (sin anestesia).
- Establecer los cambios en la respuesta a la terapia con gammaglobulina humana y andrógenos de depósito en las lesiones corneales de los pacientes con queratoconjuntivitis seca.
MÉTODOS
Criterios de inclusión: Se incluyeron a todos los pacientes enviados por los Servicios de Córnea y Oculoplastia de nuestro Hospital, que cumpliendo los criterios diagnósticos de queratoconjuntivitis seca y no obtuvieron mejoría del cuadro inflamatorio corneal con los tratamientos tradicionales por más de 3 meses y que con previo consentimiento, desearan ser incluidos en los ensayos clínicos. (Los procedimientos seguidos se encontraban de acuerdo con las normas éticas de experimentación en seres humanos). Criterios de exclusión: Se excluyeron del estudio a los pacientes con historia de hipersensibilidad a algunos de los productos usados en el ensayo, y a los que padecían de alguna otra enfermedad oftalmológica no relacionada con el cuadro de SS; se excluyeron también del ensayo a los pacientes que presentaron cuadro inflamatorio sistémico en fase de actividad.
Criterios de salida del estudio: A los pacientes que abandonaban el tratamiento o a los que presentaron algún cuadro oftalmológico o sistémico que obligara a adicionar otros tratamientos a estos.
Preparados utilizados: - Intacglobín (R*): Es un preparado listo para su uso, tolerable por vía endovenosa o subcutánea, con IgG biológicamente activa con una concentración 5 veces superior que el suero adulto. Este producto fue obtenido por fraccionamiento de plasma humano y presentado en forma diluida (bulbos de 2,5 g) [Intacglobín R* Planta de Hemoderivados Adalberto Pasant (IMEFA)]. El producto fue administrado por vía subcutánea interescapular.
- Androgenona de depósito (ámpula por 100 mg): Producida nacionalmente por los Laboratorios Farmacéutico Juan R Franco de la IMEFA.
Pauta 1: Tratamiento con gammaglobulina humana polivalente:
Un grupo de 18 pacientes que recibió tratamiento con gammaglobulina humana por vía subcutánea (sc) a la dosis de 100 mg por kilo de peso cada 15 días durante 3 meses.
Pauta 2: En un grupo de 32 pacientes se inició tratamiento con andrógenos de depósitos a la dosis de 100 mg cada 15 días por vía intramuscular (im) por 3 meses.
Prueba de Schirner I: Se coloca una tira de papel en el fondo de saco conjuntival, en el párpado inferior y a los 5 min se mide la secreción lagrimal (sin anestesia).
A todos los pacientes se les realizó estudio microbiológico conjuntival, conteo de células sanguíneas y velocidad de sedimentación globular.
En los 18 pacientes sometidos a tratamiento con GGH, se evaluaron los niveles de inmunoglobulinas IgG, IgA, IgM e IgE por el Centro de ImmunoEnsayo de Ciudad Habana (Turbidimetría, SUMA). Se determinó también la presencia de factor reumatoideo y proteína C reactiva siguiendo las técnicas de aglutinación9 y utilizando reactivos elaborados por la Empresa Finlay.
Después de realizada la extracción de sangre para los complementarios, los pacientes fueron divididos en los 2 grupos de estudio según las pautas descritas de forma aleatoria. Ambos grupos de estudio se compararon, de acuerdo con los resultados de la prueba de Schirmer, antes y después de los 3 meses de tratamiento; paralelamente fueron evaluados en LH para valorar la actividad de las lesiones corneales. A todos los casos se les realizaron los cultivos microbiológicos antes y después de los 3 meses de ser sometidos a los esquemas de tratamiento.
Todos los casos acudieron a la consulta de inmunología cada 15 días para tratamiento y siempre que lo precisaron. En cada visita se realizó un examen general y se recogió información en relación con la tolerancia al tratamiento (cefalea, mialgias, fiebre, hipotensión y episodios febriles > 37 °C), manifestaciones oculares en relación con el cuadro de QCS (sensación de cuerpo extraño, sequedad ocular, escozor e irritación).
Análisis estadísticos: En la mayoría de los casos, los valores representaban X-DS.
El estudio de diferencias entre variables cuantitativas se realizó mediante la prueba de la t de Student. Se consideró significativo un valor de p < 0,01.
RESULTADOS
Los pacientes estudiados se encontraban entre 25 y 67 años y todos los casos del grupo tratado con gammaglobulina humana fueron del sexo femenino. De los casos que se encontraban en el grupo tratado con andrógenos, 4 fueron del sexo masculino y el resto, del femenino.De los 50 casos estudiados, 4 salieron del estudio, pues presentaron intolerancia al medicamento; uno de los casos tratados con AD presentó efectos secundarios al tratamiento de andrógenos (hirsutismo) y el otro paciente presentó aumento del dolor de su cuadro inflamatorio articular. Dos de los casos tratados con GG aunque mejoraron su cuadro ocular presentaron recaída del cuadro inflamatorio articular (dolor).
De los estudios microbiológicos realizados se aislaron gérmenes patógenos (estafilococo coagulasa positivo y negativo con prueba de patogenicidad positiva y estreptococo B hemolítico); de 22 pacientes (47,82 %), 7 permanecieron positivos después del tratamiento con el colirio antibiótico utilizado según antibiograma.
En la tabla 1 se muestran los resultados obtenidos en la VSG la cual se encontró elevada en 10 (62,5 %) de los pacientes, la PCR se encontró presente en 8 (50 %) y el FR fue positivo en 12 (75 %) de los 16 casos. Se encontró además un incremento marcado en los niveles de inmunoglobulinas. El recuento globular, el número de leucocitos y el de trombocitos no arrojaron datos de interés.
| No. | | | | | | | |
| 1 | | | | | | | |
| 2 | | | | | | | |
| 3 | | | | | | | |
| 4 | | | | | | | |
| 5 | | | | | | | |
| 6 | | | | | | | |
| 7 | | | | | | | |
| 8 | | | | | | | |
| 9 | | | | | | | |
| 10 | | | | | | | |
| 11 | | | | | | | |
| 12 | | | | | | | |
| 13 | | | | | | | |
| 14 | | | | | | | |
| 15 | | | | | | | |
| 16 | | | | | | | |
| Control normal | | | | |
En las tablas 2 y 3 y en las figuras 1 y 2 se presentan los resultados de la prueba de Shirmer antes y después del tratamiento con andrógenos, donde se encontró un incremento en la producción de lágrimas lo que coincide con un incremento en los valores de esta prueba en los pacientes tratados con gammaglobulina humana, lo que resultó estadísticamente significativo p < 0,001 de acuerdo con la comparación de las medias aplicando la prueba t Student.
| | ||||
| | | | | |
| Control | | | | |
| SSP antes | ||||
| tratamiento SSP después | | | | |
| tratamiento | | | | |
| | ||||
| | | | | |
| Control | | | | |
| SSP antes tratamiento | | | | |
| SSP después tratamiento | | | | |
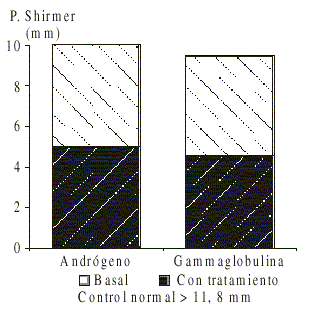
FIG. 1. Respuesta a tratamientos en el Síndrome de Sjögren.
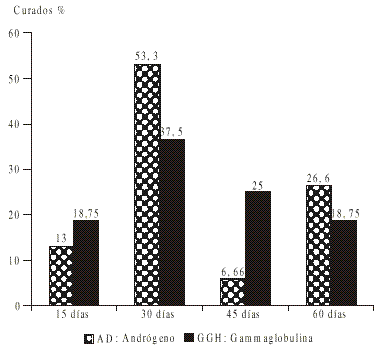
FIG. 2. Tiempo de curación de las lesiones corneales en el Síndrome de Sjögren.
La negativización de las lesiones corneales a los 3 meses de tratamiento ocurrió en 22 de los 30 pacientes sometidos a tratamiento con andrógenos, lo que representa el 73,3 % de los pacientes de ese grupo de estudio y en el grupo de 16 pacientes sometidos a tratamiento con gammaglobulina humana, 13 de los casos presentaron negativización del cuadro inflamatorio corneal a los 3 meses de tratamiento, lo que representa el 81,2 % del grupo (fig. 2 y tabla 4).
| Negativización de | | |
| lesiones corneales | | |
| 15 días | | |
| 30 días | | |
| 45 días | | |
| 60 días | | |
DISCUSIÓN
Los resultados obtenidos en nuestros casos según a los niveles de hipergammaglobulinemia, así como la presencia de PCR, FR y la elevación de la velocidad de sedimentación globular coinciden con lo reportado por otros autores.10 En cuanto a los aumentos en los niveles de inmunoglobulinas que se reportan en esta entidad se plantea que se debe a una activación de las células B; lo que no se conoces es si se debe a una activación de los clones reguladores de la respuesta inmune Ta/Ts, a una estimulación exagerada de las células B por virus autoantígenos o a una alteración intrínseca del propio linfocito B. Llama la atención el aumento de los niveles de IgA, lo que determina consecuencias patológicas serias, ya que esto se relaciona con una alteración grave de la respuesta inmune humoral, dando lugar a la formación de complejos dañinos del tipo de inmunocomplejos IgA-a 1 antitripsina que inducen a la cronicidad de los procesos inflamatorios que se observan en esta enfermedad.En los 16 pacientes tratados con GGH se encontró una respuesta favorable al tratamiento, tanto por el incremento en la producción de lágrimas valoradas a través de la prueba de Shirmer, como por la negativización de las lesiones activas del cuadro inflamatorio corneal. También hemos encontrado, igual a lo reportado por otros autores, un incremento de la producción de lágrimas con el tratamiento de andrógenos de depósito por vía sistémica coincidiendo con la mejoría en el cuadro corneal.11,12
Hay que señalar que se encontraron gérmenes patógenos en conjuntiva en 22 (47,82 %) de los 46 casos estudiados, lo cual posee una gran importancia en el manejo terapéutico de estos pacientes en nuestro medio. Lo anterior está en dependencia de una inmunidad local deprimida en el nivel de la conjuntiva, a causa de las alteraciones ya señaladas en las células inmunes y a una inadecuada producción de lágrimas no solamente en cantidad, sino también en calidad, ya que es insuficiente la producción de IgA en estos casos al igual que otros elementos necesarios para lograr una inmunidad local normal.
Con relación a otras posibles complicaciones, no se detectó la presencia de enfermedades autoinmunes ni enfermedades linfoproliferativas existentes previas al diagnóstico. En ningún caso se observaron elevaciones de las transaminasas imputables al tratamiento con gamma-globulinas ni se demostró transmisión de hepatitis B ó C ni de VIH.
Por todo lo anterior concluimos que la respuesta terapéutica con gammaglobulina humana puede considerarse favorable en comparación con los resultados reportados por otros autores con el uso de andrógenos de depósito.
Nuestros resultados representan una opción terapéutica nueva a las ya existentes en esta patología, lo que mejorará la calidad de vida de nuestros pacientes a causa de la preservación de la visión, evitándose en muchos casos el uso de técnicas más agresivas y costosas como es el trasplante de córnea.
Aunque no existen diferencias significativas entre los resultados obtenidos con ambas terapéuticas, consideramos que el uso de gammaglobulina humana presenta mayores ventajas, ya que puede ser usada en pacientes pediátricos, en afecciones que cursan con cambios hormonales y procesos neoplásicos donde el uso de esta hormona se encuentre contraindicado, además del embarazo.
Se puede añadir a los beneficios anteriores que brinda el uso de la gammaglobulina, el aporte de anticuerpos específicos presentes en estos tipos de preparaciones, lo que ayuda a combatir el cuadro infeccioso sobreañadido que acompaña a estos pacientes desprovistos de inmunidad local.
RECOMENDACIONES
Pienso que la definitiva solución en el uso de gammaglobulina y de andrógenos en un futuro, se debe focalizar en el uso local de estos preparados. Quiero hacer hincapié en que ambas posibilidades se encuentran en fase de ensayo clínico en nuestro Hospital y que incluso los preparados de IgA secretora han sido utilizados con magníficos resultados no sólo en patologías virales y alérgicas, sino también en pacientes con queratoconjuntivitis seca.AGRADECIMIENTOS
A la licenciada Silvia E. Forzate y a los compañeros de los Servicios de Córnea, Oculoplastia y al Centro de Immuno Ensayo y, en especial, al Dr. Raúl Pérez por sus valiosas sugerencias y cooperación.SUMMARY
Therapeutical responses are compared in patients diagnosed of Sjögren syndrome, presenting with keratoconjunctivitis sicca resistant to traditional treatments of artificial tears, lenses and others in two groups of patients (18 and 32 cases) treated with human gammaglobulin: intacglobin (100 mg/body weight every 15 days in a intercapsular subcutaneos way for 3 months), and depot androgens (100 mg every 15 days in an intramuscular way for three months). Level of IgG, IgA, IgM, and IgE immunoglobulins, count of blood cells-rheumatoid factor, C-reactive protein, and microbiological study. Both treatments show an significant statistically improve p < 0,001 in results obtained in Shirmer I test, and in negative corneal injuries, assessed using slit lamp after fluorescein staining. We propose advantageous use of gammaglobulins because of contraindications on utilization of androgens.Subject headings: SJOGREN´S SYNDROME; KERATOCONJUNCTIVITIS/ therapy.
REFERENCIAS BIBLIOGRÁFICAS
1. Morube del Castillo J. Mesa redonda sobre ojo seco. Congreso Anual Sociedad Oftalmológica de Madrid. Inform Oftalmol 1998;5(6):4-8.
2. _________. ¿Cuáles son los avances principales en el diagnóstico y maneo del ojo seco? Highlights of Ophthalmology. Serie 1993;21(5):66-72.
3. _________. El ojo seco. Nuevos avances en su naturaleza y manejo efectivo. Highlights of Ophthalmology. Serie 1996;24(5):76-85.
4. Sullivan DA, Edwards JA. Androgen stimulation of lacrimal gland function in mouse models of Sjögren's syndrome. J Steroid Biochem Mol Biol 1997;60(3-4):237-45.
5. Basta M, Kirshbom P, Frank MM, Fries LF. Mechanisms of therapeutic effect of high dose intravenous immunoglobulin. J Clin Invest 1989;84:1974-81.
6. Arend WP, Joslin FG, Massoni RJ. Effects of immune complexes on production by human monocyte of Interleukin Y or an Interleukin Y inhibitor. J Immunol 1985;134:3868-75.
7. Dietrich G, Kazatchkine MD. Normal immunoglobulin G (IgG) for therapeutic use (intravenous Ig) contain antiidiotypic specificities against an immunodominant, disease associated cross-reactive idiotype of human anti-thyroglobulin autoantibodies. J Clin Invest 1990;85:620-5.
8. Stevenson FK, George AJT, Glennie MJ. Anti-idiotypic therapy of leukemia and lymphomas. En: Carson DA, Chen PP, Kipps T, eds. Idiotypes in biology and medicine. Chem Immunol 1990;48:126-66.
9. Fischbach F. A manual of laboratory and diagnostic tests. 4 ed. Philadelphia: J.B. Hippincolt, 1992;138.
10. Munther A K, Josep F, Graham RV. Hughes. Enfermedades autoinmunes del tejido conectivo. Barcelona: Doyma, 1993;233-41.
11. Bruckner R. von. Uber einen erpolgreich mit Perandren behandelten Fall von Sjogrenschen Symptomen Komplex. Ophthalmologica 1945;110:37-42.
12. Radnot M, Nemeth B. Wirkung der Testosterone Preparate aut die. Tranendruse. Ophthalmologica 1955;129:376-80.
Recibido: 5 de julio de 1999. Aprobado: 25 de noviembre de 1999.
Dra. María Nila Santos Lagresa. Calle 150 No. 2134, entre 25 y 21 A, Cubanacán, Playa, Ciudad de La Habana, Cuba.
2 Especialista de I Grado en Oftalmología. Departamento de Oculoplastia.
3 Especialista de I Grado en Oftalmología. Departamento de Córnea.
4 Especialista de I Grado en Inmunología. Hospital Pediátrico del Cerro.














