Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Oftalmología
versión impresa ISSN 0864-2176
Rev Cubana Oftalmol vol.23 supl.2 Ciudad de la Habana 2010
INVESTIGACIONES
Autofluorescencia de fondo en pacientes con coriorretinopatía serosa central
Fundus autofluorescence in patients with central serous chorioretinopathy
Eva R. Santana AlasI; Danaides B. Arencibia GonzálezI; Rafael Gonzales DíazII; Ailén Garcés Fernández; Suzel Lapido PolancoI; Yolanda Velázquez VillaresII
IEspecialista de I Grado en Oftalmología. Especialista de I Grado en Medicina General Integral. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". La Habana, Cuba.
IIEspecialista de II Grado en Oftalmología. Especialista de I Grado en Medicina General Integral. Instructor. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". La Habana, Cuba.
RESUMEN
OBJETIVO: Describir las características de la autofluorescencia de fondo en pacientes con coriorretinopatía serosa central y determinar su relación con las alteraciones funcionales y anatómicas de la región macular.
MÉTODOS: Estudio descriptivo, transversal en 21 ojos (21 pacientes) con coriorretinopatia serosa central en diferentes estadios evolutivos. Se identificó el patrón de autofluorescencia en el área de desprendimiento neurosensorial, se usó el angiógrafo retinal de Heidelberg a 30°. Con la tomografía de coherencia óptica, se midió el grosor macular central y se describieron los cambios anatómicos. A 12 de los pacientes se les realizó angiografía fluoresceínica en el Angiógrafo Retinal de Heidelberg.
RESULTADOS: Se encontró hipoautofluorescencia en el 51,90 %, hiperautofluorescencia en el 42,86 %; coexisten ambos en el 4,76 %. No hubo diferencia significativa entre la hiperautofluorescencia y la hipoautofluorescencia en cuanto a agudeza visual mejor corregida (media de 0,43 y 0,49, respectivamente; p= 0,184), ni respecto al grosor macular central (media de 371,3 µm y 388,1 µm, respectivamente; p= 0,867), pero sí entre el tiempo de evolución y el patrón de autofluorescencia, (p= 0, 023). En ojos con hiperautofluorescencia se observó por tomografía de coherencia óptica irregularidad en capas externas y en epitelio pigmentario de la retina. El 83,3 % de los casos que requirieron angiografía fluoresceínica presentaron hiperfluorescencia que coincidió con la hipoautofluorescencia del sitio de fuga.
CONCLUSIONES: En la coriorretinopatía serosa central se encuentran diferentes patrones de autofluorescencia, los que reflejan cambios en la retina externa y epitelio pigmentario de la retina. La autofluorescencia puede ayudar a identificar el sitio de difusión focal en el epitelio pigmentario de la retina.
Palabras clave: Corioretinopatía serosa central, epitelio pigmentario de la retina, autofluorescencia de fondo, tomografía de coherencia óptica, angiografía fluoresceínica.
ABSTRACT
OBJECTIVES: To describe the peculiarities of the Fundus Autofluorecense in patiens with Central Serous Chorioretinopathy (CSC), and determine the relationship with functional and anatomic disturbances of the macular region.
METHODS: Cross-sectional descriptive study performed in 21 eyes (21 patients), suffering from central serous chorioretinopathy in different statings. The pattern of autofluorecense in the neurosensoral detachment was detected with the Heidelberg´s Retinal Angiograph (HRA2) on 30° position. The optical coherence tomography (3D-OCT-Topcon) (Nidek) measured the central macular thickness and exposed the anatomic changes. Flourescein angiografy with HRA2 was performed on 12 patients.
RESULTS: Hypoautofluorescense was detected in 51,90 % and hyperautofluorescense in 42,86 % of cases respectively; both disorders were present in 4,76 % of the patients. There was no significant difference between hyperautofluorecense and hypoautofluorescense as to the best corrected visual acuity (mean of 0,43 and 0,49, respectively; p= 0.184), and the central macular thickness (mean of 371.3 µm and 388.1 µm, respectively; p= 0.867). However, the difference was significant between time of evolution and the pattern of autoflorescence (p= 0.023). In those eyes affected by hyperautofluorescense, the optical coherence tomography allowed observing irregularities on the external layers and on the retinal pigmentary epithelium. The 83,3 % of cases who needed AGF presented with hyperautofluorescense that matched with hypoautofluorescence in the leakage site.
CONCLUSIONS: In the central serous chorioretinopathy, different autofluorescense patterns may be found that reflect changes in the external retina and the retinal pigmentary epithelium. The autofluorescense may help to identify the focal diffusion site.
Key words: Central serous corioretinopathy, retinal pigmentary epitelium, fundus autofluorescense, optical coherence tomography, flourescein angiography.
INTRODUCCIÓN
La coriorretinopatía serosa central (CSC) suele ser una enfermedad esporádica y autolimitada que afecta preferentemente a hombres jóvenes y de mediana edad.1 Se presenta con un buen pronóstico visual, no obstante, algunos pacientes con episodios prolongados o recurrentes pueden desarrollar algún grado de reducción permanente en su agudeza visual.2
Se caracteriza clínicamente por un desprendimiento seroso de la retina neurosensorial en el polo posterior y/o desprendimiento del epitelio pigmentario (DEP), que sucede con mayor frecuencia en pacientes varones entre 20 y 45 años de edad con personalidad tipo A.3,4
A pesar de una investigación continuada y del desarrollo de nuevos métodos de examen, la etiología y patogénesis permanece desconocida y oscura. Constituye un acertijo sin resolver si esta es una condición primaria de las coroides o del epitelio pigmentario de la retina (EPR). Se plantea la existencia de una alteración en el balance neto del flujo de líquido en el espacio subretiniano favorecido por una disfunción del EPR. Varios autores piensan que la anormalidad primaria es causada por una alteración en la permeabilidad de la vasculatura coroidea.3
Existe una hipótesis de que la coriorretinopatía serosa central se produce por una hiperpermeabilidad coroidea donde la hiperpresión comprime al epitelio pigmentario suprayacente, lo que provocan desprendimientos focales y fugas (confirmadas con AGF) en la unión del epitelio desprendido con el aplicado.5 Numerosos estudios clínicos han descrito sus características demográficas, factores de riesgo, manifestaciones clínicas y curso.6,7
El examen fundoscópico revela una elevación superficial y bien definida de la retina neurosensorial en el polo posterior. Normalmente el líquido seroso subretiniano es claro, y ocasiona una pérdida del reflejo foveal. Un reflejo brillante delimita el borde de la elevación serosa retiniana. En algunos casos, cuando la CSC lleva varias semanas de evolución, podemos observar finos precipitados amarillentos subretinianos en la superficie posterior de la retina neurosensorial desprendida. Es frecuente detectar un pequeño DEP, grisáceo o amarillento y bien circunscrito dentro de su área. Algunas veces, el DEP puede estar fuera del área del desprendimiento seroso retiniano, y también pueden ser múltiples.2
La imagen de autofluorescencia (AFF) es un método no invasivo para registrar los cambios fisiológicos del fondo de ojo inducidos por la enfermedad.3 Es una técnica que documenta la presencia de lipofucsina en el EPR,8 pigmento derivado de la degradación de los segmentos externos de los fotorreceptores,9 que exhibe una característica autofluorescente cuando es excitada con luz azul o ultravioleta (UV).4 La evaluación del nivel de autofluorescencia de fondo representa un balance entre la acumulación y la aclaración de lipofuscina, así como la actividad metabólica de los fotorreceptores y del EPR,10 así permite una evaluación de su disfunción de forma rápida y no invasiva.3
La angiografía fluoresceínica ha documentado la intensidad y distribución espacial de la autofluorescencia en estadios agudos y crónicos de la enfermedad,6 así como su relación con el sitio de filtración focal del epitelio pigmentario de la retina.9
Por otra parte el OCT permite la confirmación del desprendimiento neurosensorial, así como su detección en aquellos casos no aparentes con examen biomicroscópico, el que muestra otros signos de CSC como desprendimientos del epitelio pigmentario, sus irregularidades, exudación crónica y cambios cistoides dentro de la retina.6
El propósito de este estudio fue describir las características de la autofluorescencia de fondo en pacientes con CSC y determinar su relación con las alteraciones funcionales y anatómicas en la región macular.
MÉTODOS
Se realizó un estudio descriptivo, transversal en 21 ojos (21 pacientes, unilaterales) con CSC en diferentes estadios evolutivos de la enfermedad.
Se consideró que el paciente presentaba CSC si mostraba hallazgos oftalmoscópicos de fluido subretinal en polo posterior y/o DEP. No se incluyeron aquellos pacientes con historia o signos de inflamación intraocular, neovascularización coroidea u otras condiciones relativas a exudación subretinal, así como pacientes con alguna patología en el ojo contralateral.
Los pacientes fueron atendidos en el Servicio de Vítreo-Retina del Instituto Cubano de Oftalmología "Ramón Pando Ferrer" durante el período comprendido de mayo del 2007 hasta enero del 2009. En la anamnesis se recogió el tiempo de evolución de los síntomas, y en el examen oftalmológico se incluyó agudeza visual mejor corregida (AVMC), y biomicroscopia del polo posterior en lámpara de hendidura con lente aéreo de 90 dioptrías y oftalmoscopia indirecta.
Fueron realizadas imágenes de autofluorescencia de fondo para lo cual se usó el láser con focal SLO Heidelberg Retina Angiograph (HRA2) 300, con una excitación de longitud de onda de 488 nm y un filtro de barrera de 521 nm, también se identificó el patrón de autofluorescencia en el área del desprendimiento seroso con el empleo del Heidelberg Eye Explorer; se tomó como patrón de referencia el ojo contralateral. Se consideró patrón de hipoautofluorescencia en aquellos casos que presentaron disminución de la autofluorescencia respecto al ojo contralateral sano e hiperautofluorescencia en aquellos que existió un incremento en la autofluorescencia. Se realizó tomografía de coherencia óptica (3D-OCT-Topcon) (Nidek), protocolo radial y se describieron las alteraciones cualitativas y cuantitativas; asimismo se determinó grosor macular central con medición manual.
A los pacientes que presentaron criterios para su indicación (12 pacientes), se les realizó angiografía fluoresceínica (AGF) en el Heidelberg Retina Angiograph.
Se analizaron las variables: agudeza visual mejor corregida (AVMC), el grosor macular central y el tiempo de evolución en cada patrón de autofluorescencia. Se utilizó la prueba de Wilcoxon Mann Whitney, para lo cual se consideró un nivel de significación de 0,05.
RESULTADOS
Se estudiaron 21 ojos (21 pacientes), con edad media de 40 años y DE ± 8,8 (rango de 19 a 58 años). Prevaleció el sexo masculino con un 56,8 %. El 80,9 % de los casos presentaron la forma aguda de la enfermedad y el 19,1 % la forma crónica.
El examen oftalmológico mostró las manifestaciones típicas de pacientes con CSC dado por desprendimiento neurosensorial en todos los casos (100 %). En el 34,4 % de los casos se asoció desprendimiento seroso del epitelio pigmentario y desprendimiento neurosensorial. También se hallaron zonas o parches de atrofia del EPR y alteraciones pigmentarias.
La agudeza visual (AVMC) en el grupo estudio se presentó en el rango de 20/400 (0,05) a 20/25 (0,8) con una media de 20/40 (0,5).
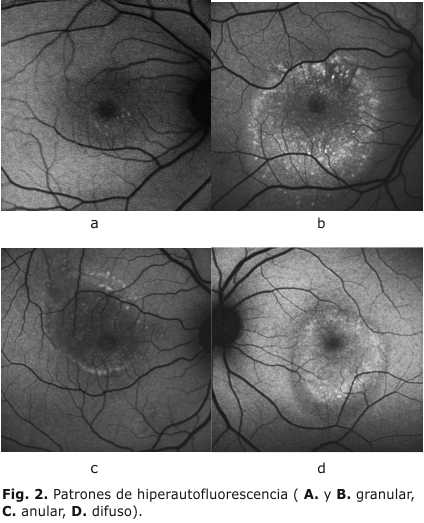
Se encontró hipoautofluorescencia en el 51,90 % de los casos mostrando variedad en su forma de presentación, siendo en algunos casos más difusa (fig. 1a) y en otros mejor delimitada y más circunscrita (fig. 1b) al centro del área macular. En cuanto a la hiperautofluorescencia esta se presentó en el 42,86 % de los casos. La misma se evidenció en una variedad de patrones morfológicos que mostraron inicialmente en casos con menor tiempo de evolución una disposición granular (fig. 2a y 2b). La presencia de un halo hiperautofluorescente a su alrededor correspondió a los pacientes de mayor tiempo de evolución de la enfermedad (fig. 2c y 2d). En el 4,76 % de los ojos se presentaron hipo e hiperautofluorescencia indistintamente.
El OCT demostró la presencia del desprendimiento neurosensorial en todos los pacientes. No se encontró diferencia significativa entre la hiperautofluorescencia y la hipoautofluorescencia en cuanto a AVMC (media de 0,43 y 0,49, respectivamente; p= 0,184), ni respecto al grosor macular central (media de 371,3 µm y 388,1 µm, respectivamente (p= 0,867). En los ojos con hiperautofluorescencia se halló irregularidad en capas externas de la retina y el epitelio pigmentario (EPR) en el OCT (fig. 3a); así como presencia de DEPR (29,8 %) como se muestra en la fig. 3b.
Se encontró diferencia significativa entre los patrones de autofluorescencia en cuanto al tiempo de evolución, el promedio de 7,18 días correspondió en el patrón hipoautofluorescente mientras que en la hiperautofluorescencia 25,3 días (p= 0,023).
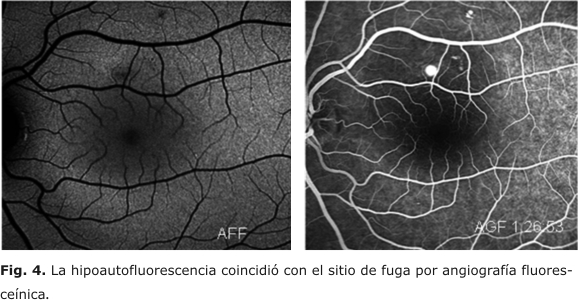
En el 83,3 % de los casos con AGF se demostró escape focal bajo el desprendimiento neurosensorial. Existió hipoautofluorescencia en el sitio de fuga determinado por angiografía fluoresceínica (fig. 4).
DISCUSIÓN
En la génesis de la coriorretinopatía serosa central se invocan dos hechos fisiopatológicos: la alteración del balance neto del flujo de líquido del espacio subretiniano favorecido por una disfunción del EPR, y más recientemente se ha planteado una anormalidad primaria causada por alteración de la permeabilidad de la vasculatura coroidea.3
En fases tempranas de la enfermedad, la agudeza visual (AV) puede conservarse a pesar de la presencia del desprendimiento macular el que puede fluctuar en un rango de 1,0 a 0,1.11,12 Se plantea que en casos de instauración reciente existe una disminución leve y transitoria de la visión central acompañado de metamorfopsias.3 En estudio revisado, el rango de AV se comportó con mayor variabilidad con AV media; fue de 0,8 y un rango de 1,0 a 0,05.13
Ocasionalmente puede recurrir o hacerse crónica en una minoría de los pacientes lo que lleva a una pérdida visual progresiva e irreversible, para el se emplea el término epiteliopatía pigmentaria difusa o coriorretinopatía serosa central crónica.3 Esta última forma de la enfermedad está asociada con atrofia y cambios degenerativos de la retina y el EPR, con consecuente disminución de la visión.11
La presencia de desprendimiento neurosensorial retinal, es característico de la forma activa de la enfermedad, excepto en raros casos en que es encontrado sólo desprendimiento del epitelio pigmentario.6 En nuestra serie todos los casos presentaron la primera condición.
La AFF es normal o presenta mínimos cambios en la etapa aguda de la CSC, se observa hipoautofluorescencia inicial en el área del desprendimiento neurosensorial.9 Frame mostró un mayor número de casos con disminución de la autofluorescencia en el área del desprendimiento neurosensorial superior a nuestros resultados.14 Este autor sustenta la hipótesis de que la disminución de la autofluorescencia se debe presumiblemente al bloqueo causado por el edema, mientras que en las formas crónicas y recurrentes se observa un aumento de la AFF irregular, posiblemente atribuible a cambios en el EPR y al desprendimiento neurosensorial, de larga evolución.15
La disposición granular hiperautofluorescente hallada en casos con menor tiempo de evolución, se piensa se corresponde con gránulos contenidos en el desprendimiento, que se acumulan en la superficie externa de la retina neurosensorial. Cuando estos gravitan, se depositan en el borde inferior y se observa un aumento de la autofluorescencia. Se piensa se deba a que los segmentos externos de los fotorreceptores no son degradados adecuadamente por la persistencia del desprendimiento neurosensorial y estos segmentos externos y los cromóforos que ellos contienen se dispersan en el espacio subretinal originando la autofluorescencia.16,17
Como plantean algunos autores en pacientes con mayor tiempo de evolución, el incremento de la autofluorescencia no sólo se debe a la presencia de los depósitos sino a una disfunción del EPR; en tales casos la hiperautofluorescencia se presenta más difusa y homogénea.
Debemos diferenciar la hipoautofluorescencia que muestran algunos pacientes cuando tienen poca acumulación de material o gránulos en la retina externa de aquellos que presentan signos de atrofia en el epitelio pigmentario.13,14,16 Se señala que zonas demarcadas de parche hipoautofluorescente e hiperautofluorescente, corresponden a áreas de atrofia y depósitos pigmentarios en el EPR respectivamente.6 En la literatura revisada esto se hace llamar patrón en "manchas de leopardo"18 descrito por angiografía fluoresceínica como bloqueo de la fluorescencia coroidea en aquellas zonas donde se encuentran estos depósitos y áreas entre los mismos hiperfluorescentes por atrofia del EPR. Esta combinación de patrones se evidenció en formas crónicas como describe la literatura.
La OCT brinda información adicional acerca del tamaño y la elevación de los desprendimientos, el desarrollo de atrofia retiniana, así como alteraciones del EPR, lo cual proporciona ayuda en el pronóstico visual luego del episodio de CCS. En casos con poco tiempo de evolución se comprueba el típico desprendimiento neurosensorial sin otras alteraciones anatómicas.
Observamos que cuando el desprendimiento de retina neurosensorial alberga en su interior un DEP cambia la morfología de la autofluorescencia, y esta se torna más compleja. Mitarai y otros19 observaron la presencia de DEP en un mayor número de casos (63 %) a los nuestros, lo que posibilita describir una elevación en forma de domo con área de poca reflectividad debajo de la capa del EPR y la presencia de un engrosamiento del EPR en el 15 % de sus pacientes afectados, esto permite señalar que la homogeneidad de la autofluorescencia en el área del DEP va a depender de la presencia o no de pigmento, así como del tiempo de evolución.
Montero y Ruiz-Moreno expresaron cambios similares en el EPR, los cuales describieron como pequeñas protuberancias del EPR, y que pueden ser observados con el OCT convencional. 20
Spaide13 correlacionó la presencia del aumento de los niveles de autofluorescencia con acumulación de material de lipofuscina en las capas externas de la retina observadas por OCT. Esto ha sido demostrado en otros estudios.7,16
Hay estudios que señalan la presencia de hipoautofluorescencia en el punto de filtración por angiografía fluoresceínica en la CSC aguda en todos los pacientes estudiados.6,13,15 Framme halló una disminución significativa de la autofluorescencia en el punto de filtración en el 72 % de sus pacientes, con valores algo inferiores a los encontrados en nuestra serie.15 Eandi y otros señalan que esto soporta el concepto de la existencia de un defecto anatómico o ausencia de epitelio pigmentario de la retina que explica el paso de fluido de la coroides interna al espacio subneurosensorial en la CSC.6 Otras fuentes especulan que el origen de la hipoautofluorescencia pudiera ser por la existencia de un escape a través del EPR cercano a la unión del EPR aplicado y el desprendido.9
Por otra parte, las áreas con atrofia de fotorreceptores y del EPR no producen lipofucsina, sino que aparece hipoautofluorescente. Esto pudiera explicar que la ruptura del EPR puede también resultar ser una imagen hipoautofluorescente.9
En otros estudios fue descrita la hiperautofluorescencia en el sitio de escape focal del epitelio pigmentario de la retina con AGF en la CSC aguda.16,17 La pérdida de fotorreceptores y agrandamiento de los segmentos externos de los fotorreceptores, con la acumulación de lipofucsina en el EPR, fueron factores citados por los autores para explicar su observación de la presencia de hiperautofluorescencia. Sus conclusiones fueron basadas en el supuesto aumento de la actividad metabólica en la vecindad del escape focal del EPR producido por la acumulación de lipofucsina y la presencia de hiperautofluorescencia. En nuestra serie no encontramos esta asociación.
Se concluyó en este estudio que en la CSC se encuentran diferentes patrones de autofluorescencia, que reflejan cambios en la retina externa y el EPR, cuyas alteraciones se relacionan con el tiempo de evolución de la enfermedad. El tipo de patrón de autofluorescencia no se relaciona con los cambios anatómicos y funcionales en la CSC. La autofluorescencia es una técnica de imagen no invasiva que aporta elementos diagnósticos y complementa los procederes convencionales empleados en esta enfermedad.
REFERENCIAS BIBLIOGRÁFICAS
1. Kanski J. Oftalmología Clínica. 3ra ed. Madrid: Mosby Doyma S.A; 1996.
2. Montesinos Ventura B, Abreu Reyes P, Gil Hernández MA. Coriorretinopatía central serosa: una presentación atípica. Arch. Soc. Canar. Oftal. 2001; 12. Disponible en: http://www.oftalmo.com/sco/revista-12/12sco12.htm
3. Katsimpris JM. Coroido-Retinopatía central serosa. Un acertijo sin resolver. Highlights of Ophthalmology. 2006;43(3):14-16.
4. Gass JDM. Stereoscopic Atlas of Macular Diseases: Diagnosis and Treatment. 4th ed. St. Louis: Mosby; 1997.
5. Wang M, Sander B, Lund-Andersen H, Larsen M. Detection of shallow detachments in central serous chorioretinopathy Department of Ophthalmology, Acta Ophthalmol Scand. 1999;77(4):4025. Disponible en: http://onlinelibrary.wiley.com/doi/10.1034/j.1600 -0420.1999.770408.x/pdf
6. Eandi CH, Ober M, Iranmanesh R, Peiretti E, Yannuzzi L. Acute central serous chorioretinopathy and fundus autofluorescence. Retina. 2005 Dec; 25(8):989-93.
7. Haimovici R, Koh S, Gagnon DR, Lehrfeld T, Wellik S. Risk factors for central serous chorioretinopathy: a case-control study. Ophthalmology 2004;111(2):24449.
8. Delori FC, Dorey CK, Staurenghi G, Arend O, Goger DG, Weiter JJ. In vivo fluorescence of the ocular fundus exhibits retinal pigment epithelium lipofuscin characteristics. Invest Ophthalmol Vis Sci. 1995;36(3):71829.
9. Spaide RF. Autofluorescence from the outer retina and subretinal. En: Holz FG, Schmitz S, Spaide R, Bird AC. Atlas of fundus autofluorescence imaging. Berlin: Springer- Verlag Heidelberg; 2007. p. 245-6.
10. Spaide RF. Deposition of yellow submacular material in central serous chorioretinopathy resembling adult-onset foveomacular viteliform dystrophy. Retina. 2004;24(2):301-4.
11. Spaide RF, Campeas L, Haas A, Yannuzzi LA, Fisher YL, Guyer DR, et al. Central serous chorioretinopathy in younger and older adults. Ophthalmology. 1996;103(12):2070-80.
12. Klais CH, Ober MD, Ciardella AP, Yannuzzi LA. Central Serous Chorioretinopathy. En: Ryan SJ. Retina. 4 ed. USA: Elsevier Mosby; 2004. p. 1135-50.
13. Spaide RF, Klancnik JM Jr. Fundus autofluorescence and central serous chorioretinopathy. Invest Ophthalmol Vis Sci. 2005;46.
14. Framme C, Walter A, Gabler B, Roider J, Sachs HG, Gabel VP.. Fundus autofluorescence in acute and chronic-recurrent central serous chorioretinopathy. Acta Ophthalmol Scand. 2005; 83(2):161-7. Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1600 -0420.2005.00442.x/full
15. Karadimas P, Goritsa A, Paleokastritis GP, Kotzabassis A, Bousas EA. Autofluorescence imaging in central serous chorioretinopathy and correlation with Fluorescein angiography and indocyanine green angiography. Invest Ophthalmol Vis Sci. 2005;46.
16. von Ruckmann A, Schmidt KG, Fitzke FW, Bird AC, Jacobi KW. Serous central chorioretinopathy: Acute autofluorescence of the pigment epithelium of the eye. Ophthalmologe. 1999;96(1):610.
17. von Ruckmann A, Fitzke FW, Fan J, Halfyard A, Bird AC. Abnormalities of fundus autofluorescence in central serous retinopathy. Am J Ophthalmol. 2002;133:7806.
18. Iida T, Spaide RF, Haas A, Yannuzzi LA, Jampol LM, Lesser RL. Leopard-spot pattern of yellowish subretinal deposits in central serous chorioretinopathy. Arch Ophthalmol. 2002;120:37-42. Disponible en: http://archopht.ama-assn.org/cgi/reprint/120/1/37
19. Mitarai K, Gomi F, Tano Y. Three-dimensional optical coherence tomographic findings in central serous chorioretinopathy. Graefes Arch Clin Exp Ophthalmol. 2006;244:141520. Disponible en: http://www.springerlink.com/content/mw5317qg45244h66/fulltext.pdf
20. Montero JA, Ruiz-Moreno JM. Optical coherence tomography characterisation of idiopathic central serous chorioretinopathy. Br J Ophthalmol. 2005;89:56264. Disponible en: http://bjo.bmj.com/content/89/5/562.full.pdf
Recibido: 12 de febrero de 2011.
Aprobado: 4 de marzo de 2011.
Dra. Eva R. Santana Alas. Servicio de Vítreo Retina. Instituto Cubano de Oftalmología "Ramón Pando Ferrer". Ave. 76 No. 3104 entre 31 y 41 Marianao, La Habana, Cuba. Correo electrónico: evasantana@infomed.sld.cu