Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Oftalmología
versión impresa ISSN 0864-2176
Rev Cubana Oftalmol vol.25 supl.1 Ciudad de la Habana 2012
INVESTIGACIONES
Evaluación del espesor corneal central y su influencia en la presión intraocular en pacientes del Hospital "Dr. Miguel Enríquez"
Evaluation of the central corneal thickness and its impact on the intraocular pressure of patients in "Dr. Miguel Enriquez" hospital
MSc. María Teresa Arrronte Alarcón,I Dr. Víctor Manuel Delgado Márquez,I Dr. Jeannette Rodríguez Vázquez,I Dra. Taymi Rodríguez Ramírez,I Dra. Yanileidy González Blanco,II MSc. Bárbara Padilla DocalIII
I Hospital "Dr. Miguel Enríquez". La Habana, Cuba.
II Instituto Cubano de Oftalmología "Ramón Pando Ferrer". La Habana, Cuba.
III Facultad de Ciencias Médicas "Dr. Miguel Enríquez". La Habana, Cuba.
RESUMEN
Objetivo: evaluar el espesor corneal central en sujetos sanos, hipertensos oculares, sospechosos de glaucoma y glaucomatosos, y su influencia en la presión intraocular.
Métodos: se realizó un estudio descriptivo y transversal que incluyó 708 ojos de 356 sujetos que acudieron al servicio de oftalmología del Hospital Universitario "Dr. Miguel Enríquez" entre enero y diciembre de 2010. A los pacientes se les midió el espesor corneal central con paquimetría ultrasónica (paquímetro US 4000). El resto de la información se obtuvo a partir de las historias clínicas de los pacientes.
Resultados: Los hipertensos oculares presentaron córneas gruesas (p=0,07); el mayor número de casos que tenían diagnóstico de sospecha de glaucoma y de glaucoma primario de ángulo abierto presentaron un grosor corneal delgado (p=0,62 y p=0,08 respectivamente). Si no se hubiese tenido en cuenta el factor de corrección para evaluar la presión intraocular se encontraría 48,1 % de los glaucomatosos y 31,5 % de los hipertensos oculares con diagnóstico inadecuado (p<0,0001).
Conclusiones: Los hipertensos oculares, en su mayoría, presentaron córneas gruesas; sin embargo, el mayor número de casos que tenían diagnóstico de sospecha glaucoma y de glaucoma primario de ángulo abierto presentaron un grosor corneal más delgado. Tener en cuenta el factor de corrección en la evaluación de la PIO disminuye el error diagnóstico.
Palabras clave: córnea, espesor corneal central, presión intraocular.
ABSTRACT
Objective: to evaluate the central corneal thickness in healthy individuals, in persons with ocular hypertension, and in suspected glaucoma and glaucomatous people, and its influence in intraocular pressure.
Methods: a cross-sectional and descriptive study was performed in 708 eyes from 356 people who had been seen at ophthalmology service of “Dr. Miguel Enríquez”, university hospital from January to December, 2010. Their central corneal thickness was measured with ultrasonic pachymetry (pachymeter US 4000). The rest of the information came from the clinical histories of the patients.
Results: Most of the ocular hypertensives presented thick corneas (p=0,07); a high number of cases that had diagnosis of glaucoma suspicion and primary open-angle glaucoma showed thin corneas (p=0,62 and (p=0,08 respectively). If the correction factor to evaluate the IOP had not been considered, then 48,1 % of the glaucomatous patients and 31,5 % of the ocular hypertensives would have been inadequately diagnosed (p<0,0001).
Conclusions: the majority of the ocular hypertensive patients had thick corneas; however, the biggest number of cases that had diagnosis of suspected glaucoma and primary open angle glaucoma showed thinner corneas. Keeping in mind the correction factor in the evaluation of the intraocular pressure reduces the diagnostic errors.
Key words: cornea, intraocular pressure, central corneal thickness.
INTRODUCCIÓN
El glaucoma afecta a 65 millones de personas en el mundo. Es una de las entidades nosológicas con mayor prevalencia en la oftalmología y genera un costo económico considerable en los sistemas de salud de todo el mundo.1 Se denomina glaucoma primario de ángulo abierto (GPAA) a la neuropatía óptica que se presenta en ausencia de trastornos oculares o sistémicos que provoquen aumento de la resistencia al flujo del humor acuoso o daño al nervio óptico, usualmente asociada con presión intraocular (PIO) elevada.2
La elevación de la PIO desde hace algún tiempo ya no es considerada un elemento clave en la definición y diagnóstico del GPAA pero es el único factor de riesgo tratable y se conoce que está asociado con la presencia y progresión de la enfermedad. La creciente evidencia de una inadecuada clasificación a algunos pacientes como resultado del artefacto inherente a la tonometría de aplanación, plantea la cuestión acerca de que, contando con la paquimetría, podemos corregir nuestras mediciones clínicas para reflejar la PIO más cercana a la real.
A la fecha, pese a que se ha intentado, no existe un nomograma simple para corregir la PIO teniendo en cuenta el espesor corneal central (ECC). Este se muestra en ocasiones, como un factor de confusión y de hecho, los diferentes métodos de medida indirecta de presión intraocular, se ven influenciados por su valor. Así con el tonómetro de aplanación de Goldman (TAG), las córneas gruesas inducen una supraestimación y las córneas delgadas una infraestimación de la lectura de la presión ocular.2,3
Entre los métodos utilizados para medir el grosor corneal se describen los paquímetros ultrasónicos (PU) como el Pacline,4-9 y ópticos como la interferometría de coherencia parcial,10 la microscopia especular,11,12 la microscopia confocal,12 la tomografía de coherencia óptica13 y la tecnología de mapas de elevación del sistema Orbscan.14-16 Los sistemas más utilizados actualmente son la PU y el Orbscan. El primero requiere contacto corneal y utiliza el efecto doppler para realizar las medidas, se caracteriza por ser portátil, de fácil manejo, exacto, confiable y presentar una baja variabilidad inter e intraoperador (operador adecuadamente entrenado para su uso). Sin embargo, utilizar un método de contacto requiere una mayor colaboración del paciente y habilidad del operador. Esto hace que sea considerado "en parte" operador dependiente.5,8,17
El segundo, Orbscan, analiza imágenes de secciones ópticas y obtiene la paquimetría en base a la diferencia entre las elevaciones de las superficies anterior y posterior de la córnea.16 El paquímetro ultrasónico Nidek digital Modo A/B Us-4000 ofrece medidas precisas del grosor de la córnea con un error máximo de 5 µm, sonda sólida de 10 MHz y puede memorizar el grosor corneal hasta 25 puntos.5
El objetivo fue identificar en qué proporción un factor anatómico puede inducir errores, que no sólo afectan la detección del GPAA, sino su manejo y pronóstico. Para esto se evaluó el ECC en pacientes sanos oculares (SO), hipertensos oculares (HTO), sospechosos de glaucoma (SG) y glaucomatosos, así como su influencia en la presión intraocular.
MÉTODOS
Se realizó un estudio descriptivo y transversal, donde se incluyeron 356 pacientes (708 ojos) que acudieron a consulta externa del servicio de oftalmología del Hospital Universitario "Dr. Miguel Enríquez" entre enero y diciembre de 2010. Estos cumplieron los siguientes criterios: mayores de 30 años, sin enfermedad ocular o con diagnóstico conocido de SG, GPAA o HTO sin tratamiento y que dieron el consentimiento informado. Se excluyeron ojos con antecedentes de cirugía o traumatismos oculares, edema corneal o cualquier otra afectación de la córnea que pudiera variar su espesor, ojos con daño no glaucomatoso del nervio óptico que provocaran excavaciones y defectos en el campo visual, con opacidad de medios que impidiera observar el fondo de ojo con nitidez y los que tuvieran imposibilidad de realizar cualquiera de las pruebas incluidas en el protocolo exploratorio. Los ojos sanos fueron seleccionados de pacientes con afecciones monoculares que no interesaran al ojo adelfo (ojo incluido), y de acompañantes que acudieron a las consultas externas del servicio de oftalmología del hospital. Los HTO, los SG y los glaucomatosos se obtuvieron a partir de los sujetos remitidos a la consulta de glaucoma.
La variable estudiada fue el ECC clasificado en cuatro rangos de valores medidos en micras (≤520, 521-550, 551-580, >580). Se estudió el ECC en los pacientes SO con PIO corregida (21 mmHg, morfología papilar y perimetría automatizada normal); en HTO (PIO corregida >21 mmHg con perimetría automatizada y morfología papilar normal); SG (PIO corregida ≤21 mmHg con perimetría automatizada y/o excavación sospechosa) y GPAA (según clasificación de la Academia Americana de Oftalmología).2
El algoritmo de corrección se obtuvo de estudios sobre ECC y su impacto en la tonometría de aplanación Goldman.8 Este algoritmo fue empleado en estudios poblacionales grandes, así como otro estudio de cohorte.18 La presión intraocular se ajustó por la paquimetría de acuerdo con el algoritmo propuesto en el meta-análisis de Doughty y Zaman,19 que disminuye o incrementa 0,6 mmHg por cada 10 µm de ECC, toma como referencia un ECC normal de 545 µm. Estos evalúan poblaciones hispanas que se asemejan más a las características étnicas de este estudio. Por otra parte, es algo más conservador que otros descritos18,20 y de esta forma se evita sobrecorrecciones de la PIO que pudieran influir en los resultados de esta investigación.
Los datos fueron recogidos en una planilla que se creó con este objetivo. El estudio fue aceptado por el comité de ética del hospital y todos los participantes firmaron el consentimiento informado, que se realizó siguiendo las directrices de la Declaración de Helsinki.21,22
Para incluir los casos en el estudio, se les realizó a los sanos oculares, un examen oftalmológico que incluyó biomicroscopia con lámpara de hendidura, oftalmoscopia directa, tonometría y perimetría automatizada. De los demás, se obtuvieron los datos de sus historias clínicas. A todos los pacientes se les tomó la tensión ocular y se les realizó la medición del ECC con paquímetro ultrasónico. Se calculó la PIO corregida en todos los casos.
Para la realización de los exámenes descritos anteriormente se utilizaron los siguientes equipos: biomicroscopia con lámpara de hendidura (HAAGSTREIT BQ 900), oftalmoscopia directa, oftalmoscopio directo (Neitz Psu1), tonómetro de aplanación de Goldman (se midió los valores de la presión intraocular con tonómetro de aplanación acoplado a lámpara de hendidura), paquimetría ultrasónica corneal central con paquímetro modelo US-4000 (NIDEK ECHOSCAN).
Las variables se analizaron mediante números absolutos, porcentajes y medias. Los datos se procesaron mediante el programa SPSS versión 10.0. Los resultados se presentaron en tablas. Se utilizó como prueba estadística el test de correlación para ver si la condición ocular (SO, HTO, SG, GPAA) se relacionaba con el ECC, y el test de chi cuadrado para ver si existía homogeneidad entre esta condición ocular y se utilizó una significación menor de 0,05.
RESULTADOS
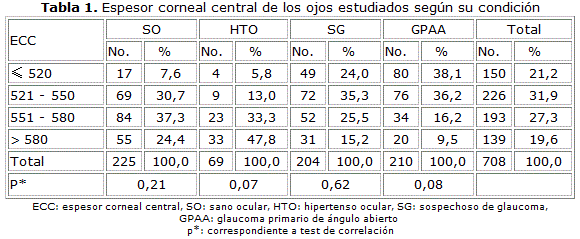
Predominaron los pacientes con espesor corneal central entre 521 y 550 µm (31,9 %). El menor número de caso estuvo por encima de las 580 µm.
Por grupo de estudio prevalecieron las córneas entre 551 y 580 µm en los sanos oculares (37,3 %). Fueron superiores a 580 µm (47,8 %), en los que presentaban hipertensión ocular. El 35,3 % de los sospechosos de glaucoma estuvo entre las 521 y 550 µm. En los glaucomatosos predominaron las córneas delgadas, menores de 520 µm (74,3 %).
Cuando se empleó el test de correlación, para valorar si la condición ocular se relacionaba con el espesor corneal central, se observó que no hubo diferencias significativas. Existió una relación más estrecha entre los pacientes con ECC mayor de 580 µm y la hipertensión ocular (p=0,07) (tabla 1).
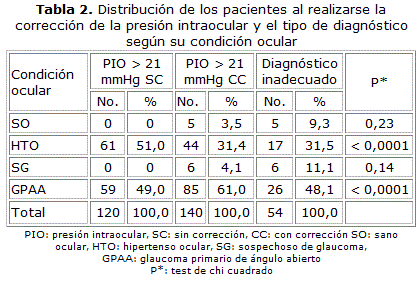
Al analizar las diferencias que se encontraron entre la PIO sin corregir y la corregida, el número de ojos que no estarían con diagnóstico adecuado varió en cada grupo. Se obtuvo que en los pacientes sanos oculares se dejaron de atender 5 ojos (9,3 %), en los sospechosos de glaucoma 6 ojos (11,1 %) y en los glaucomatosos 26 ojos (48,1 %). En los hipertensos oculares se estarían medicando 17 ojos (31,5 %) por PIO mayor de 21 mmHg si no se ajustara este valor según la paquimetría central.
Se aplicó el test de chi cuadrado para analizar si existía homogeneidad entre la condición ocular y la presión intraocular mayor de 21 mmHg sin corregir y la corregida. Se observó que hubo diferencias significativas en los casos de HTO y GPAA respecto a la PIO mayor de 21 mmHg sin corregir (p<0,0001) (tabla 2).
DISCUSIÓN
Los resultados obtenidos con relación al ECC, son similares a los encontrados por otros autores19 que estimaron el espesor corneal medio con medidas ultrasónicas en 535 µm. En otros artículos, se plantea que el valor normal del espesor corneal central es de aproximadamente 540 µm, y de 600 a 700 µm en la periferia.5 En un estudio realizado en Colombia,23 se encontraron valores medianos de paquimetría, en el grupo de pacientes diagnosticados como normales, de 542 µm. Para el caso de los glaucomatosos se encontró córneas delgadas, más del 70 % tenían córneas con valores inferiores a 550 µm.
En Cuba, en un estudio realizado en el municipio Cerro donde se incluyeron 121 pacientes, se encontró una disminución del ECC a medida que aumentaba la edad con una media de 549 µm en el grupo de glaucomatosos.24 Al igual que lo encontrado en el estudio ocular de latinos de Los Ángeles que mostró un ECC promedio de 545±38 µm en los pacientes con glaucoma primario de ángulo abierto.20 Datos similares reporta Martínez que mostró un espesor corneal central promedio de 544±40 µm, en el grupo de pacientes glaucomatosos.25
El análisis del hipertenso ocular se muestra controversial al revisar la literatura. En la pasada década hubo múltiples reportes de ECC incrementado en pacientes con hipertensión ocular. El estudio para el tratamiento de la hipertensión ocular (OHTS, por sus siglas en inglés),26 demostró que el ECC es un valor importante en la predicción del desarrollo del glaucoma en ojos con hipertensión. Los ojos con un ECC de 555 µm o menos, poseen un riesgo de desarrollar glaucoma 3 veces mayor en relación con pacientes con ECC de más de 588 µm.26 El estudio de intervención de glaucoma avanzado (AGIS, por sus siglas en inglés)27 obtuvo resultados similares, las córneas con 40 µm más delgadas estuvieron asociadas con un 32 % mayor de riesgo. Se coincide con estos estudios, se encontró los grosores corneales mayores en los hipertensos oculares. Es un hecho que algunos pacientes con presiones consideradas normales con la tonometría de aplanación de Goldman desarrollan glaucoma, y otros con presiones consideradas por encima del rango de la normalidad nunca desarrollan la enfermedad.26,27 Esto, unido a la existencia demostrada de diferencias estadísticamente significativas en cuanto a grosor corneal entre los pacientes con glaucoma de tensión normal y los pacientes hipertensos oculares, hace dudar de la validez de este tipo de tonometría a la hora de clasificar adecuadamente a pacientes con valores extremos de paquimetría.26
El espesor corneal central puede explicar la evolución tan tórpida en pacientes con un aparente control, o ser la causa de progresión de la neuropatía en ausencia de hipertensión. En esta investigación quedó demostrada la importancia de aplicar un ajuste a la tonometría de aplanación de Goldman ya que del total de ojos analizados, 48 quedarían con diagnóstico inadecuado (por infraestimación de la PIO para el caso de los que presentaban GPAA, o por sobreestimar su valor en los HTO). Ríos González encontró que la proporción de pacientes que requerían ajuste de valor de la PIO por modificaciones en el ECC fue cercana al 50 % de los casos.28 En un estudio realizado con una serie de 188 pacientes, después de aplicar el factor de corrección tras la paquimetría ultrasónica, 16 (8,5 %) tuvieron un cambio en la terapia de gotas en los ojos, 4 (2,1 %) respecto a la terapia con láser, y 6 (3,2 %) en la decisión sobre la cirugía de glaucoma.29,30
Esta investigación demuestra que el ECC tiene un efecto significativo sobre el manejo clínico de los pacientes con glaucoma y el sospechoso de glaucoma. Para otros autores,31 en su serie de 324 individuos al investigar la eficacia de los factores de corrección disponibles en la actualidad en la corrección de la PIO, sostienen que estos factores no ofrecen un alto grado de confiabilidad. Refieren que la corrección de la PIO por el efecto del ECC al utilizar estos modelos podrían ser erróneos y conducir a la sobrecorrección de la PIO, con la consecuente baja erróneamente corregida de la PIO en ojos con córneas más gruesas. Sostienen que el efecto del ECC y la PIO es menos de lo previsto, tanto por la fórmula de Ehlers y Orssengo y el modelo Pye.31
Al partir de estas discrepancias, se hace necesario buscar nuevos métodos para estimar la PIO más cercana a la real; o quizás sea mejor decir, la que proporcione niveles de protección para el nervio óptico e impida la progresión del daño glaucomatoso. Se plantea que con otros instrumentos de medición de la PIO, como el tonómetro de contorno dinámico con el cual la PIO no está supuestamente influenciada por el ECC, pudiera ser más fiable su valor.32-34 Actualmente se desarrollan investigaciones para encontrar, entre las diversas opciones con que se cuenta, cuál es el instrumento ideal que provea los mejores índices de repetitividad y reproducibilidad, que permitan incluir estas mediciones confiablemente en la práctica diaria.
En conclusión los hipertensos oculares en su mayoría presentaron córneas gruesas. Sin embargo, el mayor número de casos que tenían diagnóstico de sospecha de glaucoma y glaucoma primario de ángulo abierto, presentaron un grosor corneal más delgado. Tener en cuenta el factor de corrección en la evaluación de la PIO disminuye el error diagnóstico.
REFERENCIAS BIBLIOGRÁFICAS
1. Leske MC, Wu S, Nemesure B, Hennis A, Barbados Eye Studies Group. Causes of visual loss and their risk factors: an incidence summary from the Barbados Eye Studies. Rev Panam Salud Pública. 2010;27(4):259-67.
2. Skuta GL, Cantor LB, Weiss JS. Glaucoma. En: Basic and clinical science course. American Academy of Ophthalmology. The Eye M.D. Association, 2008-2009 Edition (5).
3. Brandt JD, Beiser JA, Kass MA, Gordon MO. Central corneal thickness in the ocular hypertension treatment study (OHTS). Ophthalmol. 2001;108(10):1779-88.
4. Gordon MO, Beiser JA, Brandt JD, Heuer DK. The Ocular Hypertension Treatment Study: baseline factors that predict the onset of primary open-angle glaucoma. Arch Ophthalmol. 2002;120(6):714-20.
5. Alezzandrini A, Frick M, Della Savia L, López M. Estudio Comparativo de Medición del Espesor Corneal Central Utilizando Paquimetría Ultrasónica y Pentacam. Arch Oftal B Aires. 2009;2(80):71-3.
6. Pandolfi A. Computational Biomechanics of the Human Cornea. En: Suvranu D, Guilak F, Mofrad RKM. Computational Modeling in Biomechanics. Holanda: Springer Netherlands; 2010. p. 435-66.
7. Kohlhaas M, Boehm AG, Spoerl E, Pürsten A, et al. Effect of Central Corneal Thickness, Corneal Curvature, and Axial Length on Applanation Tonometry. Arch Ophthalmol. 2006;124(4):471-6.
8. Wheeler NC, Morantes CM, Kristensen RM, Pettit TH, Lee DA. Reability coeficients of three corneal pachymeters. Am J Ophthalmol. 1992;113(6):645-51.
9. Drexelr W, Baumgartner A, Findl O, Hitzenberger CK, Sattmann H, Fercher AF. Submicrometer precision biometry of the anterior segment of the human eye. Invest Ophthalmol Vis Sci. 1997;38(7):1304-13.
10. Hitzenberger CK, Baumgartner A, Drexler W, Fercher AF. Interferometric measurement of corneal thickness with micrometer precision. Am J Ophthalmol. 1994;118(4):468-76.
11. Bovelle R, Káufman SC, Thompson HW, Hamano H. Corneal thickness measurements with the Topcon SP 2000 P specular microscope and an ultrasound pachymeter. Arch Ophthalmol. 1999;117(7):868-70.
12. Keisuke K, Kazunori M, Tadatoshi T, Takahiro K, Hiraoka, Tetsuro O. Central corneal thickness measurements using Orbscan II Scanning Slit Topography, Noncontact Specular Microscopy, and Ultrasonic Pachymetry in eyes with keratoconus. Clinical Sciences. 2005;8(24):967-71.
13. Dubois A, Grieve K, Moneron G, Lecaque R, Vabre L, Boccara C. Ultrahigh-Resolution Full-Field optical coherence tomography. Applied Optics. 2004;14(43):2874-83.
14. Kawana K, Tokunaga T, Miyata K, Okamoto F, Kiuchi T, Oshika T. Comparison of corneal thickness measurements using Orbscan II, non-contact specular microscopy, and ultrasonic pachymetry in eyes after laser in situ keratomileusis.. Br J Ophthalmol. 2004;88(4):466-8.
15. Sanchís-GJ, Lleó PA, Alonso L, Rahhal M. Paquimetría Orbscan: Diferencias entre observadores al realizar mediciones del espesor corneal. Arch Soc Esp. 2005;80(5):283-8.
16. Boscia F, La Tegola MG, Alessio G, Sborgia C. Acuracy of Orbscan optical pachymetry in corneas with haze. J Cataract Refract Surg. 2002;28(2):253-8.
17. Feltgen N, Leifert D, Funk J. Correlation between central corneal thickness, applanation tonometry, and direct intracameral IOP readings. Br J Ophthalmol. 2001;85(1):85-7.
18. Francis BA, Varma R, Chopra V, Lai MY, Shtir C, Azen SP and Los Angeles Latino Eye Study Group. Intraocular pressure, central corneal thickness, and prevalence of open-angle glaucoma: The Los Angeles Latino Eye Study. Am J Ophthalmol. 2008;146(5):741-6.
19. Doughty MJ, Zaman ML. Human corneal thickness and its impact on intraocular pressure measures: a review and meta-analysis approach. Surv Ophthalmol. 2000;44(5):367-408.
20. Varma R, Paz SH, Azen SP, Klein R, Globe D, Torres M, et al. The Angeles Latino Eye Study. Design, methods and baseline data. Ophthalmology. 2004;111(6):1121-31.
21. The World Medical Association. Declaration of Helsinki. 52nd WMA General Assembly. Edimburgh, Scotland: The Association; 2000.
22. Díaz Alemán VT, Fernandez-Banca Vaca G, Lozano Lopez V, Garcia Somalo M, Perera Sanz D, Gonzalez de la Rosa M. Nomograma de riesgo de progreso de hipertensión ocular basado en el Ocular Hypertension Treatment Study. Arch Soc Esp Oftalmol. 2005;80(3):151-4.
23. Rueda JC, Lesmes DP, Parra JC, Urrea R, Rey JJ, Rodriguez LA, et al. Valores de paquimetría en personas sanas y con glaucoma en la población colombiana. MedUNAB 2007;10(2):81-5.
24. Triana Casado I, Medina Perdomo JC. Espesor Corneal Central y Otros Factores de Riesgo del Glaucoma Primario de Ángulo Abierto. Rev Misión Milagro. 2009 [citado 23 de febrero de 2012];3(1). Disponible en: http://www.misionmilagro.sld.cu/vol3no1/inv3105.php
25. Luna-Martínez C. Relación del espesor corneal central y la variación en la presión intraocular con daño al nervio óptico en pacientes mexicanos con glaucoma. Rev Mex Oftalmol. 2009;83(4):193-6.
26. Kass MA, Heuer DK, Higginbotham EJ, Johnson CA, Keltner JL, Miller JP et al. The Ocular Hypertension Treatment Study: a randomized trial determines that topical ocular hypotensive medication delays or prevents the onset of primary open-angle glaucoma. Arch Ophthalmol. 2002;120(6):701-13.
27. The AGIS Investigators. The Advanced Glaucoma Intervention Study (AGIS): The relationship between control of intraocular pressure and visual field deterioration. Am J Ophthalmol. 2000;130(4):429-40.
28. Ríos González LC. Detección de glaucoma: corrección de PIO por modificaciones del grosor corneal. Rev Mex Oftalmol. 2009;83(5):284-7.
29. Shih CY, Graff Zivin JS, Trokel SL, Tsai JC. Significado clínico del espesor corneal central en el tratamiento del glaucoma. Glaucoma J. 2005;14(5):337-43.
30. Medeiros FA, Weinreb RN. Evaluación del riesgo de glaucoma e hipertensión ocular. Construcción de un modelo de riesgo para desarrollo y progresión de glaucoma. International Ophthalmology Clinics. 2009;48(4):1-12.
31. Gunvant P, O'Leary DJ, Baskaran M. Evaluation of tonometric correction factors. Glaucoma J. 2005;14(5):337-43.
32. Martinez-de-la-Casa JM, Garcia-Feijoo J, Vico E, Fernandez-Vidal A, Benitez del Castillo JM, Wasfi M. Effect of corneal thickness on dynamic contour, rebound, and goldmann tonometry. Ophthalmology. 2006;113(12):2156-62.
33. Heras M, Moreno MJ, Sadaba ELM, Mendiluce ML. Comparison of dynamic contour tonometry with pneumotonometry and Goldmann tonometry. Arch Soc Esp Oftalmol. 2007;82(6):337-41.
34. Pache M, Wilmsmeyer S, Lautebach S, Funk J. Dynamic contour tonometry versus Goldmann applanation tonometry: a comparative study. Graefes Arch Clin Exp Ophthalmol. 2005;243(8):763-7.
Recibido: 8 de marzo de 2012.
Aprobado: 8 de abril de 2012.
Dra. María Teresa Arronte Alarcón. Hospital Dr. "Miguel Enríquez". Ramón Pinto esquina Concha. La Habana, Cuba. Correo electrónico: tero@infomed.sld.cu