My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Archivo Médico de Camagüey
On-line version ISSN 1025-0255
AMC vol.15 no.6 Camagüey Nov.-Dec. 2011
ARTÍCULO ORIGINAL
Simulación de un brote de Influenza A H1N1 en una escuela primaria de Camagüey
Simulation of an outbreak of Influenza A H1N1 in a primary school from Camagüey
Dr. José A. Betancourt BetancourtI; Dra. Moura RevueltasII; Dr. Carlos DíazIII; Lic. Jorge Rivero DonesIV
I Doctor en Medicina Veterinaria. Profesor Auxiliar. Universidad de Ciencias Médicas. Camagüey, Cuba. josebetancourt.cmw@infomed.sld.cu
II Especialista de I Grado en Medicina General Integral. Dirección Nacional de Medicina del Trabajo. La Habana, Cuba.
III Especialista de I Grado en Epidemiología. Centro Provincial de Higiene y Epidemiología. Camagüey, Cuba.
IV Licenciado en Matemática. Sede Universitaria de Minas. Camagüey, Cuba.
RESUMEN
Fundamento: la dinámica de la vida moderna demuestra la necesidad del uso de modelos matemáticos y simulaciones para el análisis de la dispersión de enfermedades. Objetivo: mostrar el comportamiento de un posible brote epidémico de Influenza A H1N1, en una escuela primaria a partir de la entrada de un enfermo sin tomar ninguna medida de contención. Método: se realizó una simulación con el modelo Susceptible, Expuesto, Infectado y Recuperado, durante el mes de septiembre de 2009. Se asume en la primera simulación que no se tomó ninguna medida preventiva, en la segunda, que se tomaron medidas sólo a partir de los siete días de comenzar el brote. Se toma un índice de transmisibilidad de 0.35, una duración de la enfermedad de siete días y un período latente de un día. Resultados: el modelo de simulación mostró en el caso de no tomar ninguna medida, cómo se produciría un pico máximo de la enfermedad a los trece días de iniciado el mismo, con un total de 190 enfermos, con 99 recuperados y sólo declina de forma espontánea a los 50 días con el último enfermo, el número reproductivo básico fue de 2.22 Conclusiones: existe de forma libre y gratuita un conjunto de herramientas de cálculos y simulaciones que se pueden utilizar en la provincia por parte de los epidemiólogos y los profesores de esta rama de la Salud Pública.
DeCS: SUBTIPO H1N1 DEL VIRUS DE LA INFLUENZA A; BROTES DE ENFERMEDADES; MODELOS MATEMÁTICOS; SIMULACIÓN DE ENFERMEDAD.
ABSTRACT
Background: the dynamics of modern life has demonstrated the need for the use of mathematical models and simulations for the analysis of the spread of diseases. Objective: to show the behavior of a possible outbreak of Influenza A H1N1 in a primary school. Method: a simulation using the model Susceptible, Exposed, Infected and Recovered was performed, during September 2009. It is assumed in the first simulation that was not taken any preventive action, in the second one, those measures were taken only after a week of the outbreak onset. The transmission index of 0.35, the duration of the disease of seven days and a latent period of one day was taken. Results: the simulation model showed in the case of not taking any action, how there would be a peak of the disease to the 13 days of being initiated, with a total of 190 patients, 99 recovered; only decline spontaneously to 50 days with the last patient, the basic reproductive number was 2.22. Conclusions: there is a set of tools for calculations and simulations that may be used in the province by epidemiologists and teachers of this branch of public health for free.
DeCS: INFLUENZA A VIRUS, H1N1 SUBTYPE; DISEASE OUTBREAKS; MATHEMATICAL MODELS; MALINGERING.
INTRODUCCIÓN
Los avances médicos reducen las consecuencias de enfermedades infectas contagiosas y la prevención ocupa el primer lugar para tratarlas. Para comprender la dinámica de la transmisión de enfermedades, es muy útil la modelación matemática. Una vez que un modelo se formula, captura la esencia de la progresión y transmisión de una enfermedad en la población, se utiliza para predecir los efectos de diferentes estrategias para erradicar una epidemia. El hecho de calcular la dispersión de una nueva enfermedad emergente, permite adecuar las medidas de intervención. Actualmente es posible realizar experimentos en las computadoras que no es posible hacer en la vida real, se simula cómo sería la dispersión de una enfermedad en el tiempo, sin ninguna medida de contención y se valora el impacto de estrategias de contención y mitigación. 1
En la etapa inicial de un brote epidémico existen imprecisiones y fragmentaciones de las informaciones disponibles. La información real está limitada hasta que se hagan confirmaciones mediante exámenes específicos y análisis serológicos. Existe co-circulación de múltiples cadenas de enfermedades biológicas, pacientes asintomáticos o con síntomas leves que no se detectan ni reportan, todo lo que trae retrasos en el diagnóstico y sus reportes, por lo que empeora la situación. 2
Está disponible en la red internet el software libre R, en el que se encuentran casi todos los modelos estadísticos y gran cantidad de modelos matemáticos con código abierto y modificable, 3 entre los que se encuentran los sistemas de ecuaciones diferenciales y dentro de éste, el paquete odesolve. 4
El propósito del presente artículo es simular en el software libre R, el comportamiento de un posible brote epidémico de influenza A H1N1 en una escuela primaria a partir de la entrada de un enfermo sin tomar ninguna medida de contención.
MÉTODOS
Con el propósito de observar el comportamiento de un posible brote epidémico de influenza A H1N1, a partir de la entrada de un enfermo, se realizó una simulación epidemiológica en la escuela primaria Alfredo Gómez del municipio Camagüey, durante el mes de septiembre de 2009. El universo de estudio coincidió con la muestra y se constituyó por la población de estudiantes, 360 personas menores de trece años. La simulación se realizó con el programa R, en específico con el paquete odesolve, el cual se utilizó para resolver el modelo SEIR (Susceptible, Expuesto, Infectado y Recuperado), que consta de las siguientes ecuaciones diferenciales descritas por Anderson y May: 5
![]()
![]()
![]()
El período latente es α, β es el índice de transmisibilidad, µ el índice de mortalidad y υ el índice de recuperación de la enfermedad. En este modelo se asume una mezcla homogénea de los susceptibles (S), lo que significa que se relacionan entre sí y se exponen por igual a los enfermos (I), tienen un previo período latente (E) antes de dispersar la enfermedad, cuando no tienen la enfermedad salen del sistema (R). En este sistema se asume una población constante (N), de modo que N=S+E+I+R.
Se asume un índice de transmisibilidad de 0.35, una duración de la enfermedad de siete días y un periodo latente de un día. Se le agrega el cálculo del número reproductivo básico ( ) en una función según lo establecido para este modelo mediante la fórmula definida por Anderson and May: 5
![]()
En la primera simulación no se tomó ninguna medida preventiva, en la segunda se asume que se tomaron medidas sólo a partir de los siete días de comenzar el brote. Se comenta el manejo preventivo real que existió en la escuela.
RESULTADOS
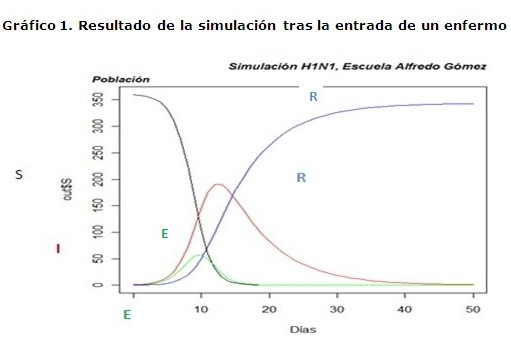
El modelo de simulación, muestra en el caso de no tomar ninguna medida como se produciría un pico máximo de la enfermedad a los 13 días de iniciado el mismo, con un total de 190 enfermos, lo que representa a un 54 % de la población expuesta con 99 recuperados que sólo declina de forma espontánea a los 50 días con el último enfermo. (Gráfico 1)
Población susceptible (S) Período latente (E) : Período infeccioso (I): Recuperados (R)
El número reproductivo básico que se refleja en la simulación es de 2.31, es decir cada paciente primario genera 2.31 pacientes secundarios. Si se toman medidas tardías a los siete días de iniciarse el brote epidémico, existe un total de 25 enfermos a aislar y tratar. (Gráfico 2)
En esta escuela, como en todas las del país, se tomaron medidas preventivas integrales con un fuerte programa educativo, dirigido a la prevención mediante el lavado frecuente de manos, la instrucción al personal docente, no docente y alumnos, dirigidos al aumento de la percepción de riesgo. Además de vigilar los pacientes febriles, resfriados, etc, para su evaluación clínica detallada, lo que fue un éxito en la prevención y dispersión de la enfermedad.
DISCUSIÓN
El modelo SEIR que se utilizó en esta experiencia, reveló el comportamiento espontáneo de la enfermedad si no se tomara ninguna medida, o al tomarla de forma tardía a los siete días de comenzar el brote epidémico. También revela cuantos pacientes secundarios genera cada paciente primario. Esta información obtenida con el modelo de simulación matemática es útil para aquellos encargados de la toma de decisiones o de convencer a autoridades competentes para tomar medidas. Este análisis se basa en los antecedentes de la enfermedad, lo cual se puede vincular a los modelos matemáticos. El número reproductivo básico (Ro) es un indicador de la marcha de las epidemias, una vez que Ro=1, cesó el brote epidémico. Se hace entonces posible diseñar las estrategias adecuadas para impedir la dispersión de enfermedades, para evaluar la estrategia de vacunación más adecuada y sus costos con una base científica. 6 En China este modelo permitió estudiar una pandemia. 7
Otros equipos de trabajo comprobaron que el control efectivo se logra en los estadios primarios de la epidemia 8 y se demostró que la vacunación es más efectiva si se realiza de forma precoz. 9
Los servicios epidemiológicos cubanos forman una red nacional intersectorial, donde están previstas las medidas de contención para cada situación. En esta escuela se implementó un detallado programa de educación para la salud, sobre el frecuente lavado de manos, tomas de temperaturas, observación y separación de pacientes febriles o con trastornos respiratorios, lo que impidió la entrada y dispersión de esta epidemia.
El gran desarrollo adquirido por diferentes ciencias, como la epidemiología, las matemáticas, la estadística, la informática, propicia que actualmente existan nuevas técnicas en procedimientos emergentes y recurrentes, en el campo de la bioestadística y bioinformática (estadística espacial, redes neuronales y análisis de datos funcionales, etc), para describir la importancia de los modelos matemáticos en las enfermedades infecciosas. Estos nuevos avances tecnológicos en biomedicina hacen que la creación de equipos multidisciplinarios sea de vital importancia. 10, 11
Los modelos matemáticos aclaran las ideas que asumieron durante el estudio, aportan indicadores umbrales, el número reproductivo básico, cantidad de contactos. 12
Estos modelos y las simulaciones constituyen una adecuada herramienta para construir y probar teorías, responder determinadas preguntas y estimar parámetros claves de la información disponible.
Diversos ejemplos y aplicaciones de este modelo SEIR están disponibles en el software libre R y en otros programas. 12-15
Sobre la utilización del indicador Ro para medir la marcha e intensidad de una epidemia existe abundante bibliografía. 16, 17
CONCLUSIONES
Existe de forma libre y gratuita un conjunto de herramientas de cálculos y simulaciones que se pueden utilizar en la provincia por parte de los epidemiólogos y los profesores de esta rama de la Salud Pública.
REFERENCIAS BIBLIOGRÁFICAS
1. Betancourt BJ, Ortiz HE, González MA, Brito SH. Enfoque de los sistemas complejos en la Epidemiología. Arch. Med. Camagüey [serie en internet]. 2009 Ago [citado 2010 Mayo 19];13(4):[aprox. 3 p.] Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&
2. Torvaldsen S, McIntyre P. Do pertussis notifications reflect incidence or surveillance practices? A comparison of infant notification rates and hospitalization data in NSW. NSW Public Health Bull. 2003;14(4):81-84.
3. R Development Core Team R: A language and environment for statistical computing. R Foundation for Statistical Computing [actualizado 16 May 2009; citado 16 Jun 2009]. Disponible en: http://www.R-project.org.
4. Anderson RM, May RM. Infectious Disease of Humans: Dynamics and Control. Oxford: Oxford University Press; 2008.
5. Woodrow RS. Odesolve: Solvers for Ordinary Differential Equations. R package version 0.5-20. [citado 2010 May 12]. Disponible en: http://www.R-project.org.
6. Merl D, Johnson LR, Gramacy RB, Mangel Duke MS. A statistical framework for the adaptive management of epidemiological interventions. [actualizado 2010 April 16; citado 2010 May 12]. Disponible en: http://ftp.stat.duke.edu/WorkingPapers/08-29.html.
7. Jinfeng W, Anthony J, McMichael L, Bin M, Niels B, Weiguo H, et al. Spatial dynamics of an epidemic of severe acute respiratory syndrome in an urban area. Bull of the WHO. 2006;84:965-968.
8. Heiden M, Buchholz U, Krause G, Kirchner G, Claus H, Walter H. Breaking the Waves: Modelling the Potential Impact of Public Health Measures to Defer the Epidemic Peak of Novel Influenza A/H1N1. Haas PLoS. 2009;4(12):1-10.
9. Orejón G. La vacunación frente a la gripe pandémica (H1N1) es más efectiva si se realiza precozmente. Rev Pediatr. 2009;5:79-82.
10. Casals M, Guzmán K, Caylá JA. Modelos matemáticos utilizados en el estudio de las enfermedades transmisibles. Rev Esp Salud Pública. 2009;83:689-92.
11. Haghdoost Ali A, Mohammad Mehdi G,Mohammad Reza B. Modelling of H1N1 Flu in Iran. Arch Iran Med. 2009;12(6):533 -541.
12. Hethcote Herbert W. The Mathematics of Infectious Diseases. Soc for Ind Applied Mathematics. 2000;42(4):599-653.
13. Hohle M, Feldmann U. An R package for working with stochastic epidemic models. Computational Statistics and Data Analysis. 2007;52(2):680-686.
14. Hohle M. Spatio-temporal epidemic modelling using additive-multiplicative intensity models. Ludwig-Maximilians-Universitat: Department of Statistics. 2008 Disponible en: http://epub.ub.uni-muenchen.de/6366/.
15. Roberts MG, Heesterbeek JA. Model-consistent estimation of the basic reproduction number from the incidence of an emerging infection. J Math Biol. 2007;55:803-16.
16. Boelle PY, Bernillon P, Desenclos JC. A preliminary estimation of the reproduction ratio for new influenza A(H1N1) from the outbreak in Mexico, 2009. Euro Surveill. 2009;14:1-10.
Recibido: 21 de Julio de 2010
Aprobado: 19 de octubre de 2010
Dr. José A Betancourt Betancourt. Email:josebetancourt.cmw@infomed.sld.cu