My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Archivo Médico de Camagüey
On-line version ISSN 1025-0255
AMC vol.20 no.1 Camagüey Jan.-Feb. 2016
ARTÍCULOS DE REVISIÓN
Estreptoquinasa a casi 30 años de demostrada su eficacia en el infarto agudo de miocardio
Streptokinase almost 30 years after its demonstrated efficacy in acute myocardial infarction
Dr. Roberto Casola Crespo I; Dr. Eugenio Casola Crespo I; Dr. Gregorio Castillo Sánchez II; Dr. Eugenio Casola Barreto I
I Hospital Universitario Manuel Ascunce Domenech. Universidad de Ciencias Médicas de Camagüey. Camagüey, Cuba.
II Hospital IESS. Latacunga, Ecuador.
RESUMEN
Fundamento: a partir del estudio del Grupo Italiano per lo Studio del la Strepto-chinasi nell’Infarto Miocardico en el año 1986, el enfoque del tratamiento del infarto agudo de miocardio cambió. No obstante, actualmente existe controversia acerca de la opción de tratamiento.
Objetivo: comparar las ventajas y desventajas de los diferentes trombolíticos en el tratamiento del infarto agudo de miocardio, así como el uso de estos versus tratamiento de intervención coronaria percutánea.
Métodos: se realizó una revisión bibliográfica de un total de 310 artículos publicados en Pubmed, Hinari y Medline mediante el localizador de información Endnote. De ellos se utilizaron 34 citas seleccionadas para realizar la revisión, 17 de ellas de los últimos cinco años.
Desarrollo: existen dos estrategias de reperfusión en el tratamiento del infarto agudo de miocardio: la farmacológica y la intervencionista. Entre los fibrinolíticos (fármacos) se encuentran los que tienen acción lítica generalizada como la estreptoquinasa y la uroquinasa y otro grupo con lisis localizada como la anistreplasa, alteplasa, tenecteplasa y reteplasa. Los del primer grupo con respecto a los del segundo tienen como desventaja el riesgo de sangramiento y la acción antigénica de la estreptoquinasa que no tienen el resto de los fibrinolíticos. En las primeras dos horas no existe diferencia significativa en la reducción de la mortalidad con una u otra estrategia; después de este tiempo mejora con el intervencionismo.
Conclusiones: la intervención coronaria percutánea es la forma óptima de reperfusión en los pacientes con infarto agudo de miocardio, pero a la vez no es una práctica habitual aun en los países desarrollados. La reperfusión con trombolíticos sigue siendo la primera alternativa de los hospitales de segundo nivel y la estreptoquinasa es una opción segura en el tratamiento.
DeCS: ESTREPTOQUINASA/uso terapéutico; RESULTADO DEL TRATAMIENTO; INFARTO DEL MIOCARDIO; INTERVENCIÓN CORONARIA PERCUTÁNEA; LITERATURA DE REVISIÓN COMO ASUNTO.
ABSTRACT
Background: from the study of the Italian Group per lo Studio del la Strepto-chinasi nell’Infarto Miocardico, in 1986 the approach of the treatment of acute myocardial infarction changed; however, there is currently controversy about the choice of treatment.
Objective: to compare the advantages and disadvantages of the different thrombolytic in the treatment of acute myocardial infarction and their use versus percutaneous coronary intervention.
Methods: a review of 310 articles published in PubMed, Hinari and Medline was made using the reference management software Endnote. Thirty-four citations were selected to make the review, 17 of them from the last five years.
Development: there are two reperfusion strategies in the treatment of acute myocardial infarction: the pharmacologic and the interventional. Among the fibrinolytic (drugs) are those with lytic action, as streptokinase and urokinase, and other group with localized lysis as anistreplase, alteplase, tenecteplase and reteplase. The first ones, with respect to the second group, have the disadvantage of the risk of bleeding and the antigenic activity of streptokinase, not presented by the rest of fibrinolytic drugs. In the first two hours there is no significant difference regarding the mortality reduction with both strategies; after this time, it improves with the intervention.
Conclusions: percutaneous coronary intervention is the ideal form of reperfusion in patients with acute myocardial infarction but, at the same time, it is not yet a common practice in developed countries. Reperfusion with thrombolytic remains the first alternative in second-level hospitals and streptokinase is a safe treatment option. Thus, it is demonstrated that the GISSI study is updated.
DeCS: STREPTOKINASE/therapeutic use; TREATMENT OUTCOME; MYOCARDIAL INFARCTION; PERCUTANEOUS CORONARY INTERVENTION; REVIEW LITERATURE AS TOPIC.
INTRODUCCIÓN
Hasta la década de los 80, los tratamientos empleados en el manejo de las enfermedades cardiovasculares carecían de una evaluación adecuada de su eficacia y seguridad. Drogas como la digital o la nifedipino, se administraban sin saber si reducían o aumentaban la mortalidad. 1 Esto sucedía porque hasta ese momento los estudios clínicos evaluaban el efecto de los fármacos sobre variables intermedias como presión arterial, arritmias, presión capilar pulmonar, gasto cardíaco, curva enzimática y otras variables, pero no estaban diseñados para determinar su impacto en la mortalidad. 2, 3 Esta situación cambió cuando el Instituto Mario Negri de Milán, con el estudio del Grupo Italiano Per lo Studio del la Strepto-chinasi nell’Infarto Miocardico (GISSI) 2 y la Universidad de Oxford, con el Second International Study of Infarct Survival (ISIS-2), 3 implementaron la investigación clínica de poblaciones. El ejemplo que permite ilustrar esto a cabalidad es el tratamiento fibrinololítico del infarto agudo de miocardio (IAM).
Entre 1959 y 1985 se habían realizado 33 ensayos clínicos 1 para evaluar la eficacia del tratamiento fibrinololítico, 19 de ellos demostraron que este fármaco reducía la mortalidad, pero 14 indicaron lo contrario, por lo que en la práctica médica no se sabía qué conducta adoptar. No es hasta 1986, en el estudio GISSI, 2 que se demuestra que laestreptoquinasa reducía la mortalidad. Dos años más tarde de divulgado el estudio, se publica el ISIS-2, 3 que arroja resultados similares.
Se realizó una revisión de la literatura que permitió comparar las ventajas y desventajas de los diferentes trombolíticos en el tratamiento del IAM, así como el uso de estos versus tratamiento de intervención coronaria percutánea y demostrar la vigencia actual o no de la estreptoquinasa.
MÉTODOS
Se realizó una revisión bibliográfica de un total de 310 artículos publicados en Pubmed (102), Hinari (114) y Medline (94) mediante el localizador de información Endnote, de ellos se utilizaron 34 citas seleccionadas para realizar la revisión, se abordaron, artículos originales, de revisión, ensayos clínicos y estudios de enfoques epidemiológicos; 17 de ellas de los últimos cinco años.
DESARROLLO
Los fármacos fibrinolíticos según Weitz JI, 4 actualmente son:
1. La estreptoquinasa (SK)
2. Anistreplasa (APSAC). Complejo estreptoquinasa-plasminógeno acilado activador
3. La urocinasa
4. El activador del plasminógeno de tipo tisular recombinante (tPA; también conocido como alteplasa o activasa)
Dos derivados recombinantes del tPA:
1. Tenecteplasa (TNK-tPA)
2. Reteplasa (r-PA)
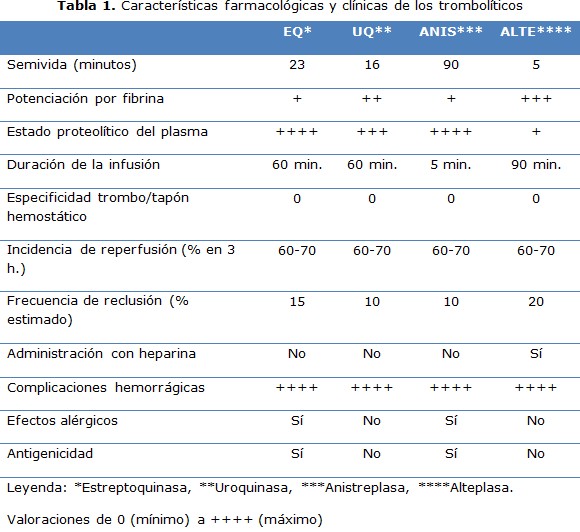
Todos estos fármacos convierten la proenzima, el plasminógeno, en plasmina, la enzima activa. Existen dos depósitos de plasminógeno: el plasminógeno circulante y el plasminógeno ligado a la fibrina. Los activadores del plasminógeno que activan preferentemente el plasminógeno ligado a la fibrina son específicos de la fibrina. Por el contrario, los activadores del plasminógeno inespecíficos no discriminan entre el plasminógeno ligado a la fibrina y el circulante. La activación del plasminógeno circulante da lugar a la producción de plasmina sin resistencia, que puede provocar un estado lítico sistémico. La alteplasa y sus derivados son activadores del plasminógeno y específicos de la fibrina, mientras que la estreptocinasa, la anistreplasa y la urocinasa son fármacos inespecíficos.
Existen consideraciones por Weitz JI, 4 sobre las diferentes características farmacológicas y clínicas que se deben conocer sobre estos fármacos (tabla 1 y 2).
La trombosis de las arterias o las venas refleja una interrelación compleja entre la pared de los vasos, las plaquetas, el sistema de la coagulación y las rutas fibrinolíticos. La activación de la coagulación también desencadena rutas inflamatorias que pueden contribuir a la trombogenia. El aumento de los conocimientos sobre la bioquímica de la agregación plaquetaria y la coagulación sanguínea y los avances en cuanto al diseño de fármacos basados en la estructura, han dado lugar al desarrollo de fármacos antitrombótico nuevos. Sin embargo, a pesar de estos avances, los trastornos tromboembólicos arteriales y venosos han sido una causa principal de morbilidad y mortalidad, lo que exige una continuidad investigativa para obtener fármacos antiagregantes, anticoagulantes y fibrinolíticos con mejores objetivos, más potentes y más seguros.
Principios para su uso
El IAM es secundario, por lo general, a la oclusión completa de una arteria coronaria específica, debido a la rotura con trombosis de una placa de ateroma que implica la necrosis o muerte celular en un período que oscila entre cuatro y 12 horas, según factores como: grado de circulación colateral, obstrucciones intermitentes del vaso y consumo de oxígeno. Es un proceso dinámico, que no se produce de forma instantánea, sino que evoluciona a lo largo de horas. El destino del tejido isquémico puede ser modificado favorablemente con la repermeabilización del vaso, lo que reduce el tamaño del infarto.
Las estrategias de reperfusión se han desarrollado para aumentar al máximo la cantidad de miocardio salvado, mediante la aceleración del proceso de reperfusión. La reducción de la mortalidad en el IAM será mayor cuando se logre reperfundir la arteria responsable del infarto con prontitud. 5 Por lo que en la actualidad casi todos los pacientes reciben terapia de reperfusión (trombolisis o intervención coronaria percutánea). 6
Una arteria relacionada con el infarto y permeable, implica muchos beneficios entre los que se encuentran:
1. Mejoría de la supervivencia y de la función ventricular.
2. Modificación favorable del proceso de remodelado ventricular.
3. Mejoría de la inestabilidad eléctrica residual.
4. Mayor apertura de redes de circulación colateral.
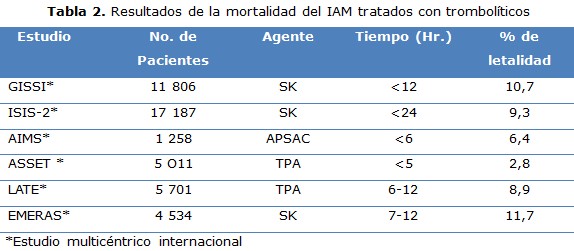
La fibrinólisis es una estrategia bien establecida de reperfusión en los pacientes con IAM; 7 se previenen aproximadamente 30 muertes prematuras por cada 1000 pacientes tratados en las primeras 6 horas desde el inicio de los síntomas (tabla 3).
El mayor beneficio se observa en los pacientes de mayor riesgo de muerte y en los ancianos. 8 El beneficio es máximo cuando los fármacos se administran de la manera más precoz posible y los mejores resultados se obtienen al administrarlos en las primeras dos horas desde el inicio de los síntomas. 9
La influencia del factor tiempo es determinante; el grupo italiano para el estudio de la estreptoquinasa en el infarto miocárdico (GISSI), 2 informó la reducción de la letalidad del 47 % cuando fue utilizado en la primera hora y el estudio Global Utilization of Streptokinasa nd Tissue (GUSTO), 10 estimó que por cada hora de retraso en el inicio del tratamiento se dejan de salvar 10 vidas entre 1 000 pacientes tratados.
Los ensayos LATE 11 y EMERAS, 12 considerados en conjunto, han aportado evidencias de que es posible encontrar una reducción de la mortalidad en los pacientes que reciben fármacos trombolíticos entre seis y 12 horas después del inicio de los síntomas isquémicos. Estos datos de los ensayos son la base para ampliar la ventana de tratamiento con fibrinolíticos hasta 12 horas desde el inicio de los síntomas.
A la llegada del paciente al sistema de urgencia
Al llegar los pacientes al servicio de urgencias hay que identificar con rapidez aquellos que necesitan un tratamiento de reperfusión urgente. Los antecedentes de dolor tipo isquémico coronario y el ECG de 12 derivaciones constituyen las herramientas principales para el diagnóstico y manejo inicial de los pacientes con IAM. 13
Existen dos estrategias de reperfusión:
1. La farmacológica (fibrinólisis)
2. Intervención coronaria percutánea (ICP)
La selección de un método depende de:
1. Tiempo desde el inicio de los síntomas al comienzo del tratamiento con reperfusión.
2. Riesgo de muerte tras un IAM.
3. Riesgo de hemorragia por fibrinólisis.
4. Tiempo necesario para el traslado a un centro con experiencia en ICP.
Actualmente existe controversia en la opción de tratamiento, sobre todo si no existe posibilidad de ICP primaria o retraso en la realización de la misma en el centro de admisión. 14 Los nuevos fármacos fibrinolíticos asociados a recientes opciones antiagregantes y anticoagulantes, han mejorado los resultados en recuperar y mantener el flujo en la arteria coronaria responsable del infarto.
Si el tiempo transcurrido entre el inicio de los síntomas y la selección de una estrategia es menor de 120 minutos, no existe preferencia por uno u otro método de tratamiento, 15 por lo que al evaluar a un paciente laselección de la forma óptima de reperfusión implica juzgar los recursos del sistema 16 y sus características individuales.
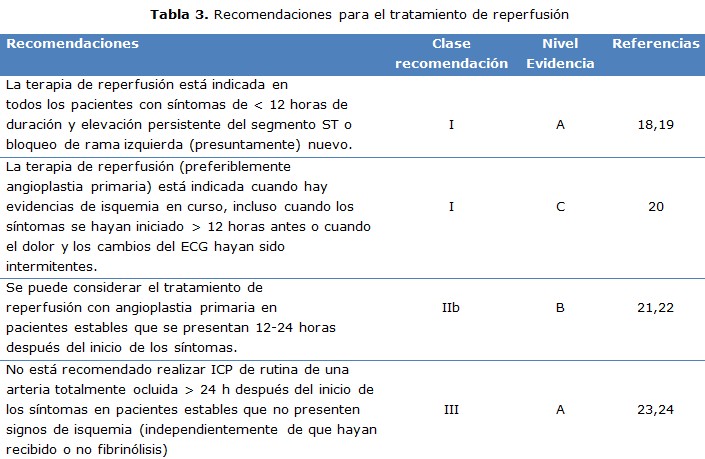
Recomendaciones para el tratamiento de reperfusión (tabla 4). 17-19
Está establecido que el beneficio del uso de los trombolíticos es máximo cuando los fármacos se administran de la manera más precoz posible y los mejores resultados se obtienen al administrarlo en las primeras dos horas desde el inicio de los síntomas. 9
Al comparar la reperfusión farmacológica y la ICP, si el tiempo transcurrido entre el inicio de los síntomas y la selección de una estrategia es menor de 120 minutos, no existe preferencia por uno u otro método de tratamiento. 15, 20-24 No obstante, no se ha investigado de forma prospectiva si la fibrinólisis pre-hospitalaria se asocia a resultados clínicos similares o mejores que la angioplastia primaria, en pacientes que se presentan de forma precoz. En el estudio STREAM, Armstrong PW, et al, 25 concluye que la fibrinólisis pre-hospitalaria resulta en una reperfusión efectiva en pacientes con IMA, con elevación del ST en fase temprana, en los que no se puede realizar un ICP primario en la primera hora tras el primer contacto médico. Sin embargo, la fibrinólisis se asoció con un riesgo ligeramente incrementado de sangrado intracraneal.
Indicaciones de los trombolíticos
La trombolisis está indicada 17, 26, 27 en todo paciente con:
1. Presentación clínica sugestiva de IAM y llegada al centro hospitalario dentro de las primeras 12 horas desde el inicio de los síntomas sin contraindicaciones para su uso.
Acompañado de una de estas dos condiciones en el ECG:
- Elevación persistente del ST de 1 mm o superior en al menos dos derivaciones contiguas.
- Bloqueo de rama izquierda nuevo o que se considere de reciente aparición.
Contraindicaciones de los trombolíticos
Absolutas
1- Hemorragia intracraneal previa o accidente cerebrovascular de origen desconocido en cualquier momento
2- Accidente cerebrovascular isquémico en los seis meses precedentes
3- Daño en el sistema nervioso central o neoplasias o malformación auriculoventricular
4- Trauma/cirugía/lesión craneal importante recientes (en las tres semanas precedentes)
5- Hemorragia gastrointestinal en el último mes
6- Trastorno hemorrágico conocido (excluida la menstruación)
7- Disección aórtica
8- Punciones no compresibles en las últimas 24 horas (biopsia hepática, punción lumbar)
Relativas
1- Accidente isquémico transitorio en los 6 meses precedentes
2- Tratamiento anticoagulante oral
3- Gestación o primera semana posparto
4- Hipertensión refractaria (presión arterial sistólica > 180 mmHg o presión arterial diastólica > 110 mmHg)
5- Enfermedad hepática avanzada
6- Endocarditis infecciosa
7- Úlcera péptica activa
8- Reanimación prolongada o traumática
La elección del agente trombolítico
Esta decisión, además de tener en cuenta la relación costo-beneficio y disponibilidad de varios agentes trombolíticos, exige analizar:
1. La utilidad de una lisis rápida
2. El tiempo transcurrido desde el inicio de los síntomas
3. La posibilidad de comienzo del tratamiento
4. El perfil de bajo o alto riesgo del paciente
5. La posibilidad elevada o reducida de hemorragia intracraneal
Se necesita conocer las características y resultados de los estudios de los fármacos trombolíticos que permitan obtener recomendaciones terapéuticas, pues los médicos deben sopesar el riesgo de mortalidad y hemorragia intracraneal a la hora de enfrentarse a un paciente con IAM susceptible de recibir fibrinólisis.
Al tener en cuenta el análisis anterior, debe considerarse la preferencia de un fármaco según la situación clínica y la decisión final tomada por el médico responsable.
Algunas recomendaciones:
- En el subgrupo de pacientes que acuden durante las primeras cuatro horas desde el inicio de los síntomas, la velocidad de reperfusión del vaso responsable del infarto tiene una importancia clave y se prefiere un régimen fibrinolítico de alta intensidad, como el tPA acelerado, salvo en los casos con bajo riesgo de muerte (un paciente joven con un IAM inferior pequeño) y con mayor riesgo de hemorragia intracraneal (hipertensión aguda), en los que la estreptoquinasa y el tPA acelerado se consideran elecciones equivalentes.
- En los pacientes que consultan entre cuatro y 12 h después de la aparición del dolor torácico, la velocidad de reperfusión del vaso responsable del infarto tiene menos importancia y se suele considerar que la estreptoquinasa y el tPA acelerados son opciones equivalentes.
- Es importante recordar que la estreptoquinasa es preferible a la tPA en los pacientes que consultan entre cuatro y 12 h después del inicio de los síntomas, con bajo riesgo de mortalidad pero aumento del riesgo de hemorragia intracraneal (ancianos con un IAM inferior, presión sistólica > 100 mmHg y frecuencia cardíaca > 100 latidos/min).
- En los pacientes candidatos a la fibrinólisis con el tPA de elección, se recomienda una embolada de fibrinolíticos, como reteplasa o tenecteplasa; ya que la fibrinólisis en embolada se administra con mayor facilidad y reduce el riesgo de errores de medicación, menos hemorragias no cerebrales y permite un tratamiento pre-hospitalario.
Dosis y administración de los fibrinolíticos
Criterios de reperfusión pos-trombolisis
Debido a la imposibilidad de verificar de manera angiográfica la lisis del trombo cuando se utiliza la vía intravenosa, Elliott M, et al, 27 recomienda basarse en cambios clínicos, electrocardiográficos y enzimáticos para reconocer el hecho y el momento de la repercusión coronaria.
- Desaparición del dolor: Se ha demostrado mediante la angiografía que la reapertura de una arteria coronaria ocluida es seguida en segundos o minutos por la desaparición del dolor. El alivio es aceptado por los pacientes, aunque antes hayan recibido dosis de analgésicos de uso común en el infarto miocárdico.
Con frecuencia antes de la reperfusión se produce intensificación, fluctuación o intermitencia del dolor como reflejo de la progresiva lisis del trombo.
- Regresión de los cambios isquémicos electrocardiográficos (ST-t): La reapertura de la arteria relacionada con el infarto se sigue en segundos por la mejoría de las alteraciones del segmento ST y la onda T. El primer cambio es disminución de la amplitud de la onda T, seguida por regresión del segmento ST en más de un 50 % a la línea isoeléctrica, aunque este último regreso no es frecuente en las primeras horas.
Dado el poder como marcador, objetivo de la reperfusión de estos cambios, se recomienda mantener monitorizada una derivación en forma continua que presente supradesnivel del segmento ST.
Se debe realizar un electrocardiograma completo antes del tratamiento y de 30 a 60 min después de terminada la infusión del agente trombolítico.
- Arritmias por reperfusión: Tras el éxito de la reperfusión es frecuente encontrar también extrasístoles ventriculares, un ritmo idioventricular acelerado y taquicardia ventricular no mantenida. Aunque Elliott M, et al, 27 plantea que las posdespolarizaciones precoces (CVP) están implicadas en la génesis de las arritmias ventriculares por reperfusión, estas posdespolarizaciones precoces existen durante la isquemia y la reperfusión, por lo cual se considera poco probable que estén implicadas en la aparición de la taquicardia o la fibrilación ventricular por reperfusión.
Cuando aparecen estas alteraciones del ritmo pueden indicar, en realidad, que se ha recuperado con éxito el flujo coronario. Un elemento a tener en cuenta, es la desaparición de los trastornos de la conducción auriculoventricular que estaban presentes antes de la reperfusión.
En muchos pacientes con infartos inferiores se produce una bradicardia sinusal transitoria en el momento de la reperfusión aguda; este fenómeno se suele asociar a cierto grado de hipotensión. Esta combinación de hipotensión y bradicardia, con un aumento súbito del flujo coronario puede relacionarse con la activación del reflejo de Bezold-Jarisch, citado por Kawasaki T, et al. 28
La resolución electrocardiográfica del segmento ST predice el pronóstico en pacientes con un IAM, así mismo, la oclusión o permeabilidad de la arteria responsable del infarto. 29
Las características clínicas son malos marcadores de la reperfusión y ningún hallazgo clínico, o constelación de ellos, permite predecir de forma fiable la permeabilidad de la arteria coronaria demostrada en angiografía.
Los biomarcadores cardíacos aparecen más tempranamente y su pico también aparece con más rapidez con la reperfusión: La actividad de la enzima creatinfosfoquinasa (CPK) y en específico su izoenzima (MB) sérica, supera el rango normal de cuatro a ocho horas desde el inicio del IAM y recupera la normalidad de dos a tres días. Aunque el pico máximo de CPK aparece a una media de 24 h, puede adelantarse en los pacientes tratados con reperfusión como consecuencia de la administración de tratamiento fibrinolítico o de recanalización mecánica.
Con la recanalización satisfactoria de la arteria relacionada con el infarto se liberan rápidamente troponinas cardíacas que pueden servir como indicador de reperfusión, aunque la mioglobina es ligeramente más eficiente para este propósito. 30
La resolución del segmento ST en más de un 50 %, desaparición o alivio del dolor combinada con los biomarcadores cardíacos, aportan una potente información pronóstica en las fases precoces del tratamiento de reperfusión en los pacientes con un IAM.
Fallo de reperfusión postrombolisis
Si a los 60 minutos después de terminada la trombolisis:
1. El dolor no desaparece, puede decirse que no se ha producido reperfusión.
2. El complejo ST-T permanece sin cambios o regresa menos de un 50 %.
Subgrupos especiales de pacientes
- Mujeres: En las mujeres el IAM tiene una mayor ocurrencia a edades más tardías 31, 32 y continúa como la principal causa de muerte, por lo tanto, es importante mantener la vigilancia en ellas con un control más estricto. Las mujeres suelen tener menor peso corporal que los de su sexo opuesto y son más susceptibles a hemorragia, por lo que los tratamientos antitrombóticos y la dosis de éstos, deben utilizarse con especial atención al riesgo hemorrágico.
- Disfunción renal: Se asocia a un peor pronóstico y aumento del riesgo de hemorragia. 33 Las decisiones sobre la reperfusión en estos pacientes se deben tomar con gran cuidado debido a este riesgo y posterior a la trombolisis, el tratamiento antitrombótico que se recomienda es el ticagrelor para evitar sangramiento, basados en el estudio PLATO. 34
- Diabéticos: Los pacientes diabéticos tienen un riesgo más elevado de muerte y complicaciones, pero la selección del tratamiento antitrombótico y de reperfusión es la misma para los no diabéticos.
Variantes de aplicación del tratamiento trombolítico
- Trombólisis de rescate: Se aconseja la posibilidad de repetir el tratamiento trombolítico en aquellos pacientes en que persisten signos y síntomas de isquemia aguda o fallo de trombolisis y que en los que no exista la posibilidad de ICP. Si se realizó con estreptoquinasa o APSAC, debe realizarse con otro agente trombolítico por las reacciones alérgicas y titulación de anticuerpos que neutralizan próximas dosis.
- Trombólisis tardía: La realizada entre las seis y 24 horas del inicio de los síntomas. El estudio LATE 11 demostró lo beneficioso de esta terapéutica al comparar el tPA con placebo, por lo que se obtiene una reducción significativa de la mortalidad de 8, 9 vs 12 % y el estudio EMERAS, 12 que utilizó estreptoquinasa vs placebo, logró una reducción de 13, 2 a 11, 7%. Los datos indican que la trombolisis tardía es beneficiosa, debido a que reduce la mortalidad entre 10 y 20 %. Los mecanismos para este beneficio se especulan y se dan como fundamentales: una mejoría del proceso de remodelamiento posinfarto, menos inestabilidad eléctrica residual y mejoría de la circulación colateral; situaciones tardías que favorecen el pronóstico al contarse con la arteria relacionada con el infarto permeable.
CONCLUSIONES
La selección de la forma óptima de reperfusión implica juzgar los recursos del sistema (centro con recursos y experiencia en intervención coronaria percutánea), los cuales se encuentran al alcance de muy pocos hospitales con atención a pacientes con síndrome coronario agudo. Por lo que la reperfusión con trombolíticos continúa como la primera alternativa de los hospitales de segundo nivel y la estreptoquinasa a pesar de sus casi 30 años de existencia y comprobada su eficacia en el tratamiento del infarto agudo de miocardio, es aún el activador del plasminógeno más fácil de producir, por tanto el más económico y a la vez una opción segura en el tratamiento.
REFERENCIAS BIBLIOGRÁFICAS
1. Sandoya E. Ensayos clínicos que cambiaron la práctica de la cardiología: fortalezas y debilidades. Rev Urug Cardiol [Internet]. Jun 2007 [citado 15 May 2013];22(1):[aprox. 5 p.]. Disponible en: http://www.scielo.edu.uy/scielo.php?pid=S1688-04202007000100006&script=sci_arttext
2. Grupo Italiano per lo Studio de la Strepto-chinasinellInfartoMiocardico (GISSI). Effectiveness of intravenous thrombolytic treatment in acute myocardial infarction. Lancet. 1986 Feb 22;1(8478):397-402.
3. ISIS-2 (Second International Study of Infarct Survival) Collaborative Group. Randomised trial of intravenous streptokinase, oral aspirin, both, or neither among 17,187 cases of suspected acute myocardial infarction: ISIS-2. Lancet. 1988 Aug 13;2(8607):349-60.
4. Weitz JI. Hemostasia, trombosis, fibrinólisis y enfermedad cardiovascular. En: Bonow OR, Mann DL, Libby P, editores. Branwuald tratado de cardiología. 9na ed. Barcelona: Elsevier; 2013. p. 1188-1891.
5. Bertomeu V, Cequier A, Bernal JL, Alfonso F, Anguita MP, Muñiz J, et al. Mortalidad intrahospitalaria por infarto agudo de miocardio. Relevancia del tipo de hospital y la atención dispensada. Estudio RECALCAR. Rev Esp Cardiol [Internet]. Dic 2013 [citado 15 May 2013];66(12):[aprox. 7 p.]. Disponible en: http://www.revespcardiol.org/es/mortalidad-intrahospitalaria-por-infarto-agudo/articulo/90255801/.
6. Zaman MJ, Stirling S, Shepstone L, Ryding A, Flather M, Bachmann M, et al. The association between older age and receipt of care and outcomes in patients with acute coronary síndromes: a cohort of the Myocardial Ischaemia National Audit Project (MINAP). Eur Heart J. 2014;35:1551–8.
7. Fibrinolytic Therapy Trialists (FTT) Collaborative Group. Indications for fibrinolytic therapy in suspected acute myocardial infarction: collaborative overview of early mortality and major morbidity results from all randomised trials of more than 1000 patients. Lancet. 1994 Feb;5(8893):311-22.
8. González Ferreiro R, Raposeiras Roubín S, Abu Assi E, Castiñeiras Busto M, García Acuña JM, González Juanatey JR. Tratamiento no invasivo del infarto agudo de miocardio. Per?l clínico de los pacientes y variables predictoras de mal pronóstico. Rev Esp Cardiol [Internet]. Abr 2015 [citado 2 Jun 2015];68(4):[aprox. 5 p.]. Disponible en: http://www.revespcardiol.org/es/tratamiento-no-invasivo-del-infarto/articulo/90398536/.
9. White HD, Chew DP. Acute myocardial infarction. Lancet. 2008 Aug 16;372(9638):570-84.
10. Kline EM, Smith DD, Martin JS. In-hospital treatment delays in patients treated with thrombolytic therapy: a report of the GUSTO yime to treatment substudy. Circulation. 1990;86(Suppl 1):702.
11. LATE Study Group. Late assessment of thrombolytic efficacy (LATE) Study with alteplase 6-24 hours after onset of acute myocardial infarction. Lancet. 1993 Sep 25;342(8874):759-66.
12. EMERAS Collaborative Group. Randomised trial of late thrombolysis in patients with suspected acute myocardial infarction. Lancet. 1993 Sep 25;342(8874):767-72.
13. Atzema CL, Austin PC, Tu JV, Schull MJ. Emergency department triage of acute myocardial infarction patients and the effect on outcomes. Ann Emerg Med. 2009 Jun;53(6): 736-45.
14. Bradley EH, Herrin J, Wang Y, Barton BA, Webster TR, Mattera JA, et al. Strategies for reducing the door-to-balloon time in acute myocardial infarction. N Engl J Med. 2006 Nov 30;355(22):2308-20.
15. Pinto DS, Kirtane AJ, Nallamothu BK, Murphy SA, Cohen DJ, Laham RJ, et al. Hospital delays in reperfusion for ST-elevation myocardial infarction: implications when selecting a reperfusion strategy. Circulation. 2006 Nov 7;114(19):2019-25.
16. Washington AE, Lipstein SH. The Patient-Centered Outcomes Research Institutepromoting better information, decisions, and health. N Engl J Med. 2011;365: e31.
17. Steg G, James SK, Atar D, Badano LP, BlomstromLundqvist C, Borger MA, et al. Guía de práctica clínica de la ESC para el manejo del infarto agudo de miocardio en pacientes con elevación del segmento ST. Rev Esp Cardiol [Internet]. Ene 2013 [citado 20 Ene 2014];66(1):[aprox. 5 p.] Disponible en: http://www.revespcardiol.org/es/guia-practica-clinica-esc-el/articulo/90180910/.
18. Boersma E, Maas AC, Deckers JW, Simoons ML. Early thrombolytic treatment in acute myocardial infarction: reappraisal of the golden hour. Lancet. 1996 Sep 21;348(9030):771-5.
19. NHS Foundation Trust. Harefield Hospital After your primary angioplasty [Internet]. London: Royal Brompton Hospital; 2012 [citado 2014 Ene 20]. Available from: http://www.rbht.nhs.uk/pati ents/condition/primary-angioplasty/.
20. Gierlotka M, Gasior M, Wilczek K, Hawranek M, Szkodzinski J, Paczek P, et al. Reperfusion by primary percutaneous coronary intervention in patients with ST-segment elevation myocardial infarction within 12 to 24 hours of the onset of symptoms (from a prospective national observational study [PL-ACS]). Am J Cardiol. 2011 Feb 15;107(4):501-8.
21. Schomig A, Mehilli J, Antoniucci D, Ndrepepa G, Markwardt C, Di Pede F, et al. Mechanical reperfusion in patients with acute myocardial infarction presenting more than 12 hours from symptom onset: a randomized controlled trial. JAMA. 2005 Jun 15;293(23): 2865-72.
22. Ndrepepa G, Kastrati A, Mehilli J, Antoniucci D, Schomig A. Mechanical reperfusion and long-term mortality in patients with acute myocardial infarction presenting 12 to 48 hours from onset of symptoms. JAMA. 2009 Feb 4;301(5):487-8.
23. Hochman JS, Lamas GA, Buller CE, Dzavik V, Reynolds HR, Abramsky SJ, et al. Coronary intervention for persistent occlusion after myocardial infarction. N Engl J Med. 2006 Dec 7;355(23):2395-407.
24. Menon V, Pearte CA, Buller CE, Steg PG, Forman SA, White HD, et al. Lack of benefit from percutaneous intervention of persistently occluded infarct arteries after the acute phase of myocardial infarction is time independent: insights from Occluded Artery Trial. Eur Heart J [Internet]. 2009 Jan [citado 2014 Jan 20];30(2):[about 6 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2639108/.
25. Armstrong PW, Gershlick AH, Goldstein P, Wilcox R, Danays T, Lambert Y, et al. Fibrinolysis or Primary PCI in ST-Segment Elevation Myocardial Infarction. N Engl J Med. 2013;368:1379-87.
26. O'Gara PT, Kushner FG, Ascheim DD, Casey DE, Chung MK, de Lemos JA, et al. ACCF/AHA Guideline for the Management of ST-Elevation Myocardial Infarction: Executive Summary: A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2013 Jan 29;127(4): 529-55.
27. Elliott M, Antman P, Morrow DA. Infarto de miocardio con elevación del segmento ST: tratamiento. En: Bonow OR, Mann DL, Libby P, editores. Branwuald tratado de cardiología. 9na ed. Barcelona: Elsevier; 2013. p. 1132-41.
28. Kawasaki T, Akakabe Y, Yamano M, Miki S, Kamitani T, Kuribayashi T, et al. Vagal enhancement as evidence of residual ischemia after inferior myocardial infarction. Pacing Clin Electrophysiol. 2009 Jan;32(1):52-8.
29. Gersh BJ, Stone GW, White HD, Holmes DR. Pharmacological facilitation of primary percutaneous coronary intervention for acute myocardial infarction: Is the slope of the curve the shape of the future? JAMA. 2005 Feb 23;293(8):979-86.
30. Goldstein P, Lapostolle F, Steg G, Danchin N, Assez N, Montalescot G, et al. Lowering mortality in ST-elevation myocardial infarction and non-ST-elevation myocardial infarction: Key prehospital and emergency room treatment strategies. Eur J Emerg Med. 2009 Oct;16(5):244-55.
31. Kang SH, Suh JW, Yoon CH, Cho MC, Kim YJ, Chae SC, et al. Sex Differences in Management and Mortality of Patients With ST-Elevation Myocardial Infarction (from the Korean Acute Myocardial Infarction National Registry). Am J Cardiol. 2012 Mar 15;109(6):787-93.
32. Zhang Z, Fang J, Gillespie C, Wang G, Hong Y, Yoon PW. Age-Specific Gender Differences in In-Hospital Mortality by Type of Acute Myocardial Infarction. Am J Cardiol. 2012 Apr 15;109(8):1097-103.
33. Szummer K, Lundman P, Jacobson SH, Schon S, Lindback J, StenestrandU, et al. Relation between renal function, presentation, use of therapies and in-hospital complications in acute coronary syndrome: data from the SWEDEHEART register. J Intern Med. 2010 Jul;268(1):40-9.
34. Ames S, Budaj A, Aylward P, Buck KK, Cannon CP, Cornel JH, et al. Ticagrelor versus clopidogrel in acute coronary syndromes in relation to renal function: results from the Platelet Inhibition and Patient Outcomes (PLATO) trial. Circulation. 2010 Sep 14;122(11):1056-67.
Recibido: 16 de noviembre de 2015
Aprobado: 2 de diciembre de 2015
Dr. Roberto Casola Crespo. Especialista de II grado en Cardiología. Máster en Urgencias Médicas. Profesor Auxiliar. Hospital Universitario Manuel Ascunce Domenech. Universidad de Ciencias Médicas de Camagüey. Camagüey, Cuba. Email: robertocasola@yahoo.es