Introducción
El síndrome linfoproliferativo (SLP) incluye un grupo de trastornos de origen clonal, que afecta a las células linfoides, con características heterogéneas desde el punto de vista clínico, histológico y molecular. Pueden tener diferentes formas de presentación entre los cuales se describen el linfoma de Hodgkin (LH) y linfoma no Hodgkin (LNH). 1) Los LNH son neoplasias malignas de los componentes celulares del sistema inmune y sus precursores.
El término de LNH comprende un conjunto de enfermedades que comparten un origen común con el sistema linfoide, con unas características patogénicas similares y que tienen, a pesar de una historia natural diversa, similitudes en el planteamiento de su estudio clínico y en su orientación terapéutica básica, en la que juega un papel el uso de la quimioterapia. 2
El LNH constituye la novena causa de cáncer en incidencia y mortalidad en el mundo es la quinta causa de cáncer en los Estados Unidos. Su incidencia se ha incrementado en las últimas tres décadas. En el Reino Unido constituye cerca del 8 % de cáncer entre jóvenes. La incidencia en España es de 12,3 casos por cada 100 000 varones/año y 10,8 en el caso de las mujeres. Ocupa el séptimo lugar en incidencia por tipo de cáncer tanto en hombres como mujeres al permanecer estable en los últimos años. En Asia las tasas de incidencia son menores aunque el incremento es similar en India, Japón y China, al de Norteamérica y Escandinavia. 3
En Cuba, se reportan en el año más de 20 000 casos nuevos de cáncer, en el año 2018 se reportaron 24 902 muertes por tumores malignos de diferentes localizaciones y de ellos, 972 tumores del tejido linfático y de los órganos hematopoyéticos, en específicos los casos de LNH, que representaron alrededor del 2,1 %, se estima que es cinco veces más frecuente que la enfermedad de Hodgkin.
Según fuentes del registro nacional de cáncer la incidencia del linfoma se ha mantenido estable en los últimos 18 años. El promedio de casos reportados al año es de alrededor de 480, de los cuales la cuarta parte pertenece a provincia La Habana. 4
Los LNH de estirpe B, constituyen un grupo muy heterogéneo de enfermedades clínico-patológicas diferenciadas en lo esencial por su comportamiento clínico. Dentro de la amplia variedad de los linfomas, son los foliculares el subtipo histológico más representado (20-45 %). 5
Los linfomas foliculares (LF) son un subgrupo de linfomas no hodgkinianos (LNH) de origen B caracterizados por presentar un patrón de remisiones y recaídas continuas. Es segundo tipo de linfoma más frecuente, ya que representan entre el 22 y 40 % de los LNH. La incidencia anual de la enfermedad se ha incrementado en las últimas décadas; desde los dos o tres casos por cada 100 000 habitantes en 1950 a los cinco y siete casos/100 000 habitantes y prevalencia de 40/100 000.
Afectan en lo fundamental a adultos ancianos con un pico de incidencia en la quinta y sexta década de la vida. Por su clínica se comportan de forma indolente y crónica, hasta el 90 % de los pacientes se encuentran al momento del diagnóstico en un estadio avanzado de la enfermedad, estadios III/IV, con una mediana de supervivencia global (SG) prolongada (alrededor de 10 años) y una tasa de SG de cinco años sobre el 75 %. 6)
En la actualidad las estrategias de tratamiento en estos enfermos se basan en la utilización de diferentes regímenes de poliquimioterapia en función de las características y factores pronósticos al diagnóstico. (7
La mayoría de los pacientes responden a los tratamientos convencionales, si bien las respuestas completas (RC) alcanzadas se sitúan entre un 40-60 % con la circunstancia desfavorable que ninguno de ellos hasta el momento ha sido capaz de modificar el curso natural de la enfermedad, caracterizado por un patrón crónico de recaídas y por lo tanto, de escasas posibilidades de obtener curaciones. 8
Las combinaciones de quimioterapia más utilizadas son ciclofosfamida, vincristina y prednisona (CVP) y ciclofosfamida, doxorrubicina, vincristina y prednisona (CHOP) administradas en ciclos cada tres o cuatros semanas. Los datos obtenidos con estas combinaciones en la que una de ellas contiene antraciclínicos, muestran un porcentaje de RC y una duración de las mismas mayor que la observada con los alquilantes como la ciclofosfamida o el clorambucil.
Sin embargo, ninguna de ellas ha conseguido demostrar un aumento de la mediana de supervivencia de estos pacientes, por lo que en la actualidad se puede considerar al linfoma folicular como una enfermedad sin tratamientos efectivos para su curación. (6,9
La monoterapia con monofosfato de fludarabina ha demostrado mejor respuesta global que otros regímenes con corticoesteroides o agentes alquilantes. La fludarabina induce mayor cantidad de remisiones y de remisiones completas (7-40 %) que otros regímenes de quimioterapia convencionales, como: ciclofosfamida, doxorrubicina, vincristina y prednisona, ciclofosfamida, vincristina y prednisona o clorambucil. 10
Entre los tratamientos de mayor efectividad se encuentra el uso del rituximab que es un anticuerpos monoclonal quimérico dirigido al antígenos CD20, antígenos de membrana localizado en los linfocitos preB y B maduros, y en el 90 % de las células B de los linfoma no Hodgkin. 11) Debido a la poca disponibilidad del rituximab y ante la ausencia de resultados definitivos en el tratamiento del linfoma folicular se decidió realizar la investigación con el objetivo de evaluar los resultados en la provincia con el uso de la fludarabina como opción terapéutica de primera línea a considerar en el tratamiento de rescate de la enfermedad.
Métodos
Se realizó un estudio observacional analítico de cohorte, longitudinal prospectivo concurrente en pacientes con diagnóstico de linfoma no Hodgkin folicular en el Servicio de Hematología del Hospital Clínico Quirúrgico Lucia Iñiguez Landín de la provincia Holguín en el período de enero 2017 a septiembre 2018.
El universo de estudio lo conformaron los pacientes que acudieron a la consulta de Hematología con diagnóstico de linfoma no Hodgkin folicular y quedó constituido por 63 pacientes, de los cuales 21 seleccionados mediante muestreo no probabilístico intencionado que recibieron tratamiento con fludarabina, conformaron cohorte de expuestos, que se compararon con 42 pacientes con similares características que recibieron otros esquemas de poliquimioterapia que no incluyó la fludarabina y que constituyó la cohorte de no expuestos.
Etapas de la investigación:
1er Etapa:
Una vez establecido el diagnóstico histológico de la hemopatía maligna linfoma no Hodgkin folicular, se definió el estadio de la enfermedad y se escogieron para el estudio los pacientes clasificados en los estadios III y IV.
2da Etapa:
En la etapa se realizó el reclutamiento de pacientes que formaron las dos cohortes fijas o cerradas según el esquema terapéutico empleado. Los pacientes que recibieron tratamiento con fludarabina formaron la cohorte de expuestos y los pacientes tratados con esquemas como ciclofosfamida-vincristina-prednisona, ciclofosfamida-adriamicina-vincristina-prednisona o leukerán-prednisona que formaron la cohorte no expuestos. Se realizó un pareo de un expuesto por cada dos no expuestos (1x2) para evadir la intervención del azar ya que la muestra evaluada es pequeña.
Para la selección de los no expuestos se tuvieron en cuenta las siguientes condiciones:
Fueron seleccionados de la misma base poblacional de donde se reclutaron los expuestos.
Son una muestra aleatoria de individuos que pertenecen a la población fuente de los expuestos.
Solo difieren de los expuestos en el tratamiento.
3er Etapa:
Se procedió al seguimiento de ambos grupos con evaluaciones cada tres meses durante el período de la investigación, al evaluar el comportamiento de las variables tiempo de sobrevida libre de enfermedad y complicaciones asociadas.
Se utilizaron técnicas para la obtención de la información como entrevista, observación, revisión documental, así como instrumentos para la recolección de la información a través de planillas.
Como variable dependiente se estudió la efectividad de la fludarabina como opción terapéutica de primera línea; el riesgo de recaída de la enfermedad según follicular lymphoma international prognostic index (FLIPI), tiempo de sobrevida libre de enfermedad y la aparición de complicaciones del tratamiento fueron las variables independientes consideradas. Se utilizó la estadística descriptiva, en forma de frecuencia absoluta y relativa (porcentaje), se expusieron de los resultados obtenidos en tablas para una mejor comprensión de los mismos.
A través de la estadística inferencial se determinó el grado de relación entre las variables cualitativas para lo cual se empleó la prueba de independencia u homogeneidad Chi cuadrado (x2). En las variables en las que se determinó x2 menor o igual que 3,84 con p>0,05 se asumió ausencia de significación estadística, en el caso de x2 entre 3,85 a 6,63 (p<0,05) se consideró asociación significativa; mientras que si x2 resultó de 6,64 a 7,87 (p<0,01) la relación fue muy significativa por último para x2>7,88 (p<0,001) se entendió como asociación altamente significativa. 12
Se hizo además, uso de la estadística analítica con el diseño de una cohorte que aportó valor metodológico a la investigación. La utilización del gestor de datos SPSS por sus siglas en inglés Statistical Program for Social Sciences, Ed. 21 permitió la generación de tablas y de otras medidas correspondientes a la estadística descriptiva.
El estudio se realizó cumpliendo con los principios éticos para la investigación médica y fue aprobado por el Comité de Ética del servicio de Hematología del Hospital Clínico Quirúrgico Lucia Iñiguez Landín de Holguín. A los participantes se les informó los motivos del estudio, de sus deberes y derechos, se les solicitó su aprobación por escrito mediante la firma del acta de consentimiento informado de participación y para la administración de quimioterapia para el tratamiento, se explicó que toda la información recogida era confidencial.
Resultados
Se estudiaron un total de 63 pacientes con diagnóstico de linfoma folicular, de ellos 36 (57,1 %) eran de sexo masculino y 27 (42,9 %) de sexo femenino, a su vez 44 (69,8 %) tenían más de 50 años y los 19 (30,2 %) restantes se ubicaron entre los 31 y 50 años.
Se observó la distribución de los pacientes por estadios según la clasificación de Cotswold, citado por Campo E et al. 13) y se pudo observar que 33 de ellos, para un 52,4 % son clasificados en el estadio IV, de ellos 29 en el subgrupo IV B y 4 en el IV A; mientras que de los 30 clasificados en el estadio III, 24 fueron III B y 6 III A (Tabla 1).
Tabla 1 Distribución según estadios de Cotswold
| Estadios | Frecuencia | % | |
|---|---|---|---|
| III | 30 | 47,6 | |
| III A | 6 | 9,5 | |
| III B | 24 | 38,1 | |
| IV | 33 | 52,4 | |
| IV A | 4 | 6,4 | |
| IV B | 29 | 46 | |
| Total | 63 | 100 | |
Fuente: planilla de recolección de datos.
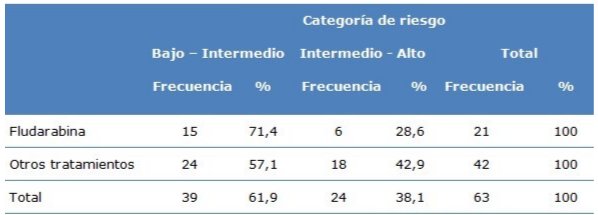
En relación al riesgo de recaída de la enfermedad según un sistema de puntuación utilizado para predecir que pacientes con linfoma folicular pueden correr un mayor riesgo de recidiva de la enfermedad, se aplica el FLIPI y se aprecia en la tabla dos que de los 21 pacientes tratados con fludarabina el riesgo de recaída en 15 (71,4 %) pacientes fue evaluado de bajo-intermedio y en seis (28,6 %) de intermedio-alto. De los 42 que recibieron otros esquemas de poliquimioterapia, el 57,1 % correspondieron a la categoría bajo-intermedio y 42,9 % a la de intermedio-alto. El riesgo de recaída de la enfermedad según FLIPI mostró relación muy significativa según el esquema de tratamiento utilizado (X2 = 6.85, p< 0.01) (Tabla 2).
Con respecto al comportamiento según sobrevida libre de enfermedad, se pudo observar que 14 pacientes con linfoma folicular de los que recibieron tratamiento con fludarabina y 10 de los pacientes que fueron tratados con otros esquemas de poliquimioterapia tuvieron una sobrevida libre de enfermedad mayor de 12 meses.
El tiempo de sobrevida libre de enfermedad mostró una relación significativa entre un esquema de polquimioterapia y otro (X2 =10.95, p<0.001) (Tabla 3).
A analizar la distribución según complicaciones derivadas del tratamiento con fludarabina y los que recibieron otros tratamientos, se observó que el 76,2 % de los pacientes que recibieron esquema de tratamiento con fludarabina no presentaron complicaciones y el 57,1 % de los que fueron tratados con otras modalidades de poliquimioterapia sin fludarabina si las presentaron. Se encontró asociación significativa (X2 = 6,1, p<0,05) entre la modalidad de tratamiento y la presencia de complicaciones. Además, de un menor riesgo de desarrollar complicaciones de los tratados con fludarabina (RR=0,84) (Tabla 4).
Discusión
En estudio realizado por Alonso Mariño OL et al. 7 en la provincia Villa Clara se obtuvo un predominio del estadio III B según la clasificación de Costwold, citado por Campo E et al. 13) lo que difiere de lo encontrado en la investigación, mientras que en estudio realizado por Ning Jiang J y Hua Sun X, 14) en China se informa que de los 200 casos con linfoma folicular que analizaron casi la mitad correspondió al estadio IV y dentro de este grupo predominaron los IV B, lo que coincide con el hallazgo de la investigación. Un estudio efectuado por Sachi S et al. 15) en 54 pacientes con linfoma folicular recurrente reporta que la mayoría de los pacientes se encontraban en estadio III y IV.
Desde el punto de vista práctico en los linfomas no Hodgkin foliculares, no solo es imprescindible un diagnóstico preciso, también es de vital importancia determinar la existencia o no de síntomas generales y precisar la extensión de la enfermedad (estadiación) para aplicar un tratamiento racional. Wang Y et al. 16) coinciden en señalar que la estadificación del linfoma no Hodgkin folicular mediante la clasificación de Ann Arbor, modificada por Costwold, según cita Campo E et al. 13) que incluye los estadios I, II, III, IV y A o B, de acuerdo con la afectación tumoral y la existencia o la ausencia de síntomas, como son la pérdida de peso mayor del 10 % del peso corporal en menos de seis meses, fiebre inexplicable de 380 C o superior y sudoración nocturna, ofrece información importante para la planificación del tratamiento.
La investigación multicéntrica llevada a cabo por Sicras-Mainar A et al. 17) informaron que el 51,2 % de los 99 pacientes con diagnóstico de linfoma folicular presentó un riesgo de recaída intermedio. La cantidad de factores de riesgo que presenta una persona define el grupo de riesgo correspondiente, lo que ayuda a predecir el riesgo de recaída. Cada punto representa un aumento en el riesgo de recaída de la enfermedad, el FLIPI permite predecir que pacientes con linfoma folicular pueden correr un mayor riesgo de recidiva de la enfermedad. 18
Esta información ayuda a los médicos a determinar la atención adecuada para pacientes que han recibido tratamiento para el linfoma folicular. Se asigna un punto por cada uno de los factores de riesgo siguientes: número de ganglios linfáticos afectados: cinco o más, nivel de deshidrogenasa láctica mayor que el límite superior normal, edad mayor de 60 años, la etapa de la enfermedad III o IV y la concentración de hemoglobina menor de 120 g/L. 19
Sicras-Mainar A et al. 17) en investigación metacéntrica realizada plantean que la supervivencia a los cinco años fue de 68,5 % con otros esquemas de poliquimioterapia que no incluyó la fludarabina. Tse E et al. 20) al abordar los avances en el tratamiento de los linfomas se refieren a las ventajas de la fludarabina respecto a otros quimioterápicos, al respecto, Novoa JE et al. 10) en estudio multicéntrico realizado en Uruguay, obtuvo como resultado la supervivencia global a 12 años fue 48 % y la supervivencia libre de enfermedad 44 %.
Foussard C et al. 21) en su estudio realizado en Francia donde se compararon los esquemas fludarabina-mitoxantrona (FM) vs. ciclofosfamida doxorrubicina- vindesina-prednisona (CHVP) en 155 pacientes con linfomas indolentes, mayores de 60 años y menores de 75 se demostró mejores tasas de remisión completa para el FM (49 % vs. 17 %, respectivamente), con una mediana de supervivencia libre de progresión de 36 meses y de 19 meses (CHVP) en el grupo total y sin lograrla a los 53 meses para el grupo que alcanzó la remisión completa.
Zinzani PL et al. 22 reportan una mejor respuesta al tratamiento cuando los pacientes portadores de linfoma folicular fueron tratados con una combinación que incluyó la fludarabina en comparación con la poliquimioterapia CHOP, al mejorar la supervivencia y evitar la progresión de la enfermedad.
Labardini Méndez JR et al. 23 utilizan como tratamiento de primera línea para los LNH foliculares grado 1, 2 y 3a, en específico para los tumores voluminosos en estadios clínicos III y IV la fludarabina, ciclofosfamida y rituximab (FCR).
En el control de las complicaciones asociadas al uso de la fludarabina se logró demostrar que existe un porciento muy bajo de complicaciones, al no ocurrir lo mismo con el uso de otros citostáticos.
En el estudio realizado por Sachi S et al. 15) en pacientes con linfoma folicular recurrente tratados con fludarabina plantean que la mayoría de las reacciones adversas hematológicas fueron transitorias y solo tres pacientes presentaron neutropenia severa y prolongada y otros tres presentaron infecciones.
Según reportes de varios estudios donde se ha utilizado la fludarabina, este fármaco es bien tolerado por los pacientes y los principales efectos adversos son hematológicos, entre los que se encuentran la neutropenia, trombocitopenia y la anemia. (24,25,26) Al analizar estudios que abordan el uso de otras opciones terapéuticas para el tratamiento del linfoma folicular se puede apreciar un mayor número de efectos secundarios. (27,28