Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Vaccimonitor
versión impresa ISSN 1025-028X
Vaccimonitor vol.21 no.1 Ciudad de la Habana ene.-abr. 2012
ARTÍCULO ORIGINAL
Sistema automatizado para la evaluación de la calidad en los laboratorios de diagnóstico con tecnología SUMA
Automated system for quality assessment in the diagnosis laboratories with SUMA technology
Alfredo Rego*, Héctor Pérez, Liliena López, Niurka Carlos
Centro de Inmunoensayo. Departamento de matemática y programación aplicada. Calle 134 y Ave 5, Cubanacán, Playa, La Habana, Cuba.
email:inprogram2@cie.sld.cu
* Ing. en Máquinas Computadoras y MSc en Sistemas Digitales.
RESUMEN
El Centro de Inmunoensayo (CIE) es una institución dedicada a investigación-producción orientada al desarrollo y producción de reactivos e instrumentos para el diagnóstico médico, basados en técnicas inmunoenzimáticas que aprovechan la gran especificidad de la interacción antígeno-anticuerpo y las ventajas de las reacciones catalizadas por enzimas. Su línea principal es el Sistema Ultra Micro Analítico (SUMA), que consiste en una tecnología integrada por equipos y reactivos para la realización de los análisis inmunoenzimáticos a un bajo costo de ejecución, lo cual lo hace particularmente adecuado para los programas de prevención de la salud, en los que se requiere el procesamiento de un gran número de muestras. Con el objetivo de lograr la garantía de la calidad se han desarrollado durante más de una década diferentes sistemas de software que se han utilizado en el proceso de evaluación de la calidad en el trabajo de los laboratorios. Con el nombre de SAC 2.0, el CIE desarrolló un sistema para el control de la calidad que puede realizar el proceso evaluativo de forma totalmente automatizada, que ofrece prestaciones similares a los sistemas más avanzados que existen actualmente. En este trabajo se describen elementos considerados en su concepción, así como las ventajas obtenidas con la automatización, las cuales demuestran cómo la herramienta desarrollada constituye un componente de vital importancia para el adecuado funcionamiento de los laboratorios de la tecnología SUMA, ubicados en Cuba y en el exterior.
Palabras clave: Automatización, control de la calidad, ELISA, SUMA.
ABSTRACT
The Center of Immunoassay (CIE) is a research-production complex aiming at the development and production of reagents and instrumentation for medical diagnosis based on immunoenzymatic techniques using the great specificity of the antigen-antibody interactions and the advantages of the reactions catalyzed by enzymes. Its main line is the Ultra Micro Analytical System (SUMA), consists of a technology of equipments and reagents to perform immunoenzymatic analyses at a low cost, which makes it particularly adequate for prevention health programs that require the processing of a big number of samples. In order to achieve a desirable quality warrant, different software systems have been developed for more than a decade, that have been used in the quality assessment process in the laboratories. Under the name of SAC 2.0, the CIE has developed a version of a system for quality control that is able to perform the assessment process totally automated. This paper describes the elements considered in its conception as well as the advantages obtained from automation, which show how important the developed tools are for the proper functioning of the SUMA laboratories allocated not only in Cuba but in other countries as well.
Keywords : Automation, Quality Control, ELISA, SUMA.
INTRODUCCIÓN
Los errores cometidos en el laboratorio de diagnóstico se clasifican en: errores aleatorios, que varían de forma impredecible en magnitud y signo, y errores sistemáticos que permanecen constantes cuando las mediciones se realizan bajo las mismas condiciones.
La evaluación de la calidad consiste en medir la inexactitud e imprecisión con la que el laboratorio ha realizado dichas mediciones. Se considera la inexactitud como la diferencia numérica entre la media de un grupo de resultados y el valor aceptado como verdadero y la imprecisión como una variable estrechamente relacionada con la desviación estándar o el coeficiente de variación (1).
Para obtener indicadores aceptables de inexactitud e imprecisión es necesario que los laboratorios realicen los dos tipos de controles de la calidad: el control interno y el control externo. El control interno consiste en la preparación de una muestra de referencia que se incluye en cada corrida del ensayo a evaluar. Su resultado se sitúa en un gráfico de control (2-6). Analizando su comportamiento se puede medir la imprecisión y utilizando las reglas de Westgard (7-11) se puede estimar la inexactitud de la medición. Los laboratorios que emplean la tecnología SUMA (12-14) disponen de una eficaz herramienta de control de calidad que le permite garantizar un adecuado desempeño intralaboratorio, todo lo cual conlleva a un diagnóstico certero de patologías tan importantes como: errores innatos del metabolismo, detectados en etapas tempranas de la vida; la detección en la etapa prenatal de defectos no compatibles con la vida, como son los marcadores alfafetoproteína y la hormona gonadotropina coriónica; así como los programas nacionales que aplica nuestro sistema de salud en la detección de seropositivos a los marcadores virales de las hepatitis (B y C), así como al VIH 1 y 2 a nivel de pesquisa en bancos de sangre y centros de higiene y epidemiología.
Los laboratorios son capaces también de procesar otros diagnosticadores desarrollados por el Centro de Inmunoensayo (CIE) que podrían complementar estudios de eficacia de vacunas humanas, como es el caso de la vacuna desarrollada en Cuba para disminuir la prevalencia de la hepatitis B.
El programa de control de la calidad desarrollado por el Centro de Inmunoensayo es potencialmente aplicable a aquellos ensayos de diagnóstico, en los cuales se desee garantizar la confianza en sus resultados. En este trabajo presentamos un sistema automatizado, denominado SAC 2.0, para el control de la calidad de la tecnología SUMA, que permite el análisis combinado de los controles internos y externos, así como la inclusión de estadígrafos que mejoran la eficacia del sistema evaluativo y resuelven las limitaciones descritas en los esquemas convencionales de control de la calidad. Permite, además, procesar un gran volumen de información y evita los errores de transcripción, disminuyendo el tiempo de respuesta.
MATERIALES Y MÉTODOS
Reactivos controles
Los reactivos utilizados fueron los controles externos e internos que tradicionalmente se han utilizado por la tecnología SUMA (12-14).
Controles internos
Los controles internos utilizados son los que habitualmente se incluyen en cada estuche de reactivos: un control por cada placa de lectura (12-14); poseen un número de identificación único de 8 dígitos (XXYYKKZZ).
Controles externos
Se utilizaron los controles producidos por la Subdirección de Producción de Reactivos y certificados por la Subdirección de Aseguramiento y Control de la Calidad del CIE. Para los ensayos cuantitativos aplicados en suero humano se producen dos controles externos mensuales y para ensayos cuantitativos de muestras en papel de filtro se producen tres controles por ensayo (12-14).
Instrumentos utilizados
Instrumento de lectura: Lectores de placas de ultramicro ELISA PR-521 o PR621 y lavador de placas MW-2001 (13-14).
Soportes informáticos utilizados
Sistema informático del laboratorio: Los laboratorios con tecnología SUMA en Cuba y en el exterior poseen gran variedad de computadoras y como sistema operativo se utiliza Windows (13, 14).
Durante el trabajo diario en el laboratorio para la comunicación con el instrumento de lectura se utiliza el software SRS 9.17 (herramienta informática utilizada para el control, cálculo e interpretación de los resultados del instrumento de lectura) (12-14).
Supervisores: Se denomina supervisor al personal que utilizando el SAC (Sistema de Aseguramiento de la Calidad) realiza la evaluación de la calidad de una red de laboratorios SUMA en un país o una región de un país determinado. En Cuba hasta el momento existen cinco supervisores: el supervisor general que se encuentra en la Subdirección de Aseguramiento y Control de la Calidad del CIE; adicionalmente existe un supervisor por cada representación regional de la representación comercial de Tecnosuma S.A (occidente, centro, oriente norte y oriente sur); en otros países existe un supervisor por cada entidad de salud que realiza el control de su propia red de laboratorios SUMA.
Desde el punto de vista de hardware, los sistemas informáticos que utilizan los supervisores que evalúan la calidad de las redes de laboratorios de diagnóstico en Cuba y en otros países son diversos, sin embargo, desde el punto de vista del software todos utilizan como sistema operativo Windows.
Sistema informático del CIE: La información relacionada con el control de la calidad y el funcionamiento de los programas de diagnóstico ha sido almacenada durante más 10 años en un servidor de bases de datos, al que adicionalmente se le ha incorporado la aplicación SAC 2.0 Servidor, que se encarga de la recepción de los mensajes provenientes de las representaciones regionales y de los laboratorios.
Evaluación de los resultados del control externo de calidad
Ensayos cuantitativos
Para realizar el análisis del control externo de la calidad se utiliza como indicador el índice de variación (V), el cual representa la variabilidad relativa de los resultados de cada laboratorio con respecto al valor medio y se calcula mediante la siguiente expresión:
V = [(X - M)/M] x 100
Donde:
V: Indicador de variabilidad
X: Valor reportado por el laboratorio
M: Valor medio o valor consenso obtenido a partir de los resultados reportados por los laboratorios participantes.
En nuestro esquema utilizamos diferentes metodologías de obtención del valor consenso M, la selección de este valor la realiza el software de forma automática en dependencia de la cantidad de laboratorios que participan en el programa. Posteriormente se calculan los indicadores de exactitud y variabilidad promedios:
IEP = (V/CVR) x 100
IVP= ½IEP½
Donde:
CVR: Coeficiente de variación de referencia (constante de valor 10% para ensayos en suero humano y 15% para ensayos en papel de filtro).
IEP: Indicador de exactitud promedio.
IVP: Indicador de variabilidad promedio (relativo al ensayo).
Para facilitar la interpretación de los resultados en los laboratorios, decidimos asignar a los resultados cuantitativos del IVP una evaluación cualitativa, clasificando los mismos de la forma siguiente:
IVP £ 100 MUY BUENO
IVP 101 a 200 BUENO
IVP 201 a 250 REGULAR
IVP ³ 251 DEFICIENTE
Ensayos cualitativos
La evaluación se realiza teniendo en cuenta el impacto diagnóstico de la concordancia. El análisis está basado en el índice de calidad (IC), indicador de la concordancia de los resultados de cada laboratorio respecto al resultado esperado.
El cálculo se efectúa como sigue:
IC máximo = 100
-Cada control con Resultado Esperado Negativo que se informa Positivo, resta 6,25 puntos.
-Cada control con Resultado Esperado Positivo que se informa Negativo, resta 25 puntos.
Los mejores resultados son los más cercanos a 100.
IC 90 a 100 MUY BUENO
IC 85 a 89 BUENO
IC 75 a 84 REGULAR
IC < 75 DEFICIENTE
Evaluación de los resultados del control interno de calidad
Los resultados del control interno se verifican mediante dos vías: La primera consiste en verificar que el resultado del mismo no exceda los límites que especifica el productor del estuche de reactivos.
La segunda consiste en analizar su comportamiento a partir de las internacionalmente conocidas reglas de Westgard (7-11), mediante las cuales se pueden definir los límites de aceptabilidad de un ensayo, trabajan a partir del comportamiento de los resultados del control interno, situados en un gráfico de control o carta de Shewhart (2, 6).
Existen seis reglas comúnmente usadas, las cuales se dividen en reglas de precaución y reglas de cumplimiento obligatorio.
Reglas de precaución :
1C2SD: Cuando el valor obtenido por un control excede 2 desviaciones estándar.
2C2SD: Cuando dos controles de forma consecutiva exceden 2 desviaciones estándar
4C1SD: Cuando cuatro controles de forma consecutiva exceden 1 desviación estándar y se encuentran posicionados a un mismo lado de la gráfica.
Reglas de cumplimiento obligatorio :
1C3SD: Cuando el valor obtenido por un control excede 3 desviaciones estándar.
R4SD: Cuando el valor obtenido por un control y su duplicado excede de 4 desviaciones estándar.
10X: Cuando 10 valores consecutivos se encuentran situados en el mismo lado del gráfico.
Al aplicar dichas reglas se puede llegar a la conclusión de que existe un comportamiento aceptable o inadecuado del control interno. En el caso negativo una persona capacitada y autorizada debe identificar las causas que originaron dicho comportamiento y tomar las medidas orientadas al respecto.
La versión SAC 2.0 incluye la utilización del índice de fiabilidad RI (15, 16) y del índice de coeficientes de variación CVI (17) en el análisis del control interno, estimadores que permiten calcular la inexactitud e imprecisión de los resultados del control interno mediante las expresiones siguientes:
RI[i] = (C[i] - MD)/SD
Donde:
RI[i]: Índice de fiabilidad obtenido por el control interno i.
C[i]: Representa la concentración obtenida en la medición del control i.
MD: Representa la media calculada considerando todos los controles internos del lote en específico.
SD: Representa la desviación estándar calculada con los controles internos del lote en específico.
En un laboratorio para un lote de controles internos se calcula:
CVI = CV L /CV G
Donde:
CVI: Índice de coeficientes de variación
CV L : Coeficiente de variación del laboratorio
CV G : Coeficiente de variación del grupo de laboratorios
Automatización del proceso de evaluación de la calidad
Las diferentes aplicaciones del SAC 2.0 (servidor, supervisor, laboratorio) han sido desarrolladas para los sistemas operativos Windows XP o Windows 7, utilizando un lenguaje IDE Visual RAD (Rapid Assisted Design) con posibilidades de programación orientada a objetos y capaz de soportar diferentes gestores de bases de datos, de los cuales se seleccionó un gestor de distribución libre con entorno gráfico que permitiera trabajar en modo cliente servidor y utilizar procedimientos almacenados.
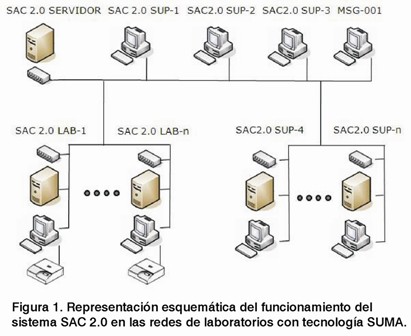
A continuación se muestra de forma gráfica su ubicación en las redes de laboratorios con tecnología SUMA (Fig. 1).
Las aplicaciones representadas en la Figura 1 se clasifican en los tres grupos que se describen a continuación:
1. SAC 2.0 SERVIDOR
La aplicación SAC 2.0 Servidor se instala en el servidor de correos del CIE o en una computadora conectada a la red local, sus funciones principales son:
· Establece una comunicación automática con el servidor de correos de la intranet del CIE y descarga los correos enviados a la dirección que se le ha asignado a esta aplicación que cumplen las especificaciones establecidas en el protocolo de comunicaciones diseñado.
· Valida la integridad del fichero adjunto (a partir de un protocolo establecido) que contiene una base de datos comprimida con la información de uno o más laboratorios.
· Si la información es válida , la almacena en una base de datos.
· Evalúa los resultados de los controles internos y externos utilizando los estimadores anteriormente mencionados.
· Para los controles internos obtiene los estadígrafos media, desviación estándar y coeficiente de variación por lotes y por ensayos con el objetivo de obtener posteriormente el resultado del índice de fiabilidad (RI) , así como el índice de coeficientes de variación (CVI).
· Responde al cliente que ha solicitado el servicio mediante un correo que posee como información adjunta una base de datos comprimida con los resultados solicitados.
2. SAC 2.0 SUP-1..n
Aplicación SAC 2.0 Supervisor (cuando se señala 1..n se está haciendo referencia a todos los sistemas supervisores representados en el gráfico); está destinada a la supervisión de una red de laboratorios (cantidad limitada a una entidad de un país específico).
Se configura como supervisor general, cuando se instala en la Subdirección de Aseguramiento y Control de la Calidad del CIE, lo que permite evaluar el comportamiento de todos los laboratorios instalados en Cuba y en el exterior.
Se puede configurar para analizar los resultados del control de la calidad de laboratorios pertenecientes a regiones y provincias de un país determinado. Por ejemplo, en el caso de Cuba el país está dividido en cuatro regiones: occidente, centro, oriente norte y oriente sur.
3. SAC 2.0 LAB-1..n
La aplicación que se instala en el laboratorio de diagnóstico se configura para trabajar en modo automático o manual.
Modo automático : El software utiliza un temporizador interno para distribuir las tareas que se describen a continuación:
· Se establece una comunicación automática con el servidor de correos de la red local, que recibe los mensajes enviados desde el SAC-2.0 Servidor.
· Se envían mensajes periódicos con la información de los resultados obtenidos en los controles internos y externos de calidad.
· Se realiza el análisis del comportamiento de los controles internos mediante las reglas de Westgard (7-11), indicando las posibles causas que los originaron.
· Se realiza el análisis de los resultados de los controles externos.
Modo manual : el usuario se encarga de realizar las funciones de introducir la información, comunicarse con el supervisor o el evaluador, así como de analizar el comportamiento de los gráficos de control.
RESULTADOS Y DISCUSIÓN
La automatización de la extracción de la información (controles internos y externos), así como de la evaluación y envío de los resultados (sin la intervención del hombre) ha permitido mejorar la eficacia de la evaluación por las razones siguientes:
1. Se obtienen los resultados del indicador de fiabilidad (RI) para cada medición realizada en el laboratorio, analizándose el 100% de las mediciones (Fig. 2).
Se observa cómo las mediciones 5, 13, 14, 15, 23, 24, 27 y 28 excedieron las 3 desviaciones estándar calculadas a partir de los resultados de todos los controles del mismo tipo, procesados por todos los laboratorios de la red (el software cuando los valores exceden las 3 desviaciones estándar fija el resultado a 3 unidades).
Resulta importante destacar la mejora en el análisis de los resultados utilizando esta herramienta con respecto a los gráficos de control (2-6) y las reglas de Westgard (7-11).
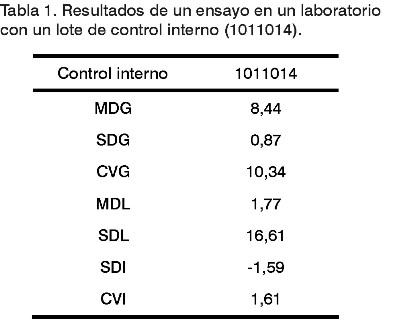
2. Se ha logrado obtener por laboratorio un indicador que permite comparar su imprecisión con la del resto que procesan el mismo control de la calidad (CVI) (Tabla 1).
MDG, SDG, CVG: representan la media, desviación estándar y coeficiente de variación obtenidos a partir de las mediciones de los controles internos procesados por todos los laboratorios. MDL, CVL, SD: representan la media, coeficiente de variación y desviación estándar obtenidos con los datos procesados por el laboratorio.
3. Se elimina la limitación que poseen los gráficos de control cuando la cantidad de mediciones es menor de 20, al ser sustituidos por los gráficos de índice de fiabilidad (al utilizarse como indicador de exactitud los resultados del RI (Fig. 2).
4. Se eliminan los errores de transcripción introducidos durante la manipulación de la información.
5. Se incorpora a la base de datos centralizada un volumen considerable de información útil en el análisis y seguimiento de los programas de diagnóstico y los estuches de reactivos.
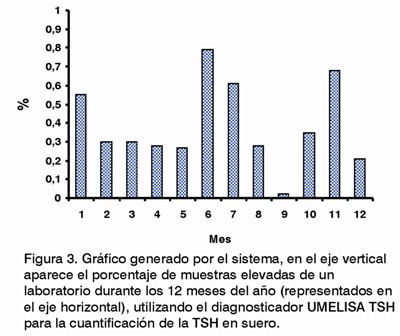
Como ejemplo mostramos (Fig. 3), una de las 25 variantes de gráficos estadísticos del comportamiento de porcentaje de muestras elevadas por laboratorio durante los 12 meses de un año (cuantificación de TSH en suero).
6. El esquema de trabajo propuesto incluye una muestra más en las corridas analíticas, con una frecuencia típica de 2 a 3 veces por mes; su resultado es desconocido por el laboratorio, se utiliza principalmente en la detección del posible error sistemático y por consiguiente constituye una herramienta efectiva en la detección de la inexactitud en las mediciones.
7. La utilización del sistema ha permitido procesar gran cantidad de información y ha disminuido el tiempo requerido para el envío de los resultados.
Como conclusión, podemos decir que el empleo de la herramienta automatizada SAC 2.0 ha potenciado la efectividad y eficiencia del proceso evaluativo, permitiendo disponer de un sistema con prestaciones similares a los más avanzados que actualmente se utilizan (17-20).
Mediante el uso de los estadígrafos presentados se han resuelto las limitaciones que poseen los esquemas convencionales de control de la calidad.
Se ha logrado evaluar de forma integral el trabajo de los laboratorios, identificándose con rapidez aquellos que poseen resultados no satisfactorios y facilitándoles tomar las acciones correctivas que garanticen su adecuado funcionamiento.
La utilización de este sistema ha tenido un impacto positivo en la elevación de la calidad de la red y una mejoría en el funcionamiento de programas de salud de elevada importancia social en Cuba y en otros países donde se utiliza esta tecnología.
REFERENCIAS
1. INIM/ Oficina Nacional de Normalización. NC-ISO 5725-1:2005 Exactitud (Veracidad y Precisión) de métodos de medición de resultados. Parte 1: Principios generales y definiciones (ISO 5725-1:1994, IDT). La Habana: INIM; 2005.
2. Shewhart WA. Economic Control of Quality of the Manufactured Product. New Cork: Van Nostrand; 1931.
3. Levey S, Jennings ER. The use of control charts in the clinical laboratories. Am J Clin Pathol 1950;20:1059-66.
4. Duncan AJ. Quality control and industrial statistics. 4th ed. Homewood, IL: Richard D Irwin; 1974.
5. Nelson L. The Shewhart control chart-tests for special causes. J. Qual Technol 1984;15:233-9.
6. Nelson L. Interpreting Shewhart X control charts. J Qual Technol 1985;17:114-6.
7. Westgard JO, Groth T, Aronsson T. Performance characteristics of rules for internal quality control: Probabilities for false rejection and error detection. Clin Chem 1977;23:1857-67.
8. Westgard JO, Falk H, Groth T. Influence of a between-run component of variation, choice of control limits, and shape of error distribution on the performance characteristics of rules for internal quality control. Clin Chem 1979;25:394-400.
9. Westgard JO, Groth T. Power functions for statistical control rules. Clin Chem 1979;25:863-9.
10. Westgard JO, Barry PL, Hunt MR, Groth T. A multi-rule Shewhart chart for quality control in clinical chemistry. Clin Chem 1981;27:493-501.
11. Westgard JO, Barry PL. Improving Quality Control by use of Multirule Control Procedures. Washington, DC: AACC Press; 1996.
12. Tecnosuma Internacional SA©. [Homepage on the Internet]. Sistema Ultra Micro Analítico (SUMA). Disponible en: http://www.tecnosuma.com . Consultado: 19 de diciembre de 2011.
13. García MA, Carlos N. Producen nueva generación de lectores SUMA. Innovación, Ciencia y Desarrollo 1997;3(3):41.
14. Díaz W, Carlos N, Rego A, Fernández JL. Software para trabajo con estuches UMELISA y lectores PR de la tecnología SUMA (Strips Reader Software SRS Ver 8.0). Registro con número I 0010132021200. La Habana: Centro de Control Estatal de Equipos Médicos (CCEEM); 2001.
15. Whitehead TP. Advances in Quality Control. Clin Chem 1977;19:175-205.
16. María LG, Giulliano B. Long Term Retrospective Control Procedures for Monitoring Performance of Laboratory Instruments. Clin Chem 1984;30:145-9.
17. Randox Laboratories [homepage on the Internet]. Quality Control. QC Software. Disponible en: http://www.randox.com . Consultado: 20 de agosto de 2011.
18. BIO-RAD [homepage on the Internet]. Unity Interlab. Disponible en: http://www.QCnet.com . Consultado: 20 de agosto de 2011.
19. CDC Atlanta [homepage on the Internet]. EQA. External Quality Assessment. Disponible en: http://www.cdc.gov/nsqap/public/default.aspx . Consultado: 20 de agosto de 2011
20. Fundación Bioquímica Argentina [homepage on the Internet]. Programas FBA. Disponible en: http://www.fba.org.ar/default.asp?. Consultado: 20 de agosto de 2011.
Recibido: Agosto de 2011
Aceptado: Noviembre de 2011