Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Vaccimonitor
versión On-line ISSN 1025-0298
Vaccimonitor vol.24 no.1 Ciudad de la Habana abr. 2015
ARTÍCULO ORIGINAL
Implementación de la técnica de micromatrices de tejidos para la investigación oncológica en Cuba
Implementation of tissue microarrays technique for cancer research in Cuba
Xiomara Escobar-Pérez, 1* Tania Lahera-Sánchez,1 María Caridad de Armas-Fernández,2 Damián Blanco-Santana, 1* Leticia Navarro-Pérez, 3 Adanays Calvo-Pérez, 1 Rosa Irene Álvarez-Goyanes 1
1 Instituto de Oncología y Radiobiología. Calle 29, Esquina F. Vedado. CP: 10400. La Habana, Cuba.
2 Departamento de Anatomía Patológica. Hospital Clínico Quirúrgico Hermanos Ameijeiras. San Lázaro No. 701. Centro Habana. CP: 10300. La Habana, Cuba.
3 Laboratorio de Patología Quirúrgica y Citología de Puebla. Universidad Autónoma del Estado de Puebla, México.
email: xescobar@infomed.sld.cu
* Licenciada en Tecnología de la Salud, especialidad en Laboratorio Clínico y Banco de Sangre. Investigador Agregado.
RESUMEN
La técnica de micromatrices de tejidos (TMA), basada en la toma de ponches cilíndricos de bloques de parafina donantes y su transferencia a un solo bloque receptor, revolucionó el campo de la patología, por la posibilidad de evaluar múltiples muestras en una sola lámina. En Cuba no existen antecedentes del tema, por lo que el objetivo de este trabajo fue implementar la técnica de TMA. Para ello, se evaluó la concordancia de los resultados que se obtienen por sección completa y por TMA, en la evaluación de los receptores de estrógeno (RE), progesterona (RP) y del factor de crecimiento epidérmico tipo 2 (HER2) en muestras de cáncer de mama. Se estudiaron 45 muestras parafinadas de mujeres con esta enfermedad que se atendieron en el Instituto de Oncología en el año 2012. Se construyeron dos bloques de TMA y posteriormente se determinó, mediante inmunohistoquímica, la expresión de los marcadores RE, RP y HER2, en la sección completa de tejido y en el TMA. Para el análisis de concordancia se empleó el índice Kappa. Se obtuvo una buena concordancia para los tres marcadores (RE k=0,8272; RP k=0,793 y HER2 k=0,716). Este trabajo constituye el primer reporte sobre la técnica de TMA en Cuba y demuestra que es una herramienta valiosa, por lo que se sugiere su potencial uso en la investigación traslacional y en los ensayos clínicos de vacunas.
Palabras clave: micromatrices de tejido, inmunohistoquímica, cáncer de mama.
ABSTRACT
The tissue microarray (TMA) technique is based on making cylindrical cores from paraffin donor blocks and transfer to a single recipient block. The TMA has revolutionized the field of pathology for the possibility to evaluate multiple samples in one slide. There is no precedent of this subject in Cuba, so the objective of this research was to implement the TMA technique. The concordance of the results obtained by complete section and the TMA were evaluated for this purpose, in the evaluation of the estrogen receptors (ER), progesterone (PR) and epidermal growth factor type 2 (HER2) in samples of breast cancer. Forty-five paraffin-embedded samples from women diagnosed with breast cancer at the Institute of Oncology in 2012 were studied. Two TMA blocks were constructed, and subsequently the expression of markers ER, PR and HER2 was determined by immunohistochemistry, in the complete section of tissue and in the TMA. Kappa index was used for concordance analysis. A good concordance was obtained for all three markers (ER k=0.8272; PR k=0.793 and HER2 k=0.716). This study constitutes the first report on the TMA technique in Cuba and shows that it is a valuable tool, suggesting its potential use in translational research and clinical trials on vaccines.
Key words: tissue microarray, immunohistochemistry, breast cancer.
INTRODUCCIÓN
En los últimos años, las limitaciones de las técnicas convencionales de patología molecular, así como los avances en los campos de la genómica y la proteómica, sustentan el desarrollo de nuevas técnicas experimentales.
Uno de los avances que revolucionó el campo de la patología, particularmente en el área de la investigación oncológica, fue la introducción de la técnica de micromatrices de tejidos (TMA, del inglés tissue microarray). Esta tecnología consiste en la toma de ponches cilíndricos de bloques de parafina donantes y su transferencia a un solo bloque receptor (1).
Si bien las primeras aproximaciones sobre las evaluaciones multi-tejidos en un solo soporte surgieron en la década de 1980 (2), no fue hasta 1998 en que se introdujo propiamente la técnica de TMA, por Kononen y cols, en el Instituto Nacional de Salud de Bethesda, Estados Unidos (3). Desde entonces, el empleo de esta herramienta tecnológica se incrementó de forma significativa, lo cual se evidencia en sus más de 15 mil publicaciones en la literatura científica (4).
Múltiples ventajas justifican el uso del TMA, fundamentalmente la posibilidad de evaluación de un elevado número de muestras a la vez, la reducción de los costos y del tiempo que se emplea en la técnica, el uso más eficiente de la muestra, así como la posibilidad de aplicarse en varios procederes como la inmunohistoquímica (IHQ), hibridación in situ fluorescente (FISH) o cromogénica (CISH) (5, 6).
En Cuba, no existen antecedentes del tema; sin embargo, es necesario el uso de la técnica de TMA, no solo por sus múltiples ventajas, sino por las particularidades de la investigación oncológica en el contexto nacional.
El cáncer constituye la principal causa de muerte en Cuba (7), por lo cual se justifica la introducción de la técnica de TMA, que facilitaría: optimizar la evaluación diagnóstica, el pronóstico, la terapéutica en estos pacientes, incluyendo el desarrollo de una medicina más personalizada, así como responder ante la creciente demanda de evaluación, en el escenario clínico, de las vacunas terapéuticas contra el cáncer.
Este trabajo constituye el primer reporte sobre la implementación de la técnica de TMA en Cuba. El objetivo de este trabajo es evaluar la concordancia de los resultados que se obtienen por sección completa y por TMA en la evaluación de los receptores de estrógeno (RE), progesterona (RP) y del factor de crecimiento epidérmico tipo 2 (HER2) en pacientes con cáncer de mama.
MATERIALES Y MÉTODOS
Muestras tumorales
Se estudiaron 45 muestras de fragmentos tumorales de mama, fijadas en formol tamponado al 10% e incluidas en parafina, conservadas en los departamentos de anatomía patológica del hospital Celestino Hernández, de Villa Clara y José López, de Matanzas. Estas muestras se enviaron al departamento de biología celular y banco del Instituto de Oncología y Radiobiología (INOR).
Las muestras procedían de las pacientes que se atendieron en el servicio de mastología de cada una de estas instituciones, con previo consentimiento de los pacientes a participar en el estudio.
Inicialmente se evaluaron por un patólogo las láminas de hematoxilina-eosina correspondientes, para corroborar que eran fragmentos representativos de tumor.
Construcción de TMA
El patólogo seleccionó un campo tumoral representativo en la lámina de hematoxilina-eosina, que luego se confrontó con el bloque de tejido correspondiente para localizar el sitio exacto para la perforación. Posteriormente, se realizaron ponches de 2 mm de diámetro de cada bloque donante que se insertaron en un bloque receptor, con capacidad para 24 muestras, empleando el dispositivo Thermo Scientific , México (Fig. 1).
Una vez que se construyó el TMA, se mantuvo a 37 °C durante 15 min para lograr que los cilindros que se insertaron se fundan con la parafina del bloque receptor.
Se realizaron cortes seriados de tejido de 4 µm, que se adhirieron a láminas portaobjetos recubiertas con poli-L-lisina, una de las láminas se tiño con hematoxilina/eosina para verificar la presencia de tejido tumoral representativo de cada paciente.
Evaluación inmunohistoquímica de RE, RP y HER2
Se realizó la técnica inmunohistoquímica en la sección completa de tejido y en el TMA. Inicialmente las láminas se incubaron a 60 °C durante 60 min para lograr una adecuada adhesión del tejido e iniciar el proceso de desparafinado.
Posteriormente se realizaron tres pases por xilol (10 min cada vez), seguido por tres pases por concentraciones decrecientes de etanol (95%, 85%, 75%) (5 min en cada uno) y finalmente por agua destilada para la rehidratación del tejido.
Con el objetivo de exponer el antígeno, las láminas se sumergieron en una solución de citrato de sodio (0,01 mol/L, pH=6,0) y se expusieron al calor en un baño termostatado en un intervalo de temperatura entre 95 °C y 99 °C, durante 30 o 40 min según las indicaciones del fabricante.
Para bloquear la peroxidasa endógena del tejido, se trataron las láminas con una solución de peróxido de hidrógeno al 3% en metanol absoluto, durante 5 min. Se aplicó el anticuerpo específico para cada antígeno durante 30 min.
Se emplearon los anticuerpos monoclonales anti-RE y anti-RP (clones SP1 y SP2 respectivamente) prediluidos (Anacrom Diagnósticos, Sevilla, España), así como el juego de reactivos Hercep Test TM (Dako, Dinamarca) para HER2.
Para la detección del RE y RP se empleó un sistema ultrasensible multiespecífico (MLINK, Anacrom Diagnósticos, S.L, España), que incluye un anticuerpo secundario marcado con biotina y un complejo de estreptavidina marcada con peroxidasa.
Para el HER2 se utilizó el sistema de detección basado en anticuerpos anti-conejo marcados con peroxidasa que se une a un polímero de dextrán, como agente de visualización, incluido en el juego diagnóstico.
Para todos los marcadores, posterior al sistema de detección, se aplicó el cromógeno 3,3'-diaminobencidina tetrahidroclorhídrica (DAB) durante 10 min, para revelar la reacción.
La reacción se contrastó con hematoxilina de Mayer (Dako, Dinamarca) durante 30 s. Finalmente se deshidrataron los tejidos en concentraciones ascendentes de etanol (75%, 85%, 95%), 5 min en cada una, se aclaró en xilol y se montaron las láminas con un medio permanente Eukitt (KinderGmbH& Co , Alemania). En cada experimento se utilizaron como control positivo, muestras de tejidos con expresión previa conocida y líneas celulares que recomienda el fabricante del juego de reactivos Hercep Test TM.
Evaluación de la inmunotinción
La expresión tisular de RE y RP se determinó por la coloración del núcleo de las células tumorales, con el uso de un microscopio de campo brillante (Zeiss). Se consideraron positivas las muestras con al menos el 1% de las células tumorales positivas (8-10).
La expresión tisular de HER2 se evaluó según la escala propuesta por Dako y aprobada por el Colegio Americano de Patología (9) que tiene en cuenta la continuidad e intensidad de coloración de la membrana citoplasmática en las células tumorales:
Negativo (0): no se observa tinción en la membrana citoplasmática en <10% de las células tumorales.
Negativo (1+): tinción débil e incompleta de la membrana citoplasmática en más del 10% de las células tumorales.
Débilmente positivo (2+): tinción completa de la membrana citoplasmática, débil o moderada, en el 10-30% de las células tumorales.
Positivo (3+): tinción de la membrana citoplasmática, completa e intensa en más del 30% de las células tumorales.
La evaluación de los marcadores inmunohistoquímicos se realizó por dos observadores y en caso de discordancia se incluyó un tercero.
Análisis estadístico
Para evaluar la concordancia entre los resultados del TMA y de la sección completa de tejido se utilizó el índice Kappa (k) (10). Además se determinó la eficacia del TMA (capacidad para detectar correctamente todos los positivos y los negativos) (10) :
Eficacia = [ (VP+VN)/(VP+VN+FP+FN) ] x 100
Donde:
VP = Verdaderos positivos o positivos correctamente detectados.
FP = Falsos positivos.
VN = Verdaderos negativos o negativos correctamente detectados.
FN = Falsos negativos.
Adicionalmente se analizó la relación entre las variables clínico-patológicas (edad, diagnóstico histológico, positividad de los ganglios y grado histológico) y el estado de los receptores hormonales y HER2, mediante el estadígrafo Chi-cuadrado (a=0,05).
Se determinó además la edad promedio de los casos estudiados y su rango. Se calculó el porcentaje de los marcadores que se evaluaron en la muestra, del diagnóstico y grado histológico, así como del número de ganglios positivos.
Para el procesamiento y análisis estadístico de los datos se utilizó el paquete estadístico SPSS, versión 20.0 para Windows.
RESULTADOS
La edad promedio de los casos estuvo entre 44,3-71,9 años, con un rango entre 27 y 83 años. Predominaron las mujeres con carcinoma ductal invasivo (84,44%) y con grado histológico 2 (37,77%) (Tabla 1).
En relación a la construcción del TMA, se destaca que todos los ponches mostraron muestra tumoral representativa. Se construyeron dos bloques de TMA, con 24 muestras cada uno, incluyendo los controles (Fig. 2).
Durante la ejecución de la técnica IHQ, se perdieron 3 muestras de RE (6,66%) y 4 muestras de RP y HER2 (8,88%), que resultaron no evaluables.
Con respecto a la expresión de los marcadores que se evaluaron en las secciones completas de tejido, se observó un predominio de pacientes con receptores hormonales positivos (RE: 68,89% y RP: 66,67%), mientras que para HER2, solo se declaró positividad en el 24,44% de los casos.
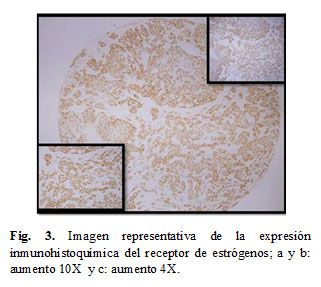
En la Figura 3 se observa la imagen microscópica de una de las muestras del TMA, donde se evaluó la expresión inmunohistoquímica de RE.
Previa clasificación de los resultados que se obtuvieron para cada marcador, se realizó el análisis de la concordancia entre el TMA y la sección completa, así como de la eficacia del nuevo método (Tabla 2).
Se puede observar una excelente eficacia, superior al 95% en los tres marcadores. De igual forma, se obtuvo una buena concordancia (RE k=0,827; RP k=0,793 y HER2 k=0,716), con valores estadísticamente significativos.
No se detectó relación estadísticamente significativa entre la expresión de RE, RP y HER2, y las variables clínico-patológicas: grupo de edad (<50 y =50 años) , diagnóstico histológico, grado histológico y número de ganglios positivos.
DISCUSIÓN
Este trabajo constituye el primer reporte sobre la técnica de TMA en Cuba. La localización que se estudió fue cáncer de mama, por ser la de mayor número de investigaciones del tema en la literatura científica y por representar, además, la segunda causa de incidencia y mortalidad por cáncer en el sexo femenino en Cuba (7). Se evaluaron tres marcadores (RE, RP y HER2), bien caracterizados y de amplio uso, por su valor pronóstico y predictivo en las pacientes con cáncer de mama. Los datos demostraron una buena concordancia entre los resultados obtenidos por TMA y por sección completa.
Estos resultados son similares a los de Zhang y cols, quienes declararon una coincidencia superior al 95% para RE, RP y HER2 en un estudio de 97 muestras de mama (11). Otras investigaciones también evidencian resultados similares (12, 13).
Aunque existen varias investigaciones sobre el empleo del TMA en la evaluación de estos marcadores (11-15), sus diseños muestran gran variabilidad en el número de muestras que se estudiaron, así como en el diámetro y número de ponches que se realizaron por cada caso, cuestiones que aún son polémicas en la literatura.
En esta investigación se realizó un ponche por muestra, que resultó concordante con la sección completa, resultado similar a otros reportes previos (11, 16). No obstante, algunos autores sugieren un mayor número de ponches, en dependencia, incluso, del marcador. Tal es el caso de Graham y cols (14), quienes recomiendan un mínimo de cuatro ponches para los estudios de HER2, mientras que Faratian y cols (17) en investigaciones de RP sugieren al menos tres. En cualquier caso, es prudente realizar una evaluación previa de las muestras para determinar si existe marcada heterogeneidad tumoral, valorar si es recomendable el uso del TMA y en tal caso identificar el mínimo de ponches necesarios, en aras de aumentar la eficiencia de la técnica.
En relación al diámetro del ponche, en este estudio fue de 2 mm, el que se encuentra dentro del rango que se declara en la literatura (0,6-2 mm), aunque el que mayormente se utiliza es de 0,6 mm (4).
El TMA es un método eficiente, económico y de alto rendimiento que permite evaluar hasta 1.000 muestras en una sola lámina. No obstante, su principal limitación radica en el riesgo de no representatividad en tumores histológicamente muy heterogéneos o cuando existe una baja proporción de células tumorales en la muestra. No se recomienda su uso en los estudios de nuevos antígenos, donde la distribución dentro del tejido se desconoce, ni en estudios de marcadores de expresión focal (18).
En Cuba, el laboratorio de biología celular y banco de tumores del INOR, es pionero en el uso de esta técnica. Actualmente se evalúa, por TMA, la expresión de la molécula NglicolilGM3 en muestras de pacientes incluidos en los ensayos de la vacuna terapéutica contra este blanco, proyecto en colaboración con el Centro de Inmunología Molecular (Cuba). Paralelamente se aplica esta técnica en dos proyectos del INOR, que se relacionan con la evaluación de biomarcadores de pronósticos en cáncer de mama y colon.
Este estudio demuestra que la técnica TMA es una valiosa herramienta, útil en la investigación traslacional. Es el propósito de esta investigación y del INOR, extender su uso a nuevos ensayos clínicos de vacunas terapéuticas y a otros proyectos de investigación oncológica.
REFERENCIAS
1. Thomson T, Zhou C, Chu C, Knight B. Tissue Microarray for Routine Analysis of Breast Biomarkers in the Clinical Laboratory. Am J Clin Pathol 2009;132(6):899-905.
2. Wan WH, Fortuna MB, Furmanski P. A Rapid and efficient method for testing immunohistochemical reactivity of monoclonal antibodies against multiple tissue samples simultaneously. J Immunol Methods 1987;103(1):121-9.
3. Kononen J, Bubendorf L, Kallioniemi A, Bärlund M, Schraml P, Leighton S, et al. Tissue microarrays for high-throughput molecular profiling of tumor specimens. Nat Med 1998;4(7):844-7.
4. Pinder SE, Brown JP, Gillet C, Purdie CA, Speirs V, Thompson AM, et al. The manufacture and assessment of tissue microarrays: suggestions and criteria for analysis, with breast cancer as an example.J Clin Pathol 2013;66(3):169-77.
5. Dolled-Filhart MP, Gustavson MD. Tissue microarrays and quantitative tissue-based image analysis as a tool for oncology biomarker and diagnostic development. Expert Opin Med Diagn 2012 ; 6(6):569-83.
6. Kumar B, De Silva M, Venter DJ, Armes JE. Tissue microarrays: a practical guide. Pathology 2004;36(4):295-300.
7. Ministerio de Salud Pública de Cuba. Dirección Nacional de Estadísticas y Registros Médicos. Anuario Estadístico de Salud 2013. La Habana: MINSAP; 2013.
8. Hammond ME, Hayes DF, Dowsett M, Allred DC, Hagerty KL, Badve S, et al. American Society of Clinical Oncology/College of American Pathologists Guideline recommendations for immunohistochemical testing of estrogen and progesterone receptors in breast cancer. J Clin Oncol 2010;28(16):2784-95.
9. Wolff AC, Hammond ME, Schwartz JN, Hagerty KL, Allred DC, Cote RJ, et al. American Society of Clinical Oncology/College of American Pathologists. Guideline recommendations for human epidermal growth factor receptor 2 testing in breast cancer. J Clin Oncol 2007;25(1):118-45.
10. Ochoa-Azze RF. Validación de inmunoensayos cuantitativos y cualitativos. En: Ochoa-Azze RF. Técnicas Inmunoenzimáticas en el Desarrollo Clínico de Vacunas. La Habana: Finlay Ediciones; 2013.p.25-41.
11. Zhang D, Salto-Tellez M, Putti TC, Do E, Koay ES. Reliability of tissue microarrays in detecting protein expression and gene amplification in breast cancer. Mod Pathol 2003;16(1):79-85.
12. Camp RL, Charette LA, Rimm DL. Validation of tissue microarray technology in breast carcinoma. Lab Invest 2000 ;80(12):1943-9.
13. Gillet CE, Springall RJ, Barnes DM, Hanby AM. Multiple tissue core arrays in histopathology research: a validation study. J Pathol 2000;192(4):549-53.
14. Graham AD, Faratian D, Rae F, Thomas J. Tissue microarray technology in the routine assessment of HER-2 status in invasive breast cancer: a prospective study of the use of immunohistochemistry and fluorescence in situ hybridization. Histopathology 2008;52(7):847-55.
15. Egervari K, Szollosi Z, Nemes Z. Tissue microarray technology in breast cancer HER2 diagnostics. Pathol Res Pract. 2007;203(3):169-77.
16. Selvarajan S, Tan SY, Sii LH, Tan PH. c-erbB-2 (HER-2/neu) immunohistochemistry in invasive breast cancer: is there concordance between standard sections and tissue microarrays? Pathology 2006;38(4):316-20.
17. Faratian D, Kay C, Robson T, Campbell FM, Grant M, Read D, et al. Automated image analysis for high-throughput quantitative detection of ER and PR expression levels in large-scale clinical studies: the TEAM Trial Experience. Histopathology 2009;55(5):587-93.
18. Escobar J, Astudillo A, Menéndez P, Belyakova E. Aplicación de los Tissue Microarrays en el estudio inmunohistoquímico de los tumores. Rev Esp Patol 2006;39(1):11-7.
Recibido: Octubre de 2014
Aceptado: Diciembre de 2014