Introducción
La seguridad sanitaria mundial se ha convertido en una prioridad internacional en el último decenio, tras el reconocimiento de que las enfermedades infecciosas no conocen fronteras en un mundo caracterizado por poblaciones cambiantes y la considerable expansión de los viajes internacionales.1 Ésta ha enfrentado la emergencia de un nuevo coronavirus, perteneciente a una familia de virus cuyos miembros generalmente causan infecciones leves del tracto respiratorio superior y algunos de ellos pueden conducir a infecciones graves del tracto respiratorio inferior, como el Síndrome Respiratorio del Medio Oriente (MERS-CoV) y el Síndrome Respiratorio Agudo Severo (SARS-CoV). Este nuevo coronavirus causa enfermedad grave y muerte en humanos.2
En diciembre de 2019, se identificaron en Wuhan (China) una serie de casos de neumonía originados por un nuevo coronavirus, SARS-CoV-2, según el Comité Internacional de Taxonomía de Virus.3
La OMS declaró la COVID-19 como pandemia el 11 de marzo de 2020 cuando la enfermedad se presentaba en 110 países,4 precedido por la connotada declaración de “emergencia de salud pública de interés internacional” (ESPI) de acuerdo con los lineamientos del Reglamento Sanitario Internacional (RSI, 2005).
El comportamiento de esta pandemia contrastó con el SARS-CoV y el MERS-CoV. La COVID-19 mostraba una tasa de letalidad de alrededor de 3,0%, comparada con la de SARS-CoV y MERS-CoV de 10 y 34%, respectivamente.5
A nivel global se acumulan 136.115.434 casos y 2.936.916 defunciones, de los cuales 43% de los casos y 48% de las defunciones han sido aportadas por la región de las Américas.6)
A la fecha de elaboración de este documento, mayo de 2020, Cuba acumulaba un total de 2.262 casos confirmados y 84 fallecidos, ubicándose en el lugar 18 de la región de las Américas. La Isla de la Juventud mostraba 42 casos de COVID-19 con una tasa de incidencia de 50,3 por 105 habitantes.
A propósito de este análisis epidemiológico, cabe resaltar, que entre las principales prioridades para facilitar las intervenciones de salud pública en los pacientes se encuentra el diagnóstico de laboratorio. La realización de la prueba de reacción en cadena de la polimerasa en tiempo real (PCR-RT, por sus siglas en inglés), es recomendada para el diagnóstico del SARS-CoV-2.7 Otros métodos coexisten, tales como las pruebas de marcadores serológicos, definidas por la detección de antígenos y anticuerpos.8
La caracterización de un ensayo, basado en conocer su sensibilidad, especificidad, valor predictivo positivo, valor predictivo negativo y razones de verosimilitud (likelihood ratios) positivo y negativo,9 es necesaria para evaluar su aplicación y la utilidad de la prueba en un contexto determinado, lo que cobra gran importancia en situaciones epidémicas.
Es necesario disponer de pruebas rápidas eficaces con elevada sensibilidad y precisión que permitan un diagnóstico precoz, para un manejo clínico y epidemiológico oportuno. En la Isla de la Juventud, se utilizaron dos pruebas rápidas de detección de anticuerpos durante la fase de transmisión autóctona limitada, sin embargo, no se alcanzaba a predecir inicialmente cuan útiles o acertados podrían ser. Es conocido que se han desarrollado en el marco de la emergencia mundial, varias pruebas rápidas a cargo de diferentes fabricantes y que la capacidad diagnóstica ha sido muy variable, alguna de ellas, no certificadas por la OMS, entonces pudiéramos preguntarnos qué valor tendrían las pruebas con las que contamos, cuán útiles y en qué medida serían capaces de discriminar entre presencia o ausencia de anticuerpos contra el virus; es importante distinguir cuáles de estas pruebas pueden ser de utilidad para los sistemas de salud dependiendo de su diseño, calidad y uso en el contexto de nuestro Municipio. Se realizó un análisis de validación de dos pruebas rápidas para detectar anticuerpos contra el virus SARS-CoV-2, en la Isla de la Juventud, en el período de abril a mayo de 2020.
Materiales y Métodos
Se realizó un estudio descriptivo de corte transversal de evaluación de pruebas rápidas diagnósticas: Wondfo (SARS-CoV-2 antibody test) y Lungene covid-19 IgG/IgM rapid test en comparación con la prueba de PCR-TR, considerada ensayo de referencia.
Descripción de las pruebas involucradas en el estudio
Prueba de referencia
Se siguió el protocolo de PCR-TR realizado en el Laboratorio Nacional de Referencia (LNR) del Instituto de Medicina Tropical Pedro Kourí (IPK) para la detección de SARS-CoV-2; se utiliza la detección del gen E como prueba de primera línea y para estudio de confirmación, la detección del gen RdRp.
Pruebas rápidas
Wondfo SARS-CoV-2 antibody test
Fabricante: Guangzhou Wondfo Biotech (China).
Técnica de detección: Inmunoensayo de flujo lateral.
Lungene covid-19 IgG/IgM rapid test
Fabricante: Hangzhou Lungene Biotech Co Ltd (China).
Técnica de detección: Inmunoensayo de flujo lateral.
Las pruebas rápidas fueron procesadas por personal capacitado, siguiendo las instrucciones del fabricante.
Toma de muestras
Se obtuvieron muestras de sangre capilar que se utilizaron en las pruebas rápidas para la detección de anticuerpos IgM/IgG, entre el día 0 y hasta 30 días de la aparición de los síntomas, y se realizó exudado nasofaríngeo para el diagnóstico molecular por PCR-TR. Se utilizaron los elementos de protección personal recomendados. Las muestras para PCR-TR fueron conservados a -20°C y enviadas al IPK para su procesamiento.
Población objeto de estudio
El alcance del estudio estuvo determinado por todos los casos que se estudiaron con pruebas rápidas y PCR-TR simultáneamente, en el período de abril a mayo de 2020, fase de transmisión autóctona limitada en la Isla de la Juventud, a partir de un universo de 711 registros que cumplían con los criterios descritos a posteriori, quedando constituidas dos muestras en número de 250 cada una, para un total de 500 pacientes e individuos incluidos en la investigación. De ellos 42 casos fueron confirmados al virus SARS-CoV-2 y 458 casos negativos.
Para la construcción de ambas muestras (determinaciones con la prueba rápida Wondfo y la de Lungene), se tomaron como base para la inclusión los siguientes criterios clínico-epidemiológicos:
Simultaneidad de estudios: (prueba rápida/PCR-TR).
Casos confirmados de COVID-19, contactos directos y casos sospechosos (geolocalizados en zonas de transmisión) los cuales incluyeron conceptualmente todas las pruebas rápidas positivas.
Muestra Wondfo: 250 pacientes, de ellos 30 casos confirmados, 153 contactos, 67 sospechosos, 230 asintomáticos y 20 sintomáticos.
Muestra Lungene: 250 pacientes, de ellos 12 casos confirmados, 100 contactos, 138 sospechosos, 205 asintomáticos y 45 sintomáticos.
Análisis estadístico
Inicialmente se realizó una revisión de la base de datos de COVID-19 del Departamento de Vigilancia en Salud de la Isla de la Juventud. Se emplearon resúmenes gráficos y tablas según pertinencia para cada variable. El análisis estadístico tuvo por objeto describir los estimativos puntuales y por intervalos de 95% de las características operativas de las pruebas con respecto al ensayo de referencia: sensibilidad, especificidad, índice de validez, valores predictivos, razones de verosimilitud e índice de Youden para cada prueba rápida, así como la comparación de las mismas y su rendimiento global, utilizando para ello la curva característica de función del receptor (ROC); se realizó además prueba de homogeneidad de áreas considerándose significativo p<0,05.
Se analizaron los indicadores de validación en diferentes escenarios para casos sintomáticos, utilizando tres intervalos de tiempo para cada prueba rápida.
Igualmente se evaluó la concordancia por consistencia entre las diferentes pruebas convencionales que se reportaron mediante índices de kappa. El análisis de datos se llevó a cabo a través del programa estadístico Epidat.
Para evaluar la calidad de las pruebas en función de la razón de verosimilitud se utilizó la siguiente escala:
Razón de verosimilitud positiva: >10 (excelente), entre 5 y 10 (buena), entre 5 y 2 (regular), <2 (inútil).
Razón de verosimilitud negativa: entre 0,5 y 1,0 (inútil), entre 0,2-0,5 (regular), entre 0,1 y 0,2 (bueno), < 0,1 (excelente).10
Clasificación del índice kappa de Cohen y grado de concordancia:11
<0,00 (no acuerdo); 0,00-0,20 (escasa); 0,21-0,40 (regular); 0,41-0,60 (moderada); 0,61-0,80 (substancial); 0,81-1,00 (casi perfecta).
Resultados
El alcance de la investigación quedó marcado por 500 individuos estudiados de manera simultánea con PCR-TR y prueba rápida, correspondiendo 250 individuos para cada prueba rápida explorada.
Los resultados obtenidos al emplear la prueba Wondfo se muestran en la Tabla 1. De un total de 250 muestras evaluadas, se obtuvieron como verdaderos positivos dos muestras, verdaderos negativos 209, falsos positivos 11 y falsos negativos 28 muestras respecto al PCR-TR; mientras que los resultados al emplear la prueba Lungene datan de 250 muestras evaluadas, obteniéndose como verdadero positivo una muestra, como verdaderos negativos 202, falsos positivos 36 y falsos negativos 11 respecto al PCR-TR.
Tabla 1 Tabla de contingencia para el cálculo de indicadores de validación de pruebas rápidas Wondfo y Lungene.
| PCR-TR | |||
| Prueba rápida Wondfo | Resultados positivos | Resultados negativos | Total |
| Resultados positivos | 2 | 11 | 13 |
| Resultados negativos | 28 | 209 | 237 |
| Total | 30 | 220 | 250 |
| PCR-TR | |||
| Prueba rápida Lungene | Resultados positivos | Resultados negativos | Total |
| Resultados positivos | 1 | 36 | 37 |
| Resultados negativos | 11 | 202 | 213 |
| Total | 12 | 238 | 250 |
Como se aprecia en la Tabla 2, la sensibilidad resultó muy baja para ambas pruebas, mientras que la especificidad lograda para la prueba Wondfo se catalogó como muy buena, definida por el 95% (IC 95 %=91,89-98,11). El índice de validez no marcó grandes diferencias entre ambas pruebas. Los valores predictivos positivos evidenciaron una disminución respecto a los valores predictivos negativos, no obstante, es importante resaltar que la prueba Wondfo alcanzó el mayor valor predictivo positivo. Se puede estimar entonces una probabilidad de un 15,3% de infección viral dado que el ensayo resulte positivo utilizando la prueba Wondfo y un 2,7% de probabilidad para la prueba Lungene. Si por el contrario el ensayo es negativo existirá una probabilidad de 88,1% y 94,8% respectivamente de no existir infección viral.
La probabilidad de tener infección viral dado que la prueba resulte positiva se incrementará 1,3 veces utilizando la prueba Wondfo (IC95%=0,31-5,73) y 0,5 veces para Lungene (IC95%= 0,08-3,69); mientras que la probabilidad de no existencia de infección viral dado que la prueba sea negativa se reduce a 0,98 (IC95%=0,89-1,09) y 1,08 (IC95%=0,90-1,29) respectivamente para ambas pruebas.
El índice de Youden mostró resultados del orden de 0,02 (IC95%= -0,08-0,11) en el caso de la prueba Wondfo y para la prueba Lungene de -0,07 (IC95 %= -0,23-0,09).
Tabla 2 Validación de pruebas rápidas. Isla de la Juventud, abril-mayo de 2020.
| Pruebas rápidas | ||||
|---|---|---|---|---|
| Criterios de validación | Wondfo SARS-CoV-2 Antibody test (n=250) | Lungene Covid-19 IgG/IgM rapid test (n=250) | ||
| Sensibilidad | 6,6 (0,00-17,26) | 8,3 (0,00-28,14) | ||
| Especificidad | 95,0 (91,89-98,11) | 84,8 (80,11-89,64) | ||
| Índice de validez | 84,4 (79,70-89,10) | 81,2 (76,16-86-24) | ||
| VPP | 15,3 (0,00-38,84) | 2,70 (0,00-9,28) | ||
| VPN | 88,1 (83,87-92,51) | 94,8 (91,63-98,04) | ||
| LR+ | 1,3 (0,31-5,73) | 0,55 (0,08-3,69) | ||
| LR- | 0,98 (0,89-1,09) | 1,08 (0,90-1,29) | ||
| Índice Youden | 0,02 (-0,08-0,11) | -0,07 (-0,23-0,09) | ||
VPP: valor predictivo positivo. VPN: valor predictivo negativo. LR+: Razón de verosimilitud positiva. LR-: Razón de verosimilitud negativa. (..) IC 95%
Atendiendo a estratificación según intervalos de tiempo utilizando los casos sintomáticos, la prueba rápida Wondfo exhibe lo siguiente (Tabla 3):
De 1 a 7 días, se incluyeron 10 casos para los que se determinó: verdadero positivo (1), verdadero negativo (7), falsos positivos (1), falsos negativos (1); por lo que se alcanzó un 50% de sensibilidad y valor predictivo positivo, mientras la especificidad y el valor predictivo negativo quedaron marcados por un 87,5%.
De 8 a 14 días, se incluyeron 6 casos para los que se determinó: verdadero positivo (0), verdadero negativo (5), falsos positivos (1), falsos negativos (0); por lo que se alcanzó un 0% de sensibilidad y valor predictivo positivo, mientras la especificidad quedó marcada por un 83% y el valor predictivo negativo exhibe un 100%.
De 14 días y más, se incluyeron cuatro casos para los que se determinó: verdadero positivo (0), verdadero negativo (4), falsos positivos (0), falsos negativos (0); por lo que se alcanzó un 0% de sensibilidad y valor predictivo positivo, mientras la especificidad y el valor predictivo negativo exhiben un 100%.
En el caso de la prueba rápida Lungene se obtuvo (Tabla 3):
De 1 a 7 días, se incluyeron 37 casos para los que se determinó: verdadero positivo (0), verdadero negativo (30), falsos positivos (5), falsos negativos (2); por lo que se alcanzó un 0% de sensibilidad y valor predictivo positivo, mientras la especificidad quedó marcada por un 100% y el valor predictivo negativo exhibe un 93%.
De 8 a 14 días, se incluyeron cinco casos para los que se determinó: verdadero positivo (0), verdadero negativo (4), falsos positivos (1), falsos negativos (0); por lo que se alcanzó un 0% de sensibilidad y valor predictivo positivo, mientras la especificidad quedó marcada por un 80% y el valor predictivo negativo exhibe un 100%.
De 14 días y más, se incluyeron tres casos para los que se determinó: verdadero positivo (0), verdadero negativo (0), falsos positivos (0), falsos negativos (0); por lo que se alcanzó un 0% de sensibilidad y valor predictivo positivo, mientras la especificidad y el valor predictivo negativo exhiben un 100%.
Tabla 3 Validación de pruebas rápidas según intervalos de tiempo utilizando casos sintomáticos. Isla de la Juventud abril-mayo de 2020.
| Prueba rápida Wondfo | ||||
| Intervalos de tiempo | Sensibilidad | Especificidad | VPP | VPN |
| 1 a 7 días | 50,0 | 87,5 | 50,0 | 87,5 |
| 8 a 14 días | 0,0 | 83,0 | 0 | 100 |
| 14 días y más | 0,0 | 100 | 0 | 100 |
| Prueba rápida Lungene | ||||
| Intervalos de tiempo | Sensibilidad | Especificidad | VPP | VPN |
| 1 a 7 días | 0,0 | 100,0 | 0 | 93,0 |
| 8 a 14 días | 0,0 | 80,0 | 0 | 100 |
| 14 días y más | 0,0 | 100,0 | 0 | 100 |
VPP: valor predictivo positivo. VPN: valor predictivo negativo.
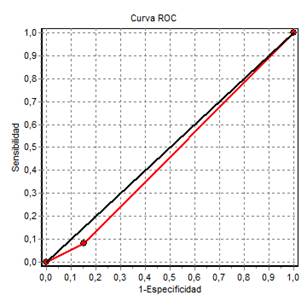
Las Figuras 1 y 2 exhiben las curvas ROC de las pruebas rápidas en estudio, observándose que ambas son no discriminativas, ya que coinciden o quedan por debajo de la línea de no discriminación; así lo demuestra, además, el área bajo la curva ROC para la prueba rápida Wondfo que fue 0,50 (IC95%=0,46-0,55) y para la prueba Lungene de 0,46 (IC95%=0,38-0,55). La prueba de homogeneidad de áreas bajo la curva no mostró diferencia significativa (p<0,39).
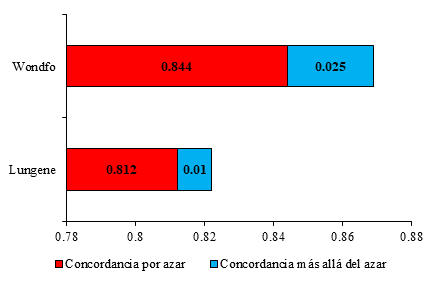
El índice kappa para la prueba Wondfo respecto a la PCR-TR fue de 0,025; mientras que para la prueba Lungene, de 0,010, de manera que para ambas la concordancia es escasa (Fig. 3).
Discusión
El mundo mira hoy, con preocupación y temor, la evolución de esta emergencia sanitaria mundial. La aparición de una nueva enfermedad infecciosa supone siempre una situación compleja, especialmente si lo hace como una pandemia de extensión o gravedad significativa. Contar con una prueba con capacidad diagnóstica adecuada servirá para realizar un mejor y más oportuno manejo clínico y epidemiológico en diferentes escenarios, de manera que permita reducir las complicaciones de la enfermedad e interrumpir la transmisión y propagación de la misma, limitando la afectación a grandes poblaciones.12
Las pruebas rápidas de anticuerpos ofrecen un resultado preliminar evidenciando una banda característica para un resultado positivo, los resultados negativos no excluyen infección por SARS-CoV-2 y no pueden utilizarse como la base única para la toma de decisiones. Los ensayos de detección de anticuerpos apoyan al diagnóstico y son útiles en los estudios de investigación epidemiológica,8 pudiendo evaluar a trabajadores de la salud, los cuales se exponen en su labor diaria, conocer si tienen anticuerpos o hacer seguimiento de pacientes e investigar cuánto tiempo duran los anticuerpos. Realizadas en poblaciones, pueden convertirse en una herramienta que ayudará a tener una dimensión real de la propagación del virus, rastrear mejor las cadenas de transmisión de la enfermedad, detectar a los individuos asintomáticos o a los que en algún momento tuvieron el virus.
Teniendo en cuenta la cinética de la respuesta inmune en pacientes con infección por SARS-CoV-2, se considera que el punto para usar pruebas serológicas son 14 días a partir del inicio de los síntomas, a partir de ese momento se ha documentado que hasta la mitad de los pacientes infectados ya podrían tener estos anticuerpos.12
En un estudio realizado por otros autores, se evaluó el perfil inmunológico de los pacientes con infección por SARS-CoV-2, demostrando que a partir del día 7 de los síntomas la mayoría de los casos evidenció un aumento importante de la IgM en un valor que es detectable.13
En el presente estudio se exhiben valores de sensibilidad y valores predictivos positivos muy bajos según estratificación por intervalos de tiempo utilizando casos sintomáticos, sin embargo, es perfectamente visible el antagonismo entre sensibilidad y especificidad, donde mejora sustancialmente la especificidad, siendo perfecta para el intervalo de 14 días y más, en la prueba Wondfo y de 1 a 7 días, y 14 días y más para Lungene; mientras que los valores predictivos negativos alcanzan un valor perfecto a partir del 8vo día en ambas pruebas.
Según la Sociedad Española de Inmunología, tras la infección se generan anticuerpos de tipo IgM y aunque empiezan a elevarse aproximadamente 5-7 días tras la infección, los ensayos los detectan mejor a los 8-14 días. Pasados 15-21 días aparecen los anticuerpos de tipo IgG.14
Otros autores exhiben en su estudio de validación de la prueba, AllTest COVID-19 IgG/IgM rapid test, una especificidad perfecta y una sensibilidad de 88,0%. Las determinaciones fueron realizadas en pacientes sintomáticos con 14 días de evolución con previa PCR positiva.15
Varios estudios confirman la generación de anticuerpos neutralizantes contra SARS-CoV-2, aunque aún no se ha determinado con exactitud cuándo comienzan a elevarse tras el inicio de la clínica y la duración de la inmunidad.16
Es importante tener en cuenta que cuando la enfermedad es grave y las consecuencias de no detectar un caso pueden ser fatales, debe primar la sensibilidad sobre la especificidad, éstos son dos indicadores inherentes a la prueba diagnóstica,17) no de la prevalencia del fenómeno que se estudia.
En el contexto actual, no se obtuvieron resultados acordes a lo planteado anteriormente, asumiendo que la capacidad de las pruebas rápidas para detectar los anticuerpos contra el virus, resultantes de la infección viral resultó muy baja, mientras que la capacidad para detectar la ausencia de la infección viral fue adecuada, en el caso de la prueba Wondfo, no así para la prueba Lungene, quedando por debajo de lo esperado. Sin embargo, los fabricantes de ambas pruebas notifican alta sensibilidad y especificidad.18
Los resultados aquí expuestos tampoco guardan relación con lo descrito por el IPK en una validación inicial para la prueba Wondfo, donde exponen una sensibilidad en sangre capilar de 43% y para suero y plasma de un 71%, mientras que la especificidad alcanza un 100% en cualquiera de las muestras analizadas. Una vez estratificado los casos sintomáticos por intervalos de tiempo y evaluado los indicadores de validación, se encuentra una semejanza en cuanto a especificidad para ambas pruebas, mientras que la sensibilidad contrasta en ambas pruebas y en los diferentes intervalos, exceptuando en el intervalo de 1 a 7 días en la prueba Wondfo, obteniendo incluso una sensibilidad similar a la encontrada en el estudio del IPK, si bien eran muy pocos casos, se logró detectar uno de dos.
En general, se han identificado causas objetivas y subjetivas que podrían explicar los valores bajos resultantes en el estudio. Una prueba para anticuerpos no va a detectarlos cuando éstos, por la propia cinética de desarrollo de los mismos en la infección, no estén presentes en las muestras; el 87% de la muestra total (incluye los individuos estudiados con Wondfo y Lungene) resultaron asintomáticos, al tomarse como punto de partida aspectos epidemiológicos relacionados con el momento del contacto para realizar la determinación, un sesgo de memoria pudiera haber influido en el momento ideal para realizar la determinación con éxito.
En el caso de los sintomáticos, representado por el 13% de la muestra total, se pudo observar que en solo el 27,3% de los casos, la prueba rápida fue aplicada en el tiempo en que se espera la elevación de títulos de anticuerpos para ser detectables.
Otra de las cuestiones sumamente importantes, es el hecho de haber utilizado para la toma de muestra la sangre capilar, que aun cuando los fabricantes de las pruebas rápidas analizadas aseguran que es correcto utilizar esta vía de obtención de fluido corporal, ya se habían avalado mejores resultados en suero y plasma por el IPK, tal como se describe anteriormente.
Si bien las pruebas rápidas exhiben falsos negativos, también ocurre con el diagnóstico de PCR-TR, tal y como se describe, se puede experimentar un 29% de falsos negativos. Es importante tener en cuenta que si la muestra contiene cantidades insuficientes del virus para amplificar y detectar con éxito obtendremos un falso negativo, de manera que es probable que la cantidad de virus en un hisopo varíe entre pacientes, el tipo y el momento de la recogida de la muestra.19
Otras cuestiones pueden enfocarse en errores pre-analíticos, que aun cuando no prevalezcan, se deben tener en cuenta. Durante la conservación y transportación de las muestras la cadena de frío es relevante para evitar afectaciones en los resultados. Éstas deben mantenerse refrigeradas (4-8°C) y enviarse al laboratorio donde se procesarán dentro de las 24-72 horas de la toma.20 Las muestras respiratorias en el caso de la Isla de la Juventud, son enviadas al LNR del IPK ubicado en La Habana.
La COVID-19 como enfermedad emergente, con magnitud pandémica, ha puesto a los profesionales a desarrollar habilidades y competencias con las que quizás no contaban antes, tal es el caso de realizar la toma de muestra, donde ha sido necesaria la incorporación de muchos laboratoristas que probablemente no habían trabajado la microbiología, siendo imperioso ejercitar la capacidad de aprendizaje para la formación en esta nueva entidad nosológica con todo lo que ello emprende.21
Vale destacar que entre las personas evaluadas por Lungene contamos con 45 individuos sintomáticos que resultaron negativos a PCR-TR, de ellos 6 fueron positivos a anticuerpos por lo que se clasificaron como falsos positivos, nos preguntamos la posibilidad de haberse visto involucradas estas muestras de PCR-TR en algún fallo del proceso antes descrito.
En el estudio realizado por Li et al se estimaron valores de sensibilidad de 88,66% y de especificidad de 90,63% para la detección de anticuerpos combinados IgG/IgM para SARS-CoV-2. Los autores refieren que la existencia de algunos falsos negativos podría deberse a bajas concentraciones de anticuerpos, variabilidad individual en su producción y la disminución de la concentración de IgM, dado que resulta difícil establecer desde cuando estuvieron infectados los pacientes.22
La probabilidad de que los individuos con una prueba positiva hayan estado infectados resultó baja para ambas pruebas, mientras que la probabilidad de que los individuos con una prueba negativa hayan estado infectados se consideró adecuada, condición que va aparejado de la disminución de la prevalencia de la entidad.10
La razón de verosimilitud positiva resultó muy baja clasificándose como inútil, tomando como partida que alcanza números infinitos; mientras que la razón de verosimilitud negativa fue muy alta, cercana a 1 en Wondfo, e incluso superior a 1 en Lungene, valorándose igualmente de inútil.
El índice de Youden identificó el punto de corte para determinar que la sensibilidad y especificidad más alta conjuntamente, correspondió a la prueba diagnóstica Wondfo; no obstante al realizar el análisis puntual para cada una de ellas y la subsiguiente comparación entre ambas, no se encontró un buen desempeño diagnóstico, quedando demostrado por el resultado del área bajo la curva, que representa la validez global de la prueba; ello sugiere, que el uso de las mismas debe valorarse con cuidado, es importante recordar que muchas pruebas de detección de antígenos y de anticuerpos desarrolladas y usadas a nivel mundial han sido discutidas como pruebas diagnósticas dadas sus limitaciones, sobretodo en cuanto a su baja sensibilidad (tasa de verdaderos positivos) y especificidad (tasa de verdaderos negativos).23 Sumado a ello, el presente estudio muestra una escasa reproducibilidad para las dos pruebas serológicas exploradas, determinada mediante el índice kappa por lo que cualquiera de ellas sería inútil para la detección de anticuerpos resultantes de la infección por SARS-CoV-2. Pese a ello, es importante resaltar que toda la batería de pruebas que se han desarrollado y que se siguen incorporando, basados en alcances cada vez más ricos y promisorios, llevados a cabo por la comunidad científica internacional, son estratégicos para cercar la enfermedad. Vale destacar la utilidad y necesidad de diferentes tipos de pruebas para combatir integral y rápidamente la pandemia.
Conclusiones
La crisis de salud pública a nivel internacional, ha marcado retos desde diferentes ámbitos. Los salubristas cada vez abogan por mejores métodos diagnósticos que ayuden a la detección oportuna de la infección por SARS-CoV-2. El uso de novedosas técnicas es cada vez más frecuente en el escenario de la pandemia, a tal efecto el estudio de validación de las pruebas Wondfo SARS- CoV-2 antibody test y Lungene covid-19 IgG/IgM rapid test, demuestra que las pruebas rápidas exploradas no son válidas, marcado por una muy baja sensibilidad, es importante resaltar que, si la toma de muestra ocurre antes del período de presencia total de IgM/IgG, el riesgo de falsos negativos es elevado.
El valor predictivo positivo y razón de verosimilitud se consideraron inadecuadas tanto negativa como positiva. No se encontró un buen desempeño diagnóstico, quedando demostrado por el resultado del área bajo la curva, que representa la validez global de la prueba.
La especificidad fue valorada como adecuada sobre todo para la prueba Wondfo, sin embargo, esta debe ser interpretada cuidadosamente en el contexto de circulación o ausencia de anticuerpos en sangre.
El análisis de validación en escenarios diferentes de casos sintomáticos arrojó una sensibilidad muy baja y una especificidad elevada, perfecta incluso para ambas pruebas después del 8vo día.
Por otra parte, el grado de concordancia resultó escaso para las dos pruebas respecto al diagnóstico de PCR-TR.