Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Plantas Medicinales
versión On-line ISSN 1028-4796
Rev Cubana Plant Med v.2003 n.2 Ciudad de la Habana Mayo-ago. 2003
Artículos originales
Centro de Investigaciones y Desarrollo de Medicamentos
Estabilidad de extractos fluidos al 70 % de Cymbopogon citratus
Lic. Jorge E. Rodríguez Chanfrau1, Lic. Leticia Fuentes2, Lic. Zenia Pardo Ruiz2 y Lic. Mayda Garma2
Resumen
Se estudió la estabilidad de 6 lotes de extractos fluidos al 70 % de Cymbopogon citratus. Para ello se valoró el comportamiento de las muestras ante el calor, la luz, pH extremos, y en "vida de estante". En todos los casos se analizaron en el tiempo las características organolépticas y el contenido de citral, por ser este componente el mayoritario en el aceite esencial presente en el extracto. Los resultados mostraron que a medida que aumentó el tiempo de exposición de la muestra al calor, la concentración inicial de citral tendió a disminuir alrededor de un 40%. La luz también provocó degradación del citral que disminuyó en aproximadamente un 30 %. Los estudios del comportamiento de las muestras en condiciones extremas de pH, demostraron que en ambos casos, pH ácido y básico, el citral sufrió una degradación total. Los estudios por el método de "vida de estante", demostraron que los extractos sólo cumplieron con los indicadores de calidad hasta los 3 meses de elaborados, siempre que se conservaron en lugares frescos y protegido de la luz.
DeCS: Plantas Medicinales/química; Plantas Medicinales/fisiología; Farmacognosia; Control de Calidad; Cromotografía.
Summary
The stability of 6 batches of fluid extracts of Cymbopogon citratus 70 % was studied. The behavior of the samples exposed to heat, light and extreme pH and in shelf life was assessed. The organoleptic characteristics and the content of citral, which is the largest component in the essential oil present in the extract, were analyzed in time in every case. The results showed that as the time of exposure of the sample to heat was higher, the initial concentration of citral tended to decrease at about 40 %. Light also produced degradation of citral that dropped by approximately 30 %. The studies on the behavior of the samples under extreme conditions of pH proved that in both cases, acid and basic pH, citral suffered a total degradation. The studies conducted by the shelf life method demonstrated that the extracts only fulfill the quality parameters up to the 3rd month provided that they are kept in cool places and protected from light.
Subject headings: Plants, Medicinal/chemistry; Plants, Medicinal/physiology; Pharmacognosy; Quality Control; Chromatography.
La especie Cymbopogon citratus (DC). Stapf (Gramineae), conocida popularmente como Caña santa es una planta perenne que generalmente no florece y se encuentra muy disponible en el país. Se han realizado diversos estudios relacionados con la agrotecnia de la planta así como otros específicos para extractos fluidos y acuosos, como son estudios sobre la actividad antiinflamatoria, analgésica, antiasmática, diurética, antiespasmódica, antimicrobiana y de toxicidad con la inclusión de la genotoxicidad.
Las investigaciones sobre la caracterización química de esta especie han permitido aislar, a partir de las partes aéreas de la planta, sustancias no volátiles entre las cuales se pueden mencionar flavonoides, ácido cafeico, fructuosa y sacarosa.1 Por otro lado se ha publicado que entre los constituyentes volátiles del aceite esencial de dicha planta se encuentran terpenos como geraniol y citronenol.2 Se ha logrado identificar en algunas especies foráneas hasta el 89 % (34 compuestos) de los componentes del aceite y se han informado como mayoritarios el geraniol (39,8 %) y el nerol (32 %).3
Estudios realizados con aceite obtenido a partir de la especie cubana demostraron que el color del mismo varía de amarillo a carmelita rojizo, con fuerte olor a limón, tiene una densidad relativa aproximadamente igual a 0,8861 y un índice de refracción de alrededor de 1,4888. El contenido de citral en el aceite oscila alrededor del 88 % y el mismo es sensible a la exposición de la luz y del aire, lo que provoca con el paso del tiempo que aumente su densidad (Guerra M, Rodríguez M, Ramos I, Garcia G, Llerena C. Antimicrobial activity of Cymbopongo citratus (DC). Stapf oil and cream, en prensa). En esta especie han sido detectados además, compuestos como geraniol, linalol, metilheptona, citronelol, limoneno, diterpenos, entre otros.4
Se conoce además, que el aceite esencial de esta especie vegetal es el responsable de los múltiples usos que popularmente se le atribuyen a esta planta, entre ellos su acción antimicrobiana. En la literatura se encuentran publicaciones que plantean actividad del aceite sobre gérmenes Gram positivos y negativos, sin embargo, algunos autores señalan mayor sensibilidad a los últimos mencionados.5,6 En estudios realizados por Guerra y colaboradores con aceite obtenido a partir de la planta cubana, se alcanzaron resultados que difieren con lo planteado en la literatura. El aceite obtenido de esta planta tiene acción bactericida excepto para S. aureus que fue bacteriostática y los microorganismos Gram positivos resultaron los más sensibles. La especie más sensible fue B. subtilis y la resistente, P. aeruiginosa (Guerra M, Rodríguez M, Ramos I, Garcia G, Llerena C. Antimicrobial activity of Cymbopongo citratus (DC). Stapf oil and cream, en prensa).
Se conoce que diferencias genéticas entre algunas cepas de Cymbopogon ejercen gran influencia en la actividad antibacteriana del aceite esencial.2 Esta acción se atribuye al citral, particularmente al geraniol (alfa citral) y al nerol (beta citral). También se plantea que el mirceno aislado no muestra actividad pero que incrementa la misma cuando se mezcla con los compuestos citados.6-8
En el Centro de Investigación y Desarrollo de Medicamentos de Cuba (CIDEM), se está desarrollando un proyecto de investigación, que tiene como objetivo fundamental la validación de la acción antimicrobiana de algunas especies de plantas medicinales cubanas a las cuales popularmente se le atribuye esta actividad. Entre estas plantas se encuentra el Cymbopogon citratus, y como parte de estas investigaciones se realizó el estudio de la estabilidad de extractos fluidos al 70 % que fue el objetivo de este trabajo.
MÉTODOS
Se emplearon muestras de extractos fluidos al 70 % de Cymbopogon citratus, correspondientes a los lotes 1, 2, 3, 4, 5 y 6, elaborados por repercolación en la Estación Experimental Dr. Juan Tomás Roig, perteneciente al CIDEM, según procesamiento tecnológico desarrollado por Fuentes y colaboradores en 1999.9
El control de la calidad de dichos lotes se realizó según la técnica de análisis desarrollada también por Fuentes y colaboradores en 1999.10
Para los estudios de estabilidad, se valoró el comportamiento de las muestras ante el calor, la luz y pH extremos y se analizaron las características organolépticas y el comportamiento del citral, por ser este el elemento mayoritario del aceite esencial presente en el extracto. Para ello se empleó el método de cromatografía en placa fina para determinación semicuantitativa del citral desarrollado por Fuentes y colaboradores en 1999.10 La fase móvil fue tolueno-acetato de etilo (4:1) y la fase estacionaria, silicagel 60 F254; la solución reveladora fue de 2,4 dinitrofenilhidrazina en ácido clorhídrico 2 mol/L. A la solución reveladora previamente se le determinó la especificidad y la linealidad, según las exigencias actuales.11
Para la determinación de la especificidad, se tomó muestra de estándar de referencia de citral y se degradó a 45 ºC durante 7 días. Transcurrido ese tiempo, se aplicó el método de determinación semicuantitativa y se comparó con muestra de estándar de referencia sin degradar.10
Para determinar la linealidad del método, se preparó una curva de calibración de citral, con concentraciones que oscilaron entre los 0,05 y 0, 5% y se aplicó el procesamiento tecnológico citado.10
Para valorar la influencia del calor sobre el extracto fluido, se colocaron muestras correspondientes al lote 4, a temperatura de 45 ºC durante 30 días y se realizaron análisis de la misma a los 7, 15 y 30 días de comenzada la experiencia.
Para estudiar el comportamiento del principio activo frente a condiciones extremas de pH, se tomaron 50 mL de extracto fluido correspondiente al lote 4 y se mezclaron con 50 mL de solución de ácido clorhídrico 0,1 mol/L o solución de hidróxido de sodio 0,1 mol/L y se dejaron en reposo durante 72 h. Transcurrido ese tiempo, se procedió a realizar el análisis correspondiente de las mismas.
Para estudiar la influencia de la luz natural sobre los extractos fluidos al 70 %, se colocaron muestras del lote 4, en frascos transparentes y se expusieron a la luz natural durante 30 días.
Para determinar la fecha de vencimiento del extracto fluido, se realizó el estudio de estabilidad por "vida de estante". Para ello se colocaron las muestras en frascos de color ámbar, a temperatura ambiente y se realizaron determinaciones a tiempo 0, 1, 3 y a los 6 meses de comenzado el estudio. Se estudiaron todas las muestras correspondiente a los lotes seleccionados.
RESULTADOS
Los resultados del control de la calidad de los extractos estudiados, se muestran en la tabla 1.
Tabla 1. Resultados del análisis inicial de cada lote
| Lotes | |||||||
| Indicadores | 1 | 2 | 3 | 4 | 5 | 6 | Límite |
| Fecha fabricación | 10/97 | 1/98 | 2/98 | 3/98 | 5/98 | 7/98 | |
| Características organolépticas | Responde | Responde | Responde | Responde | Responde | Responde | Líquido oscuro de color pardo rojizo, con fuerte olor a cítrico. |
| Identificación de citral | Responde | Responde | Responde | Responde | Responde | Responde | |
| pH | 5,83 | 5,34 | 5,60 | 5,63 | 5,55 | 5,52 | De 5,0 a 6,0 |
| Índice de refracción | 1,373 | 1,373 | 1,376 | 1,377 | 1,377 | 1,375 | De 1,300 a 1,400 |
| Densidad | 0,9254 | 0,9200 | 0,9193 | 0,9290 | 0,9140 | 0,9260 | De 0,8500 a 1,0000 |
| Contenido alcohólico | 59,9 % | 59,1 % | 60,9 % | 60,9 % | 59,1 % | 55,5 % | No menos de 55,0 % |
| Sólidos Totales | 7,74 % | 6,77 % | 7,93 % | 9,52 % | 6,73 % | 7,97 % | No menos del 5,0 % |
| Análisis capilar | Responde | Responde | Responde | Responde | Responde | Responde | |
| Contenido de aceite | 0,15 % | 0,20 % | 0,21 % | 0,24 % | 0,14 % | 0,29 % | No menos del 0,10% |
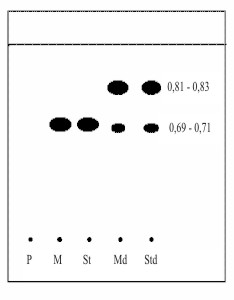
En la figura 1 se muestran los resultados alcanzados para el estudio de la especificidad del método propuesto Se observa la mancha característica del principio activo así como las manchas de los productos de degradación.
Fig 1. Cromatograma del Placebo (P), muestra (M), estandar de citral (st), muestra degradada (Md) y estandar degradado (Std).
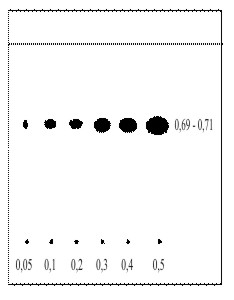
La figura 2 muestra los resultados de la curva de calibración desarrollada como parte del método de análisis propuesto. Se observó un aumento lineal en el tamaño y el color de las manchas, a medida que aumentó la concentración de citral. Todas las manchas tienen similares Rf, entre 0,69 y 0,7. No se detectaron concentraciones por debajo de 0,05 %.
Fig 2. Curva de calibración
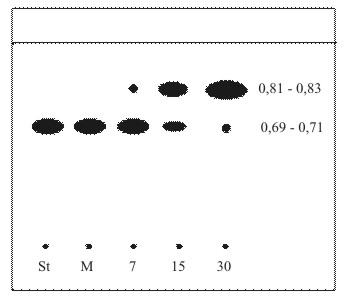
En la tabla 2 y figura 3, se pueden observar los resultados del estudio de la influencia del calor sobre el principio activo. A medida que aumentó el tiempo de exposición de la muestra al calor, la concentración inicial de citral en el aceite esencial tendió a disminuir (alrededor de un 40%) y se observó una disminución en el tamaño e intensidad de la mancha de citral y la aparición e intensificación de la mancha correspondiente al posible producto de degradación.
Fig 3. Cromatograma correspondiente al estudio de la influencia del calor.
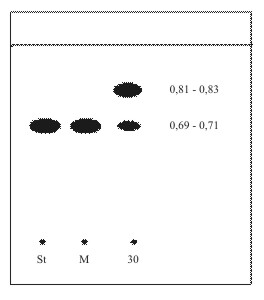
La influencia de la luz sobre dicho principio activo, se observa en la tabla 2 y figura 4. Al cabo de los 30 días de estar expuesta la muestra a la luz natural se comprobó que la concentración de citral en dicho extracto comenzó a disminuir (alrededor de un 30 %) y apareció la mancha correspondiente al posible producto de degradación.
Tabla 2. Resultados del estudio del calor y la luz
| Calor | ||||
| Indicador | Inicio | 7 días | 15 días | 30 días |
| Características organolépticas | Responde | Responde | Responde | Responde |
| % de citral | 40 - 50 | 20 - 30 | 10 - 20 | 5 - 10 |
| Luz | ||||
| Inicio | 30 días | |||
| Características organolépticas | Responde | Responde | ||
| % de citral | 40 - 50 | 10 - 20 | ||
Fig. 4. Cromatograma de la muestra expuesta a la luz durante 30 días.
En medio fuertemente ácido se observó, pasadas 72 h, la aparición de partículas en suspensión y de un precipitado oscuro. La placa de cromatografía demostró que el citral en estas condiciones se degradó totalmente, desapareció la mancha correspondiente al mismo y apareció una mancha a Rf entre 0,81 y 0,83, la cual se correspondió con el posible producto de degradación (figura 5).
Fig.5. Cromatograma de la muestra colocada en diferentes medios de ph. Estándar de citral (St), muestra (M), muestra en medio ácido (A), muestra en medio ácido con calor (Ac) muestra en medio básico (B) y muestra en medio básico con calor (Bc).
En medio básico ocurrió algo similar, con la diferencia de que en la solución no se observaron las partículas y el precipitado.
El estudio de estabilidad por "vida de estante" mostró que hasta los 3 meses el producto cumplió con los indicadores de calidad exigidos por la técnica de análisis, mientras que a los 6 meses, la mancha de citral prácticamente desapareció y se observó intensamente la mancha característica del posible producto de degradación.
DISCUSIÓN
El control de la calidad de los extractos estudiados indicó que todos cumplieron con los indicadores de calidad exigidos por la técnica del fabricante.11
Los estudios de la especificidad del método de análisis propuesto, mostraron que el citral empleado como estándar de referencia, presentó una mancha a un Rf entre 0,69 y 0,71, la cual adquirió una coloración naranja al revelarse con 2,4 dinitrofenilhidrazina en solución de ácido clorhídrico 2 mol/L.12
Por otro lado, se observó que al degradarse el mismo apareció una mancha de color amarillo naranja, a un Rf entre 0,81 y 0,83, que se separó completamente del citral, con el sistema de solventes y reveladores empleado en este trabajo (figura 1). Estos resultados permitieron afirmar que el método de análisis propuesto es especifico para la identificación y separación del citral y sus productos de degradación.
Los resultados obtenidos en la curva de calibración desarrollada con citral con el mismo sistema anterior, afirmaron que el método empleado cumplió con el parámetro de linealidad por lo que se puede usar como método semicuantitativo en el estudio de estabilidad de los extractos fluidos al 70 % de Cymbopogon citratus.
Los resultados del estudio de estabilidad acelerado, indicaron que el producto sufrió variaciones importantes por la influencia de la temperatura, la luz y el medio, por lo que se debe preservar adecuadamente.
La estabilidad por "vida de estante", confirmó que al cabo de los 3 meses, en las condiciones de trabajo propias de un laboratorio de investigaciones, el producto se degradó de forma importante por lo que perdió los indicadores de calidad establecidos.
De acuerdo con los resultados obtenidos en este estudio, se puede resumir que el extracto fluido al 70 % de Cymbopogon citratus, sólo cumplió con los indicadores de calidad hasta los 3 meses, por lo que se propone este tiempo como fecha de vencimiento y se recomienda almacenarse en lugares frescos y protegido de la luz.
Referencias Bibliográficas
- De Matouscheck BV, Stahl-Biskup E. Phytochemical study of nonvolatile substances from Cymbopogon citratus (DC.) Stapf (Poaceae). Pharm Acta Helv 1991; 66:9-10.
- Pattnaik S, Subramayam VR, Kole CR, Sahoo S. Antibacterial activity of oils from Cymbopogon inter and intraspecific differences. Microbios 1995;84(241):239-45.
- Vanden DB, Vlietinck AJ. Screening for antibacterial and antiviral agents from higher plants. Methods in Plant Biochemestry 1991;6:47-69.
- II Idrissi A, Bellakhdar J, Caniqueral S, Iglesias J, Vila R. Composition of the essential oil from citronnelle Cymbopogon citratus DC. Staft acclimatized in Morocco. Plant Med Phytother 1993;26(4):274-7.
- Roig TM. Plantas medicinales, aromáticas o venenosas de Cuba. La Habana: Ed. Ciencia y Técnica. Instituto del Libro; 1974.
- Onawunmi GO, Ogunlana EO. Study of the antibacterial activity of the essential oil of lemongrass (Cymbopogon citratus (DC.) Staft. Int J Crude Drug Res 1986;24:64-8.
- Syed M, Khalid MR, Chaudhang FM. Essential oil of gramineae family having antibacterial activity. Part I. (Cymbopogon citratus), (C. martinii) y (C. jawarancuso) oils. Pakistan J Scientif Indus Res 1990;33 (12):529-31.
- Onawunmi GO, Yisak WA, Ogunlana EO. Antibacterial constituents in the essential oil of Cymbopogon citratus (DC.) Staft. J Ethnopharmacol 1984;(12):279-86.
- Fuentes L, Garma M, Sánchez E. Proceso de obtención de extractos fluidos al 70 % de Cymbopogon citratus. Informe final. San Antonio de los Baños (La Habana): Estación Experimental Dr. "Juan Tomás Roig", Departamento de Estabilidad, 1999.
- Fuentes L, Pardo Z, Rodríguez Chanfrau JE. Cimbopogon citratus. Extracto fluido al 70 %. Técnica de análisis. Informe final. San Antonio de los Baños (La Habana): Estación Experimental Dr."Juan Tomás Roig", Departamento de Estabilidad, 1999.
- Union States Pharmacopoeia 25 Washintong DC.1996.
- Stahl E. Thin-Layer Chromatography. 2nd ed. Berlin: Ed. Springer-Verlag; 1969.
Recibido: 19 de marzo del 2002. Aprobado: 10 de junio del 2002.
Lic. Jorge E. Rodríguez Chanfrau. Centro de Investigación y Desarrollo de Medicamentos. Ave. 26 No. 1605. Nuevo Vedado. La Habana, CP10600, Cuba. E-mail:cidem@infomed.sld.cu
1 Master en Química Farmacéutica. Investigador auxiliar.
2 Licenciada en Farmacia. Investigadora Aspirante.