Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Plantas Medicinales
versión On-line ISSN 1028-4796
Rev Cubana Plant Med v.10 n.3-4 Ciudad de la Habana jul.-dic. 2005
Centro de Investigación y Desarrollo de Medicamentos (CIDEM)
Efecto de un extracto oleoso de rizoma de Zingiber officinale Roscoe (MVZ) sobre la anafilaxia pasiva cutánea y el espasmo bronquial inducido por histamina
Lic. Yanier Núñez Figueredo,1 Dra. Juana Tillán Capó,2 Téc. Carmen Carrillo Domínguez,3 Dra. Odila A. Olivares Guerra4 y Téc. Ramona Núñez Gomero5
Resumen
Para demostrar las propiedades antialérgicas conferidas al MVZ, se estudió su posible influencia sobre los mediadores anafilácticos y el espasmo bronquial inducido por histamina. En la prueba de anafilaxia pasiva cutánea se emplearon ratas Wistar machos a las cuales se les administró el MVZ a la dosis de 6,5 mL/kg (4,8 g de ácidos grasos/kg) por vía oral durante 10 días, se empleó como control positivo ketotifeno 3 mg/kg, la intensidad de la anafilaxia se determinó cuantificando la cantidad de azul de Evans extravasado. El efecto protector del espasmo bronquial se determinó en cobayos Hartley machos, induciendo brococonstricción por administración intravenosa de histamina y determinando la presión bronquial; la dosis del producto empleada fue la misma que para el ensayo anterior. Como resultado de este trabajo se encontró que el MVZ inhibió la anafilaxia pasiva cutánea en ratas y la broncoconstricción inducida por 15 µg/kg de histamina por vía endovenosa. Los resultados obtenidos sugieren que el MVZ pudiera ser efectivo en el tratamiento profiláctico de enfermedades alérgicas tipo I como el asma bronquial, lo cual justificaría su uso popular en pacientes asmáticos.
Palabras clave: Zingiber officinale Roscoe, MVZ, anafilaxia pasiva cutánea, espasmo bronquial, histamina.
La búsqueda de nuevos principios activos con actividad antialérgica, obtenidos a partir de productos naturales, es de vital importancia para incorporarlos al tratamiento de diversas enfermedades muy frecuentes en la población actual.
El MVZ es el resultado de la extracción oleosa del rizoma de Zingiber officinale Roscoe (Zingiberaceae) conocido popularmente como jengibre. Dicha planta es originaria de Asia tropical, cultivada en las regiones tropicales y subtropicales, de hasta 90 cm, con rizoma horizontal, hojas linear-lanceoladas de 18-28 cm, sentadas acuminadas. Pedúnculos de 15-25 cm, espigas elipsoideas de 4-6 cm; brácteas suborbiculares a obovadas, vellosas; corola verde-amarillenta, el tubo de 2cm. Entre los usos más significativos conferidos a dicha planta se encuentra su empleo en el tratamiento de la diarrea, vómitos, gastralgia, indigestión, gripe, tos ferina, fiebre, catarro, resfriado, entre otras afecciones.1 Informaciones más recientes aportadas por la población mexicana, recomiendan el uso del MVZ en el tratamiento de diferentes enfermedades alérgicas, dentro de las que se encuentra con mayor significación su empleo en el tratamiento del asma bronquial.
De acuerdo al uso popular del MVZ en pacientes asmáticos se decidió evaluarlo sobre las reacciones de hipersensibilidad tipo I, mediante el ensayo de anafilaxia pasiva cutánea, basada en la administración intradérmica del anticuerpo seguida de la administración intravenosa del antígeno (fenómeno de Arthus)2-4 y su comportamiento ante los eventos provocados por la histamina después de interactuar con sus receptores H1 a nivel bronquial. 5
Métodos
Sustancia de prueba
El MVZ es un extracto oleoso de Z. officinale, número de herbario 4595 de la Estación Experimental de Plantas Medicinales "Dr. Juan Tomas Roig", elaborado a partir del rizoma de la planta fresca, en una proporción solvente/material vegetal de 1: 0,6 (PCT/CU02/00008).
Es un producto semisólido untuoso, de color amarillo y olor característico agradable y sabor fuerte aromático. Es libremente soluble en éter de petróleo ligero (40º-60º) y ciclohexano, soluble en una mezcla de ácido acético-cloroformo, cloroformo-metanol e insoluble en metanol y agua.
Algunas de sus características son las siguientes:
| Perdida por desecación | 0,4 % |
| Peso especifico | 0,9095 g/mL |
| Índice de refracción (40º) | 1,462 |
| Cenizas sulfatadas | 0,3 % |
| Índice de acidez | 0,728 |
| Índice de yodo | 0,3 |
| Índice de saponificación | 227,9º |
| Ácidos grasos | 73,4 % |
Animales
La evaluación del espasmo bronquial inducido por la administración de histamina se realizó en cobayos Hartley machos (400-450 g de peso corporal) procedentes del Centro Nacional para la Producción de Animales de Laboratorios (CENPALAB). En el ensayo de anafilaxia pasiva cutánea se utilizaron ratas Wistar machos de 300 a 350 g de peso corporal y para la obtención del antisuero de ovoalbúmina, ratones albinos Suizos machos de 18 a 22 g de peso corporal procedentes de la colonia de la UCTB control Biológico (CIDEM).
Condiciones ambientales y de laboratorio
Los animales se mantuvieron en un cuarto con temperatura controlada de 22 ± 2° C, con un ciclo luz-oscuridad 12/12 h. La dieta administrada consistió en pienso convencional para cobayos CCO 1 302 y ratonina en pelotillas para ratas y ratones CMO 1 000 proveniente del CENPALAB y agua a voluntad
Reactivos y medicamentos
Difenhidramina: 25 mg tabletas. Laboratorios ERON S.A. La Habana, Cuba
Fosfato ácido de histamina. BDH, Inglaterra
Ketotifeno 1 mg tableta. Laboratorios Eron S.A., La Habana, Cuba
Albúmina de huevo. Fluka Chemie AG, CH-9740 Buchs, Suiza
El resto de los reactivos empleados provienen de la casa comercial SIGMA, EE.UU.
Anafilaxia pasiva cutánea (APC)
Obtención del antisuero de ovoalbúmina2-4Se administraron 0,2 mL de solución sensibilizante de albúmina de huevo a un grupo de 20 ratones por vía intraperitoneal, cuya composición fue: albúmina de huevo 0,1 % (10 mL), NaHCO3 8,4 % (4,5 mL), K Al (SO4)2 10 % (10 mL), PBS pH 7,4 (20 mL). Los animales se inmunizaron 2 veces con 7 días de intervalo entre ellas. Pasados 14 días después de la última administración se sacrificaron los animales y se procedió a la extracción de la sangre por la vena femoral, la que se centrifugó a 2 500 rpm por 10 min a 37° C para obtener el antisuero.
Para el ensayo de APC se confeccionaron 3 grupos de tratamientos con 4 animales cada uno, los cuales fueron identificados individualmente para la dosificación exacta de acuerdo a su peso corporal.
Los grupos de tratamientos fueron los siguientes:
Grupo I: MVZ 6,5 mL/kg (4,8 g de ácidos grasos/kg).
Grupo II: ketotifeno 3 mg/kg.
Grupo III: agua destilada 0,004 mL/kg.
El MVZ se administró por vía oral durante un período de 10 días. El ketotifeno se administró por la misma vía 1 h antes del desafío al igual que la última administración realizada del producto de ensayo.
Las ratas fueron depiladas en la parte dorsal 1 h antes de la administración intradérmica de 0,1 mL de antisuero de albúmina de huevo diluido en cloruro de sodio 0,9 % (obtenido previamente en ratones), en 6 sitios del lomo. Pasadas 24 h se provocó la reacción anafiláctica mediante la administración por vía intravenosa de 1 mL de una solución al 0,1 % de albúmina de huevo y el colorante azul de Evans 1%. Los animales fueron sacrificados 1 h después de provocada la reacción anafiláctica y se procedió a la extracción de porciones de piel que fueron colocadas en tubos de ensayo que contenían 4 mL de formamida e incubados a 370C durante 48 h; se midió la densidad óptica del colorante extravasado a una l=623 nm. Los valores de concentración de azul de Evans extravasado fueron expresados en mg/sitio. 2-4
Procesamiento estadístico
Los resultados obtenidos se procesaron mediante un análisis de varianza de una vía y posteriormente se realizó una prueba de Duncan con un nivel de significación p<0,05, se expresaron a través de la media ± desviación estándar.6
Espasmo bronquial inducido por histamina2-4
Se conformaron 3 grupos de ensayo con 4 animales cada uno, 2 de los grupos fueron tratados con MVZ 6,5 mL/kg (4,8 g de ácidos grasos/kg) y agua destilada 0,005 mL/kg por vía oral durante 7 días y el último recibió difenhidramina 60 mg/kg en dosis única por la misma vía 1 h antes del desafío
Posteriormente todos los animales fueron anestesiados con 40 mg/kg de pentobarbital sódico administrado por vía intraperitoneal para realizar la traqueotomía y ventilarlos con una bomba de respiración con 100 pulsaciones/min/kg de peso, se canalizó la vena yugular y se administraron 15 mg/kg de pentobarbital sódico vía endovenosa para producir el paro respiratorio. A continuación se realizaron 3 administraciones por vía intravenosa de 15 mg/kg de histamina tanto a los grupos tratados como al grupo control y se determinó la presión intratraqueal después de cada administración mediante un transductor de presión TP-101T acoplado a un polígrafo NIHON KOHDEN.2-4
El resultado se consideró positivo cuando la media de los valores de la diferencia de presión bronquial de cada animal provocada por la administración de histamina en los animales tratados resultó menor que el 50 % de la media de los valores de la diferencia de presión bronquial en los animales controles.2-4
Resultados
Anafilaxia pasiva cutánea (APC)
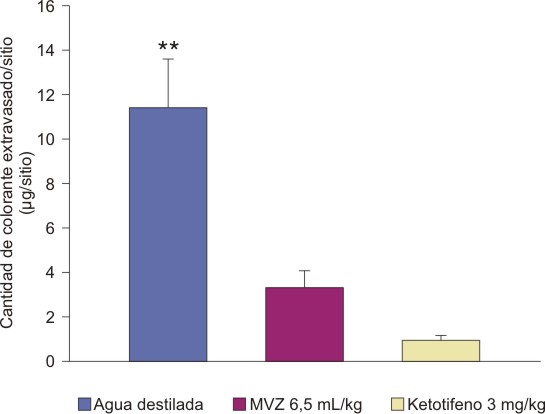
Los resultados de la administración oral del MVZ, por un período de 10 días sobre la APC en ratas, se muestran en la figura. La intensidad de la reacción anafiláctica se refleja a través de la cantidad de colorante extravasado/ sitio (mg/sitio).
De acuerdo a estos resultados se puede observar que la intensidad de la reacción anafiláctica en los animales tratados con MVZ 6,5 mL/kg (4,8 g de ácidos grasos/kg) y el ketotifeno 3 mg/kg fue similar al no existir diferencias significativas entre ellos.
Al realizar el análisis estadístico de la cantidad de colorante extravasado/sitio por grupo de ensayo se comprobó que el MVZ 6,5 mL/kg (4,8 g de ácidos grasos/kg) y el ketotifeno 3 mg/kg difieren significativamente en relación con el grupo que recibió agua destilada (p < 0,01).Fig. Efecto del MVZ sobre la APC en ratas.
** difiere con respecto a los grupos tratados con MVZ 6,5 mL/kg y ketotifeno 3 mg/kg para p < 0,01
Espasmo bronquial inducido por histamina
Los resultados se muestran en la tabla, donde se puede observar que los animales pertenecientes a los grupos tratados con MVZ 6,5 mL/kg (4,8 g de ácidos grasos/kg) y difenhidramina 60 mg/kg respondieron satisfactoriamente ante el daño fisiológico provocado, según el criterio seguido para la evaluación del producto en estudio.
Tabla. Media de los valores de la presión bronquial en los animales pertenecientes a los diferentes grupos de ensayos
| Grupos de tratamiento | Media ± DS (mmHg) |
| Agua destilada | 4,14 ± 0,73 |
| MVZ 6,5 mL/kg | 1,96 ± 0,28 Á |
| difenhidramina 60 mg/kg | 0,36 ± 0,12 Á |
Á: difieren con respecto al grupo tratado con agua destilada.
DiscusiÓn
Como es conocido, la reacción antígeno-IgE produce un cambio estructural a nivel de la membrana del mastocito que suele alterar su permeabilidad, lo que permite el rápido ingreso de diversos iones, entre ellos el calcio, el cual es esencial para la desgranulación de estas células. Además se produce un cambio bifásico en las concentraciones de AMP-cíclico, lo que hace que ocurra un incremento rápido de sus valores, seguido de una disminución notable. Es precisamente durante esta disminución notable de las concentraciones de AMP-cíclico que se liberan los mediadores de la anafilaxia.2-4, 7-13
En el ensayo donde se provocó la APC mediante un mecanismo inmunológico se observó el efecto inhibitorio de su intensidad por parte del MVZ a la dosis ensayada, probablemente debido a que este, o bien impide de alguna manera la reacción antígeno-anticuerpo, o impide la síntesis y/o liberación de los mediadores alérgicos por parte de los mastocitos especialmente de la serotonina, bradiquinina, factor activador de plaquetas, prostaglandinas y/o leucotrienos, o antagonicen sus receptores que evitaría la fragilidad capilar provocada por ellos y por lo tanto, que haya una disminución de la cantidad de colorante extravasado/sitio, ya que los productos antagonistas de estos mediadores inhiben el aumento de la permeabilidad capilar producida por los mismos.2-4, 14
También se pudo apreciar que el MVZ a la dosis de 6,5 mL/kg (4,8 g de ácidos grasos/kg) después de haber sido administrado por vía oral durante un período de 7 días, presentó efectividad en el tratamiento profiláctico de la broncoconstricción inducida por histamina, por lo que parece que el MVZ inhibe los efectos de la histamina a nivel bronquial, la cual al interactuar con los receptores H1 provoca broncoconstricción15 y por consiguiente se convierte en uno de los mediadores de las enfermedades alérgicas.5,16
Los resultados obtenidos sugieren que el MVZ pudiera ser efectivo en el tratamiento profiláctico de enfermedades alérgicas tipo I como el asma bronquial, lo cual justificaría su uso popular en pacientes asmáticos.
Summary
Effect of an oleosus extract of rhizome of Zingiber officinale Roscoe (MVZ) on the cutaneous passive anaphylaxis and the bronchial spasm induced by histamine
In order to show the antiallergic properties conferred to MVZ, it was studied its posible influence on the anaphylactic mediators and the bronchial spasm induced by histamine. In the test of cutaneous passive anaphylaxis there were used Wistar male rats that were orally administered MVZ at a dose of 6.5 mL/kg (4.8 of fatty acids/kg) during 10 days. Ketotifen 3 mg/kg was used as a positive control. The intensity of anaphylaxis was determined by quantifying the amount of extravasated Evans blue.The protective effect of bronchial spasm was determined in Hartley male guinea pigs by inducing brochoconstriction through the intravenous administration of histamine and estimating the bronchial pressure. The dose of the product used was the same as that of the previous assay. As a result, it was found that MVZ inhibited the cutaneous passive anaphylaxis in rats and the bronchoconstriction induced by 15 µg/kg of histamine by endovenous route. The outcomes suggest that the MVZ may be effective in the prophylactic treatment of type 1 allergic diseases, such as bronchial asthma, which would justify its popular use in asthmatic patients.
Key words: Zingiber officinale Roscoe, MVZ, cutaneous passive anaphylaxis, bronchial spasm, histamine.
Referencias bibliográficas
1. Roig JT. Plantas medicinales aromáticas o venenosas de Cuba. La Habana: Editorial Ciencia y Técnica;1988.p.469-71.
2. Núñez YF, Lagarto AP, Tillán JC, Lastra HV, Agüero SF, Guerra IS, et al. Efecto del extracto hidroalcohólico de Eucaliptus citriodora Hook, sobre la anafilaxia pasiva cutánea, espasmo bronquial y toxicidad aguda oral. Rev Mexicana Ciencias Farmacéuticas. 2003; 34(4):2-7.