Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Plantas Medicinales
versión On-line ISSN 1028-4796
Rev Cubana Plant Med v.11 n.3-4 Ciudad de la Habana jul.-dic. 2006
Trabajos originales
Centro de Investigaciones y Desarrollo de Medicamentos (CIDEM).
Estación Experimental de Plantas Medicinales Dr. Juan Tomás Roig.
Caracterización farmacognóstica de Indigofera suffruticosa Mill. (añil cimarrón)
MSc. Ester Sánchez Govín,1 Ing. Ana María Pérez Lamas,2 Téc. Diosothys Chávez Figueredo,3 Téc. Carlos Alberto Rodríguez Ferradá,4 Aux. Lab. María Gámez Guerrero 5 y Téc. Miralys Reyes Arias6
RESUMEN
Las investigaciones para obtener principios activos son largas y costosas y una preparación de planta bien estandarizada puede ser muy efectiva, por lo que en la actualidad, la utilización de extractos totales ha demostrado en muchos casos un efecto más beneficioso en el organismo humano que la acción del compuesto aislado. Se efectuaron las investigaciones para obtener la droga vegetal de Indigofera suffruticosa Mill. (añil cimarrón) debidamente caracterizada, con vistas a obtenerla con la calidad requerida. Para ello se realizaron descripciones macro y micromorfológica de la especie, el estudio de secado, se determinaron los índices numéricos, según normas internacionales para drogas vegetales. En los resultados, se estableció la presencia mayoritaria de flavonoides, coumarinas y triterpenos, se estandarizó un perfil cromatográfico para compuestos flavonoides. Además, se comprobó que el período óptimo de conservación de la droga vegetal es un tiempo de 10 meses en frascos de polipropileno.
Palabras clave: Indigofera suffruticosa, flavonoides, control de calidad, Farmacognosia.
Es conocido que las investigaciones para obtener principios activos, responsables de las propiedades de las plantas medicinales son largas y costosas, pero esto es cuestionable, ya que una preparación de planta bien estandarizada puede ser tan efectiva como el principio activo puro.1
La utilización de extractos totales de las plantas ejercen en muchos casos, un efecto más beneficioso en el organismo humano que la acción del compuesto aislado. Este es el principio de la Fitoterapia que en nuestros días gana más adeptos entre los investigadores.
La OMS ha promovido el uso de plantas medicinales sobre bases científicas y nuestro país está incorporando su uso en la atención primaria de salud. Para ello es necesario el estudio multidisciplinario de las especies, uno de los cuales es la caracterización farmacognóstica, donde se establecen los parámetros de calidad que se exigen para considerar una materia prima de calidad óptima para ser utilizada como medicamento herbario.
En esta investigación nos propusimos determinar los parámetros de calidad del añil cimarrón (Indigofera suffruticosa Mill.) que crece en Cuba, perteneciente a la familia Papilonaceae, a la que la población atribuye propiedades insecticidas, antiepilépticas, febrífugas, antiherpéticas, antisépticas, purgantes, antiespasmódicas y antiparasitarias.2
Además, si tenemos en cuenta que diferentes especies del género Indigofera han mostrado efecto antioxidante,3 actividad hepatoprotectora4 y que en nuestro país se han obtenido resultados alentadores al evaluar la actividad antiulcerosa de extractos de esta planta (Bárzaga P. 2005. Informe Técnico. CIDEM), pudiéramos contar con una materia prima vegetal con la calidad requerida para la obtención de medicamentos herbarios con estas propiedades.
MÉTODOS
En parcelas experimentales de la Estación Experimental de Plantas Medicinales Dr. Juan Tomás Roig sobre suelo ferralítico rojo hidratado y con aplicación de compost vegetal como fertilizante orgánico, se desarrollaron los cultivos de esta especie medicinal, en el período de octubre 2003 a febrero 2005. Cuando la planta alcanzó su estado vegetativo fueron cosechadas las partes aéreas. Fue depositado un ejemplar con el número ROIG 4594 en el herbario de nuestra estación. Se realizaron descripciones macro y micromorfológicas.
Se utilizaron 3 variantes para el secado del material vegetal: sombra, sol (cubierta de malla protectora) y estufa de recirculación de aire a 40°C, volteándolo 2 veces al día.
La presencia de metabolitos secundarios fue realizada mediante la metodología de maceración sucesiva con solventes de polaridad creciente.5 Los parámetros de calidad numéricos según las normas nacionales e internacionales para el estudio de las drogas vegetales,6,7 fueron evaluados estadísticamente mediante análisis de varianza, de doble vía y la diferencia entre las medias se determinó por la prueba de Rangos Múltiples de Duncan.
Para la identificación de algunos metabolitos presentes y su comportamiento durante la conservación de la droga se obtuvieron extractos metanólicos de 1 g de droga seca, triturada, reflujada con 10 mL de metanol durante 10 min. Se realizó el estudio cromatográfico en capa fina,8 con empleo de placas preelaboradas de silicagel G-60 de 0,25 mm de espesor y el sistema de solvente n-butanol: ácido acético, agua 20:5:25 (fase superior) para la detección de flavonoides atomizando las mismas con tricloruro de aluminio al 5 % en etanol. Posteriormente fueron observadas bajo luz UV de 365 nm.
En todas las variantes utilizadas en la investigación se describieron los perfiles cromatográficos correspondientes.
Se efectuó un experimento de envase y conservación de la droga vegetal en condiciones ambientales durante 1 año. Se utilizaron frascos de vidrio color ámbar, sobres de papel kraft, sobres de polietileno de baja densidad (35 micras) y frascos de polipropileno. Para la evaluación organoléptica del material vegetal, se utilizó una escala sensorial, donde el valor más alto se corresponde con las características óptimas y a partir del punto intermedio se rechaza el producto, además se analizó el comportamiento de los índices numéricos y el perfil cromatográfico, desde el inicio del experimento y cada 2 meses.
RESULTADOS
Macromorfología
Presenta hojas compuestas, generalmente de 5 a 10 pares de foliolos dispuestos de forma opuesta, de color verde claro, pubescente que pueden medir de 2 a 3,5 cm de largo y de 0,4 a 0,6 cm de ancho. Flores en racimos o espigas de hasta 5 cm de largo de color naranja rojizo. Legumbre lineal de hasta 2 cm de longitud y 2 mm de ancho. La droga presenta un olor característico y es urticante al tacto.
Micromorfología
En el corte epidérmico de la hoja se observaron células epidérmicas sinuosas, con estomas por ambas superficies (anfiestomáticas), sin células acompañantes, con papilas y pelos unicelulares en forma de T por ambas superficies.
En el corte transversal de la hoja se observó la epidermis monoestratificada, cutícula fina, una capa de parénquima en empalizada y parénquima lagunar.
En el corte transversal del tallo, se observó anguloso, epidermis con pelos secretores en forma de T, colénquima en las costillas y parénquima clorofílico en los laterales que se alternan, casquete de fibras, floema, cambium, xilema y parénquima medular (médula).
Secado
El material vegetal se obtuvo con su color verde natural, fueron necesarios 3 días para lograr el secado en la estufa, de 4 a 5 días para el secado al sol y 5 días a la sombra, en dependencia de las condiciones atmosféricas.
Estudio químico
Mediante el tamizaje fitoquímico se evidenció la presencia escasa de alcaloides y quinonas, mayor proporción de saponinas y en abundancia las coumarinas, triptenos y flavonoides.
Con la utilización de un sistema de solvente para compuestos flavonoides y revelador de AlCl3 + luz UV de 365 nm se detectaron 6 bandas con las siguientes características:
Banda 1: intervalo de R f (0,5 ) color violeta
Banda 2: intervalo de R f (0,54 - 0,56) color pardo
Banda 3: intervalo de R f (0,68 - 0,71) color azul violeta
Banda 4: intervalo de R f (0,80 - 0,82) color azul violeta intenso
Banda 5: intervalo de R f (0,85 - 0,88) color rosado
Banda 6: intervalo de R f (0,92 - 0,94) color pardo rojizo
En la tabla 1 se muestran los resultados obtenidos en los índices numéricos para la droga; se observó que los porcentajes de humedad en su mayoría se encuentran por debajo del 12 %, exceptuando las muestras secadas a la sombra fundamentalmente. Las cenizas totales se encuentran favorablemente para este parámetro, por debajo del 12 %. Las sustancias solubles en agua se encuentran en un rango desde 18 hasta 25 %, a excepción de la muestra cosechada en el mes de septiembre secada a 40°C con 14,61 %. Un rango de valores menores (10,28 - 23,63 %) se obtuvo para las sustancias solubles en etanol al 70 %.
Tabla 1. Índices numéricos determinados en Indigofera suffruticosa Mill
| Muestras | Humedad (%) | Cenizas totales (%) | Sust. solubles en agua (%) | Sust. solubles en etanol al 70 % |
| Dist. 90 x 40 cm S. 40°C | 8,93 g | 8,81 h | 25,45 i | 11,80 a |
| S. Sol | 14,18 a | 8,98 gh | 20,40 e | 16,34 g |
| S. Sa | 13,98 a | 8,99 gh | 17,62 g | 14,75 k |
| Dist. 90 x 60 cm S. 40°C | 11,99 cd | 8,35 f | 21,26 h | 12,84 f |
| S. Sol | 10,92 e | 9,11 g | 24,11 e | 16,62 b |
| S. Sa | 10,35 f | 9,21 fg | 21,85 d | 17,08 e |
| Dist. 90 x 90 cm S. 40°C | 11,57 d | 8,78 h | 21,40 j | 11,36 f |
| S. Sol | 10,51 ef | 9,06 g | 18,59 ij | 11,62 ij |
| S. Sa | 10,94 e | 8,84 h | 18,68 i | 11,16 i |
| FC. Marzo/04 S. 40°C | 7,29 h | 7,47 i | 18,22 h | 12,76 j |
| S. Sol | 11,68 d | 6,58 k | 20,05 j | 11,42g |
| S. Sa | 12,12 cd | 7,13 j | 22,87 j | 10,28 d |
| FC. Junio/04 S. 40°C | 7,50 h | 10,46 d | 19,43 f | 15,51 h |
| S. Sol | 9,97 f | 11,21 b | 20,31 cd | 17,32 g |
| S. Sa | 13,28 b | 10,67 c | 23,60 b | 19,20 c |
| FC. Sept/04 S. 40°C | 9,06 g | 10,31 e | 14,61 c | 17,54 l |
| S. Sol | 10,68 ef | 11,59 a | 19,16 a | 23,35 h |
| S. Sa | 12,42 c | 10,62 c | 19,07 a | 23,63 hi |
| _ ES x | 0,1467 | 0,1074 | 0,0877 | 0,0723 |
Dist. 90 x 40 cm, 90 x 60 cm, 90 x 90 cm: distancias de plantación.
FC: fecha de cosecha.
S. 40°C, S. Sol, S. Sa: secados.
ES x: error estándar de la media.
Conservación
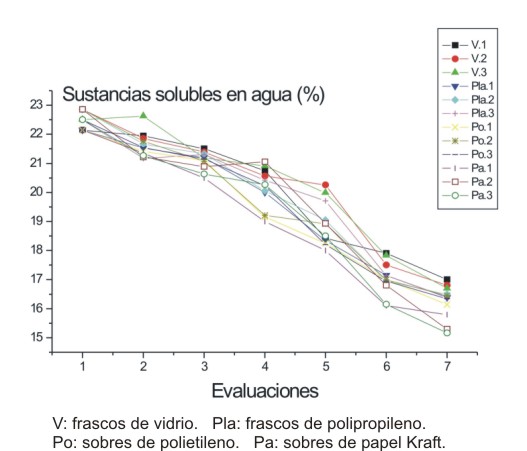
El análisis organoléptico mostró leves pérdidas en el color y el olor en los frascos de vidrio, así como mediana infestación por insectos de almacén, Losioderma serricorne, al final del experimento. Los frascos de polipropileno no se vieron afectados y los sobres de polietileno y de papel kraft sufrieron los mayores cambios a partir de los 8 meses, con mayor incidencia de insectos en los sobres de papel. Los índices numéricos mostraron cambios durante el experimento. Es de destacar que aunque la humedad aumentó en todos los envases utilizados, no sobrepasó los límites que se reportan para este parámetro. Las sustancias solubles en agua y las solubles en etanol al 70 % decrecieron en ambos casos. El perfil cromatográfico evidenció las mismas características tanto entre los envases ensayados como en las sucesivas evaluaciones (Figs. 1, 2 y 3).
Fig. 1. Comportamiento del porcentaje de humedad en el estudio de conservación de Indigofera suffruticosa Mill. durante 1 año.
Fig. 2. Comportamiento del porcentaje de sustancias solubles en etanol al 70 % en el estudio de conservación de Indigofera suffruticosa Mill. durante 1 año.
Fig. 3. Comportamiento del porcentaje de sustancias solubles en agua en el estudio de conservación de Indigofera suffruticosa Mill. durante 1 año.
Discusión
Las características morfológicas de I. suffruticosa Mill. que crece en nuestras condiciones se corresponden con las reportadas para este especie, sólo difiere el color de las flores, ya que se reportan amarillas y las muestras son de color naranja a rojas. Los procesos de secado ensayados fueron muy eficientes y mantuvieron las características organolépticas en todos los casos. Las diferencias estadísticas detectadas en el parámetro humedad, están dadas por los diferentes tipos de secado, pero a pesar de esto todas son aceptables y aprovechables a la hora de procesar en gran escala esta droga vegetal. El resto de los parámetros evaluados difieren entre sí por la selección de las muestras, la cual permite contar con un amplio rango de valores posibles a la hora de confeccionar las especificaciones de calidad de la especie. La evaluación integral del experimento de envase y conservación mostró características óptimas de la droga fundamentalmente para el frasco de polipropileno por un tiempo mayor (10 meses), que para el resto de los envases ensayados. Los parámetros evaluados permitieron confeccionar las especificaciones de calidad de esta droga vegetal, requisito de gran importancia para su utilización como materia prima de un medicamento vegetal.
Summary
Pharmacognostic characterization of Indigofera suffructicosa Mill. (wild indigo)
The researches to achieve active principles are long and expensive, and a well standardized plant preparation could be very efficacious. That is why nowadays the use of total extracts has showed, in many instances, a more beneficial effect in human organism than the action of an isolated compound. Researches have been conducted to obtain a properly plant drug from Indigofera suffruticosa Mill (wild indigo) with the required quality. To this end, macro- and micromorphologic descriptions of species were made, a drying study was undertaken, and the numerical indexes were determined, according to the international standards for plant drugs. In the results, it was observed a predominance of flavonoids, coumarins, and tryterpenes, and a chromatographic profile was standardized for flavonoid compounds. It was also confirmed that the optimal period of preservation of the plant drug is 10 months in polypropylene flasks.
Key words: Indigofera suffruticosa, flavonoids, quality control, Pharmacognosy.
REFERENCIAS BIBLIOGRÁFICAS
1. Morón F, Sierra P, Villán J, Martínez MJ. Programa de Medicina Tradicional herbolaria en Cuba. Las plantas medicinales en la terapéutica. Rev. Cub. Med Gen Integr. 1991;7(3):266-84 .
2. Fitomed II. Plantas Medicinales. La Habana. Ed. Ciencias Médicas;1993. p. 117.