Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Plantas Medicinales
versión On-line ISSN 1028-4796
Rev Cubana Plant Med v.13 n.4 Ciudad de la Habana sep.-dic. 2008
ARTÍCULO ORIGINAL
Estudios preliminares de extractos fluidos 30 % de Justicia pectoralis Jacq. var. stenophylla Leonard.
Preliminary studies of fluid extracts 30 % from Justicia pectoralis Jacq. var. stenophylla Leonard.
Jorge E. Rodríguez ChanfrauI; Ayme RocheII; Raiza VegaII; Carlos RodríguezIII; Caridad CarballoIII; Isbet GuerraIII; Carmen CarrilloIII
I Maestro en Ciencias Farmacéuticas. Investigador Auxiliar. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ciudad de La Habana, Cuba.
II Licenciada en Farmacia. Investigador Aspirante. CIDEM. Ciudad de La Habana, Cuba.
III Técnico Medio. CIDEM . Ciudad de La Habana, Cuba.
RESUMEN
INTRODUCCIÓN: Justicia pectoralis Jacq. (Acanthaceae) es una planta herbácea de amplio uso tradicional y medicinal como sedante por la población en Cuba, donde esta especie se encuentra como J. pectoralis Jacq. var. pectoralis y J. pectoralis Jacq. var. stenophylla Leonard. J. pectoralis var. pectoralis es la más difundida y estudiada en el país, esto permitió que pasara a formar parte, como sedante, de los medicamentos herbarios que emplea el sistema nacional de salud.
OBJETIVOS: comprobar si J. pectoralis var. stenophylla tiene las mismas propiedades que J. pectoralis var. pectoralis.
MÉTODOS: se realizó la caracterización química, farmacológica y toxicológica de un extracto hidroalcohólico 30 % de partes aéreas secas de J. pectoralis var. stenophylla.
RESULTADOS: el estudio fitoquímico realizado al extracto mostró la presencia de saponinas, azúcares reductores, fenoles, aminoácidos y aminas, carbohidratos, flavonoides y cumarinas. Estos resultados son similares a los reportados para la variedad pectoralis. Por otro lado, de acuerdo con la clasificación internacional establecida para los estudios toxicológicos, el extracto estudiado se clasifica como no tóxico, mientras que, el ensayo farmacológico demuestra su efecto sedante sobre el sistema nervioso central, al observarse una disminución de la agresividad de los animales dependiente de la dosis del extracto.
CONCLUSIONES: los extractos obtenidos con ambas variedades de J. pectoralis resultaron muy similares en los estudios químico, toxicológico y farmacológico realizados en igualdad de condiciones.
Palabras clave: Justicia pectoralis, caracterización química, estudios toxicológicos, estudios farmacológicos.
ABSTRACT
INTRODUCTION: Justicia pectoralis Jacq (Acanthaceae) is a herbaceous plant of wide traditional and medicinal use as sedative by the Cuban population. This species may be found as J. pectoralis Jacq. var. pectoralis and J. pectoralis Jacq. var. stenophylla Leonard. The most studied and known in the country is J. pectolaris var. pectolaris, so it becomes part, as sedative, of the herbal drugs that are used in the national healthcare system.
OBJECTIVES:to verify if J. pectoralis var. stenophylla has the same properties as J. pectoralis var.pectoralis.
METHODS: the chemical, pharmacological and toxicological characterization of 30% hydroalcohol extract from dry air parts of J. pectolaris var. stenophylla was made.
RESULTS: the phytochemical study showed the presence of saponins, reducing sugars, phenols, aminoacids and amines, carbohydrates, flavonoids and coumarins. These results were similar to those reported for the variety pectoralis. On the other hand, according to the international classification set by toxicological studies, the studied extract was classified as non-toxic whereas the pharmacological assays proved its sedative effect on the central nervous system, when extract dose-dependent abatement in aggressive behaviour of animals was observed.
CONCLUSIONS: the extracts from both varieties of J. pectoralis turned to be very similar according to the results of the chemical, toxicological and pharmacological studies performed on equal footing.
Key words: Justicia pectoralis, chemical characterization, toxicological studies, pharmacological studies.
INTRODUCCIÓN
Justicia pectoralis Jacq, especie perteneciente a la familia Acanthaceae, es una planta herbácea de amplio uso tradicional y medicinal por parte de la población en Cuba, por causa de sus propiedades tranquilizantes.
Esta planta es nativa de América tropical, se encuentra distribuida tanto en las Antillas, como en la zona continental.1 La especie J. pectoralis presenta 2 variedades en Cuba que son la variedad pectoralis y la variedad stenophylla. Esta última difiere de la anterior por presentar hojas más estrechas (lineal-lanceolada) de color verde oscuro, tener un porte erecto (alcanza alturas entre 15 y 20 cm) y ser poco ramificada.2-4
J. pectoralis var. pectoralis es la más difundida y estudiada en Cuba,5-15 esto permitió que pasara a formar parte, para ser usada como sedante, del arsenal terapéutico que emplea el Sistema Nacional de Salud cubano.16
Estudios recientes realizados con J. pectoralis var. stenophylla, cultivada en la Estación Experimental de Plantas Medicinales "Dr. Juan Tomas Roig", en la provincia La Habana, demostraron que el mes de marzo resultó la mejor fecha de plantación, y las 3 primeras cosechas resultaron las más productivas.2
Por otro lado, determinaciones macromorfológicas y micromorfológicas realizadas a esta variedad, demostraron que es una planta olorosa de hojas simples, lanceoladas, opuestas transversalmente, de base estrecha y ápice agudo, de color verde más intenso por la cara superior que la inferior, pueden medir de 4,5 a 6,5 cm de largo y de 1,0 a 1,5 cm de ancho, con el peciolo corto. Presenta el tallo cilíndrico de color verde y abundantes pelos. El raspado epidérmico mostró células epidérmicas, envés irregular, abundantes estomas diacríticos y pelos glandulares con cabezas, de 4 células, mientras la epidermis del haz está formada por células más sinuosas y con un número escaso de estomas diacríticos, además de presentar el mismo tipo de pelo.
En los cortes transversales practicados a las hojas se observa en la zona del nervio medio células epidérmicas con cutícula fina, colénquima debajo de ambas epidermis y haces conductores colaterales cerrados; se destaca uno central más grande. En la zona de los semilimbos en posición subepidérmica se observa parénquima en empalizada de una capa de células que atraviesa toda la zona del nervio medio, lo que la diferencia de la variedad pectoralis.17
El tamizaje fitoquímico realizado a la droga seca (partes aéreas) demostró la presencia de flavonoides, cumarinas, azúcares reductores, carotenos, triterpenos y esteroides. 17
Como parte de los estudios que se realizan para comprobar si J. pectoralis var. stenophylla tiene las mismas propiedades que J. pectoralis var. pectoralis, se hizo la caracterización química, farmacológica y toxicológica de un extracto hidroalcohólico 30 % de J. pectoralis var. stenophylla.
MÉTODOS
Material vegetal
Justicia pectoralis Jacq. var. stenophylla Leonard. fue cosechada (segunda cosecha, 6 meses de edad) y colectada en la provincia La Habana. Se conservó un ejemplar (número ROIG 4648) en el herbario de la Estación Experimental de Plantas Medicinales "Dr. Juan Tomás Roig".
Preparación y conservación de la muestra
La droga cruda (partes aéreas) fue lavada con abundante agua, desinfectada con solución de hipoclorito de sodio 2 %18 y secada de forma natural. El material vegetal se extendió sobre bastidores de mallas plásticas y se cubrió además con una malla protectora.17 Posteriormente, fue molido hasta pulverización y almacenado en frascos de vidrio.17
Para controlar su calidad fue evaluada según la metodología establecida para medicamentos herbarios, se determinaron las características organolépticas, el porcentaje de humedad, las cenizas totales y las sustancias solubles en agua.19
Preparación del extracto
El extracto hidroalcohólico 30 % se elaboró según el procedimiento descrito en la Norma Ramal de Salud Pública (NRSP - 311).20
Caracterización química, química física y cromatográfica
El tamizaje fitoquimico se realizó aplicando el procedimiento descrito por Rodina y Coussie.21 Las determinaciones de pH, la densidad relativa, el índice de refracción, contenido alcohólico y los sólidos totales se realizaron según la Norma Ramal de Salud Pública (NRSP-311).20
La caracterización espectrofotométrica (UV) se hizo en metanol y en una mezcla de etanol agua (1:1), mediante el procedimiento siguiente:
Se tomaronn 2 muestras de 1 mL del extracto en estudio y se trasvasaron a 2 matraces aforados de 50 mL de capacidad. Un matraz se llevó a volumen con metanol y el otro con una mezcla de etanol agua (1:1) y se mezclaron.
Se tomaron 2 mL de cada solución y se trasvasaron a matraces de 50 mL de capacidad, se llevaron a volumen con metanol o mezcla de etanol agua (1:1) según correspondía y se mezclaron.
A ambas soluciones se les determinó el espectro de absorción en la zona comprendida entre los 200 y 400 nm; para ello se empleó un espectrofotómetro UV-Vis 8700 de la firma Pye Unicam.
La presencia de cumarinas en el extracto fue identificada, por ser este uno de los componentes mayoritario presente en la variedad pectoralis y al cual se le atribuyen propiedades farmacológicas.22 Para ello se realizó la cromatografía en placa delgada de acuerdo con el procedimiento siguiente:
Se tomaron 5 mL de la muestra de análisis, se trasvasaron a un matraz aforado de 10 mL de capacidad y se llevaron a volumen con acetona (pa). Se mezcló y se filtró aproximadamente 5 mL de esta solución, se puntearon 25 mL en la placa cromatográfica. Como estándar de referencia se empleó cumarina simple (Merck).
Como sistema de fase estacionaria se utilizaron placas de sílica gel 60 F254 (5 por 20 cm, 5 micras de grosor) suministradas por la firma Merck. Como fase móvil, se empleó n hexano-éter etílico (2:2) a partir de una modificación realizada a lo reportado.23
Una vez punteada la cantidad de muestra a analizar, la placa fue colocada dentro de la cámara cromatográfica, la cual previamente había sido ambientada durante 30 min a una temperatura de 25 ± 2 ºC. El cromatograma se corrió alrededor de 15 cm del punto de aplicación y se retiró la placa de la cámara, se dejó secar al aire. Las observaciones se hicieron bajo luz ultravioleta a una longitud de onda de 254 nm.
Evaluación toxicológica
Se realizó el ensayo de toxicidad aguda mediante la prueba límite según lo establecido en la OECD24 para el estudio de dosis máxima letal - dosis mínima no letal. Para ello se emplearon ratas Wistar procedentes de la colonia de la UCTB Control Biológico del CIDEM, con una masa corporal comprendida entre los 150 y 200 g, las cuales fueron mantenidas en una sala a temperatura y humedad controlada de 20 ± 2 ºC y 75 % de humedad relativa, con un ciclo de luz/oscuridad de 12 por 12 h. La alimentación consistió en Ratonina® peletizada y agua a voluntad.
Se confeccionaron grupos de 10 animales, 5 de cada sexo, los que fueron identificados individualmente, mediante un sistema de marcaje con ácido pícrico, para garantizar la dosificación exacta de acuerdo con su peso corporal.
La sustancia de ensayo se administró por vía oral mediante cánula intragástrica a dosis de 2 000 mg/kg, con un factor de volumen de 0,021 mL/g, para lo cual se retiró la comida a los animales 18 h antes de la administración. Los animales fueron observados durante las primeras 24 h, se continuó diariamente por un período de 14 d, se registró cualquier síntoma tóxico. Al finalizar la experiencia se procedió al sacrificio de los animales bajo atmósfera de éter para realizarle la autopsia y efectuar un examen macroscópico de los órganos y tejidos.
Evaluación farmacológica
Para la realización de este estudio, se emplearon ratones albinos machos, procedentes de la colonia de la UCTB Control Biológico del CIDEM, con una masa corporal comprendida entre los 18 y 22 g. Se establecieron 4 grupos de 6 animales cada uno, los cuales fueron aislados durante 20 d para provocar agresividad,25 en tanto otro grupo de ratones se mantuvo en colectividad.
Transcurrido el período establecido, a los ratones aislados les fue administrado por vía oral, mediante cánula intragástrica, la muestra en ensayo a dosis de 64,8; 129,0 y 259,0 mg/kg (3 grupos) y agua destilada (manteniendo el factor volumen referido para el extracto) al grupo control. Pasado 30 min de haberse administrado la muestra, se colocó en la jaula de un animal aislado, un animal de los mantenidos en colectividad y se observó durante 20 min el número de acicaleos o ataques, o ambos, realizado por el animal que se encontraba aislado. Paralelamente, se evaluó la conducta agresiva en los ratones del grupo control sin tratamiento.
Se calculó en cada caso el valor medio de los ataques y los resultados obtenidos fueron evaluados estadísticamente mediante un test de Duncan.26
RESULTADOS
Los resultados del control de la calidad de la droga seca se muestran en la tabla 1.
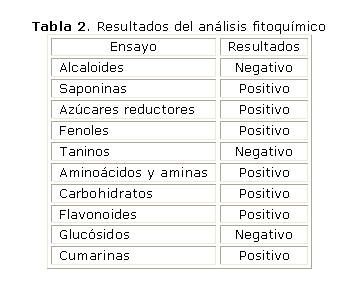
Los resultados de los análisis fitoquímico, químico y químico físico realizados al extracto se presentan en las tablas 2 y 3.
El espectro UV en la zona comprendida entre los 200 y 400 nm, mostró 3 máximos de absorción a 204, 273 y 311 nm. Por otro lado, el desarrollo de la identificación cromatográfica dio como resultado una mancha de color azul celeste bajo luz ultravioleta, a un Rf de 0,31-0,33 que coincide con el estándar de cumarina empleado. Durante el ensayo toxicológico no se presentó mortalidad en el período de observación, ni decremento en el peso corporal de los animales en estudio. Las autopsias realizadas no mostraron evidencias de alteraciones patológicas. En la figura se presentan los resultados de la media del número de ataque por grupo de tratamiento, se puede observar un efecto dosis dependiente con la disminución del número de ataques o acicaleos, o ambos.
DISCUSIÓN
Los resultados del control de la calidad de la droga seca según el proceder descrito con anterioridad, muestran que los valores de humedad obtenidos están dentro del rango descrito, entre 6 y 12 %, por Sánchez y otros17 en los estudios realizados con esta planta, lo que se considera aceptable para una buena conservación del material vegetal. Igualmente ocurre con los valores obtenidos en el análisis de las cenizas totales y sustancias solubles en agua, donde los valores están dentro de los límites reportados por los autores mencionados, que son de 16 a 26 % para las cenizas y de 22 a 36 % para las sustancias solubles en agua. Esto confirma que la calidad de la droga empleada se encuentra entre los parámetros establecidos para el cultivo de la planta en las condiciones de trabajo del CIDEM.
El estudio fitoquímico realizado al extracto mostró la presencia de saponinas, azúcares reductores, fenoles, aminoácidos y aminas, carbohidratos, flavonoides y cumarinas. Estos resultados coinciden con lo reportado por McRae y otros27 para plantas de esta variedad colectadas en el Perú y son muy similares a lo reportado para la variedad pectoralis en Cuba (Timor C, Manzini M, Menéndez R, Larinova M, Chávez M, Más R. Phytochemical studies on some Cuban medicinal plants. Celebration of the 75th Anniversary of the Research Institute for Medicinal Plants, Budakalász - Budapest, Hungría, Sept. 4-6; 1990).15
El resto de los parámetros químico-físicos determinados, está dentro de los rangos permisibles para este tipo de extracto y son muy similares a los que se alcanzan para extractos obtenidos con la variedad pectoralis.Las cumarinas son compuestos que presentan como estructura básica la fusión de anillos bencénicos y a-pirona. Por causa de su composición, es característico de ellas presentar máximos de absorción a 274 y 311 nm, atribuidos a los anillos de benceno y pirona, respectivamente.28 Al observarse los resultados obtenidos en la caracterización espectrofotométrica, se puede corroborar la presencia de cumarinas en el extracto estudiado. Estos resultados también son similares a los que reporta Benavides15 para extractos obtenidos a partir de la especie tipo.
Por otro lado, se pudo comprobar mediante la cromatografía de placa la presencia de cumarina al obtenerse una mancha a un Rf similar al del estándar de referencia empleado, se comprobaron los resultados alcanzados por Sánchez y otros17 para la droga cruda y coincide con los resultados reportados en extractos de la variedad pectoralis por diversos autores.8,10,11,14,15 De acuerdo con la clasificación internacional establecida para los estudios toxicologicos,24 el extracto estudiado se clasifica como no tóxico. Por otro lado, el ensayo farmacológico demuestra su efecto sedante sobre el sistema nervioso central, al observarse una disminución de la agresividad de los animales dependiente de la dosis del extracto.
El estudio realizado permite afirmar que los extractos obtenidos con J. pectoralis var. stenophylla son muy similares desde el punto de vista químico, toxicológico y farmacológico a los extractos obtenidos en igualdad de condiciones con J. pectoralis var. pectoralis.
REFERENCIAS BIBLIOGRÁFICAS
1. Roig JT. Plantas Medicinales, Aromáticas o Venenosas de Cuba. . La Habana: Ed. Científico-Técnica; 1974. p. 743.
2. Rodríguez C, Echevarria I, Fuentes V. Fecha y distancia de plantación en el cultivo del tilo (Justicia pectoralis Jacq. var. stenophylla Leonard). Rev Cubana Plant Med. 2003;8(1).
3. Fuentes V, Lemes C, Rodríguez C, Robineau L. Manual de cultivo y conservación de plantas medicinales. Santo Domingo: Ed. Enda-Caribe; 2000. p. 197.
4. Silva R, Acosta L, Castro I. Agrotecnología para el cultivo de tilo o curía. En: Vicente J. Yesid H, Cáceres A, editores. Fundamentos de Agrotecnología de Cultivo de Plantas medicinales Iberoamericanas. Santa Fé de Bogota: Ed. Convenio Andrés Bello (CAB) y el Programa Iberoamericano de Ciencia y Tecnología para el Desarrollo (CYTED); 2000. p. 217-28.
5. Fernández L, Pérez H, Más R. Evaluación preliminar de los efectos neurofarmacológicos de la Justicia pectoralis Jacq. Rev Cubana Farm. 1989;23(1-2):161-6.
6. Fernández L. Efecto de la Justicia pectoralis sobre la conducta exploratoria en los ratones. En: A. Álvarez, Valdés M, editores Estudios avanzados de Neurociencias. Ciudad de La Habana: Ed. Centro Nacional de Investigaciones Científicas (CNIC); 1987. p. 257-64.
7. González R, Alonso A, Mas R. Justicia pectoralis: unión con los receptores cerebrales de los aminoácidos excitatorios. Rev Cubana Farm. 1988;22(3):99-103.
8. Pérez G, Rivero R, Pardo Z, Rodríguez Chanfrau JE. Evaluación de la actividad antioxidante de Justicia pectorales Jacq. Rev Cubana Invest Biomed. 2001;20(1):30-3.
9. Rodríguez E, Virvés A, Alemán C. Estudio preliminar del efecto de la Justicia pectoralis sobre el EEG de adultos normales. Rev Cubana Farm. 1989;23(3):302-8.
10. Sánchez E, Durand D, Llanes M. Algunos parámetros farmacognósticos en plantas medicinales I. Rev Cubana Farm. 1985;19(3):450-3.
11. Sánchez E, Durand D, Carballo C. Estudio preliminar de Justicia pectoralis Jacq. Rev Cubana Plant Med. 1990;10:69-76.
12. La Serna B, Amor A, Martínez M. Caracterización química preliminar de la Justicia pectoralis. Rev Cubana Farm. 1989;23(3):256-64.
13. Rivas M. Informe sobre acción sedante del extracto fluido de tilo al 30 %. Ciudad de La Habana: Informe Técnico, CIDEM; 1991.
14. Rivero R. Extractos y tabletas de Justicia pectoralis Jacq (Tilo) [Tesis de grado para optar por el titulo de Licenciado en Farmacia]. Facultad de Farmacia y Alimentos, Universidad de La Habana; 1997.
15. Benavides A. Evaluación preliminar de la Justicia pectoralis Jacq. (Tilo) que crece en Cuba [Tesis de grado para optar por el titulo de Licenciado en Farmacia]. Universidad de La Habana; 1987.
16. MINSAP. Guía Terapéutica y Dispensarial de Fitofármacos y Apifármacos. La Habana: ECIMED; 1992. p. 109-13.
17. Sánchez E, Fuentes L, Chávez D, Rodríguez C. Estudio farmacognóstico de Justicia pectoralis Jacq. var. stenophylla Leonard. Rev Cubana Plant. Med. 2003;8(3).
18. López M, Carballo C. Lavado y desinfección de Justicia pectoralis Jacq. Ciudad de La Habana: Informe Técnico, CIDEM; 1997.
19. NRSP 309. Droga Cruda. Métodos de Ensayos. Norma Ramal del Ministerio de Salud Pública. La Habana; 1992. p. 72.
20. NRSP 311. Extractos Fluidos y Tinturas. Procesos Tecnológicos. Norma Ramal del Ministerio de Salud Pública. La Habana; 1992. p. 33-6.
21. Rondina R, Coussio J. Estudio fitoquímico de plantas medicinales argentinas (1). Rev Inv Agropecuaria. 1969;6:351-66.
22. Lino C, Traveira M, Viana G, Matos J. Analgesic and antiinflammatory activities of Justicia pectoralis Jacq. and its main constituents: coumarin and umbelliferone. Phytoter Res. 1997;11(3):211-5.
23. Mills J, Pascoe K, Chambers J, Melville G. Preliminary Investigations of the wound-healing properties of a Jamaican folk medicinal plant (Justicia pectoralis). West Indian Med J. 1986;35(3):190-3.
24. OECD. Acute Oral Toxicity: Modified Up and Down Proicedure. Guideline for testing of chemicals; 1997. p. 425.
25. Tyler C, Hiczed K. Effects of phencyclidine on aggressive behavior in mice. Pharmacol Biochem Behav. 1982;17:503-10.
26. Sigarroa A. Biometría y Diseño Experimental. La Habana: Ed. Pueblo y Educación; 1985. p. 403.
27. Mac Rae W, Towers G. Justicia pectoralis: a study of the basis for its use as a Hallucinogenic snuff ingredient. J Ethnopharmacol. 1984;12:93-111.
28. Rodríguez Chanfrau JE, López OD, Núñez Y, Rodríguez C, Carrillo C, Gil Apan JM, et al. Obtención de una materia prima de calidad farmacéutica a partir de extractos de Justicia pectoralis Jacq. mediante secado por aspersión. Desarrollo Tecnológico a partir de extracto hidroalcohólico al 30 %. Lat Am J Pharm. 2008;27(3):333-8.
Recibido: 30 de enero de 2008.
Aprobado: 4 de septiembre de 2008.
M. C. Jorge E Rodríguez Chanfrau. Centro de investigación y desarrollo de medicamentos (CIDEM). Ave. 26 No. 1605 e/ Puentes Grandes y Boyeros, Plaza. Ciudad de La Habana, Cuba. CP 10600. Correo electrónico: jorge.rodriguez@infomed.sld.cu














