Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Plantas Medicinales
versión On-line ISSN 1028-4796
Rev Cubana Plant Med vol.16 no.4 Ciudad de la Habana oct.-dic. 2011
ARTÍCULO ORIGINAL
Extracción de fracciones con actividad antioxidante en hojas de Guadua angustifolia Kunth
Extraction of fractions with anti-oxidant activity in Guadua angustifolia Kunth leaves
Prof. Mónica Valencia, Dra. Susana Durango, Prof. Juan Fernando Pinillos, Dra. C. Amanda Mejía, Dra. C. Cecilia Gallardo-Cabrera
Facultad de Química Farmacéutica, Universidad de Antioquia. Medellín, Colombia.
RESUMEN
Introducción: reportes científicos muestran que las hojas de bambú, principalmente provenientes de Phyllostachys nigra, contienen compuestos con actividad antioxidante aptos para uso alimentario. Dado que la Guadua angustofolia Kunt. es el género de bambú nativo más importante de Colombia y América tropical, se estudió si esta especie también contiene compuestos con actividad antioxidante.
Objetivo: evaluar la influencia de la técnica, del solvente y del método de extracción para obtener fracciones con actividad antioxidante a partir de hojas de Guadua angustifolia Kunth (Poaceae).
Métodos: se planteó un diseño experimental de bloques completamente aleatorizado, el factor de bloqueo principal fue la técnica de extracción (reflujo, soxhlet, ultrasonido), y como tratamiento el solvente (etanol 50 %, acetato de etilo, éter dietílico). También se realizó un estudio de comparación múltiple para evaluar 2 métodos de extracción (directo y fraccionamiento sucesivo por polaridad). Las extracciones se hicieron sobre hojas secas, molidas y desengrasadas. La actividad antioxidante se midió como la capacidad de atrapamiento del radical formado a partir de DPPH (2-2-diphenyl-1-picrylhydrazyl).
Resultados: todos los extractos obtenidos mostraron actividad antioxidante. La aplicación de diferentes técnicas de extracción o de métodos no mostró diferencias significativas en los valores de actividad antioxidante. Sí se observó diferencia estadística con el tipo de solvente usado; la actividad antioxidante resultó menor en los extractos obtenidos con éter dietílico.
Conclusiones: los extractos logrados muestran actividad antioxidante, que concuerda con la actividad presentada por otros bambús.
Palabras clave: Guadua angustifolia Kunth, bambú, actividad antioxidante.
ABSTRACT
Introduction: scientific reports show that bamboo leaves, mainly from Phyllostachys nigra, contains compounds with antioxidant activity suitable for food. Since Guadua angustifolia Kunt is the most important native bamboo genus in Colombia and tropical America, this study analyzed whether this species had compounds with antioxidant activity.
Objective: to assess the influence of the technique, the solvent and the method of extraction in obtaining fractions with antioxidant activity from Guadua angustifolia Kunth (Poaceae) leaves.
Methods: a completely randomized experimental design of blocks, was presented where the main blocking factor was the extraction technique (reflux, soxhlet, ultrasound), and as treatment was the solvent (50 % ethanol, ethyl acetate, diethyl ether). Additionally, a multiple comparison study was carried out to evaluate two extraction methods (direct and successive fractionning by polarity). The extractions were performed on dry, ground and grease-free leaves. The antioxidant activity was measured as the trapping capacity of radical derived from DPPH (2-2-diphenyl-1-picrylhydrazyl).
Results: all the extracts show antioxidant activity. The application of different extraction techniques or methods did not show significant differences in the antioxidant activity figures, but did show statistical significance with respect to the used solvent. The antioxidant activity was lower in extracts from diethyl ether.
Conclusions: the resulting extracts show antioxidant activity, in agreement with previously reported results for other bamboos.
Key words: Guadua angustifolia Kunth, bamboo, antioxidant activity.
INTRODUCCIÓN
Guadua angustifolia Kunth constituye el género de bambú nativo más importante de Colombia y América tropical, es un excelente recurso renovable de rápido crecimiento y fácil manejo.1 Llama la atención que en los países orientales se han encontrado múltiples usos al bambú, entre ellos está el hecho de que a partir de las hojas de bambú principalmente Phyllostachys nigra var. henonis, se han aislado y caracterizado compuestos con actividad antioxidante denominados AOB (antioxidant of bamboo), se ha demostrado su seguridad comestible y se han listado en los estándares nacionales de China con el código GB-2760 como antioxidantes de alimentos, con permiso otorgado por el Ministerio de Sanidad de la República Popular de China. Los principales componentes funcionales en los AOB son los flavonoides, las lactonas y los ácidos fenólicos. Las flavonas C-glucosiladas son el grupo de flavonoides más representativo en las AOB, llamadas orientina, homoorientina, vitexina e isovitexina.2-6
Este estudio tiene como objetivo evaluar, a través de un diseño experimental de bloques completamente aleatorizado, la influencia de la técnica, del solvente y del método de extracción para obtener fracciones con actividad antioxidante a partir de hojas de Guadua angustifolia Kunth.
MÉTODOS
El material vegetal de partida estuvo constituido por hojas secas y molidas de Guadua angustifolia Kunth (Poaceae), provenientes de un cultivo de 4 años ubicados en la localidad de Maracaibo-Valle-Colombia. El material vegetal fue secado en estufa a 60 ºC. La clasificación y conservación de la especie se encuentra en el Instituto de Ciencias Naturales de Colombia, código de barras COL000177528, número de catálogo 61713, número de colección 8333.
Se tomó 400 g de hojas secas y molidas y se sometieron a desengrase en Soxhlet, utilizando n-hexano como solvente, por un período de 4 h.
Métodos de extracción del material vegetal
Método 1: extracción directa, 10 g de muestra desengrasada se extrajeron con 100 mL de acetato de etilo, éter dietílico y etanol 50 %, usando 3 técnicas de extracción por separado: reflujo, Soxhlet y ultrasonido; para un total de 9 extracciones realizadas por separado. Las extracciones con reflujo se hicieron durante 1 h, en Soxhlet 3 h y en ultrasonido 2 h a 30 ºC.
Método 2: fraccionamiento sucesivo por polaridad, 30 g de muestra desengrasada se extrajeron con 300 mL de etanol 50 %, con el empleo de reflujo durante 1 h. El extracto hidroalcohólico obtenido se rotaevaporó hasta eliminar el etanol, luego se llevó a pH 3,0 con HCl 1M. Se tomaron 10 mL de este extracto acuoso concentrado y se extrajeron con 3 porciones de 20 mL de éter dietílico mediante extracción líquido-líquido. La fase acuosa resultante se extrajo de nuevo con 3 porciones de 20 mL de acetato de etilo. La fase acuosa final se llevó a 60 mL con agua desionizada y se filtró. En total se obtuvieron 4 fracciones por este método: hidroalcohólica, etílica, acetato de etilo y acuosa.
En ensayos posteriores se realizaron extracciones por percolación siguiendo el método 1, donde se pesaron 100 mg de muestra y se saturaron con 600 mL de etanol 50 % en un percolador de vidrio, permaneciendo en reposo durante 48 h, pasado este tiempo se recogieron 500 mL de percolado para los ensayos posteriores.
Determinación de la actividad antioxidante por método DPPH
Cada uno de los extractos obtenidos fue llevado a sequedad, y redisuelto con metanol hasta obtener una concentración de 50 mg.mL-1. En una celda se adicionan 20 µL de muestra y 1 980 µL de solución 0,1 M de DPPH. Se midió la absorbancia a 517 nm después de 1 min y luego cada 5 min durante 30 min. Se determinó el porcentaje de habilidad captadora de radicales libres del extracto, utilizando la ecuación siguiente:
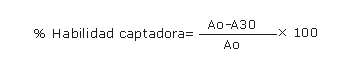
Donde A0 representa la absorbancia inicial y A30 la absorbancia a los 30 min de reacción.7
Estrategia estadística
Se planteó un diseño de bloques completamente aleatorizado y balanceado para cada método de extracción (directo y fraccionamiento sucesivo por polaridad), tomando como factor de bloqueo principal la técnica de extracción (reflujo, Soxhlet, y ultrasonido), y como tratamiento los 3 solventes (etanol 50 %, acetato de etilo y éter dietílico). El diseño de bloques permitió evaluar las técnicas de extracción con respecto a cada uno de los solventes y cómo estos influyen en la respuesta (actividad antioxidante), al valorar si existe diferencia estadística entre cada técnica (intergrupo) y diferencia estadística entre solventes (intragrupo).8 También se realizó un estudio de comparación múltiple para evaluar los 2 métodos de extracción en la obtención de extractos con mayor actividad antioxidante.
RESULTADOS
La influencia de los diferentes métodos, las técnicas y los solventes de extracción en los extractos obtenidos con actividad antioxidante, se evaluó por medio de la aplicación de diseño de bloques, cuyos resultados se muestran en la tabla 1.
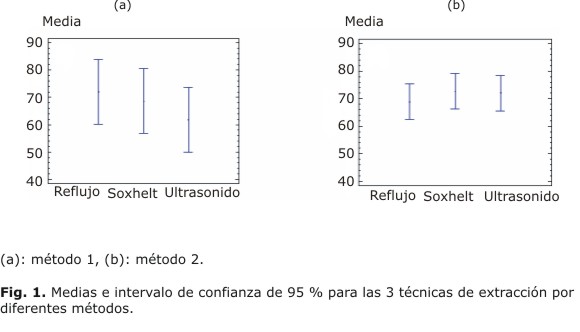
Al realizar la comparación entre bloques para evaluar la influencia de las 3 técnicas de extracción estudiadas por medio de análisis de varianza (ANOVA), se encuentra que no existe diferencia significativa en los valores de la actividad antioxidante entre las técnicas debido a que el valor p (0,6582) para el método 1 y el valor p (0,7982) para el método 2, son mayores que un valor a de 0,05 con un nivel de confianza de 95 %. El análisis de contraste de medias muestra que las medias de los bloques son muy parecidas y los intervalos de confianza están muy próximos, esto indica que entre las técnicas de extracción no existe diferencia significativa (Fig. 1), lo cual es corroborado por la prueba de rangos múltiples.
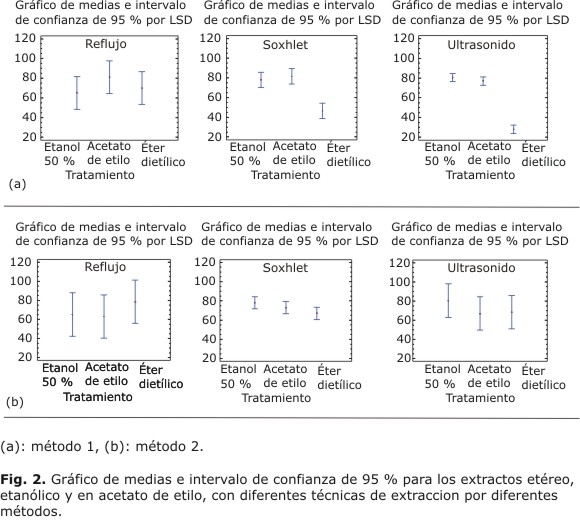
Al analizar la variabilidad entre los tratamientos en cada bloque, para evaluar la influencia del solvente, se encontraron 2 situaciones: una, en la cual el análisis de varianza (ANOVA) muestra que no hay diferencia significativa entre los valores de la actividad antioxidante de cada solvente de extracción con á del 0,05 y un nivel de confianza de 95 %; y otra, que sí hay diferencia significativa, lo cual indica que al menos uno de los tratamientos es distinto de los otros. La variabilidad entre los tratamientos se encontró en 2 bloques del método 1: Soxhlet (valor p= 0,0101) y ultrasonido (valor p= 0,0005). Para saber cuál tratamiento es distinto, se hizo una prueba de contraste de Fisher. En la figura 2 se muestran las medias e intervalo de confianza de 95 % evaluadas por Fisher, donde se observa que en el método 2 no existe diferencia estadística significativa en la actividad antioxidante evaluada por DPPH en los extractos obtenidos con cada solvente; mientras que con el método 1 sí hay diferencia entre los tratamientos, el uso del solvente éter dietílico produce la menor actividad antioxidante cuando se usa la técnica de extracción de Soxhlet y ultrasonido.
Finalmente, se compararon los 2 métodos usados: método directo y método de fraccionamiento sucesivo por polaridad; el análisis de varianza muestra que el valor p (0,8729) es mayor que un a de 0,05 con un nivel de confianza de 95 %, lo cual indica que no existe diferencia estadística significativa entre los valores de la actividad antioxidante promedio entre los 2 métodos. Este resultado se corroboró mediante la prueba de rangos múltiples que mide si hay homogeneidad entre los bloques (tabla 2). La prueba de rangos múltiples por el método de Fisher muestra que las medias de los bloques no son distintas estadísticamente en los 2 métodos.
Tabla 2. Prueba de rangos múltiples por método de Fisher entre los métodos de extracción
| Tratamiento | Conteo | Promedio | Homogeneidad de grupos |
| Ultrasonido Método 1 | 6 | 61,8 | X |
| Soxhlet Método 1 | 6 | 68,7 | X |
| Reflujo Método 2 | 6 | 68,8 | X |
| Soxhlet Método 2 | 6 | 71,0 | X |
| Ultrasonido Método 2 | 6 | 72,0 | X |
| Reflujo Método 1 | 6 | 72,0 | X |
Contraste
| Contraste | Significancia | Diferencia | Límite inferior/superior |
| Reflujo M1-Reflujo M2 | No | 3,1 | 18,5 |
| Reflujo M1-Soxhlet M1 | No | 3,3 | 18,5 |
| Reflujo M1-Soxhlet M2 | No | 1,0 | 18,5 |
| Reflujo M1-Ultrasonido M1 | No | 10,2 | 18,5 |
| Reflujo M1-Ultrasonido M2 | No | 0,0 | 18,5 |
| Reflujo M2-Soxhlet M1 | No | 0,2 | 18,5 |
| Reflujo M2-Soxhlet M2 | No | -2,2 | 18,5 |
| Reflujo M2-Ultrasonido M1 | No | 7,0 | 18,5 |
| Reflujo M2-Ultrasonido M2 | No | -3,2 | 18,5 |
| Soxhlet M1-Soxhlet M2 | No | -2,3 | 18,5 |
| Soxhlet M1-Ultrasonido M1 | No | 6,8 | 18,5 |
| Soxhlet M1-Ultrasonido M2 | No | -3,3 | 18,5 |
| Soxhlet M2-Ultrasonido M1 | No | 9,2 | 18,5 |
| Soxhlet M2-Ultrasonido M2 | No | -1,0 | 18,5 |
| Ultrasonido M1-Ultrasonido M2 | No | -10,2 | 18,5 |
Dados estos resultados, se introdujo la técnica de percolación siguiendo el método 2, dado que esta técnica es de fácil escalado a nivel industrial. Al compararla con las otras 3 técnicas de extracción estudiadas por medio de análisis de varianza (ANOVA) se observa que no hay diferencia significativa en la actividad antioxidante entre las 4 técnicas de extracción, puesto que el valor p (0,7799) es mayor que el alfa de 0,05 con un nivel de confianza de 95 %. Este resultado se ratificó, por medio de análisis de contraste de medias (Fig. 3a) donde se muestra que las medias de los bloques son muy parecidas y los intervalos de confianza están muy próximos, lo cual indica que los datos en los bloques son bastante homogéneos y por lo tanto la actividad antioxidante en los extractos obtenidos por percolación son similares a la obtenida por las otras 3 técnicas evaluadas.
Al evaluar la influencia del solvente en la percolación siguiendo el método 2, en el análisis de varianza se obtuvo un valor p (0,0118) menor que el a de 0,05 con un nivel de confianza de 95 %, y el gráfico de medias e intervalo de confianza de 95 % evaluadas por Fisher (Fig. 3b), indican que sí hay diferencia estadística entre los solventes y la más activa es la de acetato de etilo. En la tabla 3 se muestran los porcentajes de recuperación.
DISCUSIÓN
El diseño de bloques permitió determinar que la diferencia en la actividad antioxidante encontrada en los extractos obtenidos, está dada por el tipo de solventes usado más que por la técnica de extracción o el orden de extracción (método). Se determinó que los ensayos con menor efectividad para obtener extractos con actividad antioxidante de hojas de Guadua, fueron la extracción con éter dietílico tanto por la técnica de Soxhlet como de ultrasonido, siguiendo el método 1.
Esto indica que los compuestos con actividad antioxidante son compuestos polares y de mediana polaridad, lo cual podría indicar la presencia de compuestos polifenólicos como flavonoides, a los cuales se les ha atribuido la actividad antioxidante, y que han sido encontrados en hojas de bambú Phyllostachys nigra var. henonis.5,6
La técnica de percolación se puede usar para escalar la extracción, donde la fracción de mayor actividad antioxidante es la de acetato de etilo.
Los porcentajes de recuperación no cambian con el método aplicado y son más altos en la fracción etanólica.
Finalmente, las conclusiones que se pueden inferir de este trabajo son que las fracciones obtenidas a partir de hojas de Guadua angustifolia Kunt presentan actividad antioxidante por el método DPPH. Estas fracciones se pueden obtener a través de la extracción con etanol 50 % o acetato de etilo, usando técnicas como reflujo, Soxhlet, ultrasonido o percolación y haciendo la extracción de forma directa o por fraccionamiento sucesivo.
AGRADECIMIENTOS
Este proyecto se desarrolló gracias al apoyo financiero del Ministerio de Agricultura y Desarrollo Rural código 2008M3153-3330. Todos los experimentos fueron realizados bajo las normas y leyes colombianas.
REFERENCIAS BIBLIOGRÁFICAS
1. Ministerio de Agricultura y Desarrollo Rural. Observatorio Agrocadenas Colombia. Documento de trabajo Nº 65. La Cadena de la Guadua en Colombia, una mirada global de su estructura y dinámica 1991-2005. [sitio en Internet]. [citado 06 Abr 2011]. Disponible en: http://www.agronet.gov.co/www/docs_agronet/200511216197_caracterizacion_guadua.pdf
2. Zhang Y, Bao BL, Lu BY, Ren YP, Tie XW. Determination of flavone C-glucosides in antioxidant of bamboo leaves (AOB) fortified foods by reversed-phase high performance liquid chromatography with ultraviolet diode array detection. J Chromatogr A. 2005;1065(2):177-85. 3. Lou DD, Zhang Y, Wu XQ, Qi JJ, Zhuo YX. Application of antioxidant of bamboo leaves (AOB) in Weixin western sausages. Chin Food Ferment Ind. 2004;30:13-7. 4. China. Preparation method of bamboo leaf flavone. Patente Nº CN101391060 (A). Inst. of Chemical Industry of F; 2009.
5. Lu BY, Tie XW, Wu XQ, Zhang Y, Zhang Y. Toxicology and safety of anti-oxidant of bamboo leaves. Part I: Acute and subchronic toxicity studies on anti-oxidant of bamboo leaves. Food Chem Toxicol. 2005;43(5):783-92.
6. __________. Toxicology and safety of anti-oxidant of bamboo leaves. Part II: Developmental toxicity test en rats with antioxidant of bamboo leaves. Food Chem Toxicol. 2006;44(10):1739-43.
7. Antolovich M, Prenzler PD, Patsalides E, McDonald S, Robards K. Methods for testing antioxidant activity. Analyst. 2002;127(1):183-98.
8. Toutenburg H. Statistical Analysis of Designed Experiments. New York: Springer; 2002. p. 497.
Recibido: 15 de abril de 2011.
Aprobado: 12 de julio de 2011.
Cecilia Gallardo Cabrera. Calle 67 Nº 53-108, Medellín-Colombia. Teléf.:+574- 2198332 ext. 2311, Fax+574-2195457. Correos electrónicos: cgallardo@farmacia.udea.edu.co; gallardoqf@gmail.com