Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Plantas Medicinales
versión On-line ISSN 1028-4796
Rev Cubana Plant Med vol.20 no.1 Ciudad de la Habana ene.-mar. 2015
ARTÍCULO ORIGINAL
Vigilancia de las reacciones adversas por fitofármacos en Cuba en el período 2003-2010
Vigilance of adverse reactions of herbal medicines in Cuba for the period 2003-2010
Ms. Ana Karelia Ruiz Salvador,I DraC. Ana Julia García Milian,II Ms. Liuba Alonso Carbonell,III Ms. Giset Jiménez López,IV Ms. Ismary Alfonso Orta,IV Ms. Armando Carrazana LeeI
I Facultad de Ciencias Médicas “General Calixto García”. La Habana, Cuba.
II Escuela Nacional de Salud Pública (ENSAP). La Habana, Cuba.
III Centro Nacional Coordinador de Ensayos Clínicos (CENCEC). La Habana, Cuba.
IV Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (CECMED). La Habana, Cuba.
RESUMEN
Introducción: el aumento en el consumo de productos naturales es debido principalmente a la percepción de que al ser "naturales" sólo pueden ser beneficiosos y carecen de riesgos para la salud.
Objetivo: caracterizar las reacciones adversas asociadas al uso de los fitofármacos que se comercializaron en Cuba en el período 2003-2010.
Método: se realizó un estudio observacional, descriptivo y transversal. Se consideró elegible para el estudio a la totalidad de los reportes de sospechas de reacciones adversas a medicamentos producidas por fitofármacos a través, de la Unidad Coordinadora Nacional de Farmacovigilancia durante el período de estudio.
Resultados: la mayoría de los reportes de sospechas de reacciones adversas se distribuyeron en el sexo femenino (67,3 %) y en el grupo etáreo de 31-60 años (52,5 %). Predominaron los trastornos gastrointestinales como la epigastralgia (17,9 %) y el vómito (10,5 %). El Allium sativum L (ajo) tintura y jarabe (14,0 %) y el Aloe vera L (sábila) (7,7 %) fueron los fitofármacos más notificados. El órgano más afectado por las reacciones adversas fue el digestivo. La mayoría de éstas fueron clasificadas de leves y probables.
Conclusiones: las reacciones adversas, por fitofármacos, reportadas al sistema cubano de farmacovigilancia son en su mayoría leves, se presentan en las mujeres adultas y afectan al sistema digestivo y la piel con mayor frecuencia.
Palabras clave: farmacovigilancia, fitofármaco, reacciones adversas.
ABSTRACT
Introduction: increase in the consumption of natural products is largely due to the perception that being "natural" can only be beneficial and without risk to health.
Objective: to characterize the adverse reactions associated with the use of herbal medicines sold in Cuba for the period 2003-2010.
Methods: observational, descriptive and transversal study. Was eligible for the study all reports of suspected adverse drug reactions (ADRs) herbal medicines produced by the National Coordinator of Pharmacovigilance Unit during the study period.
Results: most of the reports of suspected adverse reactions were distributed in females (67.3 %) and in the age group of 31-60 years (52.5 %). Predominant gastrointestinal disorders such as epigastria pain (17.9) and vomiting (10.5). Garlic tincture and syrup (14.0 %) and Aloe Vera L (7.7) were the most commonly reported herbal medicines. The organ most affected by adverse reactions was the tract. Most of them were classified probable mild.
Conclusions: adverse reactions, for herbal medicines, reported the Cuban system of pharmacovigilance are mostly mild, occur in adult women and Digestive and skin more often.
Key words: pharmacovigilance, phytomedicine, adverse reactions.
INTRODUCCIÓN
El uso de las plantas medicinales en la terapéutica requiere, al igual que los productos sintéticos, de profundas investigaciones que no se limitan al campo de la experimentación, sino que una vez que se comercializan se siguen observando.1,2
El aumento en el consumo de productos naturales es debido en lo principal a la percepción de que al ser "naturales" sólo pueden ser beneficiosos y carecen de riesgos para la salud. Sin embargo, aunque hoy en día sabemos que las sustancias de origen vegetal no carecen de efecto biológico, las propiedades de las mismas están escasamente estudiadas y contrastadas. Existe falta de regulación de los compuestos botánicos en muchos países como Estados Unidos, en los que estos productos se consideran como suplementos dietéticos, escapando así de las exigencias aplicadas en materia de eficacia y seguridad a los fármacos convencionales.
Además, se carece de programas específicos de vigilancia post-comercialización, por lo que la incidencia y características de los efectos adversos que producen son desconocidas. Sin embargo, comienza a emerger la evidencia del riesgo de toxicidad asociada a una amplia variedad de estos productos en los últimos años, es la causa más frecuente de hepatotoxicidad en los países asiáticos.3
La medicina natural tiene mucho que ofrecer sobre todo, cuando se usa para inducir la curación de problemas crónicos continuos. A través, de su utilización adecuada, se puede lograr una profunda transformación de la salud con un menor peligro, derivados de los efectos colaterales inherentes a los medicamentos farmacológicos. No obstante, la creencia generalizada de que este tipo de producto, actúa lenta y leve no es del todo cierto. Pueden presentarse efectos adversos, sobretodo, si se eligen dosis inadecuadas o si se prescribe al paciente una planta medicinal equivocada, incluso estos pueden producir reacciones adversas dependientes del mecanismo de acción o de hipersensibilidad al compuesto.4
En Cuba se han notificado igual, sospechas de reacciones adversas a productos farmacéuticos naturales, siendo el Allium sativum L (ajo), el responsable de la mayoría de los reportes, seguido por la Citrus aurantium L. (naranja agria) y Eucalyptus spp. (el eucalipto).5-7
En los reportes de natuseguridad y los informes anuales de sospechas de reacciones adversas a medicamentos (RAM) a la Medicina Natural y Tradicional, realizados por la Unidad Coordinadora Nacional de Farmacovigilancia, se corroboran estos resultados.8-11
Es importante señalar que los productos naturales están expuestos a producir interacciones medicamentosas cuando se utilizan en combinación con los medicamentos de síntesis química, bien hayan sido estos prescritos por el médico o por autoadministración del paciente. Estas interacciones pueden ser sinérgicas o antagónicas y pueden producirse tanto en la fase farmacéutica, como farmacocinética o farmacodinámica.
En la literatura se recogen reportes de estos tipos de interacciones, por ejemplo, la potenciación del efecto anticoagulante de la warfarina con el uso del ajo, aumenta el tiempo de coagulación con sus consecuentes complicaciones, además, se reportaron dos casos de toxicidad gastrointestinal con el uso concomitante de este producto natural con el saquinavir, medicamento antirretroviral.12-13
Por el espacio que ocupan en la terapéutica farmacológica actual en Cuba, la amplia utilización de los mismos en los distintos servicios de atención médica que se presta, la repercusión social que tiene el uso de los medicamentos herbolarios y las consecuencias económicas y sanitarias de las reacciones que estos provocan, es que se decide realizar este estudio. Todo lo anterior se corrobora si se tienen en cuenta que existe gran número de usuarios de medicamentos herbarios, pero se dispone de escasa información fiable acerca de la inocuidad de los mismos.
A eso se le adiciona que las notificaciones de sospechas de reacciones adversas para estos productos son bajas e insuficientes para detectar efectos adversos no reportados o importantes. Además, los consumidores tienden a utilizar esos productos para la automedicación, a veces junto a otros fármacos, porque tienen la opinión de que son inocuos, sin tener en cuenta las posibles interacciones medicamentosas a las que se exponen.
Todos estos elementos justifican la necesidad de realizar este estudio, de tal forma que permita disponer de valiosos elementos para hacer un uso racional de los fitofármacos y apifármacos, mejorando la efectividad de éstos. En consecuencia se disminuirán los costos sanitarios y no sanitarios derivados del uso inadecuado de estos productos, al caracterizar las reacciones adversas asociadas al uso de los fitofármacos que se comercializan en el país, en el período 2003-2010.
MÉTODOS
Se trata de un estudio que clasifica como observacional, descriptivo y retrospectivo. Se consideró elegible para el mismo la totalidad de los reportes de sospechas de RAM producidas por fitofármacos a la Unidad Coordinadora Nacional de Farmacovigilancia (UCNFv) de Cuba ubicada en la Dirección Nacional de Medicamentos del Ministerio de Salud Pública durante los años 2003-2010.
La información se obtuvo de la base de datos nacional (VIGIBASE) del Sistema Cubano de Farmacovigilancia. Confeccionándose a partir de ésta, una nueva base de datos en Excel, que incluyó todas las reacciones adversas por fitofármacos y apifármacos reportadas durante el período de estudio. Se incluyeron variables demográficas (edad, sexo), tipo de fitofármaco y de RAM. Las sospechas de RAM fueron clasificadas según el órgano afectado, la severidad y la causalidad.
Para clasificar las reacciones adversas aplicando relación de causalidad, gravedad y sistema de órgano afectado, se creó un grupo de 7 expertos farmacólogos y especialistas de Medicina General Integral con experiencia en el tema de más de cinco años. Para la relación de imputabilidad se siguió los criterios de Karch y Lasagna. El sistema de órganos afectados y la severidad se clasificaron según los criterios de Uppsala Monitoring Center.
Para el análisis de los datos se utilizó la estadística descriptiva. Como medidas de resumen se presentan los datos en frecuencias relativas y absolutas. Los resultados se procesaron por el paquete estadístico Excel de Microsoft Office y se presentan en tablas para una mejor comprensión. Desde el punto de vista ético, la investigación tuvo como objetivo esencial el aspecto puramente científico, sin afectaciones del medio ambiente ni riesgos predecibles y se contó con el consentimiento informado del especialista que atiende las series de RAM de medicamentos de la UCNFv.
RESULTADOS
Las notificaciones de pacientes adultos comprendidos en las edades de 31 a 60 años, como se observa en la tabla 1, constituyeron más de la mitad (52,5 %) de los reportes analizados, mientras que la edad pediátrica solo significó el 5,9 % del total. Cabe señalar que los pacientes mayores de 60 años representaron casi el 30 %.
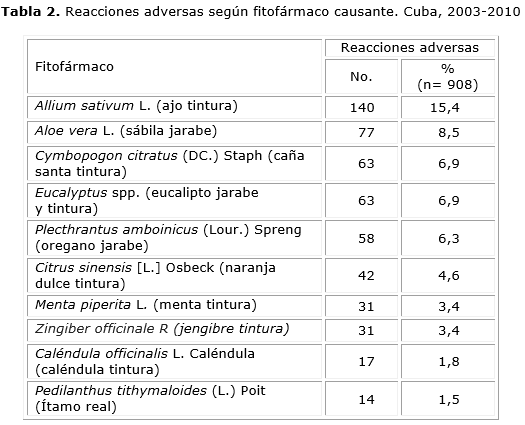
La tabla 2 recoge los 10 fitofármacos que con más frecuencia causaron RAM, se puede apreciar que el ajo resulto ser el fitofármaco causante del 15,4 % de las RAM, seguido por la sábila que produjo el 8,5 % del total.
Otros fitofármacos que ser reportaron con una frecuencia mayor del 5 % son: caña santa, eucalipto y orégano con 6,9 % los dos primeros.
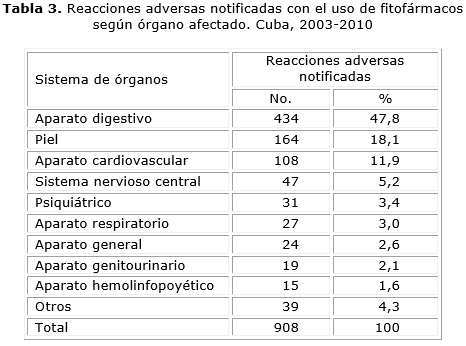
Las RAM reportadas se agruparon según sistema de órganos afectado, se encontró que el aparato digestivo pertenecen casi la mitad de las RAM (47,8 %), el segundo lugar lo ocupa la piel con el 18,1 % y el aparato cardiovascular donde se incluyeron el 11,9 % del total de RAM reportadas (tabla 3).
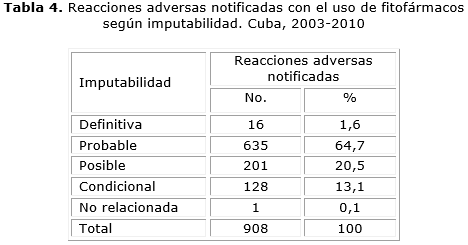
A las RAM reportadas se les aplicó el algoritmo propuesto por Uppsala Monitoring Center para definir su imputabilidad. Se encontró que las RAM probables fueron las más frecuentes con el 64,7 % del total, como posible fueron clasificadas el 20,5 %. Como definitiva fueron clasificadas 16 RAM, lo que representa el 1,6 % del total (tabla 4).
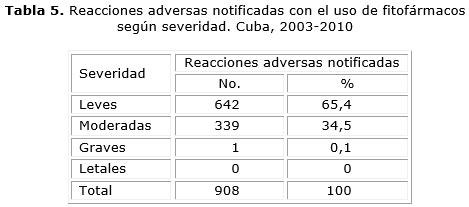
Según severidad predominaron las RAM leves con el 65,4 %, las moderadas ocuparon el segundo lugar con el 34,5 %. No se reportó ninguna RAM letal (tabla 5).
DISCUSIÓN
La vigilancia y el acopio de RAM ocurren en los últimos tiempos con mayor intensidad en los medicamentos innovadores durante su empleo por la población en los primeros años, con la finalidad de tomar decisiones oportunas y evitarlas en lo posible. Sin embargo, cuando se trata del empleo de plantas medicinales, fitofármacos, preparados herbales o análogos, la vigilancia de respuestas adversas inesperadas es escasa. El incremento del consumo de tales productos, vendidos en muchos casos como suplementos dietarios en países desarrollados, provoca que el paciente lo consuma simultáneamente con medicamentos convencionales de la práctica médica, por lo que se han descrito interacciones con estos medicamentos.14
De otro lado, el empleo de productos naturales en algunos países parece ocurrir porque el estrato mayoritario de la sociedad tiene acceso limitado a medicamentos, en algunos casos el 70 a 80 % de la población utiliza o ha utilizado productos naturales, productos herbales o fitofármacos para sus cuidados primarios de salud, solos o combinados con los convencionales.15,16
No hay dudas de las enormes potencialidades de las plantas medicinales, pues constituyen una excelente opción en la búsqueda de nuevos fármacos. Pero es conveniente, incorporar estudios clínicos a fin de distinguir sus efectos. En el concepto tradicional del empleo de plantas medicinales, se atribuyen acciones no demostrados a algunas plantas medicinales, ni siquiera empleadas en forma tradicional para tales efectos.
La vigilancia de productos naturales y fitofármacos no suele estar lo suficiente desarrollado para ofrecer datos de prevalencia, o datos con relación a interacción, porque faltan los datos de denominador, ya que son todos de venta libre. Las reacciones adversas a productos naturales se notifican apenas; sean leves, moderadas o severas.
Estudios de fármacovigilancia en hospitales han establecido una relación lineal entre edad y frecuencia de reacciones adversas a medicamentos, las que son muy bajas en personas entre 20 y 29 años y aumenta a un cuarto en adultos mayores. No obstante, según Low Dog, la población con edades comprendidas entre los 50 y 59 años tiende a aumentar el consumo de fitofármacos y por consiguiente un incremento de las reacciones adversas producidas por éstos.
La mayor frecuencia de RAM identificadas en este estudio fue en los adultos, al coincidir con lo referenciado por Ávila en 2001-2004 y difiere con la mayoría de lo reportado por la literatura, donde aparece un mayor número de reportes de reacciones adversas a los medicamentos en los ancianos.17 El reporte en los ancianos pudiera deberse a que los mismos por lo general consumen un alto número de medicamentos que pudieran provocar interacciones y favorecen el incumplimiento, a lo que se añaden cambios fisiológicos que generan modificaciones de los procesos farmacocinéticos como el metabolismo y la excreción que tienden a aumentar los niveles séricos y una menor capacidad de compensación de los efectos farmacológicos.
Un estudio realizado por Hernández Núñez en población pediátrica reportó muy baja frecuencia de aparición de reacciones adversas tal como se encontró en este trabajo. Este comportamiento pudiera explicarse por las escasas evidencias científicas que avalen el uso de esta alternativa en la terapéutica de menores. Por otra parte, las estrategias de educación a la población que desarrolla el MINSAP sobre los riesgos de medicar a los menores sin previa prescripción médica a través, los medios de comunicación, también pudieran explicar una baja frecuencia de aparición de reacciones a estos productos.
La mayor frecuencia de reportes asociados a medicamentos derivados del ajo, el eucalipto y la sábila pudiera ser derivada de la alta prevalencia en Cuba de las enfermedades para las que son usadas con mayor frecuencia. Entre estas afecciones pueden citarse las artropatías, enfermedades respiratorias o cardiovasculares, etc.17,18
Por otra parte, el uso popular de estas plantas a partir de infusiones y otras preparaciones artesanales elaboradas en el hogar hace que su consumo sea más frecuente, de acuerdo a la opinión de los autores.
La presencia de mayor número de sospechas de RAM en el aparato digestivo pudiera explicarse porque dentro de las vías de administración que existen,16 para los productos naturales, la oral es la más utilizada por la población, y dentro de ella la forma farmacéutica más empleada es la tintura.19
Esta presentación tiene como excipiente el alcohol etílico, elemento que pudiera explicar en parte la aparición de este tipo de reacciones, se conoce que el mismo produce injuria de la mucosa gástrica, con daño del endotelio microvascular que conduce al estasis microvascular, cesación del suministro de oxígeno, del transporte de nutrientes y de ahí a una necrosis por isquemia.20
Estos resultados coinciden con estudios anteriores realizados por la autora donde se comparó el comportamiento de las reacciones adversas por fitofármacos en los años 2003, 2005 y 2007,6 y otro que caracterizó las reacciones adversas asociadas al uso de los fitofármacos y apifármacos que se comercializan en Cuba en el período 2006-2010.21
Las manifestaciones cutáneas reportadas para el Aloe vera coinciden con las descritas por Ferreira22 en un estudio realizado en Portugal donde la dermatitis por este producto fue el hallazgo más frecuente. Este tipo de lesión, según Reider y col. 23 puede explicarse ya que esta planta contiene sustancias tóxicas e irritantes, compuestos que son eliminados en el proceso de producción industrial de formas farmacéuticas de uso tópico. En esta investigación que haya sido la sábila uno de los fitofármacos con mayor reporte de RAM, se considera que pudiera ser consecuencia de la automedicación de esta planta por aplicación local.
Aunque en la literatura24 existen reportes de efectos hepatotóxicos para el aloe, el ajo y la valeriana, como consecuencia de los altos contenidos de alcaloides pirrolizidínicos en estas plantas; en este estudio los reportes para esta reacción fueron muy bajos. A diferencia de lo adquirido por la literatura, donde plantea que las RAM clasificadas como posibles son los más frecuentes,25 en el estudio el mayor número de reacciones adversas fueron incluidas dentro de la categoría de probable. Estos resultados coinciden con los encontrados por Santos Muñoz y col.26 en Matanzas en un estudio similar en un período de 5 años.
Los fitofármacos causantes de la mayoría de las notificaciones, provocaron reacciones adversas leves o moderadas. Contrario a lo que muchas personas piensan sobre la seguridad de los productos naturales, o sea, que éstos son seguros e inocuos, estos sí producen reacciones adversas. Aunque en este estudio sólo se reportó una reacción adversa grave, hay un considerado número de reacciones moderadas.
Estos hallazgos constituyen una alerta para la población que consume productos naturales por automedicación, para el profesional de la salud en el momento del acto de la prescripción y para el farmacéutico durante el proceso de dispensación, donde se debe advertir al paciente de los riesgos que están sometidos cuando emplean estos productos.
Se concluye que la caracterización realizada de las sospechas de reacciones adversas (RAM) asociadas al uso de fitofármacos comercializados en Cuba período 2003-2010, muestra similitud con la reportada a los medicamentos de síntesis química; son el ajo, la sábila y la caña santa los fitofármacos responsables de la mayoría de las RAM en los adultos, que provoca manifestaciones en aparato digestivo y piel de tipo leve.
REFERENCIAS BIBLIOGRÁFICAS
1. Furones JA. Bases científicas para el desarrollo y utilización de los medicamentos. En: Farmacología general. La Habana. Editorial ECIMED. 2002:9-21.
2. Tamayo C. Fitoterapia basada en la evidencia. Revista de Fitoterapia. 2006 [citado enero 2014];6(S1). Disponible en: http://www.plantasmedicinais.com/revista/pdf/C-TAMAYO.pdf
3. Norris W, Paredes AH, Lewis JH. Drug-induced liver injury in 2007. Curr Opin Gastroenterol. 2008;24(3):287-97.
4. Valsecia M. Farmacovigilancia y mecanismos de reacciones adversas a medicamentos. [citado Junio 2010]. Disponible en: http://med.unne.edu.ar
5. Furones JA. Caracterización de las notificaciones de reacciones adversas por medicina natural y bioenergética del Sistema de Farmacovigilancia en Cuba. Años 2005-2007. [Tesis para optar por titulo de Máster en Medicina Bioenergética y Natural]. La Habana. Facultad de Ciencias Médicas. Universidad de Ciencias Médicas de La Habana. 2008.
6. García Milián AJ, Alonso Carbonel L, Avila Y, Lopez Puig P, Ruiz Salvador AK, Morón Rodríguez FJ. Reacciones adversas reportadas con el consumo de productos naturales en Cuba. 2003, 2005, 2007. Lat. Am. J. Pharm. 2009 [citado enero 2014];28(3):337-43. Disponible en: http://www.latamjpharm.org/trabajos/28/3/LAJOP_28_3_1_3_JHNOCATGCV.pdf
7. Ávila Pérez J, Jiménez López G, González Delgado B, Morón Rodríguez F, Fernández Argüelles R. Reacciones adversas a medicamentos herbarios y otras formas de medicina natural y tradicional en Cuba durante 2001-2004. Rev Cubana Plant Med. [online]. 2008;13(1). [citado enero 2014]. Disponible en: http://bvs.sld.cu/revistas/pla/vol13_1_08/pla03108.htm
8. Unidad Coordinadora Nacional de Farmacovigilancia. Informe anual de sospechas de RAM a la Medicina Natural y Tradicional. 2005. Ciudad Habana: UCNFV; 2005.
9. _____. 2006. Ciudad Habana: UCNFV; 2006.
10. _____. 2007. Ciudad Habana: UCNFV; 2007.
11. Ávila Pérez J, Jiménez López G y Alfonso Orta I. Natuseguridad 17. Unidad Coordinadora Nacional de Farmacovigilancia. 2008. Tres JC. Interacción entre fármacos y plantas medicinales. An. Sist. Sanit. Navar. 2006;29(2):233-52.
12. Remirez D, Avila J, Jiménez G, Jacobo OL, O'Brien PJ. Interactions Between Herbal Remedies and Medicinal Drugs - Considerations about Cuba. Drug Metabolism and Drug Interactions. 2009;24(2-4):183-94.
13. Goldstein LH, Elias M, Ron-Avraham G, Biniaurishvili BZ, Madjar M, Kamargash I, et al. Consumption of herbal remedies and dietary supplements amongst patients hospitalized in medical wards. Br J Clin Pharmacol. 2007;64(3):373-80.
14. Wanda GJ, Njamen D, Yankep E, Fotsing MT, Fomum ZT, Wober J, et al. Estrogenic properties of isoflavones derived from Millettia griffoniana. Phytomedicine. 2006;13(3):139-45.
15. Howell L, Kochhar K, Saywell R, Zollinger T, Koheler J, Mandzuk C, et al. Use of herbal remedies by Hispanic patients: do they inform their physician? J Am Board Fam Med. 2006;19(6):566-78.
16. Alonso J. Aplicación de los Fitofármacos en la clínica diaria. En: Lozoya X. V Simposio Internacional de Fitofármacos: Los Fitofármacos en la Clínica Moderna. México DF: IMSS-Farmassa Schwabe. 2001:79-88.
17. TRAMIL. Farmacopea vegetal caribeña. Enda/caribe. 2004;36(54):258
18. Álvarez Corredera M. Vías de administración de los medicamentos y sus formas farmacéuticas en: Farmacología general. Editorial Ciencias Médicas. La Habana. 2000:22-33.
19. Tornawski A. Mecanismos celulares y moleculares de la mucosa gástrica: la injuria a la mucosa y la acción protectora de los antiácidos. Rev. gastroenterol. Perú. 1995 [citado octubre 2011];15(1):74-8. Disponible en: http://sisbib.unmsm.edu.pe/bvrevistas/gastro/vol_15n1/mecanismos.htm
20. Ruiz Salvador AK, García Milian AJ, Jiménez López G, Alfonso Orta I, Pérez Hernández B, Carrazana Lee A. Farmacovigilancia de fitofármacos y apifármacos en Cuba durante 2006-2010. Revista Cubana de Plan Med. 2013 [citado octubre 2011];18(2). Disponible en: http://scielo.sld.cu/scielo.php?pid=S1028-47962013000200002&script=sci_arttext
21. Ferreira M, Teixeira M, Silva E, Selores M. Allergic contact dermatitis to Aloe vera. Contact Dermatitis. 2007;57(4):278-9.
22. Reider N, Issa A, Hawranek T, Schuster C, Aberer W, Kofler H, et al. Absence of contact sensitization to Aloe vera (L.) Burm. f. Contact Dermatitis. 2005;53:332-4.
23. Fernandes da Silveira P, Medeiros Bandeira MA. Farmacovigilância e reações adversas às plantas medicinais e fitoterápicos: uma realidade. Rev. Bras. Farmacogn. 2008 [citado septiembre de 2014];18(4):618-26. Disponible en: http://www.scielo.br/pdf/rbfar/v18n4/v18n4a21.pdf
24. Anónimo. Registro de acontecimientos adversos en ensayos clínicos. Boletín de la Sociedad Española de Farmacología Clínica dirigido a los Comités Éticos de Investigación Clínica. ICB 11. Instituto Catalán de Farmacología. Barcelona 1994. [citado 2008 Mayo 19]. Disponible en: http://www.icf.uab.es/icbdigital/pdf/boletines/icb1194.pdf
25. Jiménez G, Debesa F, González B, Ávila J, Pérez J. El Sistema Cubano de Farmacovigilancia: seis años de experiencia en la detección de efectos adversos. Rev Cubana Farm. 2006 [citado 19 de septiembre de 2009];40(1). Disponible en: http://bvs.sld.cu/revistas/far/vol40_1_06/far02106.htm
26. Santos Muñoz L, Perdomo Delgado J, González Pla EA. Behavior of adverse reactions caused by natural products. Matanzas 2003-2008. Revista Médica Electrónica. 2009 [citado septiembre de 2014];31(6). Disponible en: https://www.google.com.cu/?gws_rd=ssl#
Recibido: 31 de enero de 2014.
Aprobado: 12 de enero de 2015.
Ms. Ana Karelia Ruiz Salvador. Facultad de Ciencias Médicas “General Calixto García”. La Habana, Cuba.
Correo electrónico: karelia.ruiz@infomed.sld.cu