Meu SciELO
Serviços Personalizados
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Cubana de Plantas Medicinales
versão On-line ISSN 1028-4796
Rev Cubana Plant Med vol.21 no.4 Ciudad de la Habana oct.-dez. 2016
ARTÍCULO ORIGINAL
Caracterización fitoquímica y evaluación de actividad inhibitoria sobre acetilcolinesterasa de hojas de Piper pesaresanum C. DC
Phytochemical characterization and evaluation of the inhibitory activity of Piper pesaresanum C. DC leaves against acetylcholinesterase
Ledy Yolima Nitola,I Diego Ricardo Muñoz,I Oscar Javier Patiño,II Juliet Angélica PrietoIII
IUniversidad de Ciencias Ambientales y Aplicadas. Colombia.
IIUniversidad Nacional de Colombia. Colombia.
IIIPontificia Universidad Javeriana. Bogotá D.C. Colombia.
RESUMEN
Introducción: el género Piper perteneciente a la familia Piperaceae es de gran importancia económica debido a sus aplicaciones a nivel alimenticio, industrial y medicinal. Especies de este género son conocidas popularmente como cordoncillos y se caracterizan porque presentan un amplio espectro de actividades biológicas, entre las que se encuentra el efecto neuroprotector, que está asociado al tratamiento de enfermedades neurodegenerativas como el Alzheimer. En Colombia existen muchas especies a las cuales no se les han desarrollado estudios investigativos, tal es el caso de Piper pesaresanum C. DC.
Objetivo: caracterizar química y biológicamente el extracto etanólico de hojas de P. pesaresanum mediante un estudio fitoquímico biodirigido y evaluar la actividad inhibitoria sobre acetilcolinesterasa.
Métodos: a partir del extracto etanólico de hojas maduras de P. pesarenasum se realizó un estudio químico biodirigido para aislar e identificar las sustancias responsables de la actividad inhibitoria sobre acetilcolinesterasa. La evaluación de la actividad inhibitoria sobre acetilcolinesterasa se realizó por autografía directa empleando el método de Ellman. Adicionalmente se realizó un tamizaje fitoquímico preliminar mediante pruebas de coloración y precipitación llevadas a cabo en vía húmeda y cromatografía en capa delgada.
Resultados: el análisis fitoquímico preliminar sugiere la presencia de terpenos, esteroides, fenoles y cumarinas. La evaluación de la actividad inhibitoria sobre acetilcolinesterasa permitió evidenciar zonas claras de inhibición en las fracciones de éter de petróleo (EP) y cloroformo (CHCl3). El estudio fitoquímico biodirigido condujo al aislamiento e identificación por primera vez para la especie del ácido 4-metoxi-3,5-di(3'-metil-2'-butenil) benzoico.
Conclusiones: el estudio químico y de actividad biológica llevado a cabo en la especie P. pesaresanum permitió identificar al ácido 4-metoxi-3,5-di(3'-metil-2'-butenil) benzoico como uno de los compuestos responsables de la actividad inhibitoria sobre acetilcolinesterasa.
Palabras clave: Piper pesaresanum; Piperaceae; acetilcolinesterasa; análisis fitoquímico; Alzheimer.
ABSTRACT
Introduction: The genus Piper, from the Piperaceae family, has great economic importance, due to its uses on a nutritional, industrial and medicinal level. The species in this genus are commonly known as peppers, and are characterized by a broad range of biological activities, including a neuroprotective effect associated with the treatment of neurodegenerative conditions such as Alzheimer's disease. Many of the species growing in Colombia have not been studied. Such is the case with Piper pesaresanum C. DC.
Objective: Carry out a chemical and biological characterization of the ethanolic extract of P. pesaresanum leaves by means of a bioguided phytochemical study and evaluate inhibitory activity on acetylcholinesterase.
Methods: A bioguided chemical study was conducted of the ethanolic extract of P. pesarenasum mature leaves to isolate and identify the substances responsible for inhibitory activity on acetylcholinesterase. Evaluation of inhibitory activity on acetylcholinesterase was based on direct autography using the Ellman method. Preliminary phytochemical screening was also performed by means of wet color and precipitation tests, and thin-layer chromatography.
Results: Preliminary phytochemical analysis suggests the presence of terpenes, steroids, phenols and coumarins. Evaluation of inhibitory activity on acetylcholinesterase revealed clear-cut inhibition areas in petroleum ether (PE) and chloroform (CHCl3) fractions. The bioguided phytochemical study led to isolation and identification of 4-methoxy-3.5-di(3'-methyl-2'-butenyl) benzoic acid for the first time in the study species.
Conclusions: Chemical study and evaluation of the biological activity of the species P. pesaresanum led to identification of 4-methoxy-3.5-di(3'-methyl-2'-butenyl) benzoic acid as one of the compounds responsible for inhibitory activity on acetylcholinesterase.
Keywords: Piper pesaresanum; Piperaceae; acetylcholinesterase; phytochemical analysis; Alzheimer's disease.
INTRODUCCIÓN
La acetilcolinesterasa (AChE) es una enzima del grupo de las hidrolasas que está presente en la mayoría de los seres vivos, localizada generalmente en el sistema nervioso y en los músculos. Esta enzima es la responsable de la regulación de la concentración de la acetilcolina (ACh), un neurotransmisor involucrado en la sinapsis colinérgica en el sistema nervioso, que permite la transmisión de la señal nerviosa en el sistema nervioso central y periférico. Inhibición de la AChE ha encontrado aplicaciones en el tratamiento de enfermedades neurodegenerativas, como Alzheimer; en enfermedades neuromusculares, como la Miastenia Gravis (MG); y en trastornos oculares como el Glaucoma. Aunque en el mercado se encuentran medicamentos con inhibidores de acetilcolinesterasa, existe la necesidad de buscar nuevas sustancias pues para estas enfermedades los tratamientos existentes no son totalmente efectivos.1-3
Los inhibidores de AChE también han sido aplicados en la agricultura gracias a los efectos que ellos tienen sobre el sistema nervioso de algunos invertebrados que son considerados como plagas y pestes en los cultivos. Los productos usados como pesticidas incluyen algunos principios activos que pueden interactuar con el sitio activo de la enzima tanto de forma irreversible como reversible, ocasionando así el deceso del organismo que entra en contacto con el inhibidor. De esta forma muchos productos comerciales son poco selectivos, pueden causar daños en la salud de las personas que los aplican y generalmente causan serios problemas ambientales, por lo que se están buscando nuevas sustancias aplicables en este campo que sean seguras y de bajo impacto ambiental.4-5
Las plantas han sido una de las fuentes más importantes para la búsqueda de compuestos con actividad inhibitoria frente a AChE. Se han aislado diferentes tipos de metabolitos con promisoria actividad inhibitoria entre los que sobresalen los alcaloides, flavonoides y terpenos. Se destacan por su actividad fisostigmina, huperzina A y galantamina, aislados de Physostigma venenosum, Lycopodium serratum y Galanthus woronowii, respectivamente.3,6-7 A pesar de que las investigaciones en fitoquímica son cada vez más numerosas, aún existen muchas especies a las cuales no se les ha realizado ningún tipo de investigación, algunas están en peligro de extinción, por lo que su perdida involucraría también la perdida de los compuestos potencialmente útiles que estas contienen.6-7
El género Piper es uno de los más representativos de la familia Piperaceae, comprende alrededor de 700 especies distribuidas a nivel mundial principalmente en las regiones tropicales y subtropicales.8 Muchas de estas especies se caracterizan por sus usos etnobotánicos y las aplicaciones que se les han determinado a nivel alimenticio, agrícola y terapéutico.8,9 Algunas especies representativas son P. nigrum, P. methysticum y P. aduncum. La pimienta negra utilizada como especia se obtiene de la inflorescencias de P. nigrum; de las raíces de P. methysticum se elabora un preparado muy popular conocido como kava-kava, al cual se le atribuyen efectos calmantes y relajantes; P. aduncum se suele sembrar en medio de los cultivos de café dado los efecto repelentes que presenta y es una especie promisoria para el tratamiento de la enfermedad de Alzheimer dada la capacidad neuroprotectora que presenta frente al daño neuronal inducido por el péptido amiloide.8-11
En Colombia, el género Piper se encuentra ampliamente distribuido y a muchas de las especies presentes en el territorio colombiano no se les han realizado estudios investigativos, tal es el caso de la especie P. pesaresanum. Por lo que hacen de este país un lugar atractivo para emprender investigaciones multidisciplinarias a fin de caracterizar química y biológicamente las especies colombianas.
El objetivo del presente trabajo es contribuir a las investigaciones en el género Piper mediante el estudio fitoquímico del extracto de hojas de la especie P. pesaresanum y evaluar la actividad inhibitoria sobre acetilcolinesterasa.
MÉTODOS
Materiales y equipos
Los solventes empleados para la preparación de extractos y las separaciones cromatográficas fueron de grado técnico (destilados antes de su uso) y/o grado analítico. Las separaciones cromatográficas en columna se realizaron mediante cromatografía flash (CF) y cromatografía líquida al vacío (CLV). La fase estacionaria utilizada para la CF fue sílica gel 60 Merck (230-400 Mesh) y para CLV sílica gel 60 HF254 Merck. Los estudios cromatográficos, el monitoreo de las cromatografías en columna y el control de pureza se realizaron por cromatografía en capa delgada (CCD), se empleó cromatoplacas de sílica gel 60 HF254 Merck, utilizando como reveladores vapores de yodo y luz UV (254 y 365 nm). Los espectros Infrarrojo (IR) fueron registrados en el espectrómetro Nicolet iS10 Spectrometer Thermo Fisher Scientific. Los espectros de resonancia magnética nuclear de 1H y 13C, así como los experimentos DEPT 135 (Distortionless Enhancement by Polarization Transfer), COSY (Correlation Spectroscopy), HMQC (Heteronuclear Multiple Quantum Correlation) y HMBC (Heteronuclear Multiple Bond Correlation) fueron tomados en un espectrómetro Bruker Avance 300, operado a 300 MHz para 1H y a 75 MHz para 13C. Como solvente y patrón interno se empleó cloroformo deuterado (CDCl3) a una temperatura de 25 °C.
Material vegetal y obtención del extracto
El material vegetal de P. pesaresanum fue colectado en el corregimiento de Virolín, perteneciente al municipio de Charalá, departamento de Santander. La especie vegetal fue determinada por el Biólogo Ricardo Callejas y un espécimen reposa en el Herbario Nacional Colombiano, perteneciente a la Universidad Nacional de Colombia (Bogotá D.C., Colombia) bajo el número de colección COL 553307.
Las hojas maduras de P. pesaresanum se secaron a la sombra por un periodo de tres semanas y posteriormente se trituraron en un molino de cuchillas. El material vegetal seco y molido fue sometido a extracción por maceración con etanol al 96 % a temperatura ambiente. El extracto se concentró a presión reducida a 40 °C hasta obtener un extracto seco (120 g).
Análisis fitoquímico preliminar
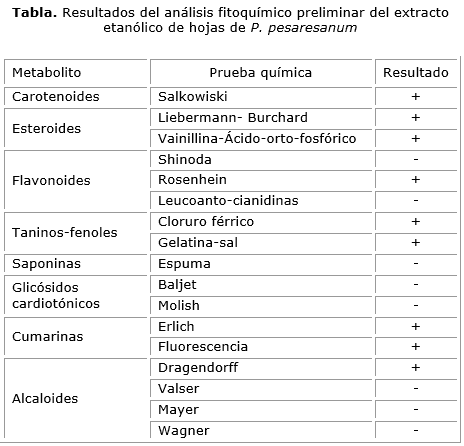
Se tomaron 2 g del extracto etanólico y se realizaron las pruebas cualitativas de coloración, precipitación y en cromatografía en capa delgada (CCD), siguiendo las metodologías descritas en la literatura.12-14 Para corroborar la presencia de grupos de metabolitos secundarios se usaron controles positivos y negativos en cada ensayo. Los resultados del análisis fitoquímico preliminar realizado se resumen en la tabla.
Evaluación de actividad inhibitoria sobre acetilcolinesterasa por autografía en CCD - Método Ellman
Al extracto etanólico se le realizó el ensayo de inhibición enzimática sobre acetilcolinesterasa en CCD empleando el método de Ellman. La acetilcolinesterasa de anguila eléctrica (1000 U) se disolvió en 150 mL de solución buffer fosfato 0.2 M de pH 7.8 y se estabilizó con 150 mg de albúmina de suero bovino (BSA). La disolución madre de la enzima se conservó a 4°C hasta su uso. Las placas cromatográficas se eluyeron por separado con dos sistemas de solventes (Cloroformo-metanol 95:5 y Hexano-Acetato de etilo 8:2). A cada placa se le dejó evaporar por completo el solvente y luego estas se asperjaron con una mezcla equimolar (1 mM) de ioduro de acetiltiocolina (AcTChI) y ácido 2,4-ditionitrobenzóico (DTNB). Se secaron cuidadosamente y se incubaron por tres min a 37°C, para posteriormente rociar con la disolución madre de la enzima e incubar nuevamente a 37 °C por 5 min en atmósfera húmeda. La presencia de zonas de inhibición enzimática se determinó por la aparición de regiones blancas sobre un fondo amarillo pálido en la placa.15
Fraccionamiento biodirigido
A 70 g del extracto etanólico se le realizó un fraccionamiento sólido-líquido en un equipo soxhlet con solventes de polaridad creciente: éter de petróleo (EP), cloroformo (CHCl3) acetato de etilo (AcOEt) y metanol (MeOH). Por posterior concentración de los disolventes se obtuvieron las fracciones de EP (23,8 g), CHCl3 (34,6 g), AcOEt (2,2 g) y MeOH (1,0 g). A cada una de las fracciones se les realizó el ensayo de inhibición enzimática sobre acetilcolinesterasa empleando el método de Ellman.
La fracción EP, que fue la que presentó las zonas más claras de inhibición de la acetilcolinesterasa, se fraccionó por CLV eluyendo con CH2Cl2 y mezclas de CH2Cl2:MeOH de polaridad creciente (90:10 a 0:100), se obtuvieron seis fracciones (1.1-1.6). A cada una de las fracciones se les realizó el ensayo de inhibición enzimática sobre acetilcolinesterasa. La fracción 1.3 (2,08 g) se purificó mediante CF repetitiva, se empleó sílica gel como fase estacionaria y como sistemas de elución CH2Cl2:Acetona (97:3) y Hexano:Acetona (60:40), el resultado fueron unos cristales ligeramente verdes (171 mg) correspondientes al ácido 4-metoxi-3,5-di(3'-metil-2'-butenil) benzoico.
RESULTADOS
Rendimientos de extracción
De 850 g de material vegetal recolectado se obtuvieron 120 g de extracto etanólico seco, estableciéndose un rendimiento del 14,1 % (relación entre material vegetal seco/molido y extracto obtenido). El rendimiento total del proceso de fraccionamiento del extracto fue del 88,0 %, siendo las fracciones EP y CHCl3 las que mostraron el mayor rendimiento con porcentajes del 34,0 y 49,4 % respectivamente. El rendimiento de las demás fracciones fue inferior al 4,0 %.
Los resultados del análisis fitoquímico preliminar para el extracto etanólico P. pesaresanum muestran el comportamiento en relación con el tipo de metabolito, la prueba química empleada y los resultados con signo positivo (+) para aquellas sustancias que están presentes, y con signo negativo (-) para aquellas ausentes (tabla).
Dichos resultados evidencian que la especie P. pesaresanum presenta entre sus principales constituyentes terpenos, esteroides, fenoles y cumarinas.
Evaluación de actividad inhibitoria sobre acetilcolinesterasa
El ensayo por autografía realizado al extracto etanólico para detectar grupos de sustancias que causaran la inhibición de la acetilcolinesterasa, permitió evidenciar que las sustancias de baja a media polaridad presentes en el extracto eran las responsables de la inhibición enzimática. Se fracciono el extracto con solventes de polaridad creciente con el objetivo de obtener mezclas de metabolitos secundarios de polaridad similar. Las fracciones (EP, CHCl3, AcOEt y MeOH) fueron también sometidas al ensayo de inhibición de la acetilcolinesterasa en CCD, encontrándose que en las fracciones más polares no se apreciaban zonas claras de inhibición, mientras que en las fracciones EP y CHCl3 se encontraron diversas zonas de inhibición enzimática. Para la fracción EP se observaron el mayor número de zonas blancas de inhibición enzimática, por lo que esta fue sometida a un estudio biodirigido para aislar por lo menos uno de los metabolitos secundarios responsables del efecto inhibitorio sobre acetilcolinesterasa.
Estudio fitoquímico biodirigido
El estudio fitoquímico biodirigido realizado sobre el extracto etanólico de hojas de P. pesaresanum permitió el aislamiento e identificación de un derivado de ácido benzoico conocido como ácido 4-metoxi-3,5-di(3'-metil-2'-butenil) benzoico, cuya estructura se ilustra en la figura. El compuesto se obtuvo como cristales en forma de agujas de color amarillo-verdoso, con punto de fusión 94-95 °C. Su estructura fue elucidada empleando métodos espectroscópicos y por comparación con datos de la literatura.16
La evaluación de la actividad inhibitoria sobre acetilcolinesterasa determinada por autografía permitió evidenciar que con 50 µg de ácido 4-metoxi-3,5-di(3'-metil-2'-butenil) benzoico es posible causar una inhibición detectable de la enzima, por lo que se puede postular como una de las sustancias responsables de la actividad inhibitoria observada preliminarmente en el extracto etanólico y en la fracción de éter de petróleo para P. pesaresanum.
DISCUSIÓN
Los resultados del estudio fitoquímico preliminar son consistentes con la quimiotaxonomía reportada para el género Piper, pues de acuerdo a lo encontrado en la literatura, las especies de este género se caracterizan por producir una amplia gama de metabolitos, entre los que se pueden destacar para algunas especies los terpenos, esteroides, fenoles y cumarinas.17-19 En un estudio recientemente realizado sobre un espécimen de P. persaresanum colectado en el parque regional natural Ucumarí (Pereira, Colombia), se determinaron mediante un tamizaje fitoquímico los constituyentes químicos con mayor presencia en esta especie (alcaloides, fenoles, terpenos, esteroides, saponinas, flavonoides y antraquinonas).20 Al comparar con nuestros resultados se observan algunas diferencias en la composición química para la especie, lo que puede deberse a los diferentes entornos ecológicos a los que estaban sometidos cada uno de los especímenes.
El derivado del ácido benzoico aislado se reporta por primera vez para la especie P. pesaresanum, pero dicha sustancia ha sido previamente reportada en otras especies del género Piper, como es el caso de P. aduncum y P. hispidum.16,21 El trabajo fitoquímico desarrollado en P. pesaresanum contribuye al conocimiento químico de la especie y del género Piper, pues apenas se reportan estudios fitoquímicos preliminares para la especie objeto de estudio.
El reporte del efecto inhibidor sobre la acetilcolinesterasa causado por el extracto, las fracciones y el compuesto de las hojas de P. pesaresanum constituye un nuevo aporte al conocimiento de las propiedades biológicas de especies de la familia Piperaceae. Además, proporciona información sobre posibles usos medicinales y/o agroindustriales que puede tener P. pesaresanum, ya que es una especie vegetal para la que no se reporta ningún uso tradicional. En un estudio de detección de inhibidores de la acetilcolinesterasa en plantas de la flora colombiana, en el que se usaron tres especies del género Piper recolectadas en el Parque Regional Natural Ucumarí, se determinó que el extracto metanólico de P. pesaresanum presentó una baja actividad inhibitoria de la acetilcolinesterasa, causando una inhibición inferior al 15 % con una concentración de 100 ppm.21 Estos resultados son consistentes con lo encontrado en nuestro trabajo, pues los resultados de la evaluación de la actividad inhibitoria de la acetilcolinesterasa de las fracciones indican que las sustancias capaces de inhibir la enzima se encuentran en las fracciones de baja (EP) y media polaridad (CHCl 3), y no en las fracciones polares. En otro trabajo enfocado en determinar el potencial antioxidante y antifúngico de Piperaceaes, se reportó la actividad antioxidante y antifúngica de los extractos de n-Hexano, CH2Cl2 y MeOH de P. pesaresanum, encontrando que los tres extractos evaluados presentaron promisoria actividad contra Fusarium solani y F. oxysporum.20
Teniendo en cuenta los resultados del estudio fitoquímico preliminar de la evaluación de la actividad de inhibición enzimática y que solo se realizó el aislamiento de una de las sustancias responsables de la actividad, es posible que otras sustancias fenólicas, terpenos y/o cumarinas sean las responsables de las zonas de inhibición enzimática observadas en los extractos y fracciones de hojas de P. pesaresanum.
Los resultados de este estudio de actividad inhibitoria preliminar sobre la acetilcolinesterasa contribuyen al conocimiento de las propiedades biológicas de las sustancias evaluadas, complementan los resultados de otros investigadores y constituyen el primer reporte de efectos inhibitorios sobre acetilcolinesterasa del extracto etanólico, las fracciones de P. pesaresanum y del ácido 4-metoxi-3,5-di(3'-metil-2'-butenil) benzoico, permitiendo establecer a estas sustancias como promisorias para continuar con ensayos de actividad más específicos, con el objetivo de alcanzar resultados más completos que permitan determinar si pueden llegar a convertirse en una nueva alternativa y/o compuesto plantilla para el diseño de nuevos fármacos para el tratamiento del Alzheimer o para la producción de nuevos agroquímicos.
AGRADECIMIENTOS
El presente trabajo fue realizado gracias a la colaboración de los grupos de investigación: "Grupo de investigación en productos naturales - PRONAUDCA" de la Universidad de Ciencias Ambientales y Aplicadas UDCA, "Estudio Químico y de Actividad Biológica de Rutaceas y Myristicaceas Colombianas" de la Universidad Nacional de Colombia, y "Grupo de Investigación Fitoquímica Universidad Javeriana - GIFUJ" de la Pontificia Universidad Javeriana.
CONFLICTOS DE INTERESES
Los autores declaran que no existen conflictos de intereses.
REFERENCIAS BIBLIOGRÁFICAS
1. Pohanka M. Inhibitors of Acetylcholinesterase and Butyrylcholinesterase Meet Immunity. Int J Mol Sci. 2014;15(6):9809-25.
2. Čolović MB, Krstić DZ, Lazarević-Pašti TD, Bondžić AM, Vasić VM. Acetylcholinesterase Inhibitors: Pharmacology and Toxicology. Curr Neuropharmacol. 2013;11(3):315-35.
3. Houghton PJ, Ren Y, Howes MJ. Acetylcholinesterase inhibitors from plants and fungi. Nat Prod Rep. 2006;23(2):181-99.
4. Pang YP, Brimijoin S, Ragsdale DW, Zhu KY, Suranyi R. Novel and viable acetylcholinesterase target site for developing effective and environmentally safe insecticides. Curr Drug Targets. 2012;13(4):471-82.
5. Polsinelli GA, Singh SK, Mishra RK, Suranyi R, Ragsdale DW, Pang YP, et al. Insect-specific irreversible inhibitors of acetylcholinesterase in pests including the bed bug, the eastern yellowjacket, German and American cockroaches, and the confused flour beetle. Chem Biol Interact. 2010;187(1-3):142-7.
6. Murray AP, Faraoni MB, Castro MJ, Alza NP, Cavallaro V. Natural AChE Inhibitors from Plants and their Contribution to Alzheimer's Disease Therapy. Curr Neuropharmacol. 2013;11(4):388-13.
7. Mukherjee PK, Kumar V, Mal M, Houghton PJ. Acetylcholinesterase inhibitors from plants. Phytomedicine. 2007;14(4):289-00.
8. Celis A, Mendoza C, Pachón M, Cardona J, Delgado W, Cuca L. Extractos vegetales utilizados como biocontroladores con énfasis en la familia Piperaceae. Agronomia Colombiana. 2008;26(1):97-06.
9. Nunkoo D, Mahomoodally M. Ethnopharmacological survey of native remedies commonly used against infectious diseases in the tropical island of Mauritius. J Ethnopharm.2012;143(2):548-64.
10. Zaa C, Valdivia M, Marcelo A. Efecto neuroprotector del extracto hidroalcohólico de Piper aduncum "matico" en un modelo in vitro de neurodegeneración. Rev Per Biol. 2012;19(3):249-56.
11. Plazas E. Estudio fitoquímico y Evaluación de actividad leishmanicida de la especie Piper hispidum Kunth. Tesis de maestría. Bogotá: Facultad de Ciencias, Departamento de Química, Universidad Nacional de Colombia; 2008; pp. 20-3.
12. Sanabria A. Análisis fitoquímico preliminar. Metodología y su aplicación en la evaluación de 40 plantas de la familia Compositeae. Bogotá: Facultad de Ciencias, Departamento de Farmacia, Universidad Nacional de Colombia; 1983.
13. Bilbao M. Investigación fitoquímica. Pereira: Universidad del Quindío. Facultad de Ciencias Básicas y tecnológicas. Programa de Química de Productos Vegetales; 1994.
14. Merck E. Reactivos de coloración para cromatografía en capa fina y en papel. Darmstadt. R. F. Alemania: Merck; 2000.
15. Rhee IK, Meent MV, Ingkaninan K, Veerporte R. Screening for acetylcholinesterase inhibitors from Amaryllidiaceae using silica gel thin-layer-chromatography in combination with bioactivity staining. J Chromatogr A. 2001;915(1-2):217-23.
16. Orjala J, Erdelmier CAJ, Wright AD, Rali T, Sticher O. Five new prenylated p-hydroxybenzoic acid derivatives with antimicrobial and molluscicidal activity from Piper aduncum leaves. Planta Med. 1993;59(6):546-51.
17. Parmar VS, Jain SC, Bisht KS, Jain R, Taneja P, Jha A, et al. Phytochemistry of the genus Piper. Phytochemistry. 1997;46(4):597-73.
18. Navickiene HMD, Alécio AC, Kato MJ, Bolzani V da S, Young MC, Cavalheiro AJ, et al. Antifungal amides from Piper hispidum and Piper tuberculatum. Phytochemistry. 2000;55(6):621-6.
19. Marques JV, de Oliveira A, Young MCM, Kato MJ. Antifungal piperolides, coumarins, pyrones and amides from Piper species and synthetic analogs. Planta Med. 2008;74(9):84.
20. Correa YM, Palomino LR, Mosquera OM. Actividad antioxidante y antifúngica de piperaceaes de la flora colombiana. Rev Cubana Plant Med. 2015; 20(2):167-81.
21. Baldoqui DC, Kato MJ, Cavalheiro AJ, Bolzani V da S, Young MC, Furlan M. A chromene and prenylated benzoic acid from Piper aduncum. Phytochemistry. 1999;51(7):899-02.
22. Valencia D. Detección in vitro de inhibidores de la acetilcolinesterasa en plantas de la flora colombiana por el método de Ellman. Trabajo de Grado. Pereira: Facultad de Tecnologías, Escuela de Tecnología Química, Universidad Tecnológica de Pereira; 2015; pp. 43-54.
Recibido: 30 de septiembre de 2015.
Aprobado: 8 de octubre de 2016.
Juliet Angélica Prieto. Pontificia Universidad Javeriana Bogotá D.C., Colombia. Correo electrónico: juliet.prieto@javeriana.edu.co