Introducción
El cáncer de páncreas es considerado un tumor agresivo, letal, debido a su rápida propagación a los ganglios linfáticos y órganos distantes, además, los síntomas específicos precoces son escasos o no están presentes, también hay pocos biomarcadores exactos para la detección precoz, comúnmente su diagnóstico es demorado y hay pocas opciones de tratamientos efectivos, por lo general, en el instante del diagnóstico, los pacientes tienen la enfermedad localmente avanzada e incluso con metástasis a distancia, lo que imposibilita el tratamiento quirúrgico-curativo.
En los países desarrollados el cáncer de páncreas ocupa el décimo lugar y alcanza del 2 al 3 % de todos los tumores sólidos. El adenocarcinoma de páncreas es el segundo tumor maligno gastrointestinal más frecuente.1,2,3
La prevalencia anual global para el cáncer de páncreas es de unos 8/100 mil habitantes. La incidencia del cáncer de páncreas varía a través de las regiones geográficas y poblaciones. La tasa de incidencia en el 2012 fue alta en Norteamérica 7,4/100 mil habitantes y se estimó que para el 2017 habría 53 670 nuevos casos. En el este de Europa la incidencia fue 7,3/100 mil habitantes, seguida por otras regiones de Europa y Australia/Nueva Zelandia 6,5/100 mil habitantes, respectivamente. Se pronostica que para 2030, de mantenerse las condiciones actuales, aumente su incidencia en un 50 %, transformándose en la segunda causa de muerte por cáncer y causando más muertes que el cáncer de próstata, colón o mama.
El cáncer de páncreas constituye la cuarta causa de muerte por cáncer. La tasa de mortalidad internacional para el cáncer de páncreas también varía en las diferentes regiones geográficas. La tasa de mortalidad en el 2012 fue alta en Norteamérica 6,9/100 mil habitantes y en el 2015 fue de 40 560 fallecidos y se estimó que para el año 2017 habría 43 090 muertes por esta causa. En el Este de Europa la tasa de mortalidad fue de 6,8/100 mil habitantes, seguidas por otras regiones de Europa y Australia/Nueva Zelandia 6,0 para cada una de ellas.
La tasa general de sobrevida a los cinco años está alrededor del 6,0 %, con un rango entre 2-9 %, esto refleja, de modo parcial, la variación de la calidad de los datos recogidos e informados en el mundo. En los Estados Unidos más de la mitad, 52,0 %, de todos los casos fueron diagnosticados en un estadio avanzado de la enfermedad con una tasa de sobrevida a los cinco años de 2,6 %.1-4
El adenocarcinoma de páncreas es un tumor que metastiza rápidamente a los ganglios regionales e infiltra órganos vecinos como el duodeno, la vía biliar principal y los grandes vasos adyacentes como la arteria y vena mesentérica superior, la porta y el tronco celiaco. En las metástasis a distancia uno de los órganos más afectados es el hígado, no siendo así con el bazo.
Por todo lo anterior, se están realizando avances significativos para enfrentar esta enfermedad, entre ellos tenemos: medios diagnósticos de imágenes más precisas, protocolos de quimioterapia nuevos y más eficaces, creación y producción de fármacos y moléculas específicas, incluso se está ensayando y en algunos casos utilizando, la eficacia de la inmunoterapia con resultados prometedores.
El cáncer de páncreas excepcionalmente hace metástasis al bazo lo que motivó la publicación de este caso, que revela un paciente con un adenocarcinoma pancreático con metástasis esplénica tratado con nimotuzumab y gemcitabina.
Presentación del caso
Paciente ECL de 69 años, masculino, mestizo, HC 59-57-60. Fue ingresado por coloración amarilla de piel y mucosas.
Refirió orinas oscuras, heces fecales de color blanquecino, prurito y pérdida de unos 3 Kg de peso, todo desde hace unos 30 días.
APP: Pancreatitis crónica, diabetes mellitus, hipertensión arterial.
En el examen físico se constató ictericia. En el abdomen se palpó la vesícula biliar aumentada de tamaño, no dolorosa y huellas de rascado en la piel.
Se le realizaron los estudios hemoquímicos del hígado cuyos resultados arrojaron una ictericia obstructiva. En los estudios de imaginología en el ultrasonido se observó una imagen hipoecoica en la cabeza del páncreas de 4,13x5,0 8 cm de diámetro y en la tomografía axial computarizada una imagen hipodensa en la misma área de 4,5 cm. Diagnóstico: ictericia obstructiva extrahepática por neoplasia de cabeza de páncreas. Se intervino quirúrgicamente y se le realizó una colecistoyeyunostomía con yeyunoyeyunostomía por ser irresecable el tumor, estadio IV. Se tomó biopsia del tumor.
El resultado de la biopsia (16-5835) fue un adenocarcinoma poco diferenciado con necrosis focal del páncreas. Se le dio el alta y a los seis meses presentó ictericia obstructiva por estenosis de la colecistoyeyunostomía. En esta ocasión no recibió quimioterapia por negación del paciente. Fue intervenido nuevamente y se le realizó una intrahepatoductoyeyunostomía por catéter en el segmento III del hígado. La ictericia desapareció. Se envió a la consulta de Oncología y le administró quimioterapia con 5 fluoracilo y ácido folínico.
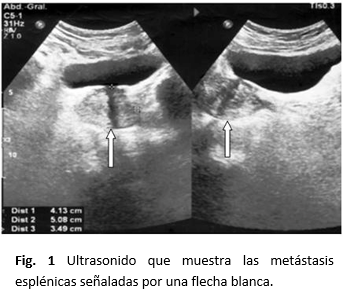
Al realizarle los estudios de control debido al tratamiento con quimioterapia, en el ultrasonido aparecieron dos imágenes hipoecoicas en el bazo: una midió 29x28 mm y la otra 34x33 mm; en la tomografía de éste mismo órgano se observaron dos imágenes hipodensas, la mayor de ellas midió 35x33 mm, de 48 UH que en el estudio endovenoso realzó hasta 67 UH que son interpretadas como metástasis esplénica. Se discutió el caso y se decidió incluirlo en el ensayo clínico EC: IIC RD-EC166 y aplicarle tratamiento con nimotuzumab con dosis de 400 mg semanal hasta la toxicidad inaceptable, muerte o negativa del paciente y gemcitabina a la dosis de 1000 mg/m2 (infusión intravenosa de 30 min) días 1, 8, 15, descansar una semana y repetir el régimen anterior hasta progresión de la enfermedad.
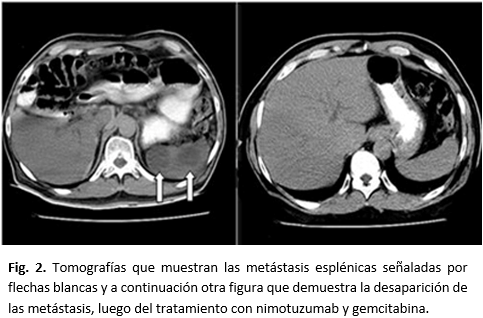
Se le aplicaron cuatro ciclos de tratamiento: 13 con nimutuzumab y 10 con gemcitabina. En los estudios evolutivos no se apreciaron las imágenes metástasis que se observaron antes del tratamiento lo que presupone la utilidad de estos fármacos para el control de estas (Figura 1 y Figura 2).
El paciente se incluyó en el ensayo clínico el 21 de noviembre de 2017 y falleció el 2 de febrero de 2018. La causa de la muerte fue la enfermedad neoplásica. Este paciente recibió un total de 42 inmunizaciones y un total de 22 ciclos de quimioterapia.
Discusión del caso
Las metástasis esplénica por tumores sólidos son infrecuentes, con un rango de prevalencia de 2,3-7,1 %.5 Lam y Tang3 tuvieron una incidencia de metástasis esplénicas halladas en autopsias de 0,6 % y en las esplenectomías de 1,1 %.
Las metástasis esplénicas cuyo origen es el páncreas son excepcionales. Grauer, en 1939, citado por Abrams6, en 34 casos de cáncer de páncreas halló cuatro metástasis en el bazo 11,7 %, Nash7, en 1966, en 37 pacientes con adenocarcinoma de páncreas halló dos metástasis en el bazo 5,4 %. Lam y Tang3, en el 2000, en un periodo de estudio de 25 años y 92 pacientes con metástasis en el bazo, de estos 11 tuvieron cáncer de páncreas.
El tratamiento para el cáncer de páncreas localmente avanzado o metastásico tiene varias modalidades que se pueden combinar entre sí: quirúrgico, quimioterapia, radioterapia e inmunoterapia. La inmunoterapia, a su vez, tiene varias modalidades de aplicación: anticuerpo monoclonales, inmunoterapias no específicas, terapia con vacunas, virus oncolíticos y terapia con células T.
El tratamiento de las metástasis esplénicas es la esplenectomía, cuando son únicas y no forman parte de metástasis en otros órganos. En el paciente que se estudió no se realizó la esplenectomía, ya que en ese momento, estaba recibiendo tratamiento para el adenocarcinoma de páncreas con inmunoterapia combinada con quimioterapia, nimotuzumab y gemcitabina.
El nimotuzumab (CIMAher)8,9,10) es un anticuerpo monoclonal humanizado anti receptor del factor de crecimiento epidérmico (EGF-R) al cual reconoce con gran afinidad. El EGF-R es una glicoproteína de membrana de 170 Kd. Su dominio intracelular está asociado a actividad proteína tirosina quinasa específica y su sobreexpresión por las células tumorales altera la regulación del ciclo celular (incrementando la proliferación), bloquea la apoptosis, promueve la angiogénesis, incrementa la motilidad, la adhesividad y la capacidad invasiva. El nimotuzumab bloquea la unión del ligando al EGF-R y funciona inhibiendo la actividad tirosina quinasa del receptor interfiriendo con la ruta de señalización celular involucrada en la proliferación celular. El nimotuzumab posee efectos antiangiogénico, antiproliferación celular y proapoptótico en aquellos tumores que sobreexpresan el EGF-R, por lo tanto, inhibe el crecimiento de células tumorales de origen epitelial.
La gemcitabina11 (un antimetabolito) es el citostático de primera línea contra el cáncer de páncreas localmente avanzado o metastásico.
Al momento del diagnóstico del cáncer de páncreas, aproximadamente, el 30,0 % de los pacientes se presentan con la enfermedad localmente avanzada. Para esta situación hay muchas opciones de tratamiento, incluyendo la quimiorradiación y la quimioterapia seguida por reestadiamiento y tratamiento con quimiorradiación o quimioterapia sola.11
El régimen de quimioterapia a menudo incluye gemcitabina o 5 fluoracilo, que muchos oncólogos alternan con capecitabina por su tolerancia y eficacia. La quimioterapia sin radiación a menudo incluye regímenes tales como gemcitabina con o sin nab-paclitaxel o FOLFIRINOX (leucovorin, 5 fluoracilo o ácido folínico, oxaliplatino, irinotecan) de elevada toxicidad. Sin embargo, aquellos que puedan someterse a esta terapia agresiva logran una sobrevida general de hasta 12 meses.11
Para la National Comprehensive Cancer Network (NCCN)(2) la primera línea de quimioterapia para las metástasis del cáncer de páncreas depende de su estado de rendimiento. Para los pacientes con un estado de rendimiento de 0-1, la primera línea de tratamiento es el FOLFIRINOX o gemcitabina en combinación con paclitaxel, capecitabina, erlotinib o cisplastino (NCCN).11
Otros regímenes usados infrecuentemente comprenden dosis fijas de gemcitabina, docetaxel y capecitabina (GTX) o una combinación de capecitabina y oxaliplatino (CapeOx). Para aquellos con un pobre estado de rendimiento la gemcitabina es recomendada.11
En los estudios evolutivos que se le realizaron al paciente (estudios de imágenes ultrasonido y tomografía axial computarizada) no se apreciaron las imágenes metástasis que se observaron antes del tratamiento con nimotuzumab y gemcitabina lo que presupone la utilidad de estos fármacos para el control de éstas.
Una limitación de esta investigación es que no fue posible realizar biopsia esplénica para confirmar ésta hipótesis. No obstante, la contribución de este estudio está en que se socializa el hecho.
Consideraciones finales
El resultado de este estudio podría ser la primicia en el reporte de la utilidad de nimotuzumab y gemcitabina para en el tratamiento del cáncer de páncreas y metástasis esplénica, pues en la literatura científica consultada, no se encontró una información similar a que se expresa en este artículo.