Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Endocrinología
versión On-line ISSN 1561-2953
Rev Cubana Endocrinol vol.23 no.1 Ciudad de la Habana ene.-abr. 2012
ENFOQUE ACTUAL
Control glucémico en el proceso perioperatorio de los pacientes con diabetes mellitus
Glycemia control in the perioperative process of patients presenting with diabetes mellitus
Dra. Yudit García García,I Dr. Manuel Emiliano Licea Puig,II Dr. Francisco Garciga Cardoso,III Dra. Yamilé Álvarez Delgado,IV Dr. José Arnaldo Barnés Domínguez,I MSc. Dra. Silvia Almaguer García,I Lic. Juan Carlos Soca MedinaI
IInstituto Nacional de Angiología y Cirugía Vascular (INACV). La Habana, Cuba.
IIInstituto Nacional de Endocrinología (INEN). La Habana, Cuba.
IIIHospital Clinicoquirúrgico de 10 de Octubre. La Habana, Cuba.
IVHospital General "Iván Portuondo". Artemisa, Cuba.
RESUMEN
El paciente diabético requiere con frecuencia algún tipo de cirugía o la realización de un proceder diagnóstico invasivo, que puede, incluso, ser realizado de urgencia. En la actualidad el riesgo quirúrgico del diabético ha disminuido gracias a los avances en las técnicas anestésicas y al control metabólico perioperatorio, aunque las complicaciones aún son más frecuentes, y generan una hospitalización prolongada y una tasa mayor de invalidez. En la evaluación preoperatoria se deben precisar las características de la diabetes, el tipo de proceder quirúrgico, el riesgo anestésico quirúrgico, y realizar los ajustes necesarios al tratamiento habitual. La infusión continua de insulina endovenosa con aporte de glucosa es el método más racional y fisiológico en la mayoría de las intervenciones quirúrgicas, lo que implica monitoreo glucémico frecuente con ajustes inmediatos. Algunas situaciones especiales, como las cirugías complejas o las de urgencia, requieren esquemas terapéuticos específicos, por lo que cada equipo debe tener su protocolo de trabajo, según las particularidades de las intervenciones quirúrgicas que realicen. El control metabólico perioperatorio es esencial para evitar las alteraciones metabólicas e hidroelectrolíticas agudas y favorecer la evolución satisfactoria en el posoperatorio. Por su importancia, se realiza una revisión con un enfoque actual, que ayude a mejorar la calidad de la atención al paciente diabético que requiere de una intervención quirúrgica.
Palabras clave: cirugía, diabetes mellitus, control glucémico, evaluación preoperatoria.
ABSTRACT
The diabetic patients require frequently some type of surgery or the implementation of an invasive diagnostic procedure which may even be carried out as an emergence. Nowadays the surgical risk of the diabetic patient has decrease thanks to the advances in the anesthetic techniques and to the perioperative metabolic control, although the complications are more frequent and to generate a lengthy hospitalization and a great disability rate. In the preoperative assessment it is necessary to specify exactly the diabetes's features, the type of surgical procedure, surgical anesthetic risk and to perform the fitting necessary in the habitual treatment. The continuous infusion of intravenous insulin with glucose is the more rational and physiologic method in most of surgical interventions, involving the frequent glycemia monitoring with immediate fittings. Some special situations including complicated surgeries or those of emergence, require specific therapeutical schemes, thus each staff must to have its work protocol, according the peculiarities of the surgical interventions performed. The perioperative metabolic control is essential to avoid the metabolic and acute hydroelectrolytic alterations and to favor the satisfactory course during the postoperative period. Due its significance, authors carried out a review with the current approach helping to improve the quality of care of diabetic patient requiring a surgical intervention.
Key words: surgery, diabetes mellitus, glycemia control, preoperative assessment.
INTRODUCCIÓN
Con frecuencia el paciente diabético requiere algún tipo de cirugía o la realización de un proceder diagnóstico invasivo, que puede, incluso, ser realizado de urgencia. Se ha estimado que un diabético tiene un 50 % de probabilidad de requerir una intervención quirúrgica a lo largo de su vida. Algunos de estos procederes no están relacionados directamente con la diabetes mellitus (DM), otros se presentan con mayor frecuencia en esta enfermedad, mientras que algunos son realizados especialmente en diabéticos.1
En la era preinsulínica, las cirugías constituían un verdadero problema debido a la alta mortalidad en estos enfermos. En la actualidad el riesgo quirúrgico del diabético ha disminuido considerablemente gracias a los avances en las técnicas anestésicas y al control metabólico perioperatorio. La mortalidad se aproxima a la de la población general, sin embargo, las complicaciones posoperatorias aún son más frecuentes, lo que se debe a numerosos factores, como son: mayor probabilidad de desarrollar infecciones y complicaciones cardiovasculares, las que generan una hospitalización prolongada y una tasa mayor de invalidez.2-4
Un enfoque integral e individualizado del paciente diabético por parte del equipo quirúrgico con protocolos concisos, seguros, y de fácil aplicación, mejora los resultados al disminuir la morbilidad y mortalidad relacionadas con la cirugía. Con este trabajo nos proponemos realizar una revisión sobre el control glucémico del paciente diabético sometido a un proceder quirúrgico, que ayude a mejorar la calidad de la atención por parte del equipo de salud involucrado en los procederes quirúrgicos.
Respuesta al estrés y regulación de la glucemia durante la cirugía
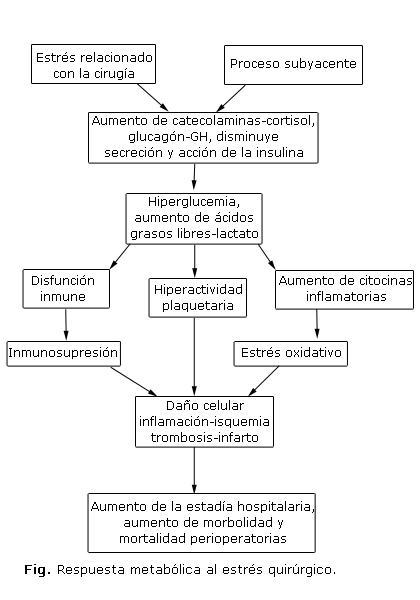
Las alteraciones en el control metabólico son frecuentes durante la cirugía, ya sea por el proceso subyacente, como puede ser una infección, la anestesia y el propio estrés relacionado con el acto quirúrgico, situaciones que generan un aumento de la liberación de las hormonas contrarreguladoras como el cortisol, las catecolaminas, el glucagón y la hormona del crecimiento (GH). Además, se produce inhibición de la secreción y acción de la insulina, que crea un estado de resistencia a la insulina (RI) e hipercatabolismo (figura).2,3,5
La inhibición de los efectos anabólicos de la insulina genera una disminución de la captación y utilización de la glucosa, así como de la síntesis del glucógeno. Se inhiben la captación de aminoácidos, la síntesis proteica y de ácidos grasos por el músculo esquelético y el hígado, respectivamente.3,5 La pérdida de los efectos anticatabólicos de la insulina incluyen: aumento de la glucogenolisis, gluconeogénesis, lipólisis, oxidación de ácidos grasos y formación de cuerpos cetónicos, así como degradación de proteínas, que, unido a los efectos directos de las hormonas contrarreguladoras, provoca el estado hipercatabólico del perioperatorio.3,5
La RI y la hiperglucemia crean un estado proinflamatorio con aumento de citocinas inflamatorias, como las interleucinas (IL-6, IL-18), y el factor de necrosis tumoral alfa (FNTa) que favorecen el estrés oxidativo y la disfunción endotelial. Los trastornos en la agregación plaquetaria están dados por un aumento de la síntesis del tromboxano, del fibrinógeno y de la actividad del factor von Willebrand, lo cual incrementa el riesgo de trombosis.6,7
Control glucémico perioperatorio
Durante mucho tiempo se ha debatido sobre cuál debe ser el control metabólico del paciente diabético en el perioperatorio. Es bien conocida la relación existente entre la glucemia y la aparición de complicaciones en el trans y posoperatorio. Hay evidencias que avalan la hiperglucemia como un predictor sensible de infecciones nosocomiales.8-10 Se ha demostrado un incremento del riesgo de infección con glucemias mayores de 11,1 mmol/L, debido a disfunción fagocitaria de los neutrófilos y monocitos.10 Valores elevados de HbA1c en pacientes sometidos a cirugía cardiaca se asocian con mayor frecuencia a complicaciones como infarto agudo del miocardio en el perioperatorio.11,12 Basado en lo anterior, se deben lograr las metas de buen control metabólico previo a la cirugía electiva, lo cual puede requerir ajustes en el tratamiento habitual (tabla 1).13
En el transoperatorio, el objetivo de lograr glucemias de modo muy estricto incrementa el riesgo de hipoglucemias en un paciente bajo los efectos de la anestesia. Los trabajos iniciales que evaluaron la terapia insulínica intensiva observaron una disminución de la morbilidad y mortalidad, sin embargo, las nuevas evidencias no demuestran beneficios con estas metas, por el contrario, se ha reportado aumento en la incidencia de ictus y muerte.14-17 La meta es mantener niveles razonables de glucemia en el transoperatorio entre 7,0 y 11,1 mmol/L, que eviten las alteraciones metabólicas e hidroelectrolíticas agudas, lo cual requiere de una adecuada monitorización de la glucemia durante todo el proceder.
Evaluación preoperatoria
En la evaluación preoperatoria se deben precisar las características de la diabetes, el tipo de proceder quirúrgico, determinar el riesgo anestésico quirúrgico, y realizar los ajustes necesarios al tratamiento habitual. Con respecto a la diabetes, es necesario precisar el tipo de diabetes, los años de evolución, el tratamiento actual, así como el control glucémico, las complicaciones y las comorbilidades asociadas. La valoración inicial por su diabetólogo, de forma ambulatoria, implica ajustes necesarios al tratamiento habitual, lo cual disminuye la estadía hospitalaria y mejora el pronóstico final.
El tipo de DM y su tratamiento nos orienta sobre la reserva pancreática funcional y las necesidades insulínicas en el perioperatorio, así por ejemplo, los diabéticos tipo 2 suelen presentar menor secreción de insulina y mayor RI relacionado con el estrés quirúrgico. Los diabéticos tipo 1 siempre requieren tratamiento insulínico continuo. La falta de aporte de insulina durante unas horas, como puede ser por la administración en bolo de esta, por su escasa vida media, puede activar la cetogénesis, con los trastornos metabólicos que ello genera.18,19
Es importante definir la presencia de complicaciones crónicas y su severidad. La enfermedad renal crónica puede dificultar el manejo de los líquidos, electrólitos y afectar la farmacocinética de la insulina, además, implica una cuidadosa selección de los medicamentos que requieren ajuste de dosis por su eliminación renal, o de los que tienen efecto nefrotóxico. La hiperpotasemia es frecuente en los estadios avanzados, mientras que la hipopotasemia puede acompañar la poliuria y ser agravada por el tratamiento insulínico sin reposición de potasio.20,21
La neuropatía autonómica cardiovascular debe ser investigada según los recursos disponibles, por el alto riesgo de complicaciones durante la inducción anestésica. La identificación de hipotensión ortostática en el examen físico, así como la variabilidad del ritmo cardiaco, y las pruebas de Ewing, entre otras, ayudan en la identificación de los pacientes afectados. Por su parte, la neuropatía genitourinaria (vejiga neurogénica) aumenta el riesgo de retención urinaria en el posoperatorio, y la gastroparesia diabética puede retrasar el inicio de la alimentación por vía oral. En la historia clínica se debe precisar si existen antecedentes de hipoglucemia sin aviso, ya que estos pacientes tienen mayor riesgo de episodios severos.22
Los complementarios deben incluir la HbA1c, que orienta sobre el control metabólico en las semanas previas, y en su defecto, el perfil glucémico que incluya determinaciones preprandiales y posprandiales. El electrocardiograma debe ser realizado independientemente de si padece o no de enfermedad cardiovascular diagnosticada previamente, por el riesgo de isquemia silente, y otros signos que avalan la neuropatía autonómica. La determinación de potasio a través del ionograma permite el adecuado tratamiento de los electrolitos en el transoperatorio.19,22
Los parámetros para evaluar la función renal incluyen la albuminuria, la creatinina y el filtrado glomerular. La estimación de este último a través de ecuaciones establecidas es aceptable en la práctica clínica. Para ello se pueden emplear, la fórmula de Cockcroft-Gault, la del estudio Modification of Diet in Renal Disease (MDRD), disponible en programas computarizados, entre otras.23
Factores de riesgo quirúrgico para las personas con DM:19-22
- Edad.
- Años de evolución de la DM.
- Descontrol metabólico.
- Neuropatía autonómica cardiovascular, digestiva y genitourinaria.
- Enfermedad renal crónica.
- Hipertensión arterial, cardiopatía isquémica, cardiomiopatía.
- Obesidad.
- Presencia de infecciones.
- Función pulmonar alterada.
Otro aspecto a considerar son las características de la cirugía, que determinan también el tratamiento intraoperatorio y la técnica anestésica:
1. Electiva o de urgencia.
2. Menor (incluidos los procederes diagnósticos invasivos), o mayor (complejas o no), por requerir períodos quirúrgicos prolongados y estancia en unidad de cuidados intensivos (UCI) en el posoperatorio, como la cardiocirugía, las revascularizaciones, los trasplantes, entre otras.
Recomendaciones generales
Se deben ingresar al menos 12-24 h previas a la intervención quirúrgica, a los diabéticos que requieran una cirugía mayor y los que tengan descontrol glucémico, para estabilizarlos desde el punto de vista metabólico. Todos ellos demandan un control intensivo en el preoperatorio, el cual incluye terapia insulínica. El esquema con múltiples dosis de insulina logra este objetivo, e implica la administración de insulina basal y en bolos preprandiales con Neutral Protamine Hagedorn (insulina NPH) y regular, respectivamente, por vía subcutánea. En los pacientes que ya usaban insulina se mantiene su dosis basal, y en ambos se hacen los ajustes necesarios con suplementos adicionales. Quedaron en desuso los esquemas de insulina deslizantes, por no mostrar ventajas y ser menos efectivos.24-27
El monitoreo glucémico incluye determinaciones de glucemia antes de la intervención (la noche anterior y el día de la cirugía), en el transcurso, y posterior a esta. De identificarse hiperglucemia la noche previa, es conveniente descartar un estado de cetosis asociada, a través de la reacción de Imbert, o tiras reactivas para cetonuria.
Las intervenciones quirúrgicas deben ser realizadas, de ser posible, en las primeras horas de la mañana, en ayunas desde la noche anterior. Cuando ello no puede ser posible, se deben tomar las medidas necesarias por parte del equipo quirúrgico para evitar complicaciones por la prolongación del estrés quirúrgico, y las relacionadas con el régimen de tratamiento empleado (período de ayuno extendido, administración de soluciones hipotónicas e hiponatremia dilucional, entre otras).
Tratamiento durante la cirugía menor o ante una técnica diagnóstica invasiva
Pacientes controlados con tratamiento dietético exclusivo o con fármacos orales reguladores de la glucemia: estos pacientes tienen una reserva de insulina endógena limitada, sin embargo, los que tienen buen control metabólico no requieren una intervención especial, y el tratamiento insulínico no suele ser necesario durante estos procederes.20,21,25-28
Las sulfonilureas y las glinidas estimulan la secreción de insulina, y por ello, suelen mantenerse hasta el día previo a la cirugía y retirarse el día de la intervención. Las de acción prolongada, como la clorpropramida, deben ser suspendidas 72 h previas al proceder. Las biguanidas se retiran 48 h antes; si se usa un medio de contraste endovenoso, no reintroducirla hasta pasadas 48-72 horas.
Los fármacos agonistas del receptor del péptido 1 semejante al glucagón (glucagon-like peptide-1 [GLP-1]), los inhibidores de las alfa-glucosidasas y de los fármacos inhibidores de la enzima dipeptidil-peptidasa 4 (DPP-4), mejoran la hiperglucemia posprandial, por lo que no son eficaces durante los períodos de ayuno, y se suspenden el día de la intervención. El grupo de las glitazonas mejoran la utilización de la glucosa en los tejidos periféricos, pero provocan retención de líquidos, por lo que su uso actual es controversial y tienen indicaciones muy limitadas, deben ser interrumpidos días previos a la cirugía.20,21,25-28
Si aparece hiperglucemia durante el proceder, se deben realizar los ajustes necesarios con insulina regular. Si fuese necesario prolongar esta intervención, se debe pasar, como alternativa, a un esquema con aporte de glucosa e insulina por vía endovenosa. El tratamiento habitual se reincorpora cuando se reinicie la vía oral.
Los pacientes con infección concurrente o descontrol metabólico deben ser insulinizados previo a la intervención, y requieren un tratamiento en el perioperatorio similar al de los pacientes con tratamiento insulínico previo.29,30
Pacientes con tratamiento insulínico previo: este grupo de pacientes debe lograr su control metabólico óptimo con el ajuste de la dosis de insulina, o como alternativa cuando no se logre cambiar a un régimen más efectivo, como las múltiples dosis de insulina, y siempre deberán recibir glucosa e insulina en el transoperatorio.25-31
Las nuevas evidencias no justifican la sustitución de los análogos de acción prolongada, por las de acción intermedia (NPH) previo a la intervención, por el contrario, la ausencia de picos de acción de las primeras disminuye el riesgo de hipoglucemias. Es recomendable administrar 2/3 de la dosis habitual de insulina NPH la noche anterior, si emplea análogos de acción prolongada, se puede administrar la dosis habitual, y los pacientes con bomba de infusión podrán mantener similar ritmo de infusión.32-34
El día de la intervención no se inyecta la dosis de insulina de la mañana y se instaura un régimen de perfusión de glucosa-potasio-insulina (GKI), realizando monitoreo glucémico capilar cada 1-2 h, con ajustes de ser necesario. La administración de insulina NPH por vía subcutánea el día de la cirugía, tiene una absorción menos predecible e incrementa el riesgo de hipoglucemia. Los procederes quirúrgicos sencillos y de muy corta duración pueden ser una excepción a esta recomendación.26-31
Tratamiento durante la cirugía mayor
La cirugía mayor supone un estrés quirúrgico superior con respecto a una intervención menor, por lo que los diabéticos sometidos a este proceder requieren un aporte constante de glucosa e insulina, con un monitoreo glucémico más estrecho. Otra situación a considerar son las cirugías complejas, por su prolongado tiempo quirúrgico o porque requieren circulación extracorpórea, fármacos inotrópicos, hipotermia inducida, entre otras situaciones. En estas condiciones aumentan las necesidades insulínicas, y el tratamiento de los líquidos y electrolitos se hace más complejo.
Existen diferentes modalidades para el tratamiento de los líquidos y de la insulina en el transoperatorio; la selección dependerá de las características del paciente y del proceder en cuestión, así como de las características particulares de la unidad quirúrgica donde se realice. El aporte de insulina debe ser continuo y por vía endovenosa durante la cirugía mayor. Quedaron en desuso los regímenes de no insulina-no dextrosa (período de ayuno prolongado) por la elevada mortalidad asociada a este, así como los que incluyen el empleo subcutáneo de la insulina, por ser poco predecible su absorción y el uso en bolo por vía endovenosa, teniendo en cuenta su corta vida media. Un breve período de insulinodeficiencia genera picos y valles en la insulinemia circulante, con deterioro del control glucémico, que puede ser grave, sobre todo, en los diabéticos tipo 1. Por lo tanto, la infusión continua de insulina endovenosa es el método más racional y fisiológico en el tratamiento perioperatorio en los diabéticos que requieran cirugía mayor, en las de urgencia, así como en pacientes con DM inestable.18,20,21,26-29,32,33
Aporte de líquidos, electrólitos e insulina
Glucosa: el aporte adecuado de glucosa (aproximadamente 120 g al día [5 g/h]) evita el catabolismo proteico en adultos no diabéticos. Con el ayuno preoperatorio y el estrés quirúrgico, los requerimientos calóricos en la mayoría de los diabéticos son de 510 g de glucosa por hora.21,26-29,33 La concentración de la solución de dextrosa puede variar según las necesidades del volumen de líquidos a administrar. Las más concentradas se usan en los casos con sobrecarga de volumen, a diferencia de las menos concentradas, reservadas para cuando es necesario aportar mayor volumen, con la precaución de que su administración por períodos prolongados puede producir hiponatremia dilucional. La dextrosa al 10 % es la más utilizada en la mayoría de los protocolos quirúrgicos.21,27-29,33
Insulina, estimación de las necesidades: no existe un método exacto para predecir las necesidades de insulina en el transoperatorio, es individual para cada paciente. Se basa en el tipo de diabetes, la terapia previa, el grado de control glucémico en relación con la cantidad total diaria de insulina administrada (dosis total preoperatoria), y en la presencia de situaciones asociadas que puedan aumentar las necesidades insulínicas. A pesar de ello, la experiencia clínica con los sistemas de infusión insulínica ha demostrado similares necesidades para la mayoría de las personas con DM que reciben tratamiento quirúrgico, excepto para los pacientes sometidos a intervenciones prolongadas y complejas, o aquellos con procesos asociados a RI.
La dosis inicial estimada es de 0,5-1 U/h para los diabéticos tipo 1 y de 1-2 U/h para los tipo 2. De manera general, la dosis varía de 1-3 U/h, que equivalen a 0,10-0,30 U de insulina por cada gramo de glucosa aportado en la mayoría de los diabéticos. En las situaciones relacionadas con RI (obesidad, hepatopatías, sepsis, tratamiento esteroideo, entre otras), los requerimientos varían entre 0,40-0,80 U de insulina por g de glucosa aportado. En pacientes sometidos a una cirugía a corazón abierto, las necesidades pueden llegar hasta 0,80-1,20 U de insulina por g de glucosa aportado debido al mayor estrés.26,27,29,33,35,36
El monitoreo horario durante la intervención evita que se produzcan episodios de hipoglucemia, ya que bajo condiciones de estrés, es poco probable que ocurran descensos de la glucemia a una velocidad mayor de 2,8 mmol/L/h, a menos que se administre una gran cantidad de volumen. Los análogos ultrarrápidos pueden ser usados por vía endovenosa, pero estos no confieren ventajas con respecto a la insulina regular en el transoperatorio.
Potasio: la administración de insulina y glucosa inducen el paso del potasio al medio intracelular, lo cual requiere un aporte adecuado de este electrólito. Su determinación en el preoperatorio permite calcular las necesidades. De manera general, el potasio se administra a razón de 10-20 mmol/L en pacientes con función renal normal, en el resto de los sujetos debe ser reajustado.26-29,32,33
Regímenes empleados durante la cirugía mayor
La administración simultánea de glucosa e insulina podrá ser juntas en la misma infusión, o por separado, cada una con sus ventajas y desventajas. La selección dependerá del tipo de cirugía, de los recursos disponibles y de la experiencia del equipo que la realiza:
Régimen 1: glucosa e insulina juntas en la misma infusión (bomba glucosa-potasio-insulina o GKI). Constituye el método más usado por su sencillez y eficacia. Puede ser empleado en diabéticos tipo 1 o 2 cuando el requerimiento insulínico durante la cirugía es estable y no se pronostican grandes variaciones en las necesidades de insulina, como procedimientos electivos, cortos, como cirugías laparoscópicas u otras de menos de 2 h de duración, y en la cirugía menor en pacientes con tratamiento insulínico previo.26-29,32,33,37 Tiene como desventajas la rigidez para variar el aporte de cada uno de los componentes de la solución, y la necesidad del cambio de la solución cada vez que sea necesario hacer una modificación en la dosis. Se recomienda: dextrosa 10 % 500 mL (aporta 50 g de glucosa) + insulina regular 15 U + cloruro de potasio (ClK) 10 mmol (si se dispone de ionograma, ajustar el potasio según el mismo).
Se inicia temprano en la mañana (2-3 h previas a la cirugía), con el propósito de obtener un control uniforme y óptimo. Realizar una determinación de glucemia, y si es normal, iniciar la infusión endovenosa de la solución GKI a 100 mL/h. El ritmo de esta infusión aporta cada 1 hora: 100 mL de líquidos, 10 g de glucosa, 2 mmol de ClK, 3 U de insulina, o sea, 0,3 U por g de glucosa aportado, lo cual cumple con los requerimientos generales en el perioperatorio de la mayoría de los pacientes. Se debe controlar la glucemia capilar cada 1-2 h, y reajustar las unidades de insulina de la solución si la glucemia está fuera del rango deseado.26-29,32,33,37 Una variante se muestra en la tabla 2. Otra alternativa, si la glucemia es superior a 16,0 mmol/L, es cambiar a solución salina fisiológica (SSF) 0,9 % con insulina regular, repitiendo la glucemia hasta lograr un control estable, momento en el que reiniciaremos el suero glucosado.
Régimen 2: infusión simultánea e independiente de glucosa e insulina. Este régimen puede ser empleado cuando los requerimientos insulínicos son variables, como sucede en las cirugías complejas.26-29,32,33,35,36 La administración de modo continuo de glucosa e insulina en infusiones por separado proporciona, por un lado, el suero glucosado con potasio, y la insulina en solución salina por otro, con bombas de perfusión que aseguren un aporte constante y exacto en todo momento con ajustes horarios de la velocidad de cada una de las infusiones independientemente. Tiene como ventajas con respecto al GKI su eficacia y flexibilidad, al permitir ajustar independientemente la velocidad de ambas infusiones con gran rapidez, sin embargo, requiere de un control estricto, mayor complejidad y dispositivos como la bomba de infusión. Se recomienda: administrar con bomba de infusión de forma simultánea en Y (nunca alternando):
- Solución 1: SSF 0,9 % 50 mL + insulina regular 50 U (1 U/1 mL).
- Solución 2: dextrosa 10 % 500 mL + ClK 10 mmol.
Se realiza una glucemia temprano en la mañana y se inicia la infusión. Administrar la solución 1 a razón de 2 mL/h, y la solución 2 a razón de 100 mL/h. Este ritmo de infusión aporta en 1 hora: 100 mL de líquidos, 10 g de glucosa, 2 mmol de ClK y 2 U de insulina (0,2 U por g de glucosa aportado). Se deben realizar determinaciones de glucemia cada 1-2 h, y ajustar el aporte insulínico de acuerdo con el resultado, aunque rara vez son necesarios. Una variante se muestra en la tabla 3. Ajustar el ritmo de perfusión en las situaciones que requieren un aporte mayor de insulina.
Tratamiento en el posoperatorio
La recuperación del paciente, una vez terminada la cirugía, sigue siendo un período crítico, porque aún pueden aparecer complicaciones y se requiere un control estricto de todos los parámetros vitales. El monitoreo de la glucemia se mantiene, pero se van espaciando cada 2 ó 3 h según el grado de estabilidad del paciente. Es fundamental mantener la glucemia entre 6,6-10,0 mmol/L durante el período inmediato que sigue a la operación.26-29,32,33,38,39
La infusión de insulina en el paciente parcialmente recuperado del estrés quirúrgico se mantiene hasta que la tolerancia oral es estable, y se interrumpe pasados 30-60 min de administrarse la primera dosis subcutánea, ello es fundamental para evitar períodos sin cobertura insulínica. Los pacientes sometidos a una cirugía mayor y que requieran en el posoperatorio mantenerse en la UCI, deben mantener la infusión de insulina mientras se precise este tipo de cuidados.
En los pacientes tratados con insulina puede ser necesario seguir un régimen con dosis múltiples de insulina, con el propósito de mantener un buen control glucémico antes de iniciar la pauta de tratamiento habitual. En los diabéticos tratados con dieta y/o fármacos orales, es factible prescribir su medicación habitual, si tolera adecuadamente la ingesta vía oral y la cifra de glucemia es inferior a 10 mmol/L. Cuando las cifras de glucemia son mayores, puede ser necesaria la administración temporal de insulina.
Cirugía de urgencia
Aproximadamente el 5 % de la población diabética requiere una intervención quirúrgica de urgencia. Estos pacientes requieren un método más agresivo para controlar la glucemia y las posibles alteraciones hidroelectrolíticas cuando son ingresados de urgencia para un proceder de este tipo.26-29,32,33 Se recomiendan los sistemas de infusión por separado, de glucosa e insulina, para la corrección de modo rápido y seguro de estas situaciones.
La cetosis y la cetoacidosis diabética pueden acompañar con frecuencia las situaciones que requieren cirugía de urgencia. Cuando sea posible, la intervención debe ser retrasada 4-6 h hasta corregir, o al menos mejorar, estos trastornos. El tratamiento implica una elevada velocidad de infusión de la insulina en solución salina, por lo que el uso de dextrosa se pospone hasta tanto se normalice la glucemia.
En resumen, el paciente diabético sometido a una intervención quirúrgica requiere un tratamiento integral que incluye variadas medidas para lograr el control metabólico durante el perioperatorio, lo cual evita las alteraciones metabólicas e hidroelectrolíticas agudas y favorece su evolución satisfactoria.
Agradecimientos
Nuestro especial agradecimiento al Grupo Provincial de Endocrinología por la colaboración en la realización del protocolo para el tratamiento del control glucémico en el proceso perioperatorio de los pacientes con DM.
REFERENCIAS BIBLIOGRÁFICAS
1. Clement S, Braithwaite S, Magee M, Ahmann A, Smith EP, Schafer RG, et al. Management of Diabetes and Hyperglycemia in Hospitals. Diabetes Care. 2004;27:553-91.
2. Alberti KGMM, Gill GV. The care of the diabetic patient during surgery. En: Alberti KGMM, Zimmet P, DeFronzo RA, Keen H, eds. International Textbook of Diabetes Mellitus. 2nd ed. Chichester: Wiley; 1997. p. 1243-53.
3. Smiley DD, Umpierrez GE. Perioperative glucose control in the diabetic or nondiabetic patient. South Med J. 2006;99:580-91.
4. Debing E, Aerden D, Van den Brande P. Diabetes Mellitus is a Predictor for Early Adverse Outcome after Carotid Endarterectomy. Vascular Endov Surg. 2011;45:28-32.
5. Watkins PJ, Amiel SA, Howell SL, Turner E. Management of Diabetes During Surgery and other illnesses. In: Watkins PJ, Amiel SA, Howell SL, Turner E. Diabetes and its Management. 6th ed. London: Ed. Blackwell Publishing; 2003. p. 95-103.
6. Esposito K, Nappo F, Marfella R, Giugliano G, Giugliano F, Ciotola M, et al. Inflammatory cytokine concentrations are acutely increased by hyperglycemia in humans: role of oxidative stress. Circulation. 2002;106:2067-72.
7. Gresele P, Guglielmini G, DeAngelis M, Ciferri S, Ciofetta M, Falcinelli E, et al. Acute, short-term hyperglycemia enhances shear stress-induced platelet activation in patients with type II diabetes mellitus. J Am Coll Cardiol. 2003;41:1013-20.
8. Pomposelli JJ, Baxter JK III, Babineau TJ, Pomfret EA, Driscoll DF, Forse RA, et al. Early postoperative glucose control predicts nosocomial infection rate in diabetic patients. J Parenteral Enteral Nutr. 1998;22:77-81.
9. Dronge AS, Perkal MF, Kancir S. Long-term glycemic control and postoperative infectious complications. Arch Surg. 2006;141:375-80.
10. Rassias A, Givan A, Marrin C, Whalen K, Pahl J, Yeager M. Insulin increases neutrophil count and phagocytic capacity after cardiac surgery. Anesth Analg. 2002;94:1113-9.
11. Alserius T, Anderson RE, Hammar N, Nordqvist T, Ivert T. Elevated glycosylated haemoglobin (HbA1c) is a risk marker in coronary artery bypass surgery. Scand Card J. 2008;42:392-8.
12. Knapik P, Cieœla D, Filipiak K, Knapik M, Zembala M. Prevalence and clinical significance of elevated preoperative glycosylated hemoglobin in diabetic patients scheduled for coronary artery surgery. Eur J Cardiothorac Surg. 2011;39:484-9.
13. Manual de atención integral a personas con diabetes [homepage en internet] [citado 2011 junio 14] Disponible en: http://www.sld.cu/galerias/pdf/sitios/diabetes/manual de_atencion_integral_a_personas_con_diabetes.pdf
14. Gandhi GY, Nuttall GA, Mullany CJ, Schaff HV, O'Brien PC, et al. Intensive intraoperative insulin therapy versus conventional glucose management during cardiac surgery: a randomized trial. Ann Intern Med. 2007;20:233-43.
15. Chan R, Galas F, Hajjar L, Auler J. Intensive Perioperative Glucose Control Does Not Improve Outcomes of Patients Submitted to Open-Heart Surgery: A Randomized Controlled Trial. Clinics (Sao Paulo). 2009;64:51-60.
16. Leibowitz G, Raizman E, Brezis M, Glaser B, Raz I, Shapira O. Effects of moderate intensity glycemic control after cardiac surgery. Ann Thorac Surg. 2010;90:1825-32.
17. The NICE-SUGAR Study Investigators. Intensive verses conventional glucose control in critically ill patients. NEJM. 2009;360:1283-97.
18. Moghissi ES, Korytowski MT, DiNardo M. American Association of Clinical Endocrinologists and American Diabetes Association consensus statement on inpatient glycemic control. Endocr Pract. 2009;15:353-69.
19. Dávila E. Evaluación preoperatoria del paciente quirúrgico. En: Dávila E, Gómez C, Álvarez M, Saínz H, Molina RM (ed.). Anestesiología Clínica. La Habana: Editorial Ciencias Médicas; 2006. p. 1-14.
20. Santos E, Gómez Peralta F, Salvador J. Diabetes y cirugía: principios generales de tratamiento II. Rev Med Univ Navarra. 2002;46:24-37.
21. Álvarez C, Hillman N, Castro E, Pallardo LF. Protocolo terapéutico del enfermo diabético sometido a cirugía. Medicine. 2000;8:1086-8.
22. Cordero I. Consideraciones anestésicas en el paciente diabético con neuropatía autonómica. Rev Cubana Anest. 2010;9:24-31.
23. Rigalleau V, Lasseur C, Perlemoine C, Barthe N, Raffaitin C, Liu C, et al. Estimation of glomerular filtration rate in diabetic subjects: Cockcroft formula or modification of Diet in Renal Disease study equation? Diabetes Care. 2005;28:838-84.
24. Umpierrez GE, Smiley D, Jacobs S, Peng L, Temponi A, Mulligan P, et al. Randomized Study of Basal Bolus Insulin Therapy in the Inpatient Management of Patients With Type 2 Diabetes Undergoing General Surgery (RABBIT 2 Surgery). Diabetes Care. 2011;34:256-61.
25. Hirsch IB. Sliding scale insulin-time to stop sliding. JAMA. 2009;301:213-4.
26. Meneghini LF. Perioperative management of diabetes: Translating evidence into practice. Clev Clin J. 2009;76:S53-S59.
27. Rittler P, Broedl UC, Hartl W, Göke B, Jauch K. Diabetes mellitus perioperative management. Chirurg. 2009;80:412-5.
28. Martín I, Valero MA. Insulinoterapia. Protocolo terapéutico del paciente diabético sometido a cirugía. En: Botella JI, Valero MA, Beato P, Canovas B, Martín I, Álvarez F, et al. (eds.). Manual de Endocrinología y Nutrición. Madrid: Novo Nordisk Pharma; 2007. p. 65-7.
29. Dagogo-Jack S, Alberti KGMM. Management of Diabetes Mellitus in Surgical Patients. Diabet Spectrum. 2002;15:45-8.
30. Grosembacher L. Cuidados del paciente diabético en el perioperatorio. Rev Soc Arg Diabetes. 2008;42:247-50.
31. Vann MA. Perioperative management of ambulatory surgical patients with diabetes mellitus. Curr Opin Anaesthesiol. 2009;22:718-24.
32. Molina B, Montoya T, Olivar J, Monereo S. Guías de actuación clínica de la diabetes mellitus. Algoritmo diagnóstico y terapéutico del paciente diabético intervenido quirúrgicamente. Endocrinol Nutr. 2006;53:48-55.
33. Marks JB. Perioperative management of diabetes. Am Fam Physician. 2003;67:93-100.
34. Kang H, Ahn KJ, Choi JY, Park HJ, Park SJ, Lee SK. Efficacy of insulin glargine in perioperative glucose control in type 2 diabetic patients. Eur J Anaesthesiol. 2009;26:666-70.
35. Emam IA, Allan A, Eskander K, Dhanraj K, Farag ES, El-Kadi Y, et al. Our experience of controlling diabetes in the peri-operative period of patients who underwent cardiac surgery. Diab Res Clin Pract. 2010;88:242-6.
36. Wong J, Zoungas S, Wright C, Teede H. Evidence-based Guidelines for Perioperative Management of Diabetes in Cardiac and Vascular Surgery. World J Surg. 2010;34:500-13.
37. Fan Y, Zhang AM, Xiao YB, Weng YG, Hetzer R. Glucose-insulin-potassium therapy in adult patients undergoing cardiac surgery: a meta-analysis. Eur J Cardiothorac Surg. 2011;40:192-9.
38. Duncan AE, Abd-Elsayed A, Maheshwari A, Xu M, Soltesz E, Koch CG. Role of intraoperative and postoperative blood glucose concentrations in predicting outcomes after cardiac surgery. Anest. 2010;112:860-71.
39. Hoogwerf BJ. Perioperative management of diabetes mellitus: how should we act on the limited evidence? Clev Clin J Med. 2006;73(Suppl 1):s95-s99.
Recibido: 3 de agosto de 2011.
Aprobado: 26 de noviembre de 2011.
Yudit García García. Instituto Nacional de Angiología y Cirugía Vascular (INACV). Calzada del Cerro # 1 551 esquina Domínguez, municipio Cerro. La Habana, Cuba. Correo electrónico: ygarciagarcia@infomed.sld.cu