Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Endocrinología
versión On-line ISSN 1561-2953
Rev Cubana Endocrinol vol.26 no.3 Ciudad de la Habana dic. 2015
Rev Cubana Endocrinol. 2015;26(3)
REVISIÓN BIBLIOGRÁFICA
Déficit de estrógeno e inmunidad, una aproximación sugerente a la mujer posmenopáusica
Shortage of estrogen and immunity, a suggestive approach to the postmenopausal woman
Dr. Emigdio José León Toirac,I Dra. Nerys Magdalena Toirac Utria,II Dra.C. Daisy Navarro DespaigneI
IInstituto Nacional de Endocrinología. La Habana, Cuba.
IIFacultad de Ciencias Médicas “Gral. Calixto García”. La Habana, Cuba.
RESUMEN
La reducción en la concentración de estrógenos producida durante la transición del estado reproductivo al estado posmenopáusico, como expresión del envejecimiento femenino, es responsable de las alteraciones metabólicas que se producen en diferentes sistemas, como el neurológico y el inmunológico, entre otros. La identificación oportuna de estas características clínicas constituye una necesidad para el tratamiento integral y personalizado de este grupo de mujeres, a nivel regional e internacional. Se verifica en la literatura científica la repercusión de la disminución de los niveles de estrógeno en el desempeño de los mecanismos inmunológicos de la mujer posmenopáusica. Para ello se realizó una revisión bibliográfica, a través del sitio web PubMed de la Biblioteca Médica Nacional de EUA, de las revistas especializadas más actualizadas y de libre acceso referentes al tema. Del total de 158 publicaciones encontradas, 42 fueron consultadas de manera íntegra y más del 50 % de estas pertenecen a los últimos 5 años. Existen evidencias que reflejan la asociación existente entre la senectud ovárica y la inmunológica. La inmunosenescencia implica cambios en la inmunidad innata y la adquirida. Estas transformaciones han sido atribuidas a la deprivación estrogénica, ya que pueden ser reversibles con terapia hormonal sustitutiva. La contribución del déficit estrogénico al declive de la función inmunológica, no está bien dilucidada. Aún es insuficiente el nivel de conocimiento existente en este campo de las investigaciones biomédicas; el bajo índice de publicaciones científicas actualizadas así lo confirman. Escrutar con precisión los mecanismos patogénicos que desencadenan estos fenómenos permitiría un eficaz tratamiento integral, diagnóstico y terapéutico, de este grupo poblacional.
Palabras clave: inmunidad, menopausia, déficit de estrógeno, senescencia, mujer posmenopáusica.
ABSTRACT
Reduction in the estrogen concentration during the transition from the reproductive state to the postmenopausal condition, as an expression of female aging, accounts for the metabolic alterations occurring in different systems like the neurological and the immune ones among others. The timely detection of these clinical characteristics is a requirement for the comprehensive customized treatment of this group of women at regional and international levels. The impact of the decline in estrogen levels on the performance of the immune mechanisms of the postmenopausal woman was verified in the scientific literature. To this end, a literature review was made through the PubMed website of the National Medical Library of the United States to find the most updated open access specialized journals that dealt with the topic. Out of the 158 journals found, 42 were fully reviewed and over 50% of them were published in the last 5 years. There is some evidence that shows the association between ovarian senescence and the immune senescence. The immunosenescence means the changes occured in the innate immunity and the acquired immunity. These changes have been attributed to lack of estrogen because they may be reverted with the aid of an hormone replacement therapy. The estrogen shortage contribution to the decline in the immune function has not been yet solved. The level of knowledge in this field of biomedical research is still poor, which is confirmed by the low number of updated scientific publications. An accurate exploration of the pathogenic mechanisms triggering these phenomena would allow the comprehensive, effective diagnostic and therapeutic treatment of this population section.
Keywords: immunity, menopause, shortage of estrogen, senescence, postmenopausal women.
INTRODUCCIÓN
El envejecimiento es un proceso que comienza con la unión del óvulo con el espermatozoide y termina con la muerte; de manera que, obviamente, transcurre en el curso de todo periodo vital.1 Durante este, se ponen de manifiesto diferentes modificaciones, adaptaciones o disfunciones en órganos y tejidos, que así expresan su vulnerabilidad a los procesos oxidativos y a los diferentes cambios metabólicos que la senescencia impone.1-3 La menopausia, entendida como la conclusión del ciclo menstrual; y el climaterio, como el conjunto de manifestaciones que se producen alrededor de este evento, son momentos definitorios que indican el declive de la vida reproductiva femenina.3
A principios del pasado siglo la edad media de la mujer era baja. Hoy alcanza los 80 años, por lo que casi la tercera parte de su vida, transcurre después de la menopausia.4 Además, en la actualidad se considera que el 95 % de las mujeres de países desarrollados deben transitar la etapa del climaterio, por lo que se estima que este grupo poblacional sobrepase la cifra de varios millones.5,6
Indicadores estadísticos regionales muestran que la población femenina de Cuba no se encuentra ajena a esta realidad. El envejecimiento poblacional en nuestro país se hace evidente tras observar la fluctuación de algunas variables epidemiológicas; fundamentalmente, el acrecimiento de la esperanza de vida y la disminución de la natalidad. Por tanto, esta situación constituye hoy una inquietud primordial en el ámbito socioeconómico de la nación.7 Varios investigadores del tema8-10 coinciden en que la reducción en la concentración de estrógenos producida durante la transición del estado reproductivo al estado posmenopáusico, como expresión del envejecimiento femenino, es responsable de las alteraciones metabólicas que se producen en diferentes sistemas, tales como el neurológico, el inmunológico, entre otros. Este deterioro sistémico quiebra la salud y el estado de bienestar, comprometiendo por sí mismo la calidad de vida de la mujer.11
Estos planteamientos justifican la necesidad de la comprensión y estudio de las constantes moleculares y clínicas que determinan esta etapa biológica, lo cual contribuirá a la identificación oportuna de estas características en cada escenario asistencial. Además, permitirá incrementar la eficacia en el tratamiento integral y personalizado de este grupo de mujeres, para favorecer su mejor inserción en su entorno familiar y social. El presente trabajo se propuso verificar en la literatura científica la repercusión de la disminución de los niveles de estrógeno en el desempeño de los mecanismos inmunológicos de la mujer posmenopáusica.
DESARROLLO
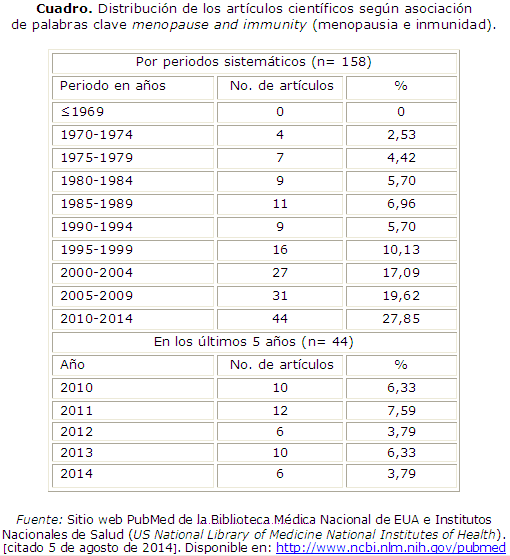
Para la confección de este trabajo se realizó una revisión bibliográfica de material digital empleando los recursos informáticos a nuestro alcance. A través de la navegación en Internet, específicamente del sitio web PubMed de la Biblioteca Médica Nacional de EUA e Institutos Nacionales de Salud (US National Library of Medicine National Institutes of Health), con dirección electrónica http://www.ncbi.nlm.nih.gov/pubmed, disponible en el sitio de informática médica cubano Infomed (http://www.infomed.sld.cu), fueron consultadas las revistas especializadas más actualizadas y de libre acceso referentes al tema. Para la localización de las publicaciones fueron empleadas las palabras clave immunity y menopause (inmunidad y menopausia). La asociación de estos términos arrojó un total de 158 citas bibliográficas, cuya distribución por períodos sistemáticos aparece en los resultados contenidos en el cuadro.
La distribución del total de los artículos obtenidos en esta pesquisa, muestra un ascenso gradual, pero aún discreto, si se comparase con otros temas de investigación. Existe una mayor tendencia de ubicación de publicaciones a partir del año 2000, respaldada por el desarrollo científico tecnológico alcanzado en estos últimos años, y por el interés de algunos investigadores en esta área del conocimiento. Los nuevos hallazgos moleculares sobre la interconexión de los circuitos hormonales y la rama humoral del sistema inmune, los péptidos neuronales, entre otros, han permitido la revitalización de la teoría del circuito psiconeuroinmunoendocrino,3,9 contribuyendo con certeza a este comportamiento. A su vez, la discreta presencia de artículos científicos en el periodo anterior a 1995, evidencia la reciente incorporación de la Inmunología al patrimonio de las ciencias;12 así como, la particularización del cuadro mundial de salud de esa época en la cual las entidades inducidas por el envejecimiento y el climaterio no resultaban prioritarias.
En cuanto al análisis de la distribución de los artículos publicados en el periodo 2010-2014, se observó una media de 9 ± 3 artículos por año. En este caso, debe considerarse la no conclusión del año 2014 como un posible modificador de este resultado. Si se compara este comportamiento con el ocurrido en la sumatoria de los espacios temporales anteriores, se verifica que cerca del 30 % de la bibliografía específica de esta temática se ha escrito en el periodo más reciente (cuadro). Finalmente, fueron confrontados un total de 42 trabajos, teniendo en cuenta el nivel de actualización y la posibilidad de consultar el artículo de manera íntegra.
Ante el suceso biológico del envejecimiento, el ovario disminuye su capacidad para cumplir el ciclo folicular, con la consiguiente disminución de la producción hormonal de estrógenos y progesterona, entre otras sustancias, hasta su desaparición total, que implica la pérdida de la capacidad reproductiva.10,13,14 En esta etapa la mujer se encuentra en la edad mediana (45-59) años, y el conjunto de síntomas y signos que se expresan clínicamente, constituyen el climaterio, o lo que algunos autores7,11 han denominado “la edad crítica de la mujer”. Durante este periodo ocurre el cese total de la menstruación (amenorrea), cuya permanencia por un periodo de un año, permitirá establecer el diagnóstico de menopausia.2,3,6 Por otro lado, la posmenopausia es la etapa que se extiende desde la menopausia hasta los 64 años.15
En Cuba, la menopausia ocurre entre los 47 y 48 años. Si se toma en cuenta que la esperanza de vida de la mujer cubana está en las proximidades de los 80 años, puede plantearse que vivirá alrededor de 30 años en la posmenopausia. Este logro obtenido —en lo que se refiere a expectativa de vida— no se comporta de igual modo en cuanto a calidad de esta, pues se sabe que con el déficit de la producción de estrógenos el estado de salud de la mujer se hace vulnerable.7,17-21
Proyectos de investigación de corte clínico y epidemiológico nacionales4,8,16 e internacionales,1,3,10,11 han demostrado que la posmenopausia constituye un factor de riesgo independiente para entidades patológicas crónicas, como la enfermedad coronaria isquémica, la osteoporosis, la enfermedad de Alzheimer. Aun cuando en el momento actual se discute el protagonismo de los estrógenos en la génesis causal de algunas enfermedades como aterosclerosis y diabetes mellitus, su papel como factor predisponente o precipitante, es indudable.8,22-24
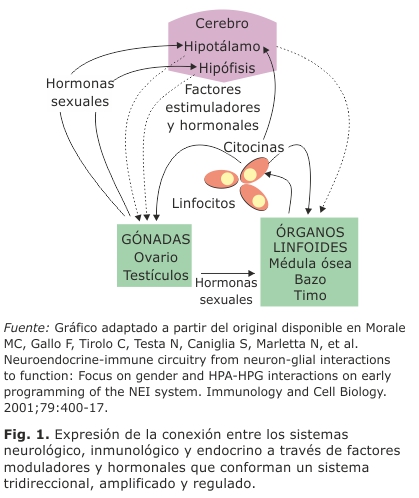
Existen fuertes evidencias clínicas y experimentales que confirman la presencia de una estrecha intercomunicación entre los sistemas inmune, nervioso y endocrino.24-26 Esta red neuroinmunoendocrina es crucial para garantizar los mecanismos homeostáticos fisiológicos, particularmente en el terreno de las funciones reproductivas.26 Uno de los ejes endocrinos principalmente involucrado en estas funciones es el hipotalámico-pituitario-gonadal (HPG).13,26 Este eje utiliza para su comunicación sistemas de señales moleculares que actúan sobre otras moléculas diana o receptores. Este sistema de comunicación en red conforma la base para el control de cada paso o de cada nivel de la fisiología reproductiva26 (Fig. 1).
Los decapéptidos hipotalámicos pueden modular directamente las funciones inmunológicas a través de efectos locales autocrinos o paracrinos en las células inmunitarias, e indirectamente a través de la activación del eje HPG. Esta regulación sobre la respuesta inmunitaria garantiza la coordinación de los mecanismos homeostáticos generales.3,27 Los estrógenos, como el 17β-estradiol y el estriol, la progesterona y la testosterona, son señales generadas por el eje HPG que actúan notablemente a diferentes niveles de este circuito de regulación.23,27 Los estrógenos ejercen sus funciones y se unen a receptores intracelulares cognados, los cuales son expresados por muchos tipos de células, incluyendo las inmunitarias, tales como, los linfocitos T y B, las células dendríticas, los macrófagos, los neutrófilos y las células asesinas naturales (NK, del inglés natural killer). Esta presencia sugiere que los estrógenos tienen un rol crucial en la modulación de la inmunocompetencia de los individuos.28-30
Las mujeres tienen un elevado número de linfocitos T cooperadores (CD4+) y de la subpoblación linfocitaria T reguladora (Treg CD4+, Foxp3+, CD25+) que experimentan numerosas fluctuaciones en relación con el ciclo ovárico, y que potencialmente afectan la capacidad de regulación y control de estas células sobre la respuesta inmunitaria global. Este equilibrio repercute, de manera directa, en el mantenimiento de la tolerancia a antígenos propios, que en caso de perderse, podría desencadenar la autorreactividad del sistema y su traducción clínica: las enfermedades autoinmunes, cuya base radica, entre otros principios, en el mantenimiento de ambientes inflamatorios perpetuados y no controlados.28,31,32 Además de la influencia de los estrógenos sobre las células inmunes, estas hormonas también actúan sobre las células endoteliales de los vasos sanguíneos, e inducen en ellas la secreción de factores atrayentes o de adhesión a las células inmunitarias, para favorecer una respuesta inmunológica en ese sitio.22,23
La menopausia marca el final del ciclo funcional reproductivo del ovario en la mujer. Esta etapa se acompaña de grandes cambios hormonales caracterizados por el declive en la secreción de estrógenos, progesterona, y en menor grado, de testosterona.2,10 El envejecimiento del ovario se hace evidente por el continuo descenso del total de folículos primordiales y ovocitos, establecidos durante la vida fetal, lo cual genera cambios endocrinos subsecuentes a la pérdida de la retroalimentación negativa que producen las hormonas ováricas en el eje HPG.2
La senectud, de manera general, es un proceso caracterizado por un decremento de todas las funciones celulares, inducido, entre otras razones, por el estrés oxidativo. El sistema endocrino, fundamentalmente a través de sus hormonas sexuales, influye en el metabolismo y favorece en este un predominio oxidativo. En este sentido se ha corroborado que existen diferencias entre ambos sexos en la expresión de marcadores de oxidación, las cuales son homogeneizadas en mujeres sometidas a ovariectomía, o cuando alcanzan la etapa biológica del climaterio.
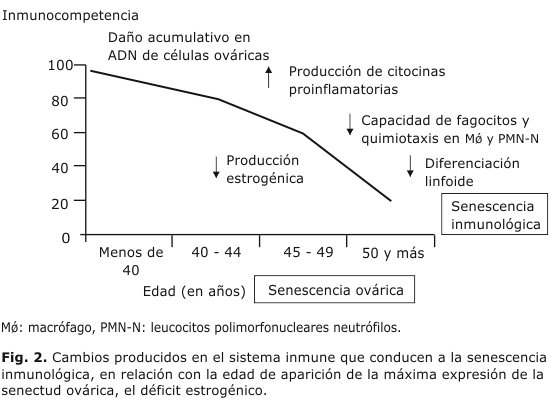
La asociación existente entre el estrés oxidativo y el envejecimiento ovárico se manifiesta en las altas concentraciones de especies reactivas de oxígeno inductoras de daño en el ADN, que se generan a lo largo de los ciclos ovulatorios que ocurren en la vida de la mujer. Otra forma de expresión de la asociación antes referida es el debilitamiento de los factores antioxidantes presentes en el ovocito, en las células de la granulosa y en el líquido folicular.33 También existen evidencias que reflejan la asociación existente entre la senectud ovárica y la inmunológica. Este vínculo se percibe con mayor claridad en la mujer posmenopáusica.34-36 El concepto de inmunosenescencia implica cambios en la inmunidad innata y en la adquirida, en cuanto a componentes de índole humoral y celular (Fig. 2). Estas transformaciones han sido atribuidas a la deprivación estrogénica correspondiente con este período biológico, ya que las modificaciones encontradas en los patrones inmunológicos pueden ser reversibles con terapia hormonal sustitutiva, aunque la contribución del déficit de las hormonas ováricas al declive de la función inmunológica no está aún bien dilucidada.32,35-37
Entre los mecanismos que conforman la primera línea de defensa del sistema inmune se encuentran los llamados sistemas de barreras físicas, químicas y biológicas, dentro de los cuales la piel deviene modelo integrador de las peculiaridades antes mencionadas. En este órgano los efectos del envejecimiento han sido ampliamente estudiados y notificados por diversos colectivos de investigación, debido a su condición holística y a su accesibilidad.38,39 La piel senil se caracteriza por una disminución en su contenido de colágeno. Esta reducción es el resultado de la producción local de citocinas proinflamatorias (TNF-α, del inglés tumor necrosis factor-alpha) que inhiben la síntesis de esta molécula; así como de la producción de metaloproteinasas (MMP-9), que favorece la aceleración de su catabolismo. El establecimiento de esta homeostasis anormal de esta proteína resulta crucial para la pérdida de la integridad funcional de la barrera cutánea.39
En lo referente a los mediadores séricos de la inmunidad innata, existe un amplio cuerpo de evidencias que avalan la presencia de elevados niveles de citocinas proinflamatorias, factores de coagulación y reactantes de fase aguda durante el envejecimiento.34-39 El término de “senectud inflamada” (del inglés inflamm-ageing) ha sido acuñado para describir este fenómeno.39
La elevación de la producción basal de citocinas IL (interleucina) 1 e IL-6 por las células musculares lisas de las paredes vasculares y la disminución en la producción local de TNF-α por los macrófagos (a pesar de la elevación de esta citocina a nivel plasmático), son factores que contribuyen al mantenimiento de un ambiente inflamatorio, que genera un estado de disfunción inmunológica con tendencia a la orquestación de respuestas de tipo autorreactivo, es decir, contra antígenos propios.32,37 En este sentido se ha planteado que la menopausia precoz es un factor de riesgo para la artritis reumatoide. A su vez, la esclerosis sistémica y la arteritis de células gigantes, también pueden verse afectadas negativamente por la aparición de la menopausia.32 Este estatus inflamatorio es reforzado por el desequilibrio metabólico que generalmente se desarrolla de manera paralela al trastorno inmunológico y endocrino. La redistribución de macrófagos en el tejido adiposo y la producción de citocinas proinflamatorias por los adipocitos, contribuye a una disfuncionalidad metabólica que se caracteriza por sensibilidad a la insulina y la obesidad, entre otras expresiones mórbidas.38
Las células que forman parte de la inmunidad innata, en este caso los polimorfonucleares neutrófilos, eosinófilos y basófilos, así como los monocitos, macrófagos y células dendríticas, muestran una activación incrementada, pero poco efectiva, en respuesta a las citocinas presentes en este medio inflamatorio.37,40-42 Además, se reporta el hallazgo de la disminución de la actividad citotóxica de las células NK.36,37 En la mayoría de los casos, este carácter entrópico de la inmunidad innata favorece la caída de la inmunovigilancia contra agentes infecciosos (particularmente el citomegalovirus y el virus de influenza), antígenos vacunales y tumorales.38
En cuanto a los efectores humorales de la inmunidad específica se ha reportado una disminución ligera de inmunoglobulinas G (IgG), aunque los restantes isotipos séricos (IgM, IgA e IgE) permanecen sin modificaciones cuantificables.41 El nivel celular de la respuesta inmune muestra un balance negativo de sus constituyentes, con una disminución del recuento linfocitario global, fundamentalmente a nivel de los linfocitos T cooperadores (CD4+) y los linfocitos B.36
A pesar de estos resultados existe consenso en la totalidad de autores revisados en este acápite particular en la necesidad de nuevos estudios que permitan corroborar estos hallazgos.34-42 La comprensión de las bases biológicas que sustentan las alteraciones de los mecanismos inmunitarios en el envejecimiento, es un reto que implica una sustancial importancia clínica.38 La apropiación de este saber permitirá su aplicación clínica, especialmente en la esfera de los medios de evaluación diagnóstica, y en el diseño de recursos terapéuticos hasta ahora no disponibles. A este respecto algunos grupos de investigación se han proyectado con verdadero comedimiento, evaluando fundamentalmente la rama humoral de la respuesta inmune a través de inmunoensayos quimioluminiscentes y los nefelométricos,31,36-39 o los elementos de la inmunidad innata de manera exclusiva.20,26,29,40,42
Otros autores34,37,41 se han aproximado a evaluar las diversas poblaciones inmunitarias a través de la citometría de flujo, procedimiento de gran alcance tecnológico, pero de escasa disponibilidad en nuestro contexto. Incluso, algunos de estos trabajos34,41 describen la fluctuación de las concentraciones celulares en sangre periférica, tras la aplicación de terapia hormonal sustitutiva en mujeres posmenopáusicas. Los resultados exhibidos, si bien constituyen en sí mismos un gran aporte, siguen siendo exiguos.
Se concluye que el desequilibrio de la respuesta inmune encontrado en las mujeres posmenopáusicas contribuye al deterioro de la salud. Las senectudes ovárica e inmunológica están estrechamente relacionadas, pues la deprivación de estrógenos influye en el sostenimiento de un ambiente proinflamatorio mediado por citocinas, y en la disminución cuantitativa y funcional de múltiples tipos celulares inmunológicos.
A pesar de la obtención de hallazgos contundentes sobre esta interrelación de los sistemas neurológico, inmunológico y endocrino que ofrecen nuevas perspectivas de análisis sobre la senescencia, aún es insuficiente el nivel de conocimiento existente en este campo de las investigaciones biomédicas. Los datos obtenidos en esta revisión bibliográfica demuestran el bajo índice de publicaciones científicas actualizadas que tratan el tema de la inmunidad en las mujeres posmenopáusicas. La posibilidad de revertir estos cambios biológicos debe constituirse en incentivo para escrutar con precisión los mecanismos patogénicos que los desencadenan, a fin de obtener herramientas que permitan un eficaz tratamiento integral —diagnóstico y terapéutico— de este grupo poblacional.
REFERENCIAS BIBLIOGRÁFICAS
1. Broekmans FJ, Knauff EA, te Velde ER, Macklon NS, Fauser BC. Female reproductive ageing: current knowledge and future trends. Trends Endocrinol Metab. 2007 Mar;18(2):58-65.
2. Stolk L, Perry JR, Chasman DI, He C, Mangino M, Sulem P, et al. Meta-analyses identify 13 loci associated with age at menopause and highlight DNA repair and immune pathways. Nat Genet. 2012 Jan 22;44(3):260-8.
3. Chou HF, Schneider JK. Self-regulation of menopause. Menopause. 2010;19(5):534-40.
4. Lugones M, Ramírez M. Menopausia sin problemas. Santiago de Cuba: Editorial Oriente; 2007. p. 3-10.
5. Ortiz N, Mariño C, Méndez B, Olarte N, Blumel J. Deterioro de la calidad de vida durante el climaterio. Rev Coloma Menopaus. 2001;7(2):201-10.
6. Coloma JM, Castello B. Menopausia: diferentes puntos de vista sobre la terapia hormonal. Revista Centroamericana de Obstetricia y Ginecología. 2008;13(4):415.
7. Lugones M. La salud integral de la mujer en el climaterio. Rev Sexología y Sociedad. 2003;9(23):28-32.
8. Navarro DA, Duany A. Expresión del cese de la función reproductiva del ovario. En: Artiles L, Navarro DA, Manzano BR, editores. Climaterio y menopausia. La Habana: Editorial Científico-Técnica; 2007. p. 156.
9. Lee SJ, Lee SH, Ha NC, Park BJ. Estrogen prevents senescence through induction of WRN, Werner syndrome protein. Horm Res Paediatr. 2010;74:33-40.
10. Broekmans FJ, Soules MR, Fauser BC. Ovarian aging: mechanisms and clinical consequences. Endocr Rev. 2009;30:465-93.
11. Aedo S, Porcile A, Irribarra C. Calidad de vida relacionada con el climaterio en una población chilena de mujeres saludables. Rev Chil Obstet Ginecol. 2006;71(6):402-9.
12. Macías C, Villaescusa R, Ustariz C, Ballester JM. Tres décadas del desarrollo de la Inmunología: su significación clínica y experimental. Rev Cubana Hematol Inmunol Hemoter. 1996;12(2):145-53.
13. Morozova EA, Lin’kova NS, Poliakova VO, Kvetnoĭ IM. Ovary: ontogenesis and aging. Adv Gerontol. 2011;24(3):393-6.
14. Hunter P. The cost of living longer. Fertility trades with immunity and life expectancy. EMBO Rep. 2011;12(10):1000-2.
15. Sarduy M, Lugones M. 2do Consenso Cubano sobre Climaterio y Menopausia. La Habana: Editorial Cimeq; 2007. p. 6-7.
16. Heredia B, Lugones M. Edad de la menopausia y su relación con el hábito de fumar, estado marital y laboral. Rev Cubana Obstet Ginecol [serie en Internet]. 2007 [citado 10 de agosto de 2014];33(3). Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0138-600X2007000300008&lng=es&nrm=iso&tlng=es
17. Del Prado M, Fuenzalida A, Jara D, Figueroa R, Flores D, Blumel J. Evaluación de la calidad de vida en mujeres de 40 a 59 años mediante la escala MRS (Menopause Rating Scale). Rev Méd Chile. 2008;136:1511-7.
18. Albala C, Lebrão ML, León Díaz EM, Ham-Chande R, Hennis AJ, Palloni A, et al. Encuesta Salud, Bienestar y Envejecimiento (SABE): metodología de la encuesta y perfil de la población estudiada. Rev Panam Salud Pública. 2005;17(5/6):307-22.
19. Manolio TA. Genomewide association studies and assessment of the risk of disease. N Engl J Med. 2010;363:166-76.
20. Chen W, Yang CC, Todorova Al, Khuzaei S, Chiu HC, Worret WI, et al. Hair loss in elderly women. Eur J Dermatol. 2010 Mar-Apr;20(2):145-51.
21. Santisteban S. Atención integral a las mujeres de edad mediana. Rev Cubana Obstet Ginecol [serie en Internet]. 2011 [citado 10 de agosto de 2014];37(2). Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0138-600X2011000200015&lng=es&nrm=iso&tlng=es
22. Stevenson JC. A woman's journey through the reproductive, transitional and postmenopausal periods of life: impact on cardiovascular and musculo-skeletal risk and the role of estrogen replacement. Maturitas. 2011 Oct;70(2):197-205.
23. Rozenberg S, Vandromme J, Antoine C. Postmenopausal hormone therapy: risks and benefits. Nat Rev Endocrinol. 2013;9:216-27.
24. Osório J. Less estrogen, more neuroinflammation? Nature Reviews Endocrinology. 2012;8:381.
25. Libert C, Dejager L, Pinheiro I. The X chromosome in immune functions: when a chromosome makes the difference. Nature Reviews Immunology. 2010 August;10:594-604.
26. Morale MC, Gallo F, Tirolo C, Testa N, Caniglia S, Marletta N, et al. Neuroendocrine-immune circuitry from neuron-glial interactions to function: Focus on gender and HPA-HPG interactions on early programming of the NEI system. Immunology and Cell Biology. 2001;79:400-17.
27. Fahey JV, Wright JA, Shen L, Smith JM, Ghosh M, Rossoll RM, et al. Estradiol selectively regulates innate immune function by polarized human uterine epithelial cells in culture. Mucosal Immunology. 2008 July;1(4):317-25.
28. Fish EN. The X-files in immunity: sex-based differences predispose immune responses. Nature Reviews Immunology. 2008 September;8:737-44.
29. Lüthje P, Hirschberg AL, Brauner A. Estrogenic action on innate defense mechanisms in the urinary tract. Maturitas. 2014 Jan;77(1):32-6.
31. Sakiani S, Olsen NJ, Kovacs WJ. Gonadal steroids and humoral immunity. Nat Rev Endocrinol. 2013;9:56-62.
32. Sammaritano LR. Menopause in patients with autoimmune diseases. Autoimmun Rev. 2012 May;11(6-7):A430-6.
33. Vitale G, Salvioli S, Franceschi C. Oxidative stress and the ageing endocrine system. Nat Rev Endocrinol. 2013;9:228-40.
34. Ghosh M, Rodriguez-Garcia M, Wira CR. The immune system in menopause: Pros and cons of hormone therapy. J Steroid Biochem Mol Biol. 2014;142C:171-5.
35. Engelmann F, Barron A, Urbanski H, Neuringer M, Kohama SG, Park B, et al. Accelerated immune senescence and reduced response to vaccination in ovariectomized female rhesus macaques. AGE. 2011;33:275-89.
36. Gameiro C, Romão F. Changes in the immune system during menopause and aging. Front Biosci (Elite Ed). 2010 Jun 1;2:1299-303.
37. Gameiro CM, Romão F, Castelo-Branco C. Menopause and aging: changes in the immune system-a review. Maturitas. 2010 Dec;67(4):316-20.
38. Shaw AC, Goldstein DR, Montgomery RR. Age-dependent dysregulation of innate immunity. Nature Reviews Immunology. 2013 Dec;13:875-7.
39. Borg M, Brincat S, Camilleri G, Schembri-Wismayer P, Brincat M, Calleja-Agius J. The role of cytokines in skin aging. Climacteric. 2013;16(5):514-21.
40. Zeller T, Wild P, Szymczak S, Rotival M, Schillert A, Castagne R, et al. Genetics and beyond the transcriptome of human monocytes and disease susceptibility. PLoS One. 2010;5(5):e10693.
41. Medeiros SF, Maitelli A. Cellular and humoral immune responses after short-term oral hormone therapy in postmenopausal women. Climacteric. 2011 Dec;14(6):677-82.
42. Sárvári M, Hrabovszky E, Kalló I, Solymosi N, Likó I, Berchtold N, et al. Menopause leads to elevated expression of macrophage-associated genes in the aging frontal cortex: rat and human studies identify strikingly similar changes. J Neuroinflammation. 2012 Dec 3;9:264.
Recibido: 27 de diciembre de 2014.
Aprobado: 2 de abril de 2015.
Emigdio José León Toirac. Instituto Nacional de Endocrinología (INEN). Calle Zapata y D, Vedado, municipio Plaza de la Revolución. La Habana, Cuba. Correo electrónico: emigdio.leon@infomed.sld.cu