Introducción
El avance de la resistencia bacteriana es indetenible y ocurre con mayor rapidez que el surgimiento de nuevos antimicrobianos para combatir las bacterias multirresistentes.
Aunque en algunos países del mundo los estudios de resistencia antimicrobiana son escasos, es cierto que se trata de un fenómeno global.1
El estudio SMART-España (Study forMonitoring Antimicrobial Resistance Trends) informa un incremento en la frecuencia de E. coli, K. pneumoniae, K. oxytoca y Proteus mirabilis, productores de betalactamasas de espectro extendido (BLEE) de origen comunitario, y de K. pneumoniae productora de BLEE de origen nosocomial en el período de 2002 a 2015.2
En hospitales del sudeste de EE.UU., durante el período de 2009 a 2014 se registra un incremento en la incidencia de E. coli productora de BLEE, así como en el número de hospitales que la notifican.3
En América Latina también hay un incremento en el número de microorganismos productores de BLEE.4,5,6,7.8,9
Aunque en microorganismos gramnegativos la producción de enzimas betalactamasas es el mecanismo más común de resistencia, las BLEE en particular constituyen un grupo muy importante por su capacidad de inactivar las cefalosporinas de tercera y cuarta generación y el aztreonam. En la práctica clínica, los carbapenémicos son el único tipo de betalactámicos útiles para el tratamiento de los microorganismos con BLEE.10
Además, con mucha frecuencia las BLEE están acompañadas con otros mecanismos de resistencia, lo que implica multidrogorresistencia, mientras que la transmisión a través de plásmidos facilita su diseminación.10
La detección en los laboratorios de microbiología de BLEE es imprescindible, porque ofrece información en cuanto al antibiótico más útil en cada caso y permite implementar medidas de aislamiento para evitar la dispersión de los microorganismos que las portan.10
En Cuba, a pesar de no existir numerosos estudios de BLEE, se conoce que entre los años 2014 y 2017 su prevalencia en enterobacterias varió entre 32 y 57 %, según diferentes estudios realizados.11,12,13
Por todo lo anterior, nos propusimos determinar la incidencia y principales características de los aislados de Escherichiacoli y Klebsiellapneumoniae productores de betalactamasas de espectro extendido en muestras no urogenitales.
Métodos
Estudio transversal realizado en el hospital “Salvador Allende” durante el año 2017. Se incluyó la información referente a todos los aislados deE. Coli y K. pneumoniae productores de BLEE de muestras no urogenitales obtenidas en el citado hospital durante el año 2017; se excluyeron aislados repetidos, no se eliminó ningún aislado previamente incluido.
A partir de la revisión del libro de registro de antibiogramas del laboratorio de microbiología, se obtuvo el número de aislados de E. coli y K. pneumoniae productores de BLEE, se determinó su procedencia según el servicio del hospital y las muestras clínicas, así como su sensibilidad a los antimicrobianos;también se calculó su porcentaje con respecto al número total de aislados de E. coli y K. pneumoniae. Losresultados se expresaron en frecuencias absolutas y relativas.
El aislamiento e identificación de los microorganismos se realizó mediante las pruebas bioquímicas convencionales utilizadas para enterobacterias. Los antibiogramas se hicieron según el método de Kirby-Bauer, y para su lectura e interpretación se siguieron las indicaciones del Instituto de Estándares de Laboratorios Clínicos (CLSI por sus siglas en inglés).14
Para la determinación de BLEE se utilizó el método de doble disco descrito por Jarlier,15) para lo cual a un lado de un disco de augmentín (30 µg) a una distancia de 25 mm, se colocó un disco de ceftriaxona (30 µg) o de cefotaxima (30 µg), y al otro lado, uno de aztreonam (30 µg). Todos los discos utilizados eran del fabricante italiano Liofilchem.
Se consideraron microorganismos productores de BLEE los que presentaron halos de inhibición en el rango que recomienda el CLSI para considerar sospecha de BLEE, y que además mostraron la imagen confirmatoria de sinergia o efecto huevo entre el disco de augmentín y uno de los dos o los dos discos que se colocaron a ambos lados.
Como cepa control negativo se utilizó la Escherichia coli ATCC 25922, sensible a todos los antibióticos, y como controles positivos, cepas previamente conocidas de E. coli y K. pneumoniae productoras de BLEE.
Para el diseño y ejecución de este estudio se tuvo en cuenta la Declaración de Helsinki de la Asociación Médica Mundial.16 No se utilizó información personal de los pacientes ni se les ocasionó perjuicio alguno.
Resultados
De 99 aislados de E. coli obtenidos en el período de estudio, 46 (46 %) fueron productores de BLEE; de 44 aislados de K. pneumoniae, 22 (50 %) fueron productores de BLEE.
La mayoría de estos aislados productores de BLEE provenían demuestras de las dos salas del Instituto de Angiología (está ubicado en áreas del hospital “Salvador Allende”), seguidos en frecuencia porl os de las salas de cirugía, los de consultas externas y los procedentes de otros servicios (Fig.1). La piel fue el sitio anatómico de donde más se aislaron. (Tabla 1)

Fuente: Libro de registro de antibiogramas del laboratorio de microbiología del hospital “Salvador Allende”, 2017.
Fig. 1 Origen de los aislados con BLEE según servicios.
Tabla 1 Origen de los aislados con BLEE según tipo de muestra
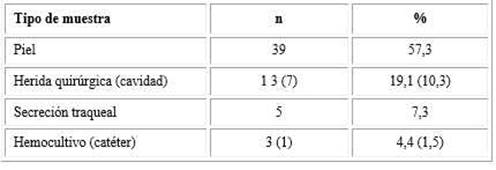
Fuente: Libro de registro de antibiogramas del laboratorio de microbiología del hospital “Salvador Allende”, 2017.
Los aislados de E. coli productores de BLEE procedían con mayor frecuencia de las salas del Instituto de Angiología y de cirugía, donde constituyeron más de la mitad de las E. coli aisladas. En la UCI se aislaron tres E. coli, todas productoras de BLEE. K. pneumoniae productora de BLEE fue más frecuente en las salas del Instituto de Angiología, la UCI y las consultas externas; en los dos primeros servicios constituyeron más de la mitad de los aislados de esta especie. (Tabla 2)
Tabla 2 Distribución de los aislados de E. coliyK. pneumoniae, total y productores de BLEEsegúnservicios

UCI: unidad de cuidados intensivos; UCIM: unidad de cuidados intermedios.
Fuente: Libro de registro de antibiogramas del laboratorio de microbiología del Hospital ¨Salvador Allende”.
Para ambos microorganismos productores de BLEE, el antimicrobiano con mayor efectividad fue el meropenem, seguido del cloranfenicol. De los aislados de E. coli, 95 % fue sensible a la amikacina, pero solo lo fue 58 % de los de K. pneumoniae. (Fig. 2)
La sensibilidad de ambos microorganismos para el resto de los antimicrobianos estuvo por debajo de 80 %, no hubo aislados sensibles a las cefalosporinas de 3ra. generación y solo 7 % de E. coli fue sensible a cefepime. (Fig 2)
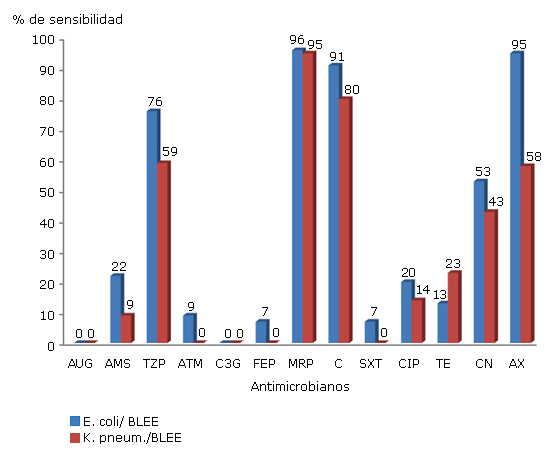
AUG: augmentín; AMS: ampicillín/sulbactam; TZP: piperacillina/tazobactam; ATM: aztreonam; C3G: cefotaxima o cefriaxona; FEP: cefepime; MRP: meropenem; C: cloramfenicol; SXT:trimetoprim/sulfametoxazol; CIP: ciprofloxacino; TE: tetraciclina; CN: gentamicina; AX: amikacina. Fuente: Libro de registro de antibiogramas del laboratorio de microbiología del Hospital ¨Salvador Allende¨.
Fig. 2 Sensibilidad antimicrobiana de los aislados de E. coli y K. Pneumoniae productores de BLEE.
Discusión
En la actualidad las BLEE se encuentran diseminadas por todo el mundo y así lo confirman numerosos estudios. En Europa en 2017, los aisladosde E. coli y K. pneumoniae resistentes a cefalosporinas de tercera generación alcanzan 14,9 y 31,2 %, respectivamente, de ellos la mayoría son productores de BLEE.17 En 2015, 6,9 % de aislados de E. coli, K. pneumoniae y P. mirabilis que se notifican en hospitales de EE. UU., portan BLEE.18
Aunque existe una tendencia al aumento de enterobacterias productoras de BLEE en los países desarrollados, la mayor prevalencia se localiza en los subdesarrollados.19) En América Latina las cifras de enterobacterias productoras de BLEE que se informan en años recientes, son en general más altas que las que notifican los países desarrollados y oscilan entre 11,8 y 43 %,4,5,6,7,8,9 en dependencia de las muestras, las edadesy los países que se tienen en cuenta al realizar los estudios. En Cuba se registra una prevalencia de 57 % en aislados de E. coli en muestras de hospitales entre 2014 y 2016.13
Existe consenso en que los individuos gravemente enfermos, que tienen una larga estadía en el hospital y necesitan de sonda vesical, tubo endotraqueal o abordaje venoso central, son más propensos a desarrollar colonización o infección por microorganismos productores de BLEE.20
Mención aparte merece el uso previo de antibióticos, algunos autores plantean que este factor de riesgo unido al antecedente de ingreso al menos por un día, en un entorno de alto riesgo para adquirir un microorganismo productor de BLEE, ambos en los últimos seis meses, eleva el riesgo de portar dichos microorganismos en 100 %.20,21
En este estudio, en las salas del Instituto de Angiología se aisló el mayor número de E. coli y K. pneumoniae productoras de BLEE. La permanencia de los pacientes en estas durante períodos largos, debido a la naturaleza crónica de sus lesiones, generalmente de piel o heridas quirúrgicas, facilitaría dicha adquisición. En coincidencia, estos fueron los sitios anatómicos de los que se obtuvieron la mayoría de los aislados con BLEE en este estudio. Es conocido que entre 40 y 80 % de las úlceras en el pie diabético se infectan,22) y se informa una frecuencia de 31 % de enterobacterias productoras de BLEE en estas lesiones.23
En estas salas es práctica común tanto el uso de antibióticos de amplio espectro como la realización de procederes invasivos, y estas características también son propias dela UCI, donde siete de los nueve aislados de E. coli y K. pneumoniae en total, portaban BLEE.
La presencia de BLEE complica el pronóstico no solo por el limitado número de antibióticos que son efectivos, sino por ser frecuente la corresistencia a quinolonas y a otros grupos de antibióticos,19,24,25 debido a que muchos de los genes causantes de las corresistencias (aad, aac,aph, dhfr, qnr, tet) se transfieren con los genes blaBLEE.26
En este estudio, de forma general, hubo un mayor porcentaje de aislados de K. pneumoniae productores de BLEE con respecto a los de E. coli; de forma particular lo mismo sucedió con los aislados procedentes de las salas del Instituto de Angiología. Otros autores también registran predominio de BLEE en K. pneumoniae con respecto a otras enterobacterias.17,27
Una posible explicación a este hecho pudiera estar en los resultados de un estudio que incluyó 11 420 pacientes de 13 UCIs europeas, que demuestra que aislados de enterobacterias no E. coli, con predominio de K. pneumoniae, pueden ser 3,7 veces más transmisibles que los de E.coli.,28 En este hecho constituye un factor importante la capacidad de K. pneumoniae de sobrevivir en superficies secas inanimadas, entre 2 horas hasta 30 meses, en contraposición con el tiempo que lo hace E. coli, que puede ser de 1,5 horas a 16 meses.29
La presencia de BLEE implica resistencia en grado variable a cefalosporinas de tercera y cuarta generación, sin embargo, se mantiene la sensibilidad a los carbapenémicos, a menos que coexistan otros mecanismos de resistencia. Así se confirmó en este estudio, en coincidencia con muchos otros realizados en diversas áreas geográficas;4,6,17,25,27,30,31
también se observó que la sensibilidad de K. pneumoniae a meropenem fue discretamente menor que la de E. coli, hecho que de igual modo se ha informado.28
En relación con los aminoglucósidos y las quinolonas, el estudio de vigilancia de resistencia antimicrobiana europeo EARS-Net, de 2017,17 notifica una alta resistencia a estos grupos, y es mayor en K. pneumoniae que en E. coli. En el presente trabajo también se observó una mayor resistencia de K. pneumoniae a aminoglucósidos y ciprofloxacina, así como al resto de los antimicrobianos probados, excepto a la tetraciclina. K. pneumoniae, por su capacidad de sobrevivir largo tiempo en el ambiente hospitalario,29) puede infectar a los pacientes y de estos nuevamente a las superficies y al instrumental, en un círculo vicioso que favorece la selección de los aislados más resistentes por el uso de antibióticos de amplio espectro.
En cuanto a E. coli, la sensibilidad a la amikacina en este estudio fue tan alta como al meropenem (Fig. 2). En otros, la sensibilidad a la amikacina en enterobacterias productoras de BLEE varía; pero con respecto a inhibidores de la vía del folato como el trimetoprim/sulfametoxazol, la ciprofloxacina y la tetraciclina, hay coincidencia en la baja sensibilidad observada.4,30,32,33
Como limitación del presente trabajo, además del pequeño tamaño de la muestra, existe la posibilidad de un subregistro, debido a que el método de detección utilizado puede enmascarar la presencia de BLEE en caso de existir otros mecanismos de resistencia añadidos, como alteraciones de permeabilidad, resistencia simultánea a los inhibidores de ß-lactamasas o producción de carbapenemasas.34,35
Este estudio demuestra una alta incidencia de aislados de Escherichia coli y Klebsiella pneumoniae productores de betalactamasas de espectro extendido en el Hospital “Salvador Allende” de La Habana, más marcada en las salas del Instituto de Angiología y en muestras de piel.
Recomendamos tener en cuenta la ineficacia de las cefalosporinas de tercera generación como tratamiento empírico en algunos servicios del hospital, así como la importancia de la lectura interpretada del antibiograma para la identificación temprana de BLEE, en aras de utilizar una adecuada política de antibióticos y de tomar medidas para el control de infecciones que contribuyan a frenar su diseminación.
Recomendamos además, mantener el control sobre el uso de antimicrobianos de amplio espectro, especialmente los carbapenémicos, por ser los únicos betalactámicos eficaces en la práctica clínica frente a los microorganismos productores de BLEE.















