Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Angiología y Cirugía Vascular
versión On-line ISSN 1682-0037
Rev Cubana Angiol Cir Vasc vol.16 no.2 La Habana jul.-dic. 2015
Rev Cubana Angiol Cir Vasc. 2015;16(2)
ARTÍCULO DE REVISIÓN
Terapia antimicrobiana utilizada de forma empírica y prudente en los pacientes con enfermedades vasculares periféricas
The empiric and prudent anti-microbial therapy used in the patients with vascular peripheral disease
DrC. Andrés Samuel Fleitas Estévez
Instituto Nacional de Angiología y Cirugía Vascular. La Habana, Cuba.
RESUMEN
Introducción: el uso inadecuado de los antimicrobianos ha traído un incremento de la resistencia de los microorganismos, aumento de los costos hospitalarios y calidad deficiente en los servicios brindados.
Objetivo: orientar una política terapéutica racional de los antimicrobianos sobre todo cuando son utilizados de forma empírica.
Fuente de datos: revisión bibliográfica realizada entre 2000-2014 en las bases de datos MedLine, Hinari, Cochrane, PubMed, de revistas líderes en la publicación de artículos de interés. Las palabras claves fueron: antibióticos, resistencia bacteriana, tratamiento antimicrobiano. Se consultaron estudios de cohorte prospectivos, retrospectivos, clínicos, epidemiológicos, revisiones bibliográficas y ensayos clínicos.
Síntesis de los datos: aportamos información que puede ser útil en la práctica médica y procederes y métodos creados por diferentes equipos de especialistas en el tema y de consensos internacionales. Siempre que sea posible, debe tenerse en cuenta la toma de un exudado para cultivo y antibiograma que muestre los posibles antimicrobianos a los que el germen es sensible y seleccionar el apropiado según su efectividad con el espectro más estrecho posible, menos efectos indeseables y el más económico para utilizarlo en la dosis adecuada y durante el tiempo necesario según el peso, la talla, la edad y afecciones renales o hepáticas del paciente, para ajuste de las dosis; además, aplicarlo por la vía de administración más sencilla y menos riesgosa, para alcanzar el efecto terapéutico durante el tiempo más corto posible.
Conclusiones: se sugiere una terapia antimicrobiana racional y prudente, sobre todo cuando es utilizada de forma empírica. Su efecto es elevar la eficacia de los fármacos empleados en pacientes con afecciones infecciosas frecuentes en angiología.
ABSTRACT
Introduction: inadequate use of the antimicrobial drugs has brought about increase microorganism resistance, the rise of hospital costs and poor quality of the rendered services.
Objective: to advise on the rational therapeutic policy for the use of antimicrobials, mainly when used empirically.
Data source: literature review conducted from 2000 to 2014 MedLine, Hinari, Cochrane PubMed databases and in leading journals that publish articles of interest. The following keywords were used: antibiotics, bacterial resistance and antimicrobial treatment. Prospective, retrospective, clinical, epidemiological cohort studies as well as literature reviews and clinical assays were all consulted.
Data synthesis: this paper provided some useful information in medical practice, as well as some procedures and methods created by teams of experts on this topic and international consensus on the theme. One must take into account whenever possible exudates for culturing and antibiogram that show the likely antimicrobials to which the microorganism is sensitive, and select the most appropriate based on its narrowest spectrum effectiveness, less adverse effects and the most economic to be used at the right dosage and for the required time depending on weight, size, age and renal or liver conditions of the patient. Additionally, the antimicrobial should be applied through the simplest and less risky way of administration in order to achieve the best results of treatment at the shortest term.
Conclusions: It is suggested that rational and prudent antimicrobial therapy should be used in patients, mainly if it is empirically applied. Its effect is to increase efficacy of drugs for patients suffering frequent vascular infections.
INTRODUCCIÓN
Los agentes antimicrobianos constituyen uno de los grupos fármaco-terapéuticos más prescrito en la práctica médica moderna. La contribución de estos medicamentos a la terapéutica antinfecciosa continúa siendo vital. Correctamente utilizados, los antimicrobianos permiten prevenir y curar la mayoría de las infecciones bacterianas con un significativo impacto sanitario, social y económico.
El surgimiento de infecciones resistentes a los antibióticos está llegando a niveles sin precedentes y nos estamos quedando sin medicamentos efectivos para combatirlas. Las cepas resistentes son muy difíciles de tratar con los antibióticos disponibles. El mundo está a punto de perder sus curas milagrosas: los antibióticos. Se requieren medidas globales concertadas y urgentes de gobiernos, profesionales de la salud, industria y sociedad civil para volver más lenta la propagación de la resistencia a estos fármacos.1-4
El mundo se está dirigiendo hacia una era posantibióticos, en la cual muchas infecciones comunes ya no podrán curarse y una vez más, comenzarán a matar con toda su fuerza. Cuando los antibióticos, compuestos capaces de destruir o disminuir el crecimiento de las bacterias, fueron descubiertos a fines del siglo XIX, el tratamiento y control de las infecciones cambió a la medicina y la historia humana. Las enfermedades que entonces causaban enorme devastación y muerte, como la lepra, tuberculosis, gonorrea y sífilis, pudieron curarse con estos fármacos. Ahora, sin embargo, la guerra contra algunas de las infecciones, como la tuberculosis, parece haber vuelto a tomar fuerza debido al surgimiento de nuevas cepas resistentes a los medicamentos disponibles.1
También están las infecciones letales de las llamadas superbacterias que se contraen por lo general en los hospitales y que pueden ser mortales por la dificultad para tratarlas. Tan solo en Europa más de 25 000 personas mueren cada año debido a infecciones de superbacterias, imposibles de tratar incluso con los antibióticos más nuevos.1,5
Esta tendencia es muy preocupante y en parte causada por el mal uso (tanto por exceso de uso, como del uso inadecuado) que ha hecho la humanidad con los antibióticos. Porque cada vez que se usa un fármaco que mata a las bacterias, siempre hay, entre los millones de cepas que pueden tener estos microbios, una que puede mutar y resistir el ataque de este antibiótico. Así que el fármaco puede matar a la gran mayoría de esos microbios pero ciertamente la cepa resistente no muere y el sistema inmune no puede atacarla. Esa cepa puede crecer y eventualmente puede multiplicarse hasta reemplazar a todas las cepas no resistentes. Con cada nueva generación, el microorganismo genéticamente resistente se vuelve más dominante lo cual provoca una reincidencia de la enfermedad, hasta que los antibióticos se vuelven inefectivos. Esta es la selección natural de las bacterias, la forma con la cual se aseguran de sobrevivir.
Aunque la industria farmacéutica también ha ido avanzando, no ha logrado hasta ahora ganarle la carrera a los microorganismos. A través de la historia el hombre ha respondido a esta lucha desarrollando nuevos antibióticos para combatir a cada nueva cepa resistente que ha ido surgiendo.6-10
La presente revisión tuvo como objetivo orientar hacia una política terapéutica racional de los antimicrobianos en los servicios de angiología y elevar la eficacia de los mismos, sobre todo cuando son utilizados de forma empírica.
FUENTE DE DATOS
Se realizó una revisión bibliográfica entre 2000-2014 en las bases de datos MedLine, Hinari, Cochrane, PubMed; de revistas líderes en la publicación de temas y artículos de interés. La búsqueda se realizó con las palabras claves siguientes: antibióticos, resistencia bacteriana, tratamiento antimicrobiano. Se consultaron estudios de cohorte prospectivos, retrospectivos, clínicos, epidemiológicos, revisiones bibliográficas y ensayos clínicos.
SÍNTESIS DE LOS DATOS
El uso racional de antibióticos puede producir beneficios desde el punto de vista médico y social, pero su uso en ocasiones es inadecuado por lo que la terapéutica antibiótica debe ser objeto de una vigilancia especial y sistemática.
En la práctica clínica habitual se ha observado que el celo del médico por curar al paciente, quizás una información deficiente sobre el espectro antimicrobiano en la comunidad además de la sensibilidad del germen o la resistencia del mismo lleva a una prescripción inadecuada. En ocasiones, unas veces diagnosticadas una infección bacteriana no se toman en consideración el posible germen infectante según el cuadro epidemiológico y la localización de la sepsis y se seleccionan erróneamente los antibióticos o se indican combinaciones irracionales de los mismos, no se obtiene el resultado deseado y se logra el terrible efecto de la resistencia bacteriana.
Por eso, siempre que sea posible, debe tenerse en cuenta la toma de un exudado para cultivo y antibiograma que muestre los posibles antimicrobianos a los que el germen es sensible y seleccionar el apropiado según su efectividad con el espectro más estrecho posible, menos efectos indeseables y el más económico para utilizarlo en la dosis adecuada y durante el tiempo necesario según el peso, la talla, la edad y otras afecciones renales o hepáticas del paciente, para ajuste de las dosis; además, aplicarlo por la vía de administración más sencilla y menos riesgosa, para alcanzar el efecto terapéutico durante el tiempo más corto posible. Es aconsejable, cuando se van a utilizar dos antimicrobianos, que no sean de la misma familia, así como tener en cuenta el sinergismo de estos y prescribir un bactericida junto a un bacteriostático. Recordar el efecto posantibiótico del agente que puede ser utilizado.
Se debe identificar en los diferentes servicios de la especialidad la situación concreta en relación con la infección. Si es posible construir el mapa microbiológico que permita conocer la resistencia a los antibióticos que se han utilizado, así como la prioridad de cada paciente de acuerdo al estado de la afección.10-13
La calidad de la atención médica pasa por el camino de la eficiencia económica, ya que la utilización racional de los recursos materiales, humanos y financieros, al tiempo que expresa una elevada calificación científico-técnica y organización del trabajo, asegura una mayor dedicación de estos recursos en beneficio del paciente.14,15
Para asegurar el cumplimiento de una política de antibióticos en un hospital o servicio es necesario la aplicación de un conjunto de medidas, previamente consensuadas, y la participación activa de numerosos especialistas de todas las áreas de asistencia, en colaboración con representantes de diferentes especialidades básicas (microbiología, farmacia, farmacología, medicina preventiva) ya que son los responsables de diseñar las estrategias terapéuticas más adecuadas a la situación de cada servicio. Así deben estar estrechamente relacionados los servicios de microbiología, epidemiología y el médico de asistencia de los pacientes.13
Entre las malas prácticas más frecuentes en el uso de antimicrobianos se encuentra la indicación de antibióticos sin la toma de cultivos, se indica un antibiótico inicial inadecuado por no considerar el patrón de susceptibilidad del centro, se mantienen tratamientos por periodos muy largos y se utilizan múltiples combinaciones innecesarias, otras veces no se ajustan las dosis por insuficiencia renal o hepática o no se hacen ajustes al tratamiento de acuerdo con los cultivos. En ocasiones se utiliza la vía parenteral en casos en que puede usarse la vía oral para alcanzar buenas concentraciones séricas y otras veces no se considera el precio de las diferentes opciones.14-16
Cabe señalar que se le debe recordar a los paciente evitar la automedicación y a los médicos el manejo empírico de antibióticos, que no todas las fiebres son infecciosas, ni bacterianas; además que no todas las infecciones bacterianas requieren de antibióticos, estos deben emplearse solo cuando estén bien justificados y evitar la mezcla indiscriminada.
La selección del antibiótico cuando se carece de antibiograma debe ser hecha sobre las bases clínicas y epidemiológicas locales y no sobre reportes internacionales ya que la susceptibilidad varía en el tiempo y en el espacio. También se debe estar atento a los signos de superinfección para tratarlas oportunamente.16,17
Se debe reconocer que no siempre es posible contar con un aislamiento y un antibiograma, pero en esos casos es entonces indispensable contar con una información epidemiológica y estadística confiable que permita dar un tratamiento adecuado y oportuno. Es deber de los laboratorios de microbiología apoyar a los Comités de Prevención y Control de Infecciones brindando información sistemática sobre las floras predominantes tanto a nivel hospitalario como en la comunidad.16-18
En muchas ocasiones se ha contrapuesto el resultado científico empírico, cuando se indica un antimicrobiano sin cultivos microbiológicos, en contra de lo que en la actualidad se denomina “La medicina basada en la evidencia”, que sería la misma indicación pero fundamentada en un resultado del laboratorio.
Cuando algún facultativo indica un medicamento antimicrobiano con el objetivo de combatir cualquier tipo de infección, aún cuando no tenga el cultivo, valga decir la constatación científica de cual es la bacteria sensible a ella, de alguna forma en la base de su pensamiento clínico, hay una gran evidencia científica, esta es: su experiencia personal. Esta cualidad implica un conjunto de conocimientos previos que han adquirido y acumulado a lo largo del tiempo, en la lucha contra el control de la sepsis en determinado tipo de pacientes y además enriquecido por el colectivo de su grupo básico de trabajo.
La experiencia demuestra que cuando un paciente se encuentra mejorando, la pregunta difícil de responder es cuándo ha llegado el momento de retirar el antimicrobiano o la combinación utilizada, más aún, en muchas ocasiones el médico se encuentra muy preocupado en correr el riesgo de dejar a su paciente desprotegido, de manera que lo verdaderamente dificultoso sería tener la pericia, la intuición y la experiencia necesarias para poder prescindir del tratamiento anti-microbiano cuando se considere oportuno.16-19
Se cree que los indicadores clínicos, los marcadores de sepsis que brinde el laboratorio, unido al buen juicio clínico, son suficientes para la toma de una decisión adecuada en el momento preciso. El dictamen que se da no estará restringido por los términos cualitativos “sensible” y “resistente”, ya que ningún organismo lo es de manera absoluta y estricta, sino que en cierto modo es una cuestión de dosis.
Actualmente, la tecnología automatizada le permite a los laboratorios medir de manera rápida, fácil y económica la susceptibilidad relativa de un organismo a los agentes antimicrobianos. Al combinar la susceptibilidad relativa con la información farmacológica de los medicamentos, el clínico cuenta con información suficiente, basada en evidencia científica, para elegir determinado fármaco, calcular sus dosis y elegir la ruta de administración adecuada, que conduzca a una máxima eficacia terapéutica con un mínimo de efectos colaterales para el paciente y que represente una mejora en el indicador costo/beneficio.16,20
Al tener en cuenta el análisis de los patrones de resistencia bacteriana, hay que tener en cuenta la necesidad de preservar algunos antibióticos, sobre todo los de utilización estratégica; esto se refiere a poder resguardar, en el marco de la dinámica de la resistencia de nuestra flora bacteriana, un pequeño grupo de antibióticos utilizable en un momento determinado, por ejemplo cuando está en juego la vida de un paciente porque se encontró en una evolución tórpida, un germen resistente a los antimicrobianos o a las combinaciones utilizadas con anterioridad. Se considera que el concepto es válido siempre, pero que con el análisis periódico del fenómeno puede cambiar.19,20
Al hacer un uso científico racional y equilibrado de los antimicrobianos, la calidad de atención al paciente es superior. Esta reflexión nos lleva a preguntarnos: ¿Cuánto daño dejamos de hacer?, ¿cuántas insuficiencias renales evitó nuestra política?
A continuación se hace referencia a algunas afecciones infecciosas muy relacionadas con la especialidad de angiología y cirugía vascular, que el especialista tiene que enfrentar frecuentemente:
a) Infecciones de piel y anexos:
– Celulitis aguda: (Staphylococcus aureus, Streptococcus Grupo A; Penicilina resistente a penicilinasas; cefalosporinas 1ra., 2da. o 3ra generación.
– Celulitis anaeróbica: (Enterobacterias + Anaeróbios; Streptococci, Bacteroides, Clostridium; Penicilina + Aminoglucósido; Clindamicina + Aminoglucósido).
– Celulitis en pacientes diabéticos: (Polimicrobiana incluyendo anaeróbios; Clindamicina + Aminoglucósido; Cefalosporinas 1ra., 2da. o 3ra. generación + Metronidazol).
– Fascitis necrotizante: (Enterobacterias + anaeróbios; Streptococci, Bacteroides, Clostridium; Penicilina + Aminoglucósido, Clindamicina + Aminoglucósido).
– Gangrena gaseosa: (Enterobacterias + anaerobios: Streptococci, Bacteroides, Clostridium); Penicilina + Aminoglucósido, Clindamicina + Aminoglucósido).
– Impétigo: (Estreptococci Grupo A, Staphylococcus aureus; Penicilina resistente a penicilinasas; Eritromicina).
b) Infecciones asociadas al sistema vascular periférico. Entre las infecciones asociadas al sistema vascular periférico se encuentran:
– La tromboflebitis séptica post parto o post aborto: (Bacteroides spp, Enterobacterias, Clostridium spp, Estreptococci spp; Clindamicina + Aminoglucósido, Cefalosporinas 1ra, 2da. o 3ra generación + Metronidazol).
– La tromboflebitis séptica por catéter: (Staphylococcus aureus, Staphylococcus Epidermidis, Candida spp., Pseudomonas spp. Enterobacterias; Penicilina resistente a penicilinasas; Clindamicina + Aminoglucósido).
La mayoría de los microorganismos anaerobios son susceptibles a la penicilina; con excepción de algunas especies de Bacteroides. En el caso especifico del B. fragilis se debe considerar “a priori” como resistente a la penicilina y el 50 % de los B. melaninogenicus también lo son, por lo que cuando se sospeche la presencia de estas bacterias el manejo deberá llevarse a cabo con Cloramfenicol, Clindamicina o Metronidazol.20
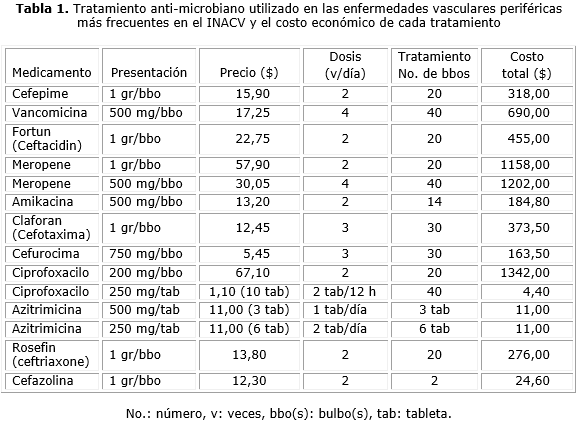
Para lograr los objetivos propuestos, los angiólogos y cirujanos vasculares de cada uno de los servicios (Arteriología, Flebolinfología, y Angiopatía Diabética) del Instituto Nacional de Angiología y Cirugía Vascular (INACV), analizaron y discutieron las guías y las normas internacionales, así como se tuvo en cuenta la experiencia médica de los mismos, para decidir los antibióticos más empleados en las afecciones anteriores, y la disposición de fármaco en el Cuadro Básico Nacional de Medicamentos Se llegó al acuerdo sobre cuál era el tratamiento antimicrobiano a seguir en las enfermedades más frecuentes en el INACV, que puede ser adoptado en otros servicios de Angiología del país. Además se valoró el costo económico de cada tratamiento (tabla 1).
Atendiendo a la experiencia de los facultativos y a los resultados empíricos obtenidos en el INACV en los últimos tiempos se decidió establecer una política de tratamiento antimicrobiana que se expone a continuación:
PROFILAXIS
La profilaxis antimicrobiana es referida a la prevención de la infección por administración de un fármaco. Para las enfermedades infecciosas, un agente antimicrobiano se administra a un individuo en riesgo de desarrollar una infección debido a una exposición inusual o a una alteración de las defensas propias. Uno de los procesos de eficacia probada en la prevención y control de la infección nosocomial es la utilización de la profilaxis perioperatoria con antimicrobianos. Bajo este término se entiende la utilización adecuada de antimicrobianos profilácticos en aquellos pacientes que van a ser sometidos a una intervención quirúrgica, con el objetivo de reducir la incidencia de infecciones postoperatorias del sitio anatómico en el que se incluye las áreas superficiales, profundas o incluso de órganos o espacios donde se ha realizado la intervención.
De acuerdo con el grado de contaminación bacteriana, y con el riesgo posterior de infección, los procedimientos quirúrgicos se han clasificado en cuatro, a propuesta y a partir de los años sesenta del: National Research Council de Estados Unidos de Norteamérica en: 1) cirugía limpia, 2) limpia-contaminada, 3) contaminada y 4) sucia. La profilaxis antimicrobiana en la cirugía está dirigida a trata de evitar el crecimiento microbiano y contaminar la herida quirúrgica.
El fármaco utilizado debe alcanzar niveles óptimos en el líquido intersticial y en el interior de las mallas de fibrina y hematomas, si el antibiótico está presente en el suero mientras la fibrina o el hematoma están en formación, el fármaco podrá penetrar en el interior de las mismas. Este debe alcanzar niveles elevados en el suero durante el proceso quirúrgico y durante unas horas más y después del cierre de la incisión. Se debe tener presente que la sangre que se pierde durante el acto quirúrgico puede hacer descender aún más los niveles séricos del antibiótico utilizado, por tal razón el intervalo entre las dosis debe acortarse.6,7
Hay un consenso entre los cirujanos, donde se expresa, que la administración del antimicrobiano debe realizarse siempre dentro de un período de dos horas antes que se inicie el procedimiento quirúrgico, siendo lo más recomendable en el momento previo a la incisión (inducción anestésica); por la vía endovenosa, que es la de elección. Además, se ha planteado que todas las cefalosporinas deben ser administradas en infusión durante cinco minutos; los aminoglucósidos y la Clindamicina en 30 minutos, mientras que la Vancomicina y el Metronidazol deben ser infundidos más lentamente, en un período de 60 min.19,20
También se ha señalado que la dosis del antibiótico administrado deber ser elevada, superior a la dosis terapéutica, si la intervención quirúrgica es muy prolongada (superior al tiempo esperado) o hubo una pérdida considerable de sangre (más de un litro), está indicado dar una segunda dosis del mismo antibiótico, la cual debe ser administrada en un intervalo de tiempo con respecto a la primera no mayor a dos veces la vida media del fármaco.21-23
Para la mayoría de los procesos quirúrgicos, existe un acuerdo generalizado sobre los beneficios del uso de cefalosporinas de primera generación (Cefazolina). En los procesos quirúrgicos que afectan a íleon distal y colon se recomienda un antimicrobiano con actividad frente a bacterias anaerobias estrictas, incluido Bacteroides fragilis.10-14,18,19
RECOMENDACIONES
Se recomienda el uso profiláctico de antimicrobianos en los siguientes procederes quirúrgicos en la especialidad de angiología y cirugía vascular:
1. Aterosclerosis obliterante grado IV donde se realizará una amputación infracondílea.
2. Pie diabético isquémico con amputación infra o supracondílea.
3. Simpatectomía lumbar o torácica.
4. Angioplastia transpercutánea.
5. Embolectomías, tromboendarteriectomías y en las derivaciones arteriales.
6. Várices quirúrgicas con úlceras limpias.
7. Exéresis de angiodisplasias.
8. Fístulas arteriovenosas complejas.
9. Cirugía de várices con gran manipulación quirúrgica.
10. Cirugía del linfedema.
11. Injerto de piel.
Se utilizará 1,0 g de Cefazolina endovenoso 3 h antes de la cirugía y durante la cirugía si la misma es prolongada.
POLÍTICA DE TRATAMIENTO ANTIMICROBIANO MÁS FRECUENTE EN LOS DIFERENTES SERVICIOS DE ANGIOLOGÍA Y CIRUGÍA VASCULAR
Infecciones más frecuentes en el servicio de Arteriología
En este servicio las infecciones más frecuente son la sepsis de la prótesis arterial y la gangrena gaseosa (tabla 2).
Infecciones más frecuentes en el servicio de Angiopatía Diabética
La presencia de infección en los miembros inferiores de los pacientes con enfermedad vascular periférica, sobre todo si es asociada a la isquemia, es la causa más frecuente de amputación del miembro afectado en la población general, y más aún en los diabéticos con “pie diabético”, disminuyendo su calidad de vida; y de ingreso hospitalario.
El 15 % de los diabéticos van a sufrir a lo largo de su vida una infección a nivel del pie, con una incidencia anual del 1-4 %, precedida en más del 80 % de los casos de una úlcera en la pierna o el pie. Estas infecciones son complejas, en cuyo pronóstico influyen muchos factores, que dependerán de la propia úlcera (localización, extensión, cronicidad, amputación previa, grado de isquemia) y del tipo de paciente (edad, insuficiencia renal, tiempo de evolución de la diabetes, comorbilidades asociadas), lo que hay que tener en cuenta a la hora de plantear su tratamiento.
Es conocido que las infecciones son clasificadas en función de su gravedad (leve, moderado-leve, moderado-grave y grave); que su tratamiento es complejo y debe ser multidisciplinario. En el caso del pie diabético debe incluir desbridamiento, descarga, antibiótico-terapia adecuada, revascularización y cura de la úlcera.24-28
El pie diabético constituye una grave complicación de la Diabetes Mellitus. Por lo general, los pacientes acuden a la consulta varios días después de detectarse una infección para ser tratados con los antibióticos disponibles en las áreas de salud, cuando se decide su hospitalización es porque esta terapia ha fracasado e ingresan de urgencia.
El INACV ha utilizado, a lo largo del tiempo, varias combinaciones de antibióticos de forma empírica en el tratamiento de urgencia de dichos pacientes, pero desde hace aproximadamente tres años es utilizado como tratamiento inicial, la combinación Ceftriaxona-Metronidazol.
Ante un paciente con pie diabético complicado por presentar una infección sobreañadida se impone aplicar un tratamiento antibiótico inicial enérgico antes de obtener los resultados de los estudios microbiológicos, pues no es ético esperar los mismos ante la severidad de la infección, y lo anterior es una norma aceptada internacionalmente. El antibiótico que se emplee debe tener baja nefrotoxicidad y un costo aceptable.
Es aceptado que el antibiótico de elección para comenzar el tratamiento de urgencia tiene que tener un amplio y poderoso espectro, recomendándose aquellos que, independientemente de su costo, sean capaces de neutralizar de manera eficaz la infección; puesto que en el caso contrario lo más probable es que el paciente termine amputado, por tal razón es que se obvia la primera y segunda línea de antibióticos y se inicia la terapéutica con poderosos antimicrobianos de 3ra. y 4ta. generación. Lo que parece a simple vista un gasto mayor, en realidad significará un ahorro en estadía y piernas salvadas.
La sepsis asociada al pie diabético no puede ser tratada con los mismos principios en que se basa la terapéutica de otras enfermedades infecciosas ya que el paciente diabético complicado habitualmente está inmunodeprimido, con daño renal, vascular y neurológico, lo que lo hace susceptible a la sepsis grave. Por esta razón, en las normas internacionales se plantea iniciar la terapéutica con antibióticos tales como: Amoxicilina, ácido Clavulónico, Ticarcilina, Clindamicina, entre otros, según el mapa microbiológico de los diferentes lugares. Siempre que se tenga un antibiograma con cultivo que aparezca un antibiótico sensible al germen y que sea eficaz y menos costoso se pasara al empleo de este.11-15
Se conoce que estos antibióticos son de uso restringidos fundamentalmente a salas cerradas (terapias) por motivos de conservar la sensibilidad a los gérmenes habituales del medio, sin embargo, en el Instituto de Angiología y Cirugía Vascular, los pacientes que son graves en su mayoría, están en peligro de perder un miembro e incluso la vida; por estas causas se considera a la sala de angiopatia diabética como una sala de terapia.29-31
En el análisis realizado por el Comité Fármaco-Terapéutico del Instituto, se decidió que de los antibióticos disponibles, con las características antes planteadas es la Ceftriaxona el que más se asemeja a las cualidades ideales, es el más barato, el menos nefrotóxico de su grupo (no exige reajuste de dosis según las concentraciones de creatinina), cumple con un amplio espectro antimicrobiano para Gram negativos y positivos, al ser de 3ra generación y se tiene una existencia constante del mismo. Se asocia con el Metronidazol por la alta frecuencia y probabilidad de que se sumen gérmenes anaeróbicos a la variada flora microbiana que acompaña estas lesiones (tabla 3).
Cuando se disponga de suficiente Amoxicillina con Sulbaltan o Tasobaltan y Clindamicina se podría trazar una nueva política antimicrobiana en el tratamiento del paciente con pie diabético. La experiencia obtenida hasta el momento, es que en aproximadamente el 80 % de los pacientes donde se utiliza este tratamiento inicial no es necesario un segundo antibiótico.
La atención del pie diabético es un proceso bien caro para cualquier servicio donde se atienda a los diabéticos, consume gran cantidad de recursos, la batalla contra esta afección no se ganará escogiendo el antibiótico ideal, sino que hay que comenzarla desde la atención primaria, con la prevención y el control metabólico de los pacientes. Una vez que aparezca la lesión, casi la mitad de los pacientes que lo padezcan llevará algún tipo de amputación, ya en esta fase, no utilizar lo mejor con que se cuente puede ser iatrogénico.25-27
Las afecciones vasculares infectadas de las venas y los vasos linfáticos difieren en gran medida de las relacionadas con los pacientes diabéticos y de las enfermedades arteriale (tabla 4).
Hay que recordar que las tetraciclinas están contraindicadas en niños y gestantes.
Siempre que pueda utilizarse el Ciprofloxacino 250 mg por vía oral es preferible a otras vías pues se absorbe en más de un 90 %. Es útil en el tratamiento antiseudomonas.
Vancomicina siempre endovenosa. Su uso está restringido para el tratamiento del estafilococo meticillin resistente. En el Instituto se usa en la sepsis de la prótesis.
En pacientes excepcionales, que no responden a los antibióticos habituales, previo cultivo y antibiograma y muy excepcionales empíricamente se puede utilizar el Aztreonan con que ya se cuenta.28
Las misiones encomendadas están cargadas de verdaderas dificultades. Además un centro es en esencia lo que son sus facultativos y el personal que lo compone. La terapia antimicrobiana empírica en pacientes con afecciones vasculares periféricas debe ser racional y prudente.
Siempre que tengamos un antibiograma con cultivo que aparezca un antibiótico sensible al germen y que sea eficaz y menos costoso se pasará al empleo de este.
Estos antibióticos muchas veces son de uso restringidos fundamentalmente a salas cerradas (terapias) por motivos de conservar la sensibilidad a los gérmenes habituales del medio pero en nuestro caso los pacientes son graves en la mayoría de los casos, están en peligro de perder un miembro e incluso la vida, por estas causas consideramos a lsa sala de Angiopatía Diabética como salas de terapia.
En el análisis realizado por el grupo de especialistas que trata pacientes con pie diabético se decidió que de los antimicrobianos disponibles, es la Cefuroxima el que más se asemeja a las cualidades ideales, no es de los mas caro, es el menos nefrotóxico de su grupo, cumple con un amplio espectro antimicrobiano y es de fabricación nacional, debe asociarse a Clindamicina por la alta frecuencia y probabilidad de que se sumen gérmenes anaeróbicos a la variada flora microbiana que acompaña estas lesiones.
Si la evolución favorable, se pasa a la vía oral con Cefalexina, Ciprofloxacilo o Amoxicillina con Sulbaltan. Si la evolución es no favorable, entoces se debe utilizar antimicrobianos como Aztreonan, Cefepime, Piperacillina tasobaltan, Ceftriaxona más Clindamicina, Cefotaxima más Metronidazol Ceftacidima.
Se sugiere una terapia antimicrobiana racional y prudente, sobre todo cuando es utilizada de forma empírica. Su efecto es elevar la eficacia de los fármacos empleados en pacientes con afecciones infecciosas frecuentes en angiología.
REFERENCIAS BIBLIOGRÁFICAS
1. Molejón García M. Estrategias de la alianza para el uso prudente de antibióticos en cuba. MEDISAN. 2013 [citado 1 Dic 2013];17(10). Disponible en: http://bvs.sld.cu/revistas/san/vol17_10_13/san011710.pdf
2. March García JR. Secciones y grupos de trabajos de la SEACV. En Historia de la SEACV (50º aniversario: 1959-2009). Sociedad Española de Angiología y Cirugía vascular. Ed. Glosa SA. Barcelona, 2010:131-142.
3. Blanes Mompo JI, Lozano F, Clará A, Alcalá D, Doiz E, Merino R, González del Castillo J, Barberán J, Zaragoza R, García Sánchez JE. Consensus document on treatment of infections in diabetic foot. Rev Esp Quimioter 2011;24(4):233-62.
4. Sotto A, Richard JL, Combescure C, Jourdan N, Schuldiner S, Bouziges N, et al. Beneficial effects of implementing guidelines on microbiology and costs of infected diabetic foot ulcers. Diabetologia. 2010;53:2249-2255.
5. Eleftheriadou I, Tentolouris N, Argiana V, Jude E, Boulton AJ. Methicillin-resistant Staphylococcus aureus in diabetic foot infections. Drugs. 2010;70:1785-1797.
6. Appleman MD, Citron DM. Efficacy of vancomicin and daptomycin against Staphylococcus aureus isolates collected over 29 years. Diagn Microbiol Infect Dis. 2010;66:441-444.
7. Shakil S, Khan AU. Infected foot ulcers in male and female diabetic patients: a clinico-bioinformative study. Ann Clin Microbiol Antimicrob. 2010;9:2.
8. Chakraborti C, Le C, Yanofsky A. Sensitivity of superficial cultures in lower extremity wounds. J Hosp Med 2010;5:415-420.
9. Joseph WS, Lipsky BA. Medical therapy of diabetic foot infections. J Vasc Surg. 2010;52(3 Suppl):67-71.
10. Pola BF, Patricio NM, Pohlenz A, Otaíza O. Costo de las infecciones intra-hospitalarias en hospitales chilenos de alta y mediana complejidad. Rev Chilena Infect. 2003;20(4):285-90.
11. Fisher TK, Wolcott R, Wolk DM, Bharara M, Kimbriel HR, Armstrong DG. Diabetic foot infections: A need for innovative assessments. Int J Low Extrem Wounds 2010;9:31-36.
12. Richard JL, Sotto A, Lavigne JP. New insights in diabetic foot infection. World J Diabetes 2011;2:24-32.
13. Garza Velasco R, Zúñiga Rangel O, Perea Mejía LM. La importancia clínica actual de staphylococcus aureus en el ambiente intra-hospitalario. Educ Quím. 2013 [citado 1 dic 2013];24(1):8-13. disponible en: http://www.educacionquimica.info/search_volume.php?id_revista=120
14. Dinh T, Snyder G, Veves A. Current techniques to detect foot infection in the diabetic patient. Int J Low Extrem Wounds 2010;9:24-30.
15. Puchades Gimeno F, Valero Domenech A, Zaragoza Crespo R. Biomarcadores en sepsis. En M Borges, R. Ferrer, R. Zaragoza Libro blanco 2010 Actualizaciones en sepsis en el paciente crítico. Vol 1. Ed. Edikamed. Barcelona 2011. p. 21-35.
16. Dellit TH, Owens RC, Mc Gowan JE, Gerding DN, Weinstein RA, Burke JP, et al. Infectious diseases Society of America and the Society for Health-care Epidemiology of America Guidelines for developing an institutional program to enhance antimicrobial stewardship. Clin Infect Dis. 2007;44:159-77.
17. Bouadma L, Luyt CE, Tubach F, Cracco C, Alvarez A, Schwebel C, et al; PRORATA trial group. Use of procalcitonin to reduce patients' exposure to antibiotics in intensive care units (PRORATA trial): a multicentre randomised controlled trial. Lancet 2010;375:463-74.
18. NICE Guideline, 2010. Diabetic foot problems: inpatient management of diabetic foot problems. [citado 27 Dic 2013]. Disponible en: http://www.nice.org.uk/guidance/index.jspaction=folder (Septiembre 2010).
19. Dellinger EP, Gross PA, Barret TL, Krause PJ, Martone WJ, Mc Gowan JE, et al. Quality standard for antimicrobial prophylaxis in surgical procedures. Clin Infect Dis. 1994;18(3):422-7.
20. Cisneros JM. Poor antimicrobial training of clinicians in Spain. Enferm Infect Microbiol Clin. 2013 [citado 1 Dic 2013];31:197–203. Disponible en: http://www.ecdc.europa.eu
21. Rincón S, Panesso D, Díaz l, Carvajal LP, Reyes J, Munita JM, Arias CA. Resistencia a antibióticos de última línea en cocos Gram positivos: la era posterior a la Vancomicina. Biomédica. 2014 [citado 1 Dic 2013];34(Supl 1):191-208. Disponible en: http://dx.doi.org/10.7705/biomedica.v34i0.2210
22. Cainzos M, Lozano F, Dávila D. Asociación española de cirujanos. Protocolos recomendables de profilaxis antibiótica. Rev Cir Esp. 1996;59(1):3-6.
23. Rodríguez-Baño J, Pardo Pardo JR, Álvarez Rocha L, Asensio A, Calbo E, Cerce-Nado E, et al. Programas de optimización de uso de antimicrobianos (PROA) en hospitales españoles: documento de consenso GEIH-SEIMC, SEFH y SEMPSPH. Enferm Infecc Microbiol Clin. 2012;30(22):1-23.
24. Mensa J, Cratel JM, Jiménez de Aqnta MT, Prats G, Domínguez-Gil A. Guía de terapia antimicrobiana. Duodécima edición. Barcelona: Edición Mason; 2002.
25. Cisneros JM, Pérez-Moreno A, Gil-Navarro MV. Política de antibióticos. Comisión de infecciones y uso de antimicrobianos. Enferm Infecc Microbiol Clin. 2014 [citado 9 Ene 2015];32(8):533–6. Disponible en: http://www.seimc.org/contenidos/documentoscientificos/eimc/seimc_eimc_v32n08p533a536.pdf
26. González Alemán M. Resistencia antimicrobiana, una amenaza mundial. Rev Cubana Pediatr. 2013 [citado 1 Dic 2014];85(4):414-7. Disponible en: http://scielo.sld.cu/pdf/ped/v85n4/ped01413.pdf
27. Quirós Enríquez M, Fernández Ruíz DR, Barrios Romero B, Milián Vázquez PM, Cisneros Napóles Y, Noa Justafé L. Las oxazolidinonas como alternativa en el tratamiento del staphylococcus aureus multi-resistente. MEDISUR. 2013 [citado 27 Dic 2013];11(2):159-66. Disponible en: http://medisur.sld.cu/index.php/medisur/article/view/2115
28. Cantona B, Ruíz-Garbajosa P. Formación médica continuada: Infección nosocomial. fundamentos y actuación clínica. Infecciones causadas por bacterias Gram positivas multi-resistentes (staphylococcus aureus y enterococcus spp). Enferm Infecc Microbiol Clin. 2013;31(8):543-51.
29. Traunmüller F, Schintler MV, Metzler J, Spendel S, Mauric O, Popovic M, et al. Soft tissue and bone penetration abilities of daptomycin in diabetic patients with bacterial foot infections. J Antimicrob Chemother. 2010;65:1252-7.
30. Matsumoto K, Takeshita A, Ikawa K, Shigemi A, Yaji K, Shimodozono Y, et al. Higher Linezolid exposure and higher frequency of thrombocytopenia in patients with renal dysfunction. Int J Antimicrob Agents. 2010;36:179-81.
31. Rogers LC, Andros G, Caporusso J, Harkless LB, Mills JL, Armstrong DG. Toe and flow: Essential components and structure of the amputation prevention team. J Vasc Surg. 2010;52:23s-27s.
Recibido: 30 de diciembre de 2014.
Aprobado: 27 de febrero de 2015.
Andrés Samuel Fleitas Estévez. Instituto Nacional de Angiología y Cirugía Vascular. Calzada del Cerro 1551, esquina Domínguez. La Habana. Cuba.
Dirección electrónica: bionuel@infomed.sld.cu