Introducción
La enfermedad arterial periférica afecta en el mundo a alrededor de 200 millones de personas y se considera la mayor causa de hospitalización, con riesgo de amputación de la extremidad afectada y muerte debido a la enfermedad per se o sus complicaciones. El tratamiento mínimamente invasivo por técnica endovascular se ha convertido en el patrón de oro para mitigar la enfermedad arterial periférica. Dado el éxito clínico y el bajo riesgo de complicaciones, se tiene actualmente como la mejor opción de tratamiento para evitar la amputación.1,2,3
Posterior al proceder de revascularización periférica es preciso determinar la repercusión inminente del tratamiento en la circulación periférica, para evaluar la necesidad de tratar de inmediato territorios vasculares contiguos, evaluar la repercusión del proceder en la perfusión tisular local y determinar el pronóstico de la extremidad afectada.
Se reporta la experiencia relativa al tratamiento de un paciente con macroangiopatía diabética, que provoca isquemia crítica de miembros inferiores dada por estenosis del 64 % de la arteria ilíaca común izquierda y estenosis variable de los segmentos fémoro-poplíteos bilaterales. Se decidió realizar colocación de stent para revascularización de la arteria ilíaca izquierda y evaluación del proceder, a través de perfusión bidimensional en angiografía por sustracción digital (2D-ASD).
A partir de estas observaciones, el objetivo general de este artículo fue describir la utilidad del estudio de 2D-ASD y su valor como herramienta para determinar el transproceder y la repercusión en el flujo sanguíneo de la revascularización realizada, y establecer un pronóstico funcional para el paciente.
Presentación del caso clínico
Paciente masculino de 45 años, fumador por 20 años, con diagnóstico de hipertensión arterial, diabetes mellitus y macroangiopatía diabética. Llevó tratamiento con inhibidor de la enzima convertidora de angiotensina e insulina, y doble esquema de antiagregación plaquetaria.
Comenzó a presentar claudicación intermitente de la marcha a 150 m, asociada a dolor hasta el nivel de las pantorrillas, lo que se fue agravando en un período de 3 meses, y cianosis en cuarto y quinto artejos del miembro inferior izquierdo. El índice tobillo-brazo reportó un valor de 0,6, sugestivo de enfermedad arterial moderada. Se realizó estudio de AngioTAC y se observaron lesiones ateroscleróticas en la pared de ambas arterias ilíacas comunes, con mayor afectación de la arteria ilíaca común izquierda (fig. 1 A y B).
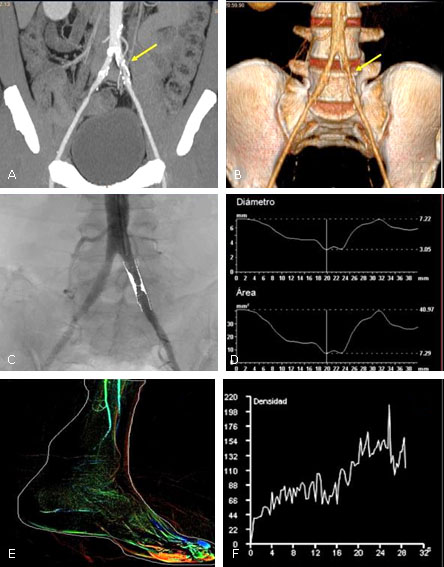
Fig. 1 -Angiotomografía computarizada con imagen de máxima intensidad de proyección (A) y reconstrucción 3D (B). Se observaron lesiones ateroscleróticas en la pared de ambas arterias ilíacas comunes, con mayor afectación de la arteria ilíaca común izquierda (flechas amarillas). Análisis del segmento estenosado, en imagen obtenida en ASD (C y D) y estudio de perfusión tisular bidimensional por ASD del pie izquierdo (E) y gráfica de densidad en función del tiempo midiendo el tiempo de llegada del flujo sanguíneo previo a la colocación del stent balón expandible (F).
Clasificación clínica e imagenológica del paciente
Clínicamente: Clasificación de Fontaine III and Rutherford 4 (dolor en reposo).
En estudio de AngioTac: Lesiones tipo TASC II-B.
Estenosis múltiples, cada una menor o igual que 5 cm de longitud, una extensión total menor o igual que 10, o una oclusión única menor o igual que 3 cm de longitud, en la arteria tibial con oclusión o estenosis, o gravedad similar o peor en las otras arterias tibiales.
Se decidió realizar proceder endovascular de revascularización en arteria ilíaca izquierda, dividido en dos fases secuenciales.
Fase 1
Previa administración de anestesia en región medial del 1/3 medio proximal del miembro superior izquierdo, se hizo punción de la arteria braquial, con técnica de Seldinger modificada. Se posicionó introductor arterial 6 Fr. Posteriormente, y a través de guía de Terumo 0,0035¨, se avanzó catéter angiográfico Pigtail 5 Fr de Merit Medical, que se posicionó a nivel de la bifurcación aórtica, para llevar a cabo ASD de ambas arterias ilíacas y sus ramas. Luego, se procedió con arteriografía selectiva de la arteria ilíaca izquierda con catéter angiográfico recto multiperforado 5 Fr de Cook Trade Mark. El segmento estenosado tenía una longitud de 35 mm, con diámetro medio de 5,52 mm; un mínimo de 3,05 mm; y un máximo de 7,14 mm, para una estenosis del 64 % del vaso, lo que evidenció el llenado tardío de las arterias tibial anterior y posterior. En este estudio no se definieron el arco plantar ni la arteria peronea (fig. 1 C y D).
Se culminó la fase diagnóstica con el estudio de perfusión tisular bidimensional y se procedió a la inyección del contraste en origen de la arteria ilíaca izquierda (30 ml Iopamidol 370, Unique Pharmaceutical) a un rango de 3 mL/seg para un volumen total de 30 ml, con presión de 600 PSI y programación de 3 imágenes/seg, con bomba inyectora automática Mark 7 Arterion. Las curvas de densidad vs. tiempo fueron calculadas automáticamente, a partir de las imágenes de la ASD con codificación de color paramétrica, que permitió la extracción de datos posprocedimiento (fig. 1 E y F).
Fase 2
Se procedió mediante la técnica de Road Mapping a la inyección de contraste en origen de la arteria ilíaca izquierda. Posteriormente, sobre guía Terumo se posicionó stent periférico (LVD Biotech SL iVascular), con aleación de cromo-cobalto (denominada L605) y dimensiones de 7 x 38 mm, premontado sobre catéter balón de 80 cm. Una vez posicionado en el segmento estenótico, ubicado en el 1/3 proximal de la arteria ilíaca común izquierda, se pasó al inflado del balón a una presión nominal de 10 atm (1013 kPa), para lograr la expansión total del stent y la corrección automática del calibre del vaso tratado. Se observó un diámetro máximo de 7,33 mm y mínimo de 6,47 mm. Se comprobó la repermeabilización lograda mediante angiografía de control inmediata (fig. 2 A, B, c y D). Se culminó la fase terapéutica con el estudio de 2D-ASD (fig. 3), con iguales requerimientos técnicos que en la fase diagnóstica (fig. 2 C y D). Se retiró el instrumental endovascular y se hizo compresión manual en el sitio de punción arterial durante 10 minutos y luego vendaje compresivo por 24 horas.
Pasado este tiempo se retiró vendaje compresivo, sin complicaciones relativas al sitio de punción arterial. Al paciente se le dio alta hospitalaria al referir disminución del adormecimiento de ambas piernas.
Dosis Kerma en aire acumulada: Frontal 508,14 mGy, Lateral 0,00 mGy
Producto dosis área (PDA) acumulada: 190 Gycm2
Tiempo de fluoroscopia: 11:43 (minutos: segundos)
Duración total del procedimiento: 1h 20min
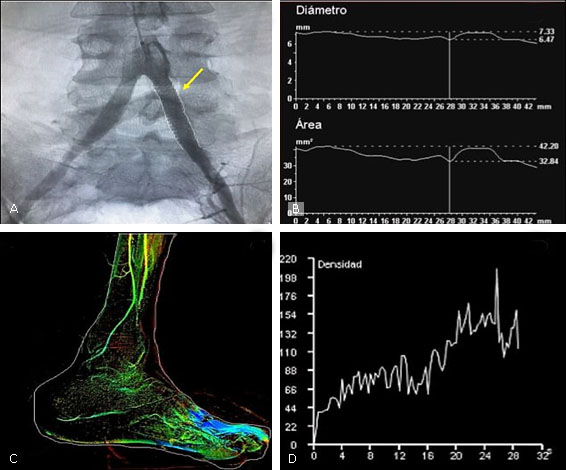
Fig. 2 - Análisis de la arteria ilíaca izquierda posterior a la liberación del stent balón expandible (flecha amarilla) en imagen obtenida en ASD (A y B) y estudio de 2D-ASD del pie izquierdo (C). Gráfica de densidad en función del tiempo midiendo el tiempo de llegada del flujo sanguíneo posterior a la colocación del stent (D).

Fig. 3 -Perfusión por angiografía 2D comparando el índice de absorción pre y poscolocación del stent, al término de los 28,9 y 24,4 segundos; se marcó elipsoide en el área de interés al nivel del tobillo y arco plantar (círculo blanco posterior al stent y morado previo al stent). La densidad del contraste en el área mencionada, pre y pos stent se representa en la curva de tiempo vs. intensidad de contraste, lo que marca un aumento del índice de absorción de forma inmediata.
Discusión
La enfermedad oclusiva arterial periférica se diagnostica por: el examen físico, la mensuración obtenida a través de estudios funcionales y los estudios de imagen. Los estudios funcionales consisten en la determinación del índice tobillo-braquial (ABI < 0,9), la presión del tobillo (≤ 50-70 mmHg), la presión del pie (≤ 50 mmHg) y la presión de oxígeno transcutánea (≤ 30 mmHg).4 La ASD se considera el gold standard para visualizar la lesión arterial, pues, al observar la propagación del medio de contraste yodado durante la adquisición de la imagen, el intervencionista obtiene una medida cualitativa del flujo sanguíneo y subjetiva de la velocidad de la sangre que pasa a través de la vasculatura. Otros métodos de imagen disponibles son el ultrasonido Doppler, la Angiorresonancia y la Angiotomografía con valor puramente diagnóstico.4,5
El objetivo del proceder de revascularización es la recanalización del vaso afectado, lo que incrementa la llegada de flujo sanguíneo a los tejidos y mejora la perfusión tisular. Para este fin se emplea desde la angioplastia con balón hasta la liberación de endoprótesis vasculares (stent) autoexpandibles recubiertos o no, y los stent balón expandibles. Este último fue elegido para el tratamiento debido a que resulta muy preciso y poco flexible.
Se ha descrito que el punto final más importante de la revascularización es el blush tisular en las imágenes de ASD. Este factor lo juzga el intervencionista, al representar un predictor cualitativo del resultado clínico. Como norma general, el éxito del proceder se define al lograr una estenosis residual menor que 30 % de la evaluación inicial y la identificación de flujo posrevascularización a nivel de las arterias infrapoplíteas hasta los territorios más distales a nivel del arco plantar.5,6,7
En este paciente en cuestión se logró una estenosis residual de 11,7 %. Sin embargo, en la ASD de control se observó una diferencia en la llegada del flujo a los territorios más distales de 4 segundos con respecto al estudio previo.
Uno de los problemas que enfrenta la realización de este tipo de proceder resulta saber in situ qué nivel de revascularización se ha logrado y su repercusión en la perfusión tisular. Para este fin se han descrito métodos como la obtención de la imagen de fluorescencia luego de la administración de Indocianina y el mapeo de la saturación tisular de oxígeno a nivel del pie. Estos han demostrado ser confiables, pero tienen la dificultad de no poderse implementar con facilidad en el salón de intervencionismo. Sin embargo, la perfusión tisular 2D por ASD podría establecerse como una herramienta objetiva para este fin, al disminuir el sesgo interobservador.7,8
Al realizar la ASD 2D, se halló un patrón en la imagen codificada en el mapa de colores muy similar al obtenido en la ASD de control. Pero, al establecer una comparación en el área de interés (tobillo y pie) por el método de Reekers,6,7,8 se obtuvo una curva de densidad en función del tiempo, que mostraba un cambio favorable en cuanto a la perfusión tisular pre- y posrevascularización.
El patrón que describe la curva de tiempo vs. intensidad de contraste, dado por un aumento notable en el índice de absorción, muestra un efecto de reversión en la perfusión del tejido, lo que traduce una mejora en el flujo sanguíneo con efecto directo en los requerimientos metabólicos regionales del área de interés marcada. Sin embargo, el patrón que describe la curva no es uniforme, por lo que no establece una relación directa entre la velocidad de realce pre- y posproceder.
La mejora en el flujo sanguíneo, dada por la diferencia en las curvas de índice de absorción pre- y posproceder, evidencia que la restauración del flujo sanguíneo distal y su repercusión en la perfusión tisular, fue dada por la mejora del flujo sanguíneo en los vasos de circulación colateral, porque las lesiones vasculares en el resto del eje afectaron directamente la distribución del flujo de forma uniforme en la extremidad comprometida.9
Los resultados a corto plazo han mostrado mayor preferencia por el tratamiento endovascular, debido a la baja morbilidad a los 30 días del posproceder, la poca tasa de reintervención a los 12 meses, y la disminución de los costos directos relacionados con la hospitalización, porque las estancias hospitalarias son breves, las tasas de complicaciones menores y no requieren estancia posoperatoria en unidades de cuidados intensivos. Las tasas de mejoría clínica se reportan entre 83 % y 100 %, la mortalidad menor de 7 % y las tasas de complicaciones con incidencia variable de 3 % y 45 % con amplias probabilidades de re-solución por la misma vía.10
Conclusiones
La elección del tratamiento de revascularización idóneo debe particularizarse en cada paciente. La utilización de un método de evaluación del éxito técnico y la repercusión funcional inmediata deben estandarizarse en el abordaje terapéutico de las oclusiones vasculares, al ser la perfusión bidimensional por ASD, como estudio cualitativo transproceder, superior a los restantes métodos actualmente disponibles.














