Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Médica Electrónica
versión On-line ISSN 1684-1824
Rev. Med. Electrón. v.32 n.4 Matanzas jul.-ago. 2010
HOSPITAL PROVINCIAL PEDIÁTRICO DOCENTE ELISEO NOEL CAAMAÑO. MATANZAS
Enfermedad de Kawasaki. Aspectos a considerar
Kawasaki disease. Aspects to take into consideration
AUTORES
Dr. Lázaro Arturo Vidal Tallet (1)
E-mail: avidata.mtz@infomed.sld.cu
Dr. Amaury Noda Albelo (2)
Dra. Andrea X. Casal Menedez (3)
Dra. Caridad A. Sánchez Hernández (4)
Dr. Oscar A. Montell Hernández (5)
Est. Idianne Linares Álvarez (6)
1) Especialista de II Grado en Pediatría. Máster en Ciencia de la Educación Superior e Infectología. Profesor Consultante. Hospital Provincial Pediátrico Docente Eliseo Noel Camaaño. Matanzas.
2) Especialista de I Grado en Inmunología. Máster en Enfermedades Infecciosas y Tropicales, y en Atención Integral al Niño. Profesor Instructor. Hospital Provincial Pediátrico Docente Eliseo Noel Camaaño. Matanzas.
3) Especialista de II Grado en Microbiología. Máster en Infectología. Profesor Asistente. Hospital Provincial Pediátrico Docente Eliseo Noel Camaaño. Matanzas.
4) Especialista de I Grado en Pediatría. Máster en Infectología. Profesor Asistente. Hospital Provincial Pediátrico Docente Eliseo Noel Camaaño. Matanzas.
5) Especialista de I Grado en Pediatría. Especialista de II Grado en Nefrología. Máster en Atención Integral al Niño. Profesor Instructor. Hospital Provincial Pediátrico Docente Eliseo Noel Camaaño. Matanzas.
6) Estudiante de 6to año de la carrera de Medicina. Hospital Provincial Pediátrico Docente Eliseo Noel Camaaño. Matanzas.
RESUMEN
La enfermedad de Kawasaki ha sido objeto de interés por epidemiólogos, clínicos e investigadores, desde su primera descripción en 1967. Su causa no se ha podido identificar, aunque las principales hipótesis apuntan a una etiología infecciosa. Desde el punto de vista patogénico, la incapacidad de recuperar un agente infeccioso en forma consistente y las evidencias anatomopatológicas y de laboratorio de una activación de la inmunidad celular y humoral, tienden a situar la enfermedad de Kawasaki en la categoría de una enfermedad autoinmune. Uno de los principales problemas actuales es la demora en el diagnóstico, que se correlaciona con un peor pronóstico en cuanto a las principales secuelas de la enfermedad, entre las que destaca el compromiso de los vasos coronarios. En este trabajo se realiza una revisión de la enfermedad y se muestra la importancia del diagnóstico y tratamiento precoz, así como se señalan apuntes del comportamiento de esta afección en el Hospital Provincial Pediátrico Docente Eliseo Noel Caamaño, de Matanzas, en el período de 2001 al 2010.
DeCS
SÍNDROME MUCOCUTÁNEO LINFONODULAR/diagnóstico
SÍNDROME MUCOCUTÁNEO LINFONODULAR/epidemiología
SÍNDROME MUCOCUTÁNEO LINFONODULAR/complicaciones
SÍNDROME MUCOCUTÁNEO LINFONODULAR/quimioterapia
ENFERMEDADES CARDIOVASCULARES/diagnóstico
ENFERMEDADES CARDIOVASCULARES/etiología
PRONÓSTICO
HUMANOS
NIÑO
ESTUDIOS
EPIDEMIOLOGÍA DESCRIPTIVA
INTRODUCCIÓN
La enfermedad de Kawasaki (EK) ha sido objeto de observación por investigadores desde que fue descrita por primera vez por el Dr. Tomisaku Kawasaki jefe del departamento de pediatría del Centro Médico de la Cruz Roja de Tokio, en 1967, como el síndrome ganglionar muco cutáneo febril agudo, la cual fue considerada como una enfermedad benigna, de etiología desconocida, autolimitada y sin secuelas. Años más tarde, se denominó síndrome muco cutáneo ocular (1). En la actualidad, es considerada como un síndrome multisistémico vascular agudo de etiología desconocida (2).
Esta afección ha sido descrita en todos los continentes y en niños de todas las razas, siendo considerada como la primera causa de enfermedad cardiovascular adquirida en los países desarrollados, desplazando así al reumatismo articular agudo (2). En 1978, se publican los primeros criterios de la EK por parte del Centro de Control y Prevención de las enfermedades (CDC), modificando los propuestos por el Dr. Kawasaki, y diez años más tarde, se aprueba el uso de la inmunoglobulina intravenosa (IGIV) por parte de la Academia Americana de Pediatría, además se aprueba la utilización conjunta del ácido acetilsalicílico (AAS) como parte del tratamiento definitivo. Los criterios decisivos para el diagnóstico, así como las guías terapéuticas de la enfermedad de Kawasaki fueron dictados en 1993 por la Asociación Americana del Corazón (AHA), y son la base del diagnóstico, a falta de otras pruebas que puedan orientarnos a esta patología. Los criterios diagnósticos determinados por la AHA, se establecieron para la detección temprana de la EK, con el fin de poder aplicar el tratamiento adecuado y así disminuir sus complicaciones, principalmente la patología cardiaca, ya que se menciona que en los países en desarrollo, la EK ha sustituido a la fiebre reumática aguda como la causa más frecuente de cardiopatía adquirida en los niños (11).
Un importante elemento a tener en consideración es su presentación atípica, lo que dificulta el diagnóstico y pone en riesgo la vida de los pacientes, motivo por el cual se realiza esta revisión y se expone nuestra experiencia.
Epidemiología
La EK ocurre mayoritariamente en niños menores de 5 años (80 %) con un pico a los 2 años. La incidencia anual varía desde 60 a 90 casos/100 000 niños en Japón y 10 casos/100 000 niños en Europa y Estados Unidos (3,4). Es más común entre los varones que en las hembras, con una relación de 1.5:1, el pico de mayor incidencia parece corresponderse con los 18 meses, y el 80 % de los casos reportados son observados por debajo de los 5 años de edad, sin tener en consideración las formas atípicas que en ocasiones pasan inadvertidas, situación que aumentaría su incidencia.
La mortalidad en Japón ha sido estimada alrededor de 0,08 % (5), mientras que en otros países, como Estados Unidos, el promedio de mortalidad es de 0,17 % (6), considerándose que la causa principal es debido a la afectación cardiovascular (6,7), y se ha observado que su mayor incidencia ocurre durante el invierno y al iniciar la primavera (8).
Etiopatogenia
La causa de la afección sigue siendo desconocida, pero los elementos clínicos epidemiológicos apuntan a una etiología infecciosa. Se ha involucrado agentes tales como virus de Epstein Barr (9), parvovirus B19 (10), adenovirus (11), herpes virus (12), virus de la inmunodeficiencia (13), parainfluenza (14), rotavirus (15) y varicela zóster (16), entre otros. Asimismo, infecciones bacterianas tales como estafilococos aureus, estreptococos (17), micoplasma pneumoniae (18) y clamidia pneumoneae (19). Los superantígenos han sido implicados en la patogenia de esta afección, dada la capacidad de activar un gran numero de linfocitos y células presentadoras de antígenos, lo cual desencadena una desproporcionada y no específica respuesta inmune (20,21). Los superantígenos, hasta hace pocos años sólo una curiosidad en biología molecular, son péptidos que activan la respuesta inmune de forma más extensa que los antígenos nominales, lo cual conduce a un verdadero desastre en los mecanismos de regulación de la respuesta, incluso puede llevar a la muerte del paciente.
Manifestaciones clínicas
El diagnóstico clásico de esta afección se basa en la presencia de fiebre, de al menos de 5 días de evolución, y cuatro o más de los elementos que aparecen en la tabla no. 1, aunque el diagnóstico puede realizarse antes del 5to día, si el paciente tiene el resto de los criterios diagnósticos. En los casos típicos, las manifestaciones clínicas descritas como básicas están presentes entre el 80 y el 90 % de los casos, excepto la adenopatía cervical, que es observada entre el 50 y 75 % de los pacientes. El curso clínico ha sido dividido en tres fases: aguda febril, la cual se puede prolongar hasta cuatro semanas; la fase subaguda, que generalmente se prolonga hasta cuatro semanas; y la fase de convalecencia, que dura de 6 a 8 semanas.
Ha sido descrito la forma atípica de la EK, conocido como forma incomplete, el cual fue reportado en la literatura en 1980 (22), en pacientes que sin reunir el cuadro descrito presentaron alteraciones de las coronarias como las que se describen en EK, observándose con más frecuencia las alteraciones coronarias en estos pacientes (24).
Aunque se describen las alteraciones oculares en el curso de la EK (tabla No. 1), es poco frecuente que se asocie a compromiso del segmento posterior del ojo, aunque se ha descrito manifestaciones de neuritis óptica (25).
El diagnóstico diferencial de la EK incluye las enfermedades virales exantemáticas agudas, las infecciones por estreptococos y estafilococos y con reacciones de hipersensibilidad a drogas (24).
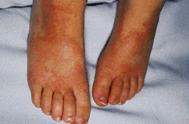

Figuras 1 y 2 (27)
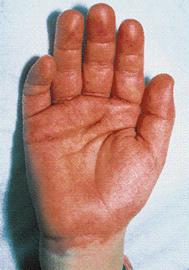 Figura 3 (27)
Figura 3 (27) 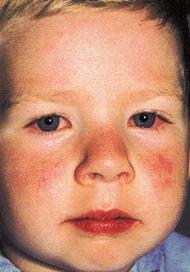 Figura 4 (27)
Figura 4 (27)
En el estudio realizado Hospital Provincial Pediátrico Docente Eliseo Noel Caamaño, de Matanzas, en los años comprendidos desde 2001 hasta el 2010. En dicho período se detectaron 10 casos, representadas las manifestaciones clínicas (gráfico 1) en el comportamiento de laboratorio (gráfico 2), la evolución fue satisfactoria en el 90 % de los pacientes (gráfico 3). Con relación a la edad, el mayor por ciento se ubicó por encima de los 4 años, a diferencia de lo que cita la literatura (3,6,11). (Gráfico 4)
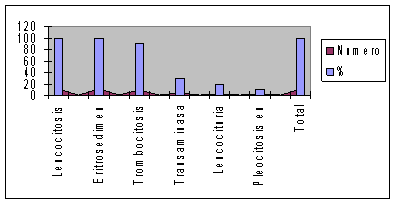
Gráfico 1
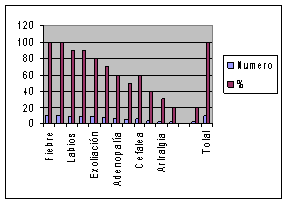
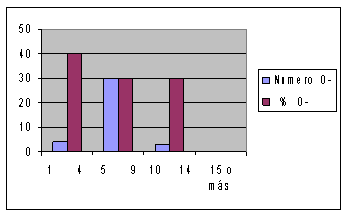
Gráfico 3
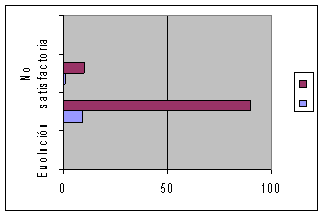
Gráfico 4
Resultó llamativa la no detección de EK atípica. Con relación a la evolución, el paciente que presentó trombocitopenia se asoció a anormalidad de la arteria coronaria, coincidiendo con el que tuvo una evolución no satisfactoria.
Tabla No. 1. Cuadro clínico y de laboratorio de la EK (27)
| Epidemiologic case definition (classic clinical criteria) [*] |
| Fiebre persistente de al menos 5 días [] |
| Presencia de al menos 4 de los siguientes signos: |
| -Cambios en las extremidades: |
| Eritema agudo de palmas y plantas; edema de manos y pies |
| Pérdida de la piel periungueal de los dedos entre la 2 y 3 semanas |
| Exantema polimorfo |
| Conjuntivitis bilateral, con o sin exudado |
| Cambios en los labios y cavidad bucal: eritema labios agrietados, lengua aframbuesada, inyección difusa oral y faringe |
| Linfoadenopatia cervical (> 1.5 cm diámetro), usulamente unilateral |
| Exclusión de otras enfermedades con singular hallazgos [] |
| Otros hallazgos clínicos y de laboratorio |
| De tipo cardiovascular |
| Insuficiencia cardiaca, miocarditis, pericarditis, regurgitación valvular |
| Anormalidades de la arteria coronaria |
| Aneurismas de arterias de mediano caliber no coronarias |
| Fenómeno de Raynaud |
| Gangrena periférica |
| Sistema músculo esquelético |
| Artritis, artralgia |
| Tractus gastrointestinal |
| Diarrea, vómitos, dolor abdominal |
| Disfunción hepática |
| Sistema nervioso central |
| Gran irritabilidad |
| Meningitis aséptica |
| Pérdida de la audición sensoneural |
| Sistema genitourinario |
| Uretritis/meatitis |
Otros hallazgos |
| Eritema, e induración en el sitio de inoculación del BCG |
| Uveítis anterior |
| Rash descamativo en ingle |
Tabla No. 2. Hallazgos de laboratorio de la EK (27)
| Leucocitosis con neutrofilia y células inmaduras |
| Eritrosedimentación acelerada |
| Proteina C reactiva elevada |
| Anemia |
| Niveles anormales de los lípidos en plasma |
| Hipoalbuminemia |
| Hiponatremia |
| Trombocitosis después de la primera semana [§] |
| Piuria esteril |
| Transaminasas elevadas |
| Gammaglutamil transpeptidasa elevada |
| Pleocitosis del liquido cefalorraquídeo |
Leyenda de las tablas Nos. 1 y 2:
* Pacientes con fiebre de al menos 5 días y más de cuatro criterios principales pueden ser diagnostico como EK, o cuando se detectan anormalidades de las arterias coronarias por 2DE o angiografía.
En la presencia de cuatro criterios principales, el diagnóstico puede ser hecho sobre el día 4 de la enfermedad.
Ver diagnóstico diferenciales.
§ Algunos niños se presentan con trombocitopenia y coagulación intravascular diseminada.
Evaluación ante la sospecha de EK incompleta (1)
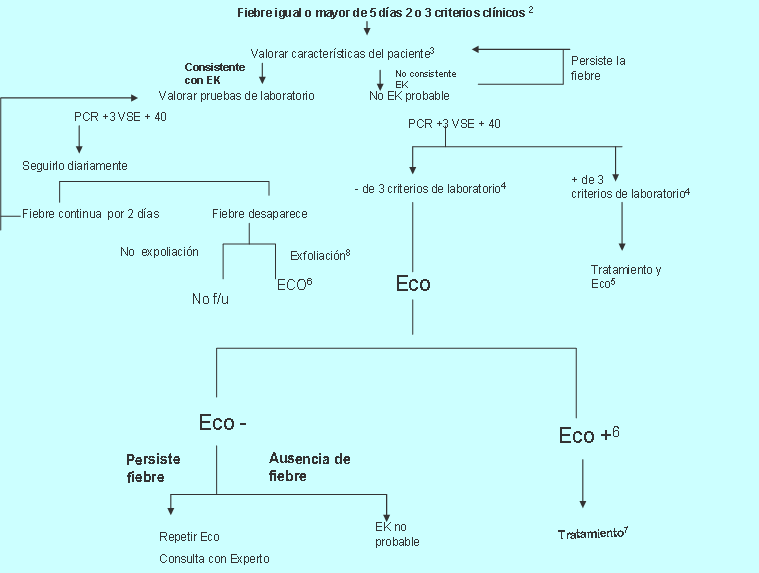
Gráfico 5. Evaluación de sospecha de EK incompleto (1) en ausencia de la regla de oro para el diagnóstico de EK. Este algoritmo puede servir de ayuda para realizar el diagnóstico (2). Niño menor de 6 meses igual o más 7 de fiebre sin explicación por pruebas de laboratorio, pero hay evidencia de inflamación en ecocardiograma, aunque no haya criterios clínicos (3). Pacientes con características que sugiere EK enumerados en la tabla No. 1: conjuntivitis exudativa faringitis, discretas lesiones en mucosa oral, rash buloso o vesicular, o generalizada adenopatías. Considerar otra alternativa de diagnóstico (4). Los criterios suplementarios de laboratorio incluye albúmina =3.0 g/dL, anemia para la edad, elevación de alanine aminotransferasa, plaquetas después de los 7 días =450,000/mm3, conteo de leucocitos en sangre =15,000/mm3, y en orina =10/campo (5). Puede ser tratado antes de realizar ecocardiograma. El ecocardiograma es considerado positivo (6) para el propósito de este algoritmo, si algunas de las tres condiciones son encontradas: t: z score de LAD o RCA =2.5 (coronaria arteries meet Japanese Ministry of Health), criteriopara aneurisma o =3 de los siguientes cuados existen, donde son incluidos: perivascular brightness, disminución de la función ventricular izquierda (LV), regurgitación mitral, efusión pericárdica, o z scores in LAD or RCA de 2–2.5 (7). Si el eco es positivo se debe iniciar tratamiento dentro de los 10 días de iniciada la afección con signos clínicos y de laboratorio (PCR y VSR) de actividad inflamatoria (8). Típica exfoliación debajo de las uñas de dedos de manos (27).
Tratamiento
El tratamiento de la EK tiene como base el uso de inmunoglobulina humana por vía endovenosa (IGHEV) y antiagregantes plaquetarios (aspirina a altas dosis).
Una vez iniciado el tratamiento, ocurre una rápida desfervesencia y resolución de los signos clínicos de la enfermedad en el 85-90 % de los pacientes. Para obtener estos resultados se recomienda iniciar tratamiento en los 10 primeros días de iniciada la afección.
La administración de la IGHEV tiene evidencia que reduce la afectación de las anormalidades coronarias observadas en esta afección. La dosis habitual es de 1 a 2 gramos x kg de peso, en una simple infusión, asociado al uso de aspirina a la dosis de 100m x kg de peso. Se ha descrito de que a pesar de el uso precoz de la IGHEV (en los primeros 10 días), alrededor del 5 % de los pacientes desarrollan una transitoria dilatación de las coronarias, y que el 1 % desarrollan aneurisma gigantes (24,26,27).
Cuando no se obtiene respuesta a la IGHEV, se recomienda el uso de mtilprednisolona a la dosis de 30 mg x kg x día (dosis máxima 1 gramo por dosis) durante tres días; otras alternativas de tratamiento no han sido evidenciadas su total efectividad (infliximab, ciclofosfamida, methotrexate y plasmaféresis).
La aspirina
Debe ser administrada a la dosis de 100 mg x kg x día, dividida en cuatro dosis por vía oral, hasta tres día después que desaparezca la fiebre, aunque hay autores que recomiendan mantenerla por 14 días.
Posteriormente, se continúa con la dosis de mantenimiento (antiagregante plaquetaria) a razón de 3-5 mg x kg x día, durante 6 a 8 semanas. Cuando se desarrollan anomalías coronarias se debe mantener por tiempo indefinido.
Otras opciones terapéuticas con el objetivo de evitar fenómenos trombóticos se resumen en el siguiente cuadro. (Tabla No. 3)
Tabla No. 3. Variantes terapéuticas para evitar fenómenos trombóticos.
| Medicamento | Vía | Dosis |
| Aspirina | Oral | 3–5 mg/kg por día |
| Clopidogrel | Oral | 1 mg/kg por día |
| Dipridamol | Oral | 2–6 mg/kg por d ay in 3 dosis |
| Abcimab | EV | Bolus de 0.25 mg x kg |
|
|
| Infusión 0,125 microgramo por minutos, por 12 horas |
| Streptokinase | Intravenousa | Bolus: 1000–4000 U/kg over 30 min |
| Urokinase | Intravenousa | Bolus: 4400 U/kg over 10 min |
|
|
| Infusión: 4400 U/kg per h |
| Warfarin | Oral | 0,1 mg/kg por día |
Otra variante terapéutica puede ser el uso de heparina, con los mismos fines anti trombóticos (24).
Complicaciones
Las consecuencias de la afectación coronaria en pacientes con EK, a largo plazo, todavía no son del todo conocidas. Se ha visto que la regresión del aneurisma no significa curación, ya que las anomalías estructurales persisten, además, la prevalencia de la estenosis coronaria continúa ascendiendo con el paso de los años.
En la EK, la trombosis coronaria, en ocasiones, es masiva, y da lugar a infarto de miocardio masivos (28,29).
Se ha descrito en pacientes seguidos a largo plazo, el desarrollo de enfermedad ateroesclerótica, no siendo conocida la causa de tal predisposición (28).
Pronóstico
Cuando no se desarrolla anormalidades coronarias la recuperación generalmente es completa. Se ha descrito recurrencias en el 1-3 % de los pacientes. El pronóstico de los pacientes que desarrollan anormalidades coronarias va a depender de la gravedad de esta.
Conclusiones
La EK está considerada la principal causa de afección cardiovascular adquirida en los pacientes en edad pediátrica de los países desarrollados. La etiología no ha sido identificada, aunque por su comportamiento epidemiológico se plantea la posibilidad de que sea desencadenada por un agente infeccioso. Su diagnóstico se fundamenta en elementos clínicos y de laboratorio, para el cual se ha propuesto algoritmos diagnósticos. Resulta cada vez más llamativa la aparición de formas incompletas de la EK, situación que debe resultar una alerta para el personal médico en general, por las complicaciones que pueden derivarse de un diagnóstico tardío o un error diagnóstico.
REFERENCIAS BIBLIOGRÁFICAS
1. Kawasaki T. Acute febrile mucocutaneous lymph node syndrome with lymphoid involvement with specific desquamation of the fingers and toes in children: Clinical obse rvations on 50 cases. Jpn J Allergy. 1967;(18):178-222.
2. Castro PU, Mendes FL, Arvalho IC. Kawasaki disease. An Bra Dermtol. 2009 Jul-Ago;84(4):317-29.
3. Baig A, Abuhammour W. Kawasaki disease. Review article. J Pediatric Infectious Diseases. 2008;(3):5–125.
4. Yanagawa H, Yashiro M, Nakamura Y, Kawasaki T, Kato H. Epidemiologic picture of Kawasaki disease in Japan: from the nation wide incidence surveys in 1991 and 1992. Pediatrics. 1995;(95):475-9.
5. Burns JC, Wiggins JW, Toews WH. Clinical spectrum of Kawasaki disease in infants younger than six months of age. J Pediatr. 1986;(109):759–63.
6. Chang RK. Hospitalizations for Kawasaki Disease among children in the United States, 1988–1997. Pediatrics. 2002;(109):87.
7. Yanagawa H, Nakamura Y, Ojima T, Yashiro M, Tanihara S, Oki I. Changes in epidemic pattern of Kawasaki disease in Japan . Pediatr Infect Dis J. 1999;(18):64–6.
8. Abuhammour WM, Hasan RA, Eljamal A, Asmar B. Kawasaki disease hospitalizations in a predominantly African-American population. Clin Pediatr. 2005;(44):721–5.
9. Machado K, Gutiérrez Pírez C. Enfermedad de Kawasaki. Arch Pediatr Urug. 2002;73(4):220-5.
10. Martínez G, Elgueta N. Manifestaciones purpúricas atípicas por parvovirus B19 en dos miembros de una familia. Caso clínico. Rev Med Chile. 2008;(5):136-8.
11. Shike H, Shimizu C, Kanegaye JT. Adenovirus, adenoassociatedvirus and Kawasaki disease. Pediatr I nfect Dis J. 2005;(24):1011–14.
12. Hagiwara K, Komura H, Kish F, Kajiand T, Yoshida T. Isolation of human herpesvirus-6 from an infant with Kawasaki disease. Eur J Pediatr. 1992;(151):867–68.
13. Johnson D, Azimi P. Kawasaki disease associated with Klebsiella pneumoniae bacteremia and parainfluenza type 3 virus infection. Pediatr Infect Dis. 1985;(4):100.
14. Muniain-Ezcurra M, Bueno-Mariscal C, Rodríguez-Bano J. Kawasaki disease and parvovirus B19 infection in an adult HIV-1 infected patient. Clin Microbiol Infect. 1998(4):609–10.
15. Kuijpers TW, Herweijer TJ, Scholvinck L, Wertheim PM, Van Dillen, Van De Veer. Kawasaki disease associated with measles virus infection in a monozygotic twin. Pediatr Infect Dis J. 2000;(19):350–53.
16. Matsuno S, Utagawa E, Sugiura A. Association of rotavirus infection with Kawasaki syndrome. J Infect Dis. 1983(148):177.
17. Lee DH, Huang HP. Kawasaki disease associated with chickenpox: report of two sibling cases. Acta Paediatr Taiwan. 2004;(45):94–6.
18. Furukawa S, Matsubara T, Umezawa Y, Okumura K, Yabuta K. Serum levels of p60 soluble tumor necrosis factor receptor during acute Kawasaki disease. J Pediatr. 1994;(124):721–25.
19. Lin CY, Lin CC, Hwang B, Chiang B. Serial changes of serum interleukin-6, interleukin-8, and tumor necrosis factor alpha among patients with Kawasaki disease. J Pediatr. 1992;(121):924–6.
20. Shulman ST, Rowley AH. Advances in Kawasaki disease. Eur J Pediatric. 2004;(163):285-91.
21. Stenberg N. The effect of TNF alfa blockade in complicated Kawasaki disease. Scand J Rheumatol. 2006;(35):318-21.
22. Kuijpers TW, Herweijer TJ, Scholvinck L, Wertheim PM, Van Dillen and Van De Veer. Kawasaki disease associated with measles virus infection in a monozygotic twin. Pediatr Infect Dis J. 2000;(19):350–53.
23. Tsai MH, Huang YC, Yen MH. Clinical responses of patients with Kawasaki disease to different brands of intravenous immunoglobulin. J Pediat. 2006;(148):38-43.
24. Lee H, Huang HP. Kawasaki disease associated with chickenpox: report of two sibling cases. Acta Paediatr Taiwan. 2004;(45):94–6.
25. Yousefa N, Ammar O, Alhmooda O, Mawria F, Kaddurahb A, Diskinc D, Abuhammourd W. Bilateral optic neuritis in patient with Kawasaki disease. J Pediatric Infectious Diseases. 2009(4):30–303.
26. Trager JDK. Kawasaki's Disease. Engl J Meded. 1995;(333):1391. (Imagen in Clinic Medicine)
27. Newburger JW, Takahashi M, Gerber MA. Diagnosis, treatment, and long-term management of Kawasaki disease. Pediatrics. 2004;(114):1708.
28. Martínez Burgui JA, Martínez Aviedo O, Garzarán TA, Rodilla F, Alonso E, Ocampo FL. Muerte súbita en un niño de 2 años con enfermedad de Kawasaki. Emergencias. 2007;(19):154-56.
29. Espinosa TM, Eduard CM. Importancia del diagnóstico temprano de la Enfermedad de Kawasaki. Rev Méd Costa Rica. 2009;(587):33-8.
SUMMARY
Kawasaki disease has been studied by epidemiologists, clinicians and researchers, since it was described firstly in 1967. Its cause has not been identified, though the main hypothesis point out to an infectious etiology. From the pathogenic point of view, the incapacity of recovering an infectious agent in a consistent way and the anatomopathological and laboratory evidences of a cellular and humoral immunity activation tend to place Kawasaki disease in the category of an autoimmune disease. One of the main current problems is the diagnosis delay, correlated with a worst prognostic of the main consequences of the disease, the compromise of the coronary vases among them. In this work we make a review of the disease and show the importance of the precocious diagnostic and treatment, and also present notes of the behavior of this disease at the Teaching Provincial Pediatric Hospital Eliseo Noel Caamaño, of Matanzas, in the period from 2001 to 2010.
MeSH
MUCOCUTANEOUS LYMPH NODE SYNDROME/diagnosis
MUCOCUTANEOUS LYMPH NODE SYNDROME /epidemiology
MUCOCUTANEOUS LYMPH NODE SYNDROME/complications
MUCOCUTANEOUS LYMPH NODE SYNDROME/drug therapy
CARDIOVASCULAR DISEASES/diagnosis
CARDIOVASCULAR DISEASES/etiology
PROGNOSIS
HUMANS
CHILD
STUDIES
EPIDEMIOLOGY, DESCRIPTIVE
CÓMO CITAR ESTE ARTÍCULO
Vidal Tallet LA, Noda Albelo A, Casal Menedez AX, Sánchez Hernández CA, Montell Hernández, OA, Linares Álvarez I. Enfermedad de Kawasaki. Aspectos a considerar. Rev Méd Electrón. [Seriada en línea] 2010;32(4). Disponible en URL:http://www.revmatanzas.sld.cu/revista%20medica/ano%202010/vol4%202010/tema07.htm. [consulta: fecha de acceso]














