Introducción
La Tomografía por Emisión de Positrones (PET, por sus siglas en inglés) es una modalidad de Imagenología Médica en la que se utiliza una sustancia radiactiva, llamada marcador, para ubicar una patología en el cuerpo. La aniquilación de los positrones produce rayos gamma que se van atenuando a medida que viajan hasta el detector, que construye las imágenes a partir de la intensidad de los rayos capturados. (1, 2, 3)
Los estudios PET permiten analizar el funcionamiento de las diferentes partes del cuerpo y los factores químicos de los procesos fisiológicos que ocurren en él. Estas características permiten revisar la función cerebral, trastornos que se puedan encontrar en ellos, además de diagnosticar cáncer. Las posibilidades brindadas por el PET en oncología, neurología, cardiología y otras disciplinas son muy amplias y están en constante crecimiento. (3, 4)
Una indicación principal del PET es el estudio de las demencias de todo tipo y de las enfermedades degenerativas cerebrales. Dada la elevada tasa de metabolismo para la glucosa de las células cerebrales, el PET puede mostrar claramente la disminución de dicho metabolismo en estadios muy iniciales. De ahí su capacidad de detectar precozmente la enfermedad de Alzheimer y otros procesos como demencia senil, atrofia multisistémica, parálisis suprarrenal progresiva, y degeneración cortico basal. También es de interés en la enfermedad de Parkinson, existencia y localización de focos epileptógenos, en especial en los casos en que se ha enfocado su tratamiento mediante resección quirúrgica; en determinadas enfermedades psiquiátricas (esquizofrenia), en secuelas de traumatismos y en el abuso de tóxicos. Además de patologías como demencia, enfermedad cerebrovascular, epilepsia, autismo, tumores cerebrales, entre otros. 4
Los estudios con imágenes por Resonancia Magnética (MRI por sus siglas en inglés) utilizan un haz pulsado de radiofrecuencia en presencia de un intenso campo magnético, para generar imágenes de alta calidad del cuerpo humano en cualquier tipo de plano. Al igual que la tomografía computarizada está formada por diversas imágenes tomográficas reconstruidas en un ordenador, aunque aquí por el contrario la información que se recoge no es la atenuación de un haz de rayos x, sino una manifestación gráfica de los datos de resonancia magnética nuclear que se obtienen de los núcleos atómicos de los tejidos orgánicos. Dicho de otro modo, para generar las imágenes utiliza la información proporcionada por la distribución de hidrógeno presente en las moléculas de agua en un organismo humano. (1, 3)
Los profesionales de la salud utilizan las imágenes por Resonancia Magnética para diagnosticar una variedad de infecciones, desde rupturas de ligamentos hasta tumores. Esta técnica presenta como ventajas una magnífica resolución de contraste, alta resolución espacial y la ausencia de radiaciones ionizantes. 1
Las limitaciones de las técnicas de neuroimagen no-invasivas que proporcionan información anatómica, fundamentalmente la Tomografía computarizada (CT por sus siglas en inglés) y MRI o funcional, Tomografía computarizada por emisión de fotón único (SPECT) y PET han llevado a la idea reciente de combinar en una sola sesión varias modalidades, tales como la fusión entre neuroimágenes CT/SPECT, CT/PET, MRI/ PET entre otras, llegando inclusive a fusionar tres tipos de neuroimágenes. La fusión de neuroimágenes es el proceso que une la información de dos o más neuroimágenes en una sola, está compuesta por un alto rango de técnicas desde neuroimágenes medias y la fusión de información en general en dirección de problemas médicos reflejados a través de neuroimágenes. La posibilidad de utilizar simultáneamente varias técnicas permite aumentar la sensibilidad y la reproducibilidad de la señal de las sondas moleculares, detectada por técnicas anatómicas. 5-8
En lo que a estas técnicas se refiere, existe un interés creciente y aplicativo a nivel internacional de las tecnologías de neuroimágenes en áreas de diagnóstico médico, análisis y documentación histórica. El incremento en esta área de investigación puede ser observada por el gran número de documentos científicos publicados en blogs y revistas científicas desde el año 2000. Esto puede ser atribuido al incremento de dispositivos para el diagnóstico por la comunidad médica. 6),(7
Con el fin de adquirir información más completa como resultado de los exámenes, es común utilizar neuroimágenes PET y MRI combinadas. Al fusionar estudios PET y MRI se obtienen neuroimágenes que integran la información de las características fisiológicas y anatómicas del cerebro de los pacientes. La PET no contiene generalmente información estructural detallada y por ello no proporciona una localización anatómica específica de la información funcional, a menos que se analice junto a una imagen anatómica, en este caso una imagen MRI. El valor añadido de las técnicas híbridas se debe a su capacidad para lograr en las neuroimágenes fusionadas una correlación espacial de la neuroimagen estructural y funcional, lo cual facilita la interpretación de las neuroimágenes en cuanto a localización de la lesión y su relevancia fisiológica. 9), (10
Los investigadores han llevado a cabo numerosos estudios de fusión de neuroimágenes en dominios espaciales y de transformación con diferentes técnicas de fusión, como la técnica de codificación de sub-bandas, el método de embolsado, la transformada de wavelet y transformada de Curvelet, entre otras. 8
Un método de fusión puede no ser tan eficiente debido a que carezca de un punto o de otro. Esto conlleva a la necesidad de desarrollar un método que tenga en cuenta las ventajas de varias reglas de fusión diferentes, por lo que es necesario utilizar una fusión híbrida. Este método realiza el procesamiento de la imagen en función de las diferentes reglas de fusión y luego integra estos resultados para obtener una sola imagen. Los resultados de las diferentes técnicas de fusión se extraen y luego se fusionan nuevamente implementando un método híbrido que presenta resultados de mejor calidad. Un solo método puede no resultar efectivo en la eliminación de los artefactos resonantes y el ruido en las imágenes de origen. Estos resultados deficientes en el desarrollo de reglas de fusión siguen un algoritmo híbrido y mejoran en gran medida la calidad visual de la imagen. 11
La presente investigación tiene como objetivo elaborar un proceso de fusión de neuroimágenes PET y MRI basado en un esquema híbrido wavelet y curvelet. Para ello es necesario definir los algoritmos y técnicas a emplear en cada actividad del proceso.
Desarrollo
Fusión de neuroimágenes de Tomografía por Emisión de Positrones y Resonancia Magnética.
Las neuroimágenes de Resonancia Magnética (MRI por sus siglas en inglés) juegan un papel importante en los diagnósticos no invasivos de tumores cerebrales y es una de las modalidades más ampliamente usadas en estudios médicos. Trabajos previos reportan fusiones exitosas de neuroimágenes MRI con diferentes tipos de modalidades. Los métodos de fusión de neuroimágenes son ampliamente aplicados para diagnósticos y tratamiento del cerebro, donde las técnicas de fusión han sido utilizadas para visualizar una mejora en el desempeño de diagnósticos e imágenes. Otras aplicaciones potenciales que incorporan las imágenes de MR basadas en fusión, incluyen regeneración de imagen, visualización potencial de campo, diagnóstico pulmón/hígado clasificación de tejidos, visualización multidimensional, tratamiento guiado de MRI, así como diagnóstico ginecológico de cáncer. Los estudios MRI junto con otras modalidades de imágenes, cuando son utilizadas junto con modernas técnicas de fusión han mostrado una mejora en la calidad de la imagen y en la práctica clínica aplicativa. Existen disímiles estudios que tienden a combinar la MRI con otra modalidad usando métodos de fusión de imágenes, algunos ejemplos de esto son: MRI-CT, MRI-CT-PET, MRI-Mamografía, Endoscopía-MRI entre otras. 12
La Tomografía por Emisión por Positrones, ampliamente conocida como imagen PET (por sus siglas en inglés) o escáner PET, es un tipo de imagen de medicina nuclear útil. Similar a la Tomografía Computarizada CT (por sus siglas en inglés) y MRI, la mayor aplicación de las imágenes PET es en estudios radiológicos para diagnóstico y tratamiento del cerebro. Existe un alto rango en la utilización de PET en la fusión de imágenes, algunos de ellos para el tratamiento de cáncer, segmentación e integración de imagen, detección y tratamiento de tumor, tratamiento de cáncer bucal, cervical, mama, pulmón, entre otras aplicaciones. Los límites de resolución en una imagen PET es una de los desafíos principales. Es común aquí un acercamiento integrado para reducir las limitaciones modelando efectos de resolución finita en reconstrucción de imagen y diseño detector mejorado. La alta sensibilidad que provee la imagen molecular es comúnmente vista como una ventaja de las imágenes PET. Existe un gran interés en usar técnicas de fusión para mejorar la calidad de la imagen. El uso de datos PET en combinación con otra de las existentes modalidades usando las técnicas de fusión de imágenes incluyen: MRI-CT-PET, MRI-SPECT-PET, MRI/CT-PET-SPECT, PET-CT-ultrasonido, entre otros. (10, 11)
La fusión de neuroimágenes se basa en la combinación coherente de dos o más neuroimágenes con el fin de obtener una que englobe toda la información complementaria. El objetivo es lograr que surjan características de interés en la imagen resultante, o bien mejorar aquellas características ya existentes. 13
La fusión PET/MRI es la combinación del estudio funcional PET con el estudio morfológico MRI, para complementar la información que se obtiene de ambas técnicas. Estas técnicas híbridas permiten explorar, guiar y monitorizar terapias locales celulares y genéticas beneficiosas para múltiples fenómenos fisiopatológicos. Los estudios PET han demostrado una alta sensibilidad en la detección de tumores malignos, como existen otras condiciones que provocan la captación de la sustancia de contraste utilizada, en ocasiones conduce a falsos positivos. En el estudio al que se hace referencia en 2 se puede apreciar como las imágenes PET han permitido decidir si en determinados pacientes existía o no un tumor maligno, en un 95% de los casos, frente al 47% de los casos en los que esto es posible mediante las técnicas convencionales. Los estudios PET/MRI permiten además caracterizar mejor los tumores primarios. (4, 14)
Los exámenes de Resonancia Magnética poseen una mejor resolución de contraste por ejemplo que las neuroimágenes de Tomografía Computarizada. Sin embargo, la resolución espacial es significativamente menor, teniendo solamente una resolución de 128 x128 pixeles.
Descripción del proceso de fusión basado en software.
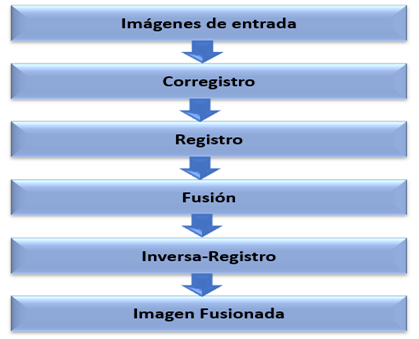
El proceso de fusión de neuroimágenes se compone de diferentes pasos. Los cuales varían dependiendo del método de fusión a emplear. En este caso les expondremos las diferentes fases, teniendo en cuenta que sí se emplea la fase de registro (Fig. 1). Los pasos son los siguientes:
Corregistro de las neuroimágenes a fusionar: Consiste en realizar una transformación para establecer una correlación espacial entre las neuroimágenes, o sea, hacerlas coincidir en posición y tamaño.
Registro: Llevar las neuroimágenes al dominio deseado por el desarrollador (HIS, Wavelet, Curvelet, entre otros). Mejora con creces el resultado de la fusión.
Fusión (Reglas de Fusión): La forma en la que son aplicadas las reglas de fusión afecta directamente a la calidad de la fusión final de las neuroimágenes. El algoritmo seleccionado puede trabajar por los diferentes valores sobre el dominio establecido en el paso anterior, o sobre los pixeles directamente.
Inversa: Se debe establecer la inversa del algoritmo seleccionado en el paso 2.
Elección del método para el corregistro de neuroimágenes.
Cuando se aplican transformaciones afines a las neuroimágenes, como por ejemplo una rotación, se presentan cambios de posición de los pixeles respecto a su posición inicial en el plano imagen, y por lo tanto se requieren métodos de interpolación numérica para los valores de intensidad que se asignarán a las nuevas posiciones en el plano imagen. 15
En el corregistro para la fusión de neuroimágenes PET/MRI, por razones de tamaño, se necesita aumentar la resolución espacial de las neuroimágenes de MRI, ya que poseen una resolución de 128 x 128 pixeles, mientras que las de PET son de 256 x 256 pixeles. El aumento de tamaño de las neuroimágenes MRI, se basa en que se aprovecharía la resolución espacial, y poder contar con sus beneficios. Para la transformación espacial de las neuroimágenes existen diferentes tipos de técnicas, entre las más conocidas y utilizadas se encuentra la técnica de interpolación. La operación de interpolación aplicada a imágenes digitales puede tener muchos objetivos, el más común sería el cambio de tamaño de una neuroimagen. Así, cuando se aumenta el tamaño de una neuroimagen discreta, los puntos originales se complementan con nuevos pixeles interpolados. Por otro lado, cuando se reduce el tamaño de una neuroimagen también se puede requerir el uso de una técnica de interpolación, ya que, aunque hay perdida de píxeles, los que quedan deben representar a los que desaparecen. Entre las técnicas de interpolación más comunes se encuentran la Interpolación por el Vecino Mas Cercano, Interpolación Bilineal e Interpolación Bicúbica. 16), (17
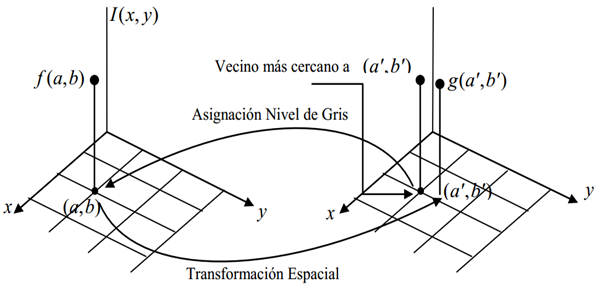
El método de interpolación de niveles de grises más simple, es el fundamentado en el del vecino más cercano, que consiste en escoger como el valor del píxel de una imagen de salida el valor del píxel de entrada más cercano en la dirección inversa. Este método, aunque es simple de implementar, presenta frecuentemente artefactos indeseables en las imágenes, tales como distorsión de líneas en imágenes de alta resolución, motivo por el cual no se aconseja para el suavizado de imágenes. Este tipo de interpolación logra producir un error espacial relativo a lo más de
El esquema consiste en tomar el píxel de la posición (x, y) = (a, b) en la imagen original, y transformarlo mediante las ecuaciones de distorsión para obtener las correspondientes coordenadas
El método se repite de la misma forma con cada uno de los píxeles restantes de la imagen hasta lograr una imagen restaurada
El error de interpolación por muestra se puede reducir significativamente cuando se utilizan los cuatro vecinos más cercanos en la interpolación. En este método, llamado de interpolación bilineal, se interpola linealmente a lo largo de cada fila de una imagen, y posteriormente el resultado se interpola linealmente en la dirección por columnas. La Interpolación Bilineal tiene en cuenta los valores en los pixeles conocidos que rodean a uno dado en una vecindad de los 2 x 2 pixeles más cercanos, tomando sus valores promedios para producir el pixel medio. Esta técnica, a pesar de que necesita más tiempo de procesado que la anterior, da como resultado una neuroimagen más suave. En el esquema (Fig.3)17 se muestra alrededor de
La Interpolación Bicúbica es el algoritmo de interpolación más utilizado en procesamiento de neuroimágenes digitales. Tiene en cuenta la vecindad de 4 x 4 pixeles conocidos más cercanos, para un total de 16 pixeles, por consiguiente, le da un mayor peso al cálculo de los más cercanos. Produce imágenes mucho más nítidas que los métodos antes expuestos. Posee la desventaja de que en caso de que se desee disminuir el tamaño de la neuroimagen entonces la cantidad de pixeles descartados seria mayor. En el esquema de la (Fig. 4) 17 se exhibe un modelo de vecindad generalizada de Interpolación Bicúbica. 18
La técnica de Interpolación a utilizar para el corregistro de la imagen MRI será la Interpolación Bicúbica por las siguientes razones:
Es la técnica más utilizada para el procesamiento de neuroimágenes digitales.
Al tener coeficientes de mayor grado, la curva de aproximación es más suave.
Posee buen balance entre tiempo y resultados.
Como el propósito es aumentar el tamaño de la neuroimagen MRI a las dimensiones de la imagen PET, se adapta el proceso de corregistro para realizar el escalado de la imagen, asegurando la utilización del método para aumentar el tamaño de la neuroimagen.
Tendencias de la fusión de neuroimágenes médicas.
Para seleccionar los métodos a tener en cuenta en el proceso de esta investigación, se realiza un análisis sobre estudios realizados por otros autores correspondientes a la fusión de neuroimágenes.
En 18 se utiliza la transformada Curvelet, la cual es una transformada multiescalar que contiene elementos direccionales. Las curvas se basan en multiscaleridgelet combinado con una operación de filtrado de paso de banda espacial para aislar diferentes escalas. Cuando la neuroimagen se descompone con la transformada Curvelet, las neuroimágenes incluyen una banda de baja frecuencia y una de alta frecuencia que tienen diferentes significados físicos. Como resultado, los coeficientes de baja frecuencia y alta frecuencia deben ser realizados con diferentes reglas de fusión. Las Reglas de Fusión y cómo se deben aplicar, afecta directamente el rendimiento final de la fusión. En los resultados que se muestran a continuación (Tabla 1) (18, se observa que el método propuesto posee más nivel de detalle que los otros.
Tabla 1- Comparación cuantitativa entre 5 métodos diferentes.
| Método | Entropía | Discrepancia | OP |
|---|---|---|---|
| Promedio de pixeles | 3.1141 | 6.1358 | 3.2292 |
| HSI | 2.7465 | 7.8387 | 3.3772 |
| Pirámide Laplaciano | 2.8755 | 7.7678 | 0.9461 |
| Wavelet | 3.0815 | 5.5806 | 1.1012 |
| Curvelet | 3.1371 | 5.5333 | 1.0148 |
Fuente: 18
Entropía se define como el monto de información contenida en una señal. Puede directamente reflejar el promedio de información contenida en una imagen. El máximo valor de entropía puede producirse cuando su nivel de escala de grises de todo el rango tiene la misma frecuencia. Si la entropía de la imagen fusionada es más alta que la imagen correspondiente, entonces la imagen fusionada posee mayor información. Discrepancia es la diferencia entre el resultado de la fusión y la PET imagen. Una pequeña discrepancia es aceptable. El desempeño general (Overall performance OP, por sus siglas en inglés) es la diferencia entre el gradiente promedio y la discrepancia. Un pequeño monto de OP significa una alta calidad de fusión general.
En 19 se evalúan varios métodos para la fusión de imágenes MRI y CT, uno basado en la Transformada Discreta de Wavelet (DWT, por sus siglas en inglés), otro en la Transformada de Curvelet de Segunda Generación, también conocida como Transformada Rápida de Curvelet (FCT, por sus siglas en ingles), y otro basado en la Transformada Discreta Rápida de Curvelet (DFCT, por sus siglas en ingles). La DFCT es una combinación de los métodos de fusión DWT y FCT. A continuación (Tabla 2) 19 se muestra como la imagen generada por el método DFCT posee características superiores a las generadas por los métodos de DWT y FCT.
Para la transformación al dominio de Wavelet se utiliza la Transformada de Haar, siendo este catalogado como el más usado para el análisis Wavelet. Una de las principales ventajas de la Transformada de Haar, es los altos niveles de Proporción Máxima de Señal a Ruido (PSNR por sus siglas en inglés) que presenta.
Para medir la calidad de las imágenes se utilizaron los parámetros de Entropía, donde un valor más bajo representa una mejor calidad, el parámetro PSNR, donde un valor más alto representa mayor calidad, y el Coeficiente de correlación (CC), -1≤CC≤ 1, representando el valor más cercano a 1 un mayor nivel de igualdad entre la imagen fusionada y la de origen.
Tabla 2- Evaluación de los parámetros.
| Reglas de fusión | Entropía (bit/pixel) | PSNR | CC |
|---|---|---|---|
| DWT | 6.72737 | 34.3313 | 0.918839 |
| FCT | 6.75950 | 34.5011 | 0.925118 |
| DFCT | 6.75037 | 43.5040 | 0.923673 |
Fuente: 19
En 20 se hace referencia a un método híbrido basado en las transformadas de Wavelet y Curvelet para realizar la fusión de imágenes de CT y MRI. El método híbrido propuesto descompone N veces las imágenes pasando por el filtro de bajas y altas frecuencias. Estas escalas son descompuestas aún más mediante la Transformada de Curvelet, luego son fusionadas mediante la Transformada de Wavelet y se aplica la Transformada Inversa de Wavelet para obtener la imagen completa.
Para evaluar la calidad de las imágenes fusionadas se utilizan los parámetros de Entropía, Coeficiente de Correlación, Raíz del Error Cuadrático Medio (RMSE, por sus siglas en inglés), PSNR, Información mutua (MI, por sus siglas en inglés) y Asociación de Bordes (representado como Qab/f). Se evaluaron estos parámetros `para varios métodos de fusión obteniéndose los resultados mostrados a continuación (Tabla 3) (20.
Tabla 3- Resultados estadísticos de varios métodos de fusión.
| Métodos de fusión | Entropía | RMSE | PSNR | CC | MI | Qab/f |
|---|---|---|---|---|---|---|
| Seleccionar máximo | 6.63 | 4.248 | 29.56 | 0.61 | 5.23 | 0.55 |
| Seleccionar mínimo | 2.89 | 15.23 | 23.25 | 0.67 | 6.92 | 0.74 |
| Promedio simple | 4.23 | 13.23 | 27.32 | 0.71 | 4.81 | 0.65 |
| Basado en componente | 6.34 | 3.421 | 36.12 | 0.88 | 5.89 | 0.79 |
| Transformada de Laplace | 7.45 | 3.921 | 39.24 | 0.90 | 4.56 | 0.80 |
| Transformada de Wavelet | 7.77 | 3.442 | 29.33 | 0.92 | 6.23 | 0.89 |
| Transformada de Curvelet | 8.54 | 3.436 | 38.77 | 0.89 | 6.85 | 0.75 |
| Transformada Híbrida | 8.81 | 3.316 | 41.91 | 0.85 | 7.44 | 0.91 |
Fuente: 20
A partir de los trabajos realizados, los autores demuestran que las imágenes fusionadas obtenidas mediante la Transformada Híbrida contienen más información útil que las resultantes usando la Transformada Wavelet o la Transformada de Curvelet, por los resultados mostrados en 19, teniendo en cuenta los criterios cuantitativos evaluados.
En 21 se utiliza la transformada de Wavelet como un método para la fusión de imágenes de una misma escena que presenta desenfoque, con el objetivo de recuperar el nivel de detalle perdido. El método utilizado para la implementación del algoritmo fue la Transformada Wavelet de Haar. Para realizar la fusión se toma, de los píxeles de las imágenes de entrada que se ubican en una determinada posición <x, y>, el de mayor coeficiente de Wavelet y se asigna ese valor al píxel en la posición <x, y> de la imagen resultante de la fusión, puesto que los coeficientes de mayor valor corresponden a los bordes y cambios más relevantes en las imágenes. En los resultados se evidencia como la imagen resultante conserva los bordes y las regiones de alto contenido de detalle y no produce pérdida de contraste.
Métodos para establecer la transformada híbrida en la fusión de neuroimágenes médicas.
La elección de los métodos para la fusión de neuroimágenes de Tomografía por Emisión de Positrones y Resonancia Magnética es fundamental para lograr cumplir el objetivo de la investigación. Luego de buscar los métodos de interés, serán elegidos los que según el estudio resulten idóneos para realizar la Transformada Híbrida.
El análisis realizado anteriormente arrojó que los métodos más utilizados y con mejor resultado son los métodos Curvelet y Wavelet, según los diferentes estudios. Pero dichos estudios poseen varias generaciones o avances.
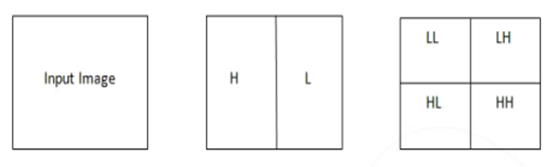
Uno de los más recientes es la Transformada Discreta de Wavelet de Haar (DWT por sus siglas en inglés), el cual es usado con propósitos de fusión de imágenes. La Transformada de Haar es uno de los algoritmos usados para análisis de Wavelet. Uno de los mayores avances de la Transformada de Haar son los altos valores de relación señal-ruido. Al usar Haar, los componentes de baja frecuencia son obtenidos al tomar el promedio de los valores de dos píxeles y la baja frecuencia de uno es obtenido al tomar la mitad de la diferencia de los dos píxeles. Después del primer nivel de descomposición debemos obtener cuatro bandas LL, LH, HL, HH como se muestra en el esquema (Fig. 5) (20. Fuera de estas cuatro bandas, la banda LL, que es la banda de baja frecuencia, contiene la mayoría de la información. Las otras tres bandas de altas frecuencias poseen menos información como los detalles de los bordes de la imagen.
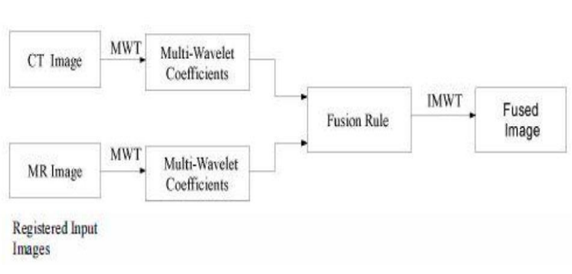
En la fusión basada en Wavelet (Fig.6) 20, primero se toman los coeficientes de las dos imágenes de entrada, en este caso Resonancia Magnética y Tomografía Computarizada.
Luego se aplica la regla de fusión a las bandas correspondientes. Luego se toma la inversa de la transformada para obtener la imagen fusionada.
La Transformada de Curvelet proviene de las desventajas de la Transformada Wavelet, mientras represente formas curvas. Existen dos tipos: Transformada Curvelet, Primera generación y Segunda generación de Curvelet. Los pasos de implementación son más complejos en la Primera generación, la Segunda generación es la más usada. También es conocida como la Transformada Rápida de Curvelet (FCT por sus siglas en inglés).
Esta transformada no usa análisis Ridglete, con el fin de reducir la complejidad de los cálculos, por lo tanto es una de las preferidas. En esta transformada toda la imagen es dividida en 30 o 40 o cualquier grado conveniente de losas. Luego se usa la técnica envoltura. Cada una de las losas es trasladada dentro de la original y luego se procede a envolver a través del centro axial. El algoritmo de envoltura es dado debajo.
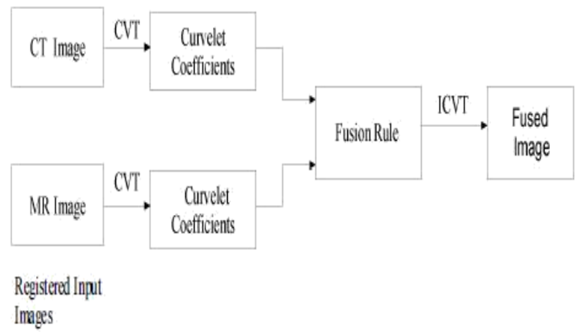
La fusión basada en Curvelet también procede como la fusión basada en Wavelet, pero en vez de utilizar la transformada Wavelet usa la Rápida de Curvelet. En la representación esquemática se muestra la fusión (Fig. 7) (20)
La DWT puede manejar puntos discontinuos, pero esto no es óptimo para las curvas, porque la base wavelet es isotópica y las curvas tienen dirección, por lo tanto toma muchos coeficientes para representar los bordes en comparación con la capacidad de representación de borde que posee Curvelet, el cual requiere un menor número de coeficientes. La idea principal es que la discontinuidad de los bordes es mejor aproximada por Curvelet que por Wavelet. Curvelet puede proveer soluciones en las limitaciones de Wavelet (Fig. 8) 21.
Por lo antes expuesto se toman como métodos de fusión para implementar el algoritmo para la Transformada Híbrida, la DWT y la FCT ya que serían las transformadas que mejor se complementan entre sí.
Regla de fusión
Para realizar la fusión de los coeficientes de las imágenes, se tiene en cuenta el estudio 2, en el que se evalúan varias reglas de fusión basadas en diversos parámetros de calidad de las imágenes resultantes. En dicho estudio, se concluye que la regla de fusión que calcula la media ponderada gaussiana, con un tamaño de ventana entre cinco y once, es el que mayores valores de calidad ofrece en la fusión de imágenes PET y MRI. Dado que ambos tamaños de ventana ofrecen valores similares de calidad, se decide utilizar en este trabajo una ventana de tamaño cinco, pues constituirá una ligera mejora en cuanto a costo computacional. En resumen, a la hora de fusionar los coeficientes de las imágenes se aplicará la media ponderada gaussiana con tamaño de ventana cinco.
Este mecanismo de fusión calcula la media aritmética de las submatrices de aproximación, mientras que para las submatrices de detalles realiza una ponderación mediante una matriz o máscara de pesos gaussiana
Con esa matriz
Transformada Híbrida
En la Figura 9 se observan los pasos para realizar la antes mencionada Transformada Híbrida, para un mejor entendimiento:
Realizar el corregistro de las neuroimágenes utilizando la Interpolación Bicúbica.
Aplicar la Transformada Discreta de Wavelet.
Aplicar la Transformada Rápida de Curvelet.
Aplicar la regla de fusión media ponderada gaussiana con tamaño de ventana 5 para la fusión de los coeficientes.
Establecer la inversa de la Transformada Rápida de Curvelet.
Por último, establecer la inversa de la Transformada Discreta de Wavelet.
Conclusiones
Se definió que la fusión basada en un esquema híbrido resalta las características más prominentes de las imágenes e inclusive de cada método de fusión, los bordes y las zonas de gran concentración de altas frecuencias.
Se determinó que las imágenes resultantes de la interpolación Bicúbica, a pesar de ser este el procedimiento de mayor complejidad computacional, poseen mayor calidad que las de la interpolación por el Vecino más Cercano y la Interpolación Bilineal.
Se puntualizó que realizar una fusión híbrida utilizando la Transformada Discreta de Wavelet y la Transformada Discreta Rápida de Curvelet disminuye el ruido en las imágenes de origen, como los artefactos resonantes.