Meu SciELO
Serviços Personalizados
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Cubana de Anestesiología y Reanimación
versão On-line ISSN 1726-6718
Rev cuba anestesiol reanim vol.11 no.1 Ciudad de la Habana jan.-abr. 2012
REVISIONES DE TEMAS
Consideraciones generales del dolor lumbar agudo
General considerations on the acute low back pain
Dr. Eduardo Martínez Suárez
Hospital Clínico Quirúrgico Hermanos Ameijeiras. C. Habana, Cuba.
Especialista de Segundo Grado en Neurocirugía. Profesor Auxiliar. Email: jemtnez@infomed.sld.cu
RESUMEN
Introducción: La lumbalgia representa un síntoma muy frecuente en la práctica médica, las causas que la producen, los mecanismos fisiopatológicos y el modo de enfrentarla. Objetivo. Actualizar al lector sobre las consideraciones generales del dolor lumbar agudo. Desarrollo: Además de las estructuras intrínsecas y extrínsecas que provocan dolor en la región lumbar, existen otros elementos relacionados con la fisiopatología como son los factores: anatómico, compresivo, vascular, inmunitario, inflamatorio y neural, que serán bien descritos en este artículo a modo de conocer cómo funciona cada uno en la aparición del dolor lumbar agudo y crónico, para posteriormente asumir nuestra responsabilidad como médicos en el tratamiento de este mal que aqueja a nuestra población. Conclusiones: el síndrome doloroso lumbar es de presentación frecuente en la consulta médica. El diagnóstico incluye la búsqueda de los signos de alarma que traducen enfermedades sistémicas, cáncer, infecciones, fracturas, entre otras. Sin embargo en la mayoría de los pacientes la lumbalgia es de tipo vertebral mecánica, con un curso benigno y puede ser resuelta favorablemente con un tratamiento adecuado en la atención primaria de salud.
Palabras clave: dolor lumbar agudo.
ABSTRACT
Introduction: The low back pain is a very frequent symptom in the medical practice, its causes, the pathophysiological mechanisms and the way to face it. Objective: To update reader on the general considerations of acute low back pain. Development: Besides the intrinsic and extrinsic structures provoking low back pain, there are other elements related to the pathophysiology including the following factors: anatomical, compressive, vascular, immune, inflammatory an neural which will be well described in present paper to know how functioning each in the appearance of chronic and acute low back pain for later to assume our responsibility as physicians in treatment of this illness involving our population. Conclusions: The lumbar painful syndrome is frequent in medical consultation. The diagnosis includes the search of alarming signs as manifestation of systemic diseases, cancer, infections, and fractures, among others. However, in most of patients the low back pain is of mechanic vertebral origin with a benign course and may be favorably solved with an appropriate treatment in the primary health care.
Key words: acute low back pain.
INTRODUCCIÓN
El dolor lumbar es tan frecuente en la población cubana que uno se pregunta si es realmente anormal experimentarlo alguna vez. Es un síntoma de presentación muy frecuente en la consulta de atención primaria. Entre 70 y 80 % de la población adulta mundial ha tenido un episodio de dolor lumbar al menos una vez en su vida, aunque la mayoría de ellos no hayan solicitado atención sanitaria. 1 De estos solo 10-12 % tendrá ciática concomitante.2
Este síndrome doloroso está entre las primeras causas de limitación física en individuos menores de 45 años.3 La lumbalgia genera un gran consumo de recursos económicos, relacionados con su alta prevalencia y sobre todo por la gran cantidad de días de trabajo perdidos, por lo que es la segunda causa de ausentismo después de las enfermedades respiratorias.1,2
Constituye el objetivo de este artículo, actualizar al lector sobre las consideraciones generales del dolor lumbar agudo.
DESARROLLO
El dolor lumbar puede ser neuropático por lesión de estructuras nerviosas (raíz o nervio periférico), caracterizado por ser: quemante, lancinante, hormigueante o parestésico y electrizante. El no neuropático o nociceptivo, debido a lesiones de estructuras no nerviosas como la de los músculos, tejidos blandos, ligamentos, periostio etc. que estimulan nociceptores por presión o inflamación, desencadenando dolor opresivo, espasmódico muy distinto al dolor neuropático.3
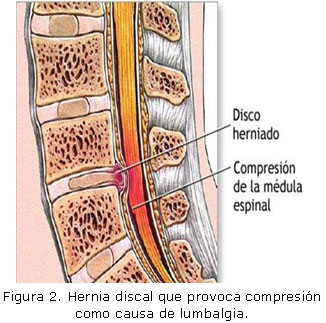
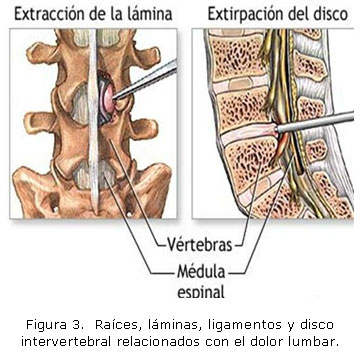
Dentro de los elementos implicados en el dolor lumbar se encuentran los intrínsecos que se originan en las estructuras que forman la columna lumbosacra (vértebras, disco intervertebral, articulaciones apofisiarias, aparato ligamentoso, músculos y raíces nerviosas) Figuras 1, 2 y 3.
El dolor lumbar de causa extrínseca o extra lumbar es el relacionado con estructuras externas a la columna lumbosacra como los dolores ginecológicos, dolores renales, dolores sacroilíacos y cuadros psicosomáticos.4
Las vértebras tienen una función de soporte corporal y de protección a las estructuras nerviosas y su parte sensible es el periostio. El disco intervertebral formado por el núcleo pulposo y anillo fibroso. Constituye un elemento amortiguador en la columna. Las articulaciones apofisiarias formada por la unión de las apófisis articulares, impiden la movilidad de las vértebras y mantienen la alineación vertebral.5-7
En el dolor lumbar de causa mecánico degenerativa intervienen factores mecánicos, inflamatorios, vasculares y de autoinmunidad, que actuando a nivel del nervio raquídeo y de sus raíces explican ciertas características clínicas que pueden ser comprendidas mejor a la luz de nuevas investigaciones. Existe evidencia clínica de que la compresión de un nervio sano produce parestesias, y la de un nervio lesionado es la que produce dolor. 5, 8 Si este concepto se aplica a nivel de la raíz, tendremos el dolor de origen radicular, de características neuropática, como la lumbociatalgía que tiene como síntoma clínico el dolor lumbar.9,10
Rull, Millares y Añez 11 describieron varios factores relacionados con la fisiopatología del dolor lumbar los cuales después de mencionarlos se describirán:
Factor anatómico
- 2 Factor compresión. Factor edema
- 3 Factor vascular
- 4 Factor inmunitario
- 5 Factor inflamatorio
- 6 Factor neural
Factor anatómico. Las raíces de los nervios espinales son elementos de transición entre el sistema nervioso central y el periférico, sus características anatómicas de protección e irrigación son distintas. Las raíces flotan en el líquido cefalorraquídeo (LCR) y sus vainas son muy finas. Su endoneuro tiene una limitada cantidad de fibras colágenas entre las fibras nerviosas ordenadas longitudinalmente. Durante la flexión de la columna las raíces se tensan, durante la extensión se relajan y ondulan. Se produce un movimiento interfascicular tanto en sentido longitudinal como transversal que sería imposible en los fascículos fijos en el perineuro de un nervio periférico.
Las raíces de los nervios espinales están bien protegidas de los traumas externos por las vértebras, pero son muy susceptibles frente a traumas directos incluso a bajos niveles de presión. La compresión conduce a edema intraneural, invasión fibroblástica y afectación crónica del transporte axonal. La secuencia de acontecimientos conduce a dolor radicular y disfunción nerviosa. La irrigación del canal espinal corre a cargo de arterias segmentarias procedentes de la aorta y de la ilíaca. Cada arteria segmentaria da una rama especifica para el sistema nervioso que se divide en sistema extrínseco, que abastece las arterias de la médula sin irrigar la raíz y que circulan por el espacio subaracnoideo y sistema intrínseco que irriga las dos raíces del nervio espinal. Las que nutren la raíz posterior forman un plexo alrededor del ganglio sensitivo. Dichas ramas se dirigen hacia la medula y se anastomosan en el tercio medio de la raíz con las ramas procedentes de la arteria espinal anterior y posterior. Esta zona anastomótica está hipovascularizada, sería una zona vulnerable y muy susceptible a la deformación mecánica.
Estos vasos intrínsecos circulan principalmente por las láminas externas de las vainas, existen además arteriolas interfasciculares que circulan paralelamente a las primeras en el endoneuro. Ambas arteriolas se comunican entre si por unas colaterales en ángulo recto, que tienen un recorrido tortuoso lo que permite una buena irrigación sanguínea incluso cuando la raíz se elonga. Las venas tienen también un recorrido en espiral en la profundidad de las raíces. La circulación venosa drena, en parte, en el plexo venoso epidural. La red arterial y venosa de las raíces espinales está menos desarrollada que en los nervios periféricos. Los vasos están localizados superficialmente en los manguitos, a diferencia de los nervios periféricos, que se sitúan más profundamente entre los fascículos.
El aporte nutricio de la raíz se hace solo en parte a partir de los vasos sanguíneos, el resto a partir del LCR. El flujo más importante del aporte vascular proviene de la arteria segmentaria, rama de la arteria lumbar. La compresión nerviosa en la zona de salida, cerca del foramen, produce una lesión isquémica mucho más importante que la compresión en la zona de entrada del canal radicular. El aporte vascular representa 35 % y el del LCR 58 %. La hipertrofia de las vainas piales reduce de manera importante el recambio metabólico afectando la nutrición de la raíz. A nivel del tejido nervioso periférico el aporte vascular representa 95 %.
Las raíces nerviosas están rodeadas de LCR que además de protección les ofrece una composición química adecuada. Está demostrada la importancia de la integridad de la barrera capilar sangre-nervio en la raíz nerviosa, barrera que se rompe con compresiones importantes y que causan edema vasogénico. Marcadores proteícos que se inyectan en el espacio subaracnoideo llegan a la luz de los capilares del endoneuro, pero los que son inyectados vía intravenosa no aparecen en el espacio endoneural, mientras la barrera capilar permanezca intacta.
Gracias al microscopio electrónico se conoce la estructura de la pared de los capilares que se clasifican en tres grupos según la presencia o no de membrana basal, según la naturaleza de sus células endoteliales, o la presencia de perícitos. Los capilares de las raíces nerviosas pertenecen al tipo continuo al igual que los capilares del sistema nervioso central y periférico. Sus células endoteliales se unen herméticamente y demuestran actuar como una verdadera barrera sangre-nervio. Estas células permiten el paso de moléculas no superiores a 2-3 nm (nanómetros o milimicras). Sustancias de mayor tamaño pueden llegar mediante pinocitosis ya que las vesículas pinocíticas de 60-100 nm de diámetro son muy abundantes en los capilares de las raíces. La peroxidasa de rábano inyectada por vía subaracnoídea aparece en la luz capilar transportada por las vesículas pinocíticas y no aparece en el espacio endoneural cuando se inyecta por vía endovenosa. Este transporte demuestra una circulación del LCR hacia el espacio endoneural. Alteraciones del flujo del LCR debidas a estenosis de canal o aracnoiditis tienen efectos adversos en la circulación intrarradicular.
La barrera sangre-nervio no se encuentra en los vasos del ganglio de la raíz dorsal, los cuales muestran capilares fenestrados. Mediante técnicas inmunohistoquímicas se ha estudiado la inervación perivascular de las arterias radiculares, tratándose de inervación somática y vegetativa. Se han detectado neuropéptidos relacionados con la transmisión del dolor: neuropéptido Y, péptido intestinal vasoactivo y CGRP (calcitonine gene-related peptide). A través de la liberación de histamina se sabe que la substancia P produce directamente extravasación plasmática e indirectamente vasodilatación.
Si bien el estuche óseo raquídeo ofrece una protección externa eficaz a la médula y a las raíces, estas últimas se hallan desprotegidas dentro de él. Las vainas protectoras son muy finas, lo que permite el deslizamiento interfascicular en los movimientos de flexoextensión y el aporte nutricio por parte del LCR, pero por este motivo son más vulnerables. Los vasos de las raíces tienen un recorrido tortuoso para garantizar la irrigación incluso cuando la raíz está tensa, pero al estar localizados superficialmente en los manguitos son vulnerables a fenómenos de compresión o inflamatorios, rompiéndose la barrera capilar sangre-nervio con extravasación del contenido plasmático y producción de edema.
Factor compresión. Factor edema. La enfermedad mecánico degenerativa de la columna puede afectar al nervio raquídeo o a sus raíces a varios niveles: cuerpo vertebral y disco, canal radicular, y agujero de conjunción. La afectación nerviosa no tiene como única causa la compresión. Hay que valorar siempre los fenómenos irritativo-inflamatorios, de tensión y estiramiento que afectan a la fibra nerviosa y a su vascularización. El proceso inflamatorio debido a microtraumatismos o por autoinmunidad frente a las proteínas liberadas del núcleo y la compresión que dificulta el retorno venoso conducen a la formación de edema que aumenta a su vez la tensión interfascicular e interfiere en la función nerviosa. Si la raíz edematizada está dentro de una estructura rígida, que es lo que ocurre cuando la raíz atraviesa el canal radicular y sale por el agujero de conjunción, se produce un síndrome compartimental, interfiriendo la microcirculación, aumentando el compromiso vascular y produciendo un compromiso axoplásmico.
Esto explica el dolor radicular de tipo neurítico vehiculizado por fibras C, que además de una distribución metamérica tiene la cualidad de quemazón y disestesia que le caracteriza. Los axones dañados son hiperalgésicos. Si la inflamación no se trata el proceso inflamatorio aumenta y se cronifica. El edema y la isquemia causan fibrosis perineural e intraneural. La lesión vascular, la fibrosis y la inflamación crónica juegan un importante papel y explicarían la existencia de dolor lumbar incluso cuando no hay un factor mecánico evidente. El edema intraradicular causado por alteración de la barrera capilar sangre- nervio es el factor más importante en la disfunción de la raíz nerviosa debido a compresión crónica.
El edema intraneural es un hecho en las lesiones por compresión de las raíces nerviosas. La presencia de edema se ha demostrado en las tomografías axiales de región espinal y en las secciones histológicas. Experimentalmente se ha demostrado que la presión requerida para inducir éstasis vascular, fundamentalmente estasis venoso, es mucho más baja en las raíces nerviosas que en los nervios periféricos. Hay una relación entre el edema de la raíz, la positividad de la ciática y la positividad del signo de Lasegue que puede tardar incluso medio año en desaparecer, lo que justificaría la persistencia de síntomas postcirugía. La presencia de edema puede dificultar la nutrición de la raíz durante un largo periodo, e iniciar la formación de una cicatriz fibrótica intraneural. Está demostrado el aumento de las relaciones albúmina del LCR/plasma, Ig G del LCR/plasma, y el valor de proteínas totales en pacientes con clínica e imágenes mielográficas de compresión radicular. Esto demuestra el paso de proteínas plasmáticas desde la raíz al LCR considerándose como un indicador de lesión de la barrera sangre-nervio. Estos parámetros bioquímicos podrían ayudar al diagnóstico de sufrimiento radicular cuando las imágenes radiográficas no fuesen muy evidentes.
Existe una relación entre los mecanismos biomecánicos y microvasculares en la producción de déficits neurológicos. La compresión, según sea aguda o crónica produce distintos cambios estructurales y neurofisiológicos. La compresión aguda produce fundamentalmente alteraciones circulatorias. Según el grado de compresión, y de menos a más se observa congestión venosa, edema intraneural con enlentecimiento de la conducción axonal. Cuando la compresión es importante y brusca (valores de tensión arterial media), se produce un stop circulatorio con caída brusca de las velocidades de conducción motora y sensitiva. La compresión crónica conduce a la desmielinización y fibrosis. Después de un mes, se observa engrosamiento de la aracnoides y duramadre con edema intraradicular por lesión de la barrera sangre- nervio. A los tres meses, se observa una perdida de fibras mielinizadas con disminución de la velocidad de conducción, se inicia la degeneración waleriana y fibrosis con formación de cortocircuitos en el interior de la raíz entre fibras gruesas propioceptivas y fibras nociceptivas. A los seis, doce meses, la degeneración waleriana y fibrosis son completas.
Hay que considerar también la rapidez con que se produce la compresión. Al instaurarse el edema el tejido nervioso es desplazado del centro de la compresión hacia zonas no comprimidas lo que produce un cizallamiento entre los distintos fascículos de la raíz, más pronunciado en los bordes. Debido a las propiedades viscoelásticas del tejido nervioso este desplazamiento probablemente requiere algún tiempo. Si la presión se aplica rápidamente, no puede adaptarse. El incremento de la presión arterial aumenta la presión de perfusión y el flujo sanguíneo en la raíz nerviosa aumentando el dintel en el que se afecta la conducción. No obstante, este hallazgo experimental no tiene aun una aplicación clínica. Las raíces nerviosas están incluidas en una extensión del saco dural, llamado manguito de la raíz, hasta que ésta sale del canal espinal. La porción extratecal está estrechamente rodeada por el manguito, en el cual es mucho más perjudicial el edema que en la porción intratecal de la raíz donde el drenaje es más fácil.
El ganglio de la raíz dorsal suele estar incluido en la porción extratecal lo que le hace más susceptible a los efectos del edema intraneural. Su situación no siempre es la misma, y existen anomalías anatómicas que lo sitúan dentro del canal espinal o fuera del foramen. Los cuerpos celulares del ganglio de la raíz dorsal muestran una elevación importante de la substancia P después de un estímulo mecánico. Esta substancia P es transportada centralmente por la neurona aferente primaria hacia la substancia gelatinosa del asta posterior de la médula, demostrando el inicio de una transmisión dolorosa. Las raíces nerviosas, junto con el ganglio, rodeadas de un manguito prolongación del saco dural, atraviesan el canal radicular. Si a este nivel se produce edema se crea un importante conflicto de espacio, "un síndrome compartimental", que dificulta la nu trición de la raíz llegando a producir lesión axonal. La rapidez con que se instaura el edema repercute en el grado de lesión al dificultar la adaptación de los fascículos nerviosos.
Factor vascular. La hipótesis apoyada en la congestión venosa y en la fibrosis, explicaría el dolor lumbar irradiado cuando no hay una lesión del disco o una compresión clara. La obstrucción venosa podría ser un factor importante en la producción de fibrosis peri e intraneural. En otras circunstancias patológicas como la cirrosis de origen cardiaco por éxtasis venoso, también se ha encontrado que la congestión venosa, conduce a una fibrosis localizada sin existir proceso inflamatorio debido a isquemia local.
Normalmente los vasos de la membrana perineural son muy delgados, pero en estas vainas engrosadas tienen una lamina amorfa subendotelial de aspecto parecido a los vasos de los pacientes diabéticos. Se supone es debido a daño endotelial secundario a isquemia local. La lesión microvascular aumenta la permeabilidad y se desarrolla edema. A falta de un buen drenaje linfático el edema drena muy lentamente y favorece la fibrosis. El defecto fibrinolítico es secundario al daño mecánico, pero si persiste puede convertirse en factor patogénico asociado colaborando a la cronicidad del problema. Dichas alteraciones de la actividad fibrinolítica serían un marcador del daño vascular. Se sabe que en los fumadores hay una mayor incidencia de dolor lumbar. El fumar se asocia a un defecto de la fibrinolisis. También se ha encontrado relación entre el dolor lumbar y el uso de anticonceptivos orales. Estos fármacos alteran la reología sanguínea lo cual empeora la nutrición del disco, favoreciendo su degeneración y al mismo tiempo favorece la congestión venosa periradicular.
Factor inmunitario. La lesión inflamatoria puede ser una respuesta de autoinmunidad frente al material discal. El núcleo pulposo está encerrado herméticamente en el anulus y no tiene contacto con la circulación sistémica. Las proteínas del núcleo por estar aisladas, al ponerse en contacto con la circulación sistémica actúan como autoantígeno y desencadena una reacción autoinmune. No siempre el anticuerpo pasa a la circulación sistémica donde se podría detectar, sino que por vía linfática va a los ganglios regionales y por vía eferente también linfática se dirige al sitio de liberación del antígeno.
Las proteínas que constituyen el núcleo pulposo, al estar aisladas de la circulación general actúan como agentes inmunológicos cuando se vierten en el espacio epidural por un desgarro del annulus. La respuesta de autoinmunidad es una de las causas de inflamación de la raíz, y origen de dolor aun en ausencia de una verdadera protusión discal.
Factor inflamatorio. El disco lumbar es un tejido con actividad biológica. Se ha demostrado su capacidad inflamatoria independiente de mecanismos inmunológicos. En discos intervertebrales de pacientes operados se encuentran niveles altos de fosfolipasa A2 (PL A2), enzima que tiene un importante papel en el proceso inflamatorio al regular la cascada del ácido araquidónico.
Si existe una interacción bioquímica entre el tejido discal y los tejidos adyacentes, la iniciación de la inflamación por factores bioquímicos en ausencia de reacción inmunológica es un mecanismo alternativo de generación de dolor.
La PLA2 del disco humano se ha demostrado que tiene capacidad inflamatoria in vitro, por lo que puede iniciar o contribuir a generar dolor por acción sobre los nociceptores del anulus o del espacio epidural, ya sea por acción directa o contribuyendo a producir mediadores inflamatorios.
En los discos herniados encuentra elevación de metaloproteinasas de la substancia intercelular, óxido nítrico, PGE2 e interleukina 6. Estos productos tienen relación con la bioquímica de la degeneración discal y la fisiopatología de la radiculopatía.
Otra substancia irritante encontrada en el tejido discal humano es la stromelysin. El líquido sinovial procedente de las articulaciones facetarias degeneradas podría también actuar como factor inflamatorio. El reconocimiento del factor inflamatorio como causa de radiculopatia apoya el uso de corticosteroides en la clínica.
La degeneración discal implica un balance bioquímico alterado. Cambios en el pH del núcleo, tamaño y agregación de proteoglicanos, contenido de agua, tipos de colágeno y tipos de enlaces son causa y efecto de los cambios fisicobioquímicos del medio. La actividad y el contenido de PLA2 es parte de este balance alterado. El acumulo de PLA2 dentro del disco puede ser el resultado de la edad y de la degeneración. Se ha demostrado un componente genético (una variante del gen de colágeno) en la degeneración discal.
Factor neural. Es lógico pensar que la compresión del ganglio sea un factor en el origen del dolor radicular. La compresión aguda del ganglio produce descargas repetidas, mientras que la compresión de un axón normal no. El ganglio de la raíz dorsal es fácilmente atrapado entre el disco herniado y las facetas. Pequeños y repetidos movimientos de las articulaciones lo traumatizan de una manera intermitente. En estudios necrópsicos se ha encontrado que en todos los casos de disco herniado, el ganglio estaba comprimido y mostraba diversos grados de degeneración.
Experimentalmente se ha demostrado que el ganglio de la raíz dorsal es muy sensible a la compresión mecánica y a la hipoxia. Se le confiere también un protagonismo en la transmisión del dolor al mostrar cambios cuantitativos de la sustancia P, durante la vibración de baja frecuencia (conocido factor mecánico que causa dolor lumbar).
Las neuronas sensitivas de primer orden reunidas en el ganglio dorsal de la raíz pueden verse afectadas no solo por fenómenos directos de compresión y vibración, sino también por el insulto químico que suponen los fenómenos inflamatorios que ocurren a nivel de la raíz. Experimentalmente, aplicando núcleo pulposo autólogo en la raíz de ratas se han observado cambio fisiopatológicos en el ganglio semejantes a los que aparecen por compresión sobre el mismo.
La lumbalgia es un problema que se caracteriza por su alta prevalencia en la población (cerca de 80 % de la población lo padece al menos una vez en la vida) y cerca de 90 % de los casos no se encuentra ningún tipo de lesión que justifique el proceso, por lo que el problema será catalogado como lumbalgia inespecífica. La lumbalgia tiene una gran trascendencia debido a sus grandes repercusiones económicas y sociales asociadas, ya que se ha convertido en una de las primeras causas de ausentismo laboral.12-14
Se concluye que el síndrome doloroso lumbar es de presentación frecuente en la consulta médica. El diagnóstico incluye la búsqueda de los signos de alarma que traducen enfermedades sistémicas, cáncer, infecciones, fracturas, entre otras. Sin embargo en la mayoría de los pacientes la lumbalgia es de tipo vertebral mecánica, con un curso benigno y puede ser resuelta favorablemente con un tratamiento adecuado en la atención primaria de salud.
REFERENCIAS BIBLIOGRÁFICAS
1. Rivas Hernández R; Santos C.A. Coto L, Manejo del síndrome doloroso lumbar. Rev Cubana Med Gral Integ 2010; 26(1)117-129
2. Buil Cosiales P, Gurpegui Resano JR, Pascual Pascual P, Gimeno Aznar A, Lizaso Bacaicoa J, Loayssa Lara R, et al. La lumbalgia en atención primaria: Guía de actuación. Navarra: Servicio Navarro de Salud; 2000. pp.51-62.
3. López Roldan V, Oviedo Mota M, Guzmán González JM, Ayala García Z, Ricardez Santos G, Burillo Bauret E, et al. Guía clínica para la atención del síndrome lumbar doloroso. Rev Med IMSS 2003;41(supl):S123-S130.
4. Haldeman SD, Kirkaldy-Willis W, Bernard TN. Atlas of Back Pain. London: The Parthenon Publishing Group; 2002. pp.151-158.
5. Curto Gamallo JM. Fisiopatología del dolor lumbar. Avances Reumatología Salamanca 2003;37-43.
6. Kendrick D, Fielding K, Bentley E, Kerslake R, Miller P, Pringle M. Radiography of the lumbar spine in primary care patients with low back pain: randomized controlled trial. Br Med J. 2001;322:400-5.
7. Pimienta L, Bellera Alonso F, León Parra M, Díaz Orduz RC. Clasificación radiográfica de la degeneración facetaria lumbar. Acta Ortopédica Mexicana 2005;19(3):95-8.
8. Boos N, Aebi M. Spinal Disorders. Fundamentals of Diagnosis and Treatment. Berlin: Springer; 2008. pp.201-225.
9. Pfirrmann CW, Dora C, Schmid MR, Zanetti M, Hodler J, Boos N. MR image-based grading of lumbar nerve root compromise due to disk herniation: reliability study with surgical correlation. Radiology 2004;230:583-8.
10. Witte DH. Resonancia magnética en ortopedia y traumatología. En: Canale ST Campbell, editor. Cirugía ortopédica. 10ma. ed. Madrid: Harcourt Brace. 2004. pp.135-9.
11. Rull M, Miralles R, Añez C. Fisiopatología del dolor radicular. Rev Soc Esp Dolor 8: Supl. II, 22-34, 2001.
12. Patel AT, Ogle AA. Diagnosis and management of acute low back pain. Am Fam Phys 2000;61(6):1779-86.
13. Ávila Ramírez J, Aguilar López R, Ávila Cervantes R. Estenosis lumbar adquirida. Características clínicas, tratamiento quirúrgico y resultado. Rev Mex Neurocir 2006;7(1):90-4.
14. Tulder MW, Jellema P, Poppel M, Nachemson A, Bouter L. Lumbar supports for prevention and treatment of low back pain. The Cochrane Database of Systematic Reviews. 2002; Issue 1. pp.56-61.
Recibido: 2 de junio de 2011.
Aprobado: 30 de agosto de 2011.