My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Cubana de Anestesiología y Reanimación
On-line version ISSN 1726-6718
Rev cuba anestesiol reanim vol.11 no.3 Ciudad de la Habana Sept.-Dec. 2012
CASO CLÍNICO
Conducta anestésica en pacientes pediátricos con pectus excavatum
Anesthetic management of pediatric patients with pectus excavatum
Dr. Néstor Sánchez Nogueira, Dr. Junior Lima Aguiar, Dr. Eugenio Selman Housein Sosa, Dr. Manuel Jaca Tornés, Dr. Luis Marcano Sanz, Dra. Jacqueline Barrial Moreno
Cardiocentro Pediátrico "William Soler". La Habana, Cuba.
RESUMEN
Introducción: el pectus excavatum es una deformidad congénita de la pared anterior del tórax. Al nacer es poco evidente su existencia, pero durante la infancia y la adolescencia se desarrolla plenamente y puede llegar a constituir un problema funcional, psicosocial y estético relevante para el paciente. La fisiopatogenia se atribuye al crecimiento anormal de los cartílagos costales. En nuestro país, su incidencia no es despreciable, un pequeño número de pacientes pediátricos se han operado; sin embargo, existen escasas referencias publicadas.
Objetivo: presentar el proceder anestésico multimodal utilizado en un paciente con pectus excavatum.
Caso clínico: varón de 15 años de edad, con trastornos respiratorios restrictivos clínicos y espirométricos que dificultaban su actividad física. La deformidad fue corregida mediante tratamiento quirúrgico convencional, con anestesia multimodal. Presentó un transoperatorio estable lo cual permitió ser extubado a su llegada a la Unidad de Cuidados Intensivos (UCI). Durante el período posoperatorio recibió analgesia por catéter epidural, cuando la Escala Visual Análoga del dolor posoperatorio (EVA) fue superior a 5.
Conclusiones: el uso de anestesia multimodal en un paciente pediátrico, hizo posible la corrección de forma satisfactoria de un niño con pectus excavatum, por lo que se puede generalizar esta técnica para la corrección quirúrgica de ésta enfermedad en instalaciones de salud especializadas en Cuba.
Palabras clave: pectus excavatum, anestesia multimodal, Escala Visual Análoga (EVA), cirugía pediátrica.
ABSTRACT
Introduction: Pectus excavatum is a congenital deformity of the anterior chest wall. Not evident at birth, it fully develops during childhood and adolescence, and may constitute a relevant functional, psychosocial and aesthetic problem for the sufferer. Its physiopathogeny is attributed to the abnormal growth of the costal cartilages. The incidence of pectus excavatum in our country is not negligible. A small number of patients have been operated on, but there are few published references on the topic.
Objective: describe the multimodal anesthetic procedure used in a patient with pectus excavatum.
Clinical case: 15-year-old male patient with clinical and spirometric restrictive respiratory disorders hindering his physical activity. The deformity was corrected by conventional surgical treatment under multimodal anesthesia. The patient had a stable transoperative period and was extubated upon arrival at the Intensive Care Unit (ICU). During the postoperative period he received analgesia through an epidural catheter when Analog Visual Scale (AVS) values for postoperative pain were greater than 5.
Conclusions: the use of multimodal anesthesia in a pediatric patient enabled the satisfactory correction of a pectus excavatum. This technique for the surgical correction of this condition may be generalized in specialized health facilities in the country.
Key words: pectus excavatum, multimodal anesthesia, Analog Visual Scale (AVS), pediatric surgery.
INTRODUCCIÓN
El pectus excavatum fue descrito desde los años 1600, es también conocido como pecho excavado, tórax en embudo, tórax hundido o deprimido, en otros idiomas como el inglés y el alemán se reconoce como funnelchest y sunkenchest respectivamente.1 Es la deformidad congénita más frecuente de la pared torácica, la cual presenta repercusiones funcionales, estéticas, psicológicas y sociales para el paciente. Se observa comúnmente en pacientes que padecen el síndrome de Down y escoliosis.2 Presenta mayor incidencia en hombres que en mujeres.
Esta deformidad del tórax se caracteriza por una profunda curvatura a nivel del cuerpo del esternón en su unión con el apéndice xifoides. El hundimiento de la porción central del esternón con respecto a los cartílagos costales, se presenta desde el nacimiento y puede ocasionar un movimiento paradójico con la respiración que puede agravarse con la edad. En los casos severos pude producir desplazamiento del corazón. El defecto se clasifica en: completo e incompleto, a su vez el incompleto en superior e inferior.3
Aunque existen controversias sobre las anomalías genéticas o cromosómicas que justifiquen esta enfermedad, las teorías planteadas evocan un desbalance hereditario del músculo esquelético entre el diafragma y la pared torácica,4 se identifica como un defecto muscular intrínseco, asociado a escoliosis, enfermedad intratorácico-visceral o por bandas subesternales anormales;5 el gen Hoxb-4 es el causante de alteraciones en el mesodermo paraxial que está relacionado con la ausencia de esternón durante la décima semana de gestación.3,6
El grado de compromiso cardiorrespiratorio que genera esta enfermedad es objeto de controversia, inclinándose la mayoría de los estudios a afirmar que la restricción pulmonar y cardiaca solo se manifiesta en niveles de severidad elevados los cuales, afectan únicamente a los individuos en momentos de plena actividad física.2,3
La intervención quirúrgica correctora de esta deformidad se basa en la remodelación de los cartílagos costales descritos por Ochsner y De Bakeyt en I9397 y que al año siguiente Lincoln público.8 En los últimos años, se han incorporado nuevas técnicas quirúrgicas por toracoscopia y videotoracoscopia modificadas por Brown y Ravitch,8 con las que se persigue un abordaje estético y la reducción del tiempo quirúrgico. Existe la técnica de Nuss con apoyo toracoscópico, publicada desde 1998, como la comúnmente practicada.9 Mediante esta técnica, se coloca una barra de acero moldeable subesternal que se hace progresar por el mediastino anterior y sale a perforar la pleura parietal, esta pieza se debe retirar pasados 2 años.10 Entre las complicaciones que presenta están: dolor posoperatorio, desplazamiento de la barra, neumotórax, aneurisma de los vasos mamarios y perforación pericárdica. Para reducir estas complicaciones, actualmente se realiza el procedimiento en el espacio extrapleural sin penetrar al mediastino.8 En un estudio realizado controlado por tomografía computarizada y pruebas de función respiratoria prequirúrgicas, en decúbito supino, se logró la obtención mínima de sangrados, se redujo el tiempo quirúrgico y la ausencia de arritmias, persistiendo el dolor torácico. En nuestro país, los especialistas no cuentan con publicaciones sobre la aplicación de estas novedosas técnicas, en las cuales se conservan las correcciones quirúrgicas convencionales para el tratamiento del pectus excavatum.
Por su asociación con trastornos cardiorrespiratorios de diversa severidad y, la incidencia elevada de dolor en el período posoperatorio, los procederes anestésicos en pacientes con esta enfermedad representan un reto elevado para a los profesionales actuantes, los cuales deben establecer estrategias previas a la aparición de complicaciones potenciales.
Constituye objetivo de este artículo poner a consideración la conducta anestésica ante un paciente pediátrico con pectus excavatum.
Caso clínico
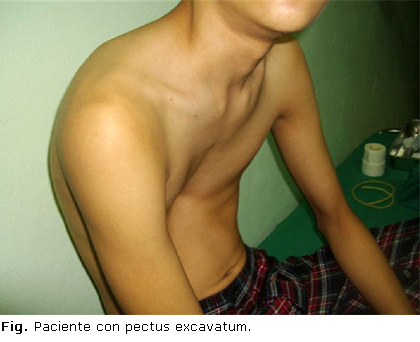
Se recibió a un paciente varón de 15 años de edad, con 58 kg de peso, con pectus excavatum (Fig.), con un retardo mental ligero, que presentó trastornos respiratorios restrictivos documentados en pruebas funcionales respiratorias y refirió dificultad para realizar su actividad física habitual.
El paciente fue programado electivamente para cirugía correctora convencional de la deformidad.
En el preoperatorio se canalizó una vena periférica, se administró medicación pre-anestésica con midazolan a 0,1 mg/kg y atropina 0,5 mg EV. Se monitorizó la tensión arterial de forma no invasiva, se realizó un electrocardiograma en DII, se tomó la temperatura distal y oximetría de pulso. Se procedió a la pre-oxigenación e inducción anestésica con lidocaína a 1 mg/kg, fentanil 3 µg/kg, bromuro de pancuronio a 0,1 mg/kg y diprivan 2,5 mg/kg. Se administró además profilaxis antibiótica con cefazolina a 50 mg/kg. Fue intubado y ventilado con presión positiva intermitente, con un volumen corriente de 7 mL/kg, frecuencia respiratoria 14 resp/min, presión positiva al final de la espiración (PEEP) de 5 mmHg y FiO2 0,4 %. Se siguió la rutina previa de asepsia y antisepsia con agua, jabón e iodo povidona, se le colocó un catéter epidural a nivel torácico T10 desde la región lumbar L2 y se comprobó efectividad del catéter con bupivacaina 0,5 % en dosis de prueba (1/5 del volumen total). Se completó instrumentación anestésica con la canalización de la arteria radial izquierda y vena yugular derecha con un catéter triple lumen 6 FR de 8 cm. Se monitorizó además la tensión arterial de manera invasiva, la presión venosa central (PVC), capnometría, capnografía, diuresis, temperatura nasal y rectal respectivamente y se realizó hemogasometría inicial.
Se administró 50 µg de fentanil epidural y 25 mg de bupivacaina al 0,5 % previa administración de cristaloides EV de 5 a 7 mL/kg. Por otra parte, el mantenimiento anestésico del estado hipnótico se efectuó con una infusión continua en jeringa perfusora con diprivan de 75 a 100 µg/kg/min. El paciente mantuvo buena estabilidad hemodinámica transoperatoria, no requirió apoyo inotrópico, ni transfusión de hemoderivados y con equilibrio metabólico y hemogasométrico adecuados. Se trasladó a la UCI donde se procedió a extubar inmediatamente a su llegada. El control del dolor posoperatorio se prescribió con morfina liofilizada por vía epidural o bloqueo simpático con el anestésico local cuando la EVA excedió el valor de 5. A las 24 horas, por su buen estado general posoperatorio, fue candidato a ser trasladado a la sala, aunque se decidió que permaneciera en la UCI para mejor control de la analgesia por el catéter epidural, no trasladándose al día siguiente. El catéter epidural se le retiró a las 72 horas con un valor de EVA de 3 y se continuó tratamiento con antinflamatorios no esteroideos (AINEs) y dipirona por vía oral.
DISCUSIÓN
La conducta anestésica de estos pacientes guarda estrecha relación con las condiciones clínicas preoperatorias existentes. Se debe prestar especial importancia a las pruebas funcionales respiratorias de indicación obligada en estos pacientes pues en la mayoría de los casos se asocia con fenómenos pulmonares restrictivos y obstructivos de la vía respiratoria que afectan los volúmenes espiratorios forzados (VEF y VEF1) y la capacidad funcional residual, pues al disminuir el diámetro anteroposterior del tórax, se limita la expansibilidad torácica y la adaptabilidad pulmonar. En casos severos pueden aparecer atelectasia o hipoplasia del lóbulo inferior del pulmón derecho que solo mejoran ligeramente tras la corrección quirúrgica.
Las estructuras cardiacas se encuentran estrechamente relacionadas e incluso pueden estar desplazadas lateralmente. Esto puede evolucionar de forma asintomática u ocasionar disritmias de diversos tipos. Es importante en el chequeo preoperatorio realizar electrocardiografía de 12 derivaciones y ecocardiografía transtorácica para determinar la relación con las estructuras cardiacas y evitar accesos accidentales. En algunos enfermos se precisa monitorización ecocardiográfica transesofágica (TEE) durante el procedimiento quirúrgico.
Los padres o tutores deben ser informados por parte del equipo médico sobre los riesgos y beneficios de este proceder y las posibles complicaciones potenciales.
Por otra parte, la anestesia multimodal en pediatría ha ganado adeptos en la actualidad11 ya que permite la combinación de varias técnicas y agentes anestésicos y facilita el abordaje adecuado de la vía respiratoria en combinación con un bloqueo simpático epidural que resulta de gran ayuda en el mantenimiento de la anestesia y en el control posoperatorio del dolor. En pacientes propuestos para intervenciones quirúrgicas torácicas se brinda la posibilidad de realizar fisioterapia respiratoria posoperatoria sin dolor y movilización precoz. No obstante, se debe desestimar su eficacia en pacientes con antecedentes de alergias a los anestésicos locales, aumento de la presión intracraneal, alteraciones del sistema de la coagulación, epilepsia, trastornos neurológicos evolutivos, malformaciones vertebrales, estados hipovolémicos no corregidos, enfermedades angiomatosas e infección cutánea en el sitio o cerca del sitio de inserción del catéter.
Por presentar este caso un retardo mental ligero, se decidió realizar la instrumentación anestésica bajo anestesia general aunque es posible realizarla con anestesia local en niños cooperadores.
Se realizó abordaje epidural solo con una sedación EV previa. El anestésico local que generalmente se utiliza por esta vía es la bupivacaína al 0,5 % de 0,15 a 0,3 mL/kg en bolo y fentanil. Estas dosis son igualmente extrapolables a ropivacaína o levobupivacaína. Algunos autores,12-14 recomiendan el uso de infusión continua de bupivacaína al 0,25 % a razón de 0,5 a 1 mL/kg/h o bupivacaína 0,125 % en infusiones continuas a 0,2 mg/kg/h, en combinación con fentanil (1-2 mg/mL).
La existencia de receptores opioides en todo el sistema nervioso y en el ámbito espinal se encuentran en la sustancia gelatinosa del asta posterior (que es el centro fundamental de la integración de la información nociceptora), donde existe mayor presencia de receptores µ seguidos de K y de d. Una vez fijados, bloquean la transmisión nociceptiva y respetan otras modalidades sensoriales. Algunos autores,15,16 recomiendan la vía epidural en niños pues la combinación de opiodes y anestésicos locales hace que la analgesia obtenida posea una calidad superior por sinergismo ya que el opioide potencia al anestésico local y sensibiliza al nervio periférico al fijarse a sus receptores específicos. La dosis de morfina oscila entre 30-100 µg/kg mientras que para el fentanil se recomiendan dosis de 1-2 µg/kg/h.
Las complicaciones más importantes atribuidas al uso de opioides, independientemente de la vía de administración, son: depresión respiratoria, prurito, náuseas y vómitos o retención urinaria; ninguna de estas fue observada en este paciente. Una variante excelente en caso de aparecer los efectos adversos, es que pueden ser revertidos con el uso de naloxona EV y continuar la analgesia mediante la administración solo de anestésicos locales epidurales.
CONCLUSIONES
Se concluye que el uso de anestesia multimodal en un paciente pediátrico, hizo posible la corrección de forma satisfactoria de un niño con pectus excavatum, por lo que se puede generalizar esta técnica para la corrección quirúrgica de esta enfermedad en instalaciones de salud especializadas en Cuba.
Por otra parte, el uso de anestesia intravenosa con diprivan para mantener el estado hipnótico permite un plano anestésico rápidamente recuperable lo que facilita la extubación precoz y, paralelamente, reserva un potente efecto antiemético18 que contrarresta este efecto indeseable anteriormente descrito para los opiodes.
REFERENCIAS BIBLIOGRÁFICAS
1. Swvoeland B, Medrick T, Nussm D. The Nuss procedure for pectus excavatum correction. AORN Journal. 2001;74(6):828.
2. Malek M, Fonkalsrud E, Cooper C. Ventilatory and cardiovascular responses to exercise in paients with pectus excavatum Chest. 2003; 124:870-82.
3. Sarper A, Necdet Oz, Arslan G, Demircan A. Complete Congenital Sternal Cleft Associated with Pectus excavatum. Tex Heart Inst J. 2002;29:286-7.
4. Lindskog, Gustaf E. Diseases of the Chest Wall. In Throracic and Cardiovascular Surgery with a related pathologies. Pathology Surg Endosc. 2003;17:1609-13.
5. Stanford W, Bowers DG, Linberg E. Silastic Implants for correction of Pectus Excavatum. Ann Thorac Surg. 1972;13:529-36.
6. Suri RK, Sharma RK, Jha NK, Sharma BK. Complete Congenital Sternal Cleft in an Adult: Repair by Autogenous Tissues. Ann Throrac Surg. 1996;62(2):573-5.
7. Ochsner A, De Bakey M. Chone-Chondrosternon. J Thoracic Surg. 1939;8:469-511.
8. Santana Rodríguez N, Hernández Rodríguez H, Gámez García P, Madrigal Royo L. Córdoba Peláez M, Varela Ugarte A. Corrección videotoracoscopica mínimamente invasiva del pectus excavatum. Arch Bronconeumol. 2002;38(8):392-5.
9. Nuss D, Kelly RE Jr, Croitoru DP, Katz ME. A 10 years review of a minimally invasive technique for the correction of pectus excavatum, J Pediatr Surg. 1998 Apr;33(4):545-52.
10. Inge TH, Owings E, Blewett CJ, Balwin CE. Reduced hospitalization cost for patients with Pectus excavatum treated using minimally invasive surgery. Surg Endosc. 2003;17(10):1609-13.
11. López-García JC, Castejón J, Moreno M, Ramírez-Navarro A. Anestesia multimodal infantil: analgesia epidural. Rev Soc Esp Dolor. 2004;7:204.
12. Polaner DM, Berde CB. A practice of anaesthesia for infants and children. Philadelphia: WB Saunders Company; 1993. pp. 451-67.
13. Berde C. Epidural analgesia in children. Can J Anaesthesia. 1994;41:7.555-60.
14. Cohen D. Management of posoperative pain in children. In: Schechter NL. Berde CHB, Yaster M, eds. Pain in infants, children and adolescents. Baltimore: Williams and Wilkins; 1993. pp. 357-83.
15. López-García JC, Castejón Casado J, Ramírez A, Valladares JC, Campuzano C, Colina L. Analgesia epidural lumbar en niños en relación al estrés quirúrgico. Rev Soc Esp Dolor. 2004;11:420-9.
16. López-García JC, Castejón Casado FJ, Palacios Blanco E, Gallego Puertollano R, Rodríguez Banqueri M, Moreno Prieto M. Eficacia comparada de analgesia epidural versus intravenosa pautada en el dolor posoperatorio pediátrico. Rev Soc Esp Dolor. 2004;7. En línea. Consultado enero 20 2011. Disponible en: http://scielo.isciii.es/scielo.php?pid=S1134-80462004000700004&script=sci_arttext
17. Salgado Borges M, Suárez González LM, Acosta Menoya A, Díaz Arteaga Y. El diprivan como reductor de la incidencia de vómitos en niños amigdalectomizados. Rev Ciencias Médicas Pinar del Río 2005;9(3):3-10. En línea. Consultado Octubre 26, 2011. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1561-31942005000300002&lng=es&nrm=iso&tlng=es
Recibido: 20 de enero de 2012.
Aprobado: 10 de abril de 2012.
Correspondencia:
Dr. Néstor Sánchez Nogueira. Cardiocentro Pediátrico "William Soler". La Habana, Cuba.