Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Anestesiología y Reanimación
versión On-line ISSN 1726-6718
Rev cuba anestesiol reanim vol.16 no.3 Ciudad de la Habana set.-dic. 2017
Revista Cubana de Anestesiología y Reanimación. 2017;16(3)
CASO CLÍNICO
Consideraciones anestésicas en la anomalía de Ebstein
Anesthetic considerations in Ebstein's anomaly
Yvonne Y. Cárdenas Torres, Niurka Segura Llanes
Instituto Nacional de Oncología y Radiobiología. La Habana, Cuba.
RESUMEN
Introducción: la anomalía de Ebstein es una rara malformación congénita cardiaca, definida por un desplazamiento apical de las valvas septal y posterior de la válvula tricúspide hacia el interior del ventrículo derecho, en vez de hacerlo a nivel del anillo auriculoventricular, lo cual conlleva un aumento del volumen de la aurícula derecha (megaurícula) a expensas de una reducción del tamaño del ventrículo del mismo lado (auriculización del ventrículo). Causa una significante regurgitación tricuspídea y reducción de la capacidad funcional del ventrículo, dilatación atrioventricular derecha, con arritmias auriculares y ventriculares, las que tienden a hacerse resistentes en ocasiones, o de difícil tratamiento. El desplazamiento del orificio valvular tricuspídeo produce una división del ventrículo derecho en una porción integrada al atrio derecho, lo que constituye "la porción atrializada" del ventrículo derecho, en tanto la porción apicotrabecular y de salida constituye su parte funcional.
Objetivo: presentar la evolución clínico-anestesiológica de una paciente con anomalía de Ebstein.
Caso clínico: paciente de 69 años de edad programada para cirugía electiva en dos ocasiones por diferentes enfermedades oncológicas, portadora de anomalía de Ebstein. Antecedentes de tromboembolismo pulmonar, tres cirugías cardiacas, diabetes mellitus e hipertensión arterial, enfermedad arterial aterosclerótica estable e infarto cerebral media derecha embólico. Se evitaron aquellas condiciones que aumenten el trabajo cardiaco y el consumo de oxígeno.
Conclusiones: el desafío que representa para el anestesiólogo, aquellos pacientes que sufren anomalía de Ebstein puede variar de paciente a paciente, en dependencia del estado físico, el tipo de enfermedad y las técnicas de monitorización.
Palabras clave: anomalía de Ebstein; malformación cardiaca; adulto.
ABSTRACT
Introduction: Ebstein's anomaly is a rare congenital cardiac malformation, defined by an apical displacement of the septal and posterior leaflets of the tricuspid valve into the right ventricle, instead of at the level of the atrioventricular ring, which leads to an increase of the volume of the right atrium (mega atrium) at the expense of a size reduction for the ventricle on the same side (auriculization of the ventricle). It causes a significant tricuspid regurgitation and reduction of the functional capacity of the ventricle, right atrioventricular dilation, with atrial and ventricular arrhythmias, which tend to become resistant at times, or difficult to treat. The displacement of the tricuspid valve orifice produces a division of the right ventricle in a portion integrated to the right atrium, which constitutes "the atrialized portion" of the right ventricle, while the apico-trabecular and exit portion constitutes its functional part.
Objective: To present the clinical-anesthesiological evolution of a patient with Ebstein's anomaly.
Clinical case: A 69-year-old patient, with Ebstein's anomaly, who was scheduled for elective surgery on two occasions for different oncological diseases. History of pulmonary thromboembolism, three cardiac surgeries, diabetes mellitus and arterial hypertension, stable atherosclerotic arterial disease, and right middle cerebral infarction. Conditions that increase cardiac work and oxygen consumption were avoided.
Conclusions: The challenge patients suffering from Ebstein's anomaly represent for the anesthesiologist can vary from patient to patient, depending on the physical state, the type of disease, and the monitoring techniques.
Keywords: Ebstein's anomaly; cardiac malformation; adult.
INTRODUCCIÓN
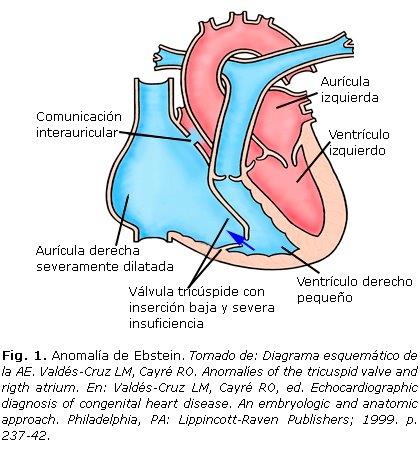
La anomalía de Ebstein es una malformación cardíaca rara que afecta por igual a ambos sexos. El desplazamiento apical de las valvas septal y posterior de la válvula tricúspide, hacia el interior del ventrículo derecho (VD)1 produce una división del VD en una porción integrada al atrio derecho, lo que constituye "la porción atrializada" del VD,2 en tanto la porción apicotrabecular y de salida constituye su parte funcional.1,2 Esto lleva a un aumento del volumen de la aurícula derecha (AD, mega aurícula) (Fig. 1) a expensas de una reducción del tamaño del ventrículo del mismo lado.3
La mayor parte de casos son esporádicos. Su mecanismo de transmisión poligénico multifactorial como en la mayoría de cardiopatías congénitas.4,5 La anomalía fue descrita sobre bases anatomopatológicas, pero el diagnóstico clínico no se realizó en pacientes vivos hasta 1949.
Se puede presentar de forma aislada o acompañada de otras malformaciones cardiovasculares como: comunicación interauricular (CIA) la cual es más frecuente (50 % de los pacientes), estenosis pulmonar valvular (EPV), persistencia del ductus arterioso (PDA), atresia pulmonar (AP). Las formas intermedias como en edades pediátricas superiores y en la adolescencia deben tenerse en cuenta la presencia de cianosis, disnea, fatiga al esfuerzo, intolerancia al ejercicio, palpitaciones, arritmias o insuficiencia cardíaca.6
La anomalía de Ebstein y la CIA predominan en el sexo femenino.3 Algunos pacientes mueren en la infancia a causa de la hipoxia, pero el 40 % llegan a la edad adulta y llevan una vida normal o casi normal. El diagnóstico específico requiere una vista de cuatro cámaras apicales en el ecocardiograma.3,7 Aproximadamente el 25 % de los pacientes sufren episodios de taquicardia auricular paroxística.3,8-14
La principal anormalidad hemodinámica que produce síntomas en la AE es la regurgitación tricuspídea que está relacionada con el grado de regurgitación (Fig. 2).
El principal problema clínico en el adolescente y adulto es la inestabilidad eléctrica, la que puede ser debido a preexcitación ventricular o a taquiarritmias ventriculares de reentrada, flutter auricular o fibrilación auricular debido a la progresiva dilatación auricular o la asociación de ambas, la arritmia tiende a ser recurrente o resistente al tratamiento con drogas.
REPERCUSIÓN HEMODINÁMICA DE LA ANOMALÍA DE EBSTEIN (AE)9,10
En la AE se observa una AD de gran tamaño con miocardio ventricular delgado en su porción inferior. La AD presenta gran llenado, su vaciamiento se dificulta aún más por la resistencia de un VD reducido, y como consecuencia aumenta la presión de la AD con una gran sístole y producción de cortocircuito de derecha a izquierda (por CIA o foramen oval permeable). La porción inferior de la AD posee miocardio ventricular derecho y se contrae en sístole (aunque débilmente), dilatándose e interfiriendo con el llenado ventricular.
VD pequeño y reducido en su porción de salida (obstrucción valvar). El llenado reducido hace caer el volumen sistólico y el flujo pulmonar, esto agrava la presencia de una insuficiencia tricuspídea (IT), de igual modo si la válvula tricúspide es estenótica.
IT o ET. La presencia de IT o estenosis tricuspídea (ET) agrava el llenado de la AD y lo reduce en el VD. Esto se acrecienta con la presencia de trastornos de conducción como bloqueo auriculoventricular (BAV) de 1er. grado, bloqueo completo de rama derecha (BCRD) o Wolff Parkinson White (WPW).
Tabique IA con CIA o foramen oval permeable. Desarrollo de cianosis e ICD.
Factores predisponentes y prevalencia. La AE ocurre a medida que un bebé se desarrolla en el útero. La causa exacta se desconoce, aunque el uso de ciertos fármacos (como el litio o las benzodiacepinas) durante el embarazo pueden influir en el desarrollo de estas malformaciones congénitas. La afección es poco frecuente y es más común en personas blancas.11
Constituye el objetivo de este caso clínico, presentar la evolución clínico-anestesiológica de una paciente con anomalía de Ebstein.
CASO CLÍNICO
Paciente NLA, de 69 años de edad, fue inscrita en el Instituto Nacional de Oncología y Radiobiología (INOR) en octubre de 2014, en su adolescencia fue diagnosticada con AE. En un examen físico fortuito para incorporarse a una escuela militar cuando tenía 14 años, aunque ya refería fatigas, cansancio, disnea ligera al ejercicio y en ocasiones presentaba ligera cianosis. Su diagnóstico fue hecho por ecocardiografía. Fue intervenida de cirugía cardiaca en tres ocasiones con circulación extracorpórea para cierre de CIA, cambio valvular por prótesis biológica y después por mecánica.
Consulta preoperatoria
Antecedentes patológicos personales: tres cirugías cardiacas, diabetes mellitus, politransfusiones, hipertensión arterial esencial, enfermedad arterial aterosclerótica estable, infarto cerebral media derecha embólico.
Historia de la enfermedad
Lleva tratamiento con: digoxina, amiodarona, furosemida, espironolactona, captopril y warfarina. Se mantiene en clase funcional II-III de la NYHA.
Examen físico
IMC> 30. Tumoración de alrededor 4 cm en región submaxilar izquierda. Herida torácica por estereotomía. Edemas bilaterales en las piernas. PA: 160/90 mm Hg.
Exámenes complementarios
Hemograma con diferencial normal. Leucocitos 5,2 × 10-9/L. Hb 11 g/d. Plaquetas 200 × 10-9. Eritrosedimentación 28 mm/h. Glucosa 7,2 mmol/L. Creatinina 67. Ácido úrico 289. Colesterol total 3,4. TGO 72. TGP 36 y orina normal.
Dentro del coagulograma completo se obtuvo valores de TTPA 28, control y paciente normal, coágulo retráctil, plaquetas normales e INR 1,71.
Telecardiograma.No alteraciones pleuropulmonares. Índice cardiotorácico > 0,5 a expensas de cavidades derechas.
Electrocardiograma. Ritmo sinusal, FC normal, Bloqueo completo de rama derecha (BRDHH).
Ecocardiograma. Medidas normales, FEVI normal en reposo, contractilidad global y regional del ventrículo izquierdo conservada en reposo, válvula aórtica normofuncionante, prótesis en posición tricuspídea con gradiente pico de 11 mm Hg y gradiente medio de 6 mm Hg. Velocidad máxima de 1,6 m/s. Gran dilatación de vena suprahepática. Flujograma mitral E> A.
Desde el año 2010 en los ecocardiogramas no hay variación en los gradientes transprotésicos describiéndose dilataciones de cavidades derecha y disminución de ligera a moderada de la función de VD, no cortocircuitos a nivel auricular.
ECO transtorácico. Se describe regurgitación tricuspídea protésica por fístula paravalvular.
ECO transesofágico. Concluye prótesis normofuncionante, no trombos intracardiacos, no cortocircuitos. Score de calcio: 0.
Evolución
Se mantiene en clase funcional II-III estable con seguimiento por consulta cada 6 meses.
Indicaciones de la consulta preoperatoria
Mantener medicación hasta el día de la operación excepto la warfarina que se suspende y se mantiene anticoagulación con heparina no fraccionada a partir que el INR esté por debajo de 2 y lograr un TTPA 2 ½ vez control. Se indicó profilaxis antibacteriana con cefazolina.
Día de la operación
La paciente fue sedada en Sala de Preoperatorio, minutos antes del procedimiento quirúrgico con midazolam 1,5 mg y 50 µg de fentanilo. Se apoyó con O2 por mascarilla facial hasta el traslado al quirófano. Se canalizaron dos venas periféricas y se evitó abordaje venoso profundo (AVP) por antecedentes de arritmias y trastornos tromboembólicos previos. Se tuvo en cuenta que la operación sería una maxilarectomia, cirugía de corta duración (criterio emitido por el cirujano). Aun así, se tomaron todas las medidas a favor del estado cardiaco de la paciente y sus padecimientos crónicos previos que estaban controlados en el momento de la cirugía. Se monitorizaron todos los parámetros vitales los cuales en el momento de la inducción anestésica estaban estables.
La inducción anestésica se realizó con midazolam 0,15 mg/kg, fentanilo 150 µg de fentanilo, utilizándose como bloqueante neuromuscular el atracurio a 0,5 mg, lidocaína 2 % 60 mg. Se ventiló con máscara facial durante algunos minutos y manteniendo una SpO2 de 100 %. La laringe fue pulverizada con lidocaína spray previo a la intubación, que fue fácil y gentil. Se utilizó tubo No 7,5. No hubo cambios hemodinámicos durante el proceder, ni tampoco fue necesaria la utilización de dispositivos accesorios. Se ventiló con modalidad presión, y una mezcla de O2 y N2O 50 % con lo cual se logró una saturación de SPO2 entre 98 y 100 % durante todo el acto quirúrgico. Se agregó a la mezcla de gases isoflurane al 0,5 %, solo por su efecto vasodilatador coronario, la analgesia perioperatoria fue con dipirona 1 200 mg, tramadol 100 mg.
La hemodinamia estuvo estable durante la intervención quirúrgica, la que tuvo una duración de aproximadamente 55 min. Un total 700 mL de ringer lactato fue infundido durante el acto quirúrgico prestándole atención a la restricción de fluidos.
Durante la emergencia anestésica se observó un flutter auricular que remitió espontáneamente. El despertar fue suave y sin otras complicaciones, la paciente no refería dolor, su recuperación fue satisfactoria. Terminó su recuperación en la Unidad de Cuidados Posanestésicos hasta el alta anestésica, y fue trasladada a UCI para vigilancia CV en las primeras horas del posoperatorio.
La segunda intervención fue 8 meses después. Esta vez para la exéresis amplia de un nódulo de mama derecho, se aplicó la misma técnica anestésica, y los mismos cuidados preoperatorios, perioperatorios, esta vez sin la aparición de ninguna eventualidad eléctrica. La recuperación transcurrió sin dificultad hasta el alta para ICU.
DISCUSIÓN
El mayor problema durante la anestesia es la inestabilidad eléctrica con aparición de arritmias, debido a la preexcitación ventricular con arritmias supraventriculares de reentrada, que pueden persistir después de la corrección quirúrgica valvular.1 Por esta razón se evitó el abordaje venoso profundo (AVP), pues su inserción puede ser causa de trastornos embólicos y arritmias.12,18 La ventilación fue ciclada por presión pues se consideró que es la más fisiológica, (ventilación a presión positiva Intermitente). sin grandes cambios del gasto cardiaco (GC) y de la resistencia venosa periférica (PVR), en comparación con la ventilación a presión positiva intermitente (IPPV ), que puede producir disminución del gasto cardiaco (GC) y aumento de la PVR.13
El propofol, a pesar de tener propiedades a favor en cirugías cortas, por la pronta recuperación que dé él depende, no fue utilizado para evitar cambios hemodinámicos que aumentaran el trabajo cardiaco como la hipotensión que puede provocar el diprivan posinducción, sobre todo en pacientes cardiópatas e hipertensos, lo que agravaría aún más el llenado de AD, pues dentro de las causas agravantes del llenado de AD y VD está la regurgitación tricuspídea acompañada de trastornos de conducción, como el BCRD,9,10 situación clínica que está presente en nuestra paciente.
La anestesia fue balanceada, no se decidió aplicar la TIVA por la brevedad del acto quirúrgico y por los recursos que en ella se emplean, dejándola para procedimientos más complicados y de larga duración. La restricción de fluidos es beneficiosa, una excesiva administración de estos puede ir en detrimento del paciente por la hipervolemia que puede provocar sobrecarga cardiaca con aumento del shunt de derecha a izquierda e hipoxemia, además de provocar falla ventricular derecha. El principal problema clínico en el adolescente y adulto es la inestabilidad eléctrica, la paciente presentó flutter auricular, de corta duración (aproximadamente 15 s), que remitió espontáneamente sin necesidad del uso de drogas. Este apareció durante la emergencia anestésica, de la primera intervención; momento crucial donde la paciente reanudó las funciones vitales se despertó y fue extubada; sin embargo, la literatura informa que estas arritmias son en ocasiones de difícil tratamiento con drogas.16 Se reinició anticoagulación 6 horas después del acto quirúrgico, con heparina no fraccionada, previa revisión de la hemostasia y sin sangramiento por herida quirúrgica, para prevenir la aparición posoperatoria de complicaciones tromboembólicas, frecuentes en estos pacientes.14
Los pacientes con debut tardío de la enfermedad y buen estado general al momento del proceder, en general tienen una mejor evolución.
La literatura publica casos aislados, pues la incidencia es muy baja y solo el 5 % sobrevive más allá de la quinta década de la vida.15,16
Actualmente nuestra paciente continúa seguimiento por cardiología y por su cirujano oncólogo respectivamente.
El desafío que representa para la anestesia aquellos pacientes que sufren de anomalía de Ebstein, puede variar de un paciente a otro en dependencia del estado físico, el tipo de enfermedad y las técnicas de monitorización.
Un minucioso control anestésico que evite el aumento del trabajo cardiaco y aumento del consumo de oxígeno, con adecuado control de los líquidos es beneficioso para evitar complicaciones graves en estos pacientes.
REFERENCIAS BIBLIOGRÁFICAS
1. Frescura C, Angelini A, Daliento L, Thiene G. Morphological aspects of Ebstein's anomaly in adults. Thorac Cardiov Surg. 2000;48:2003-8.
2. Martínez García G, Montero García R, Cruz Rodríguez L, Cárdenas Fernández Y, Hernández González A. Anomalía de Ebstein en edad adulta. Rev Cubana Med Milit [Internet]. 2009 Dic [citado 2016];38(3-4 ). Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0138-65572009000300010&lng=es
3. Pico Peña JL. Enfermedad de Ebstein. Presentación de un caso. Revista Cubana de Medicina Intensiva y Emergencias [On line]. 2006 [citado 2016];5(4-06). Disponible en: http//bvs.sld.cu/revistas/mie/vol.5-4-06mie01406.htm
4. Hoffman JIE. Cardiopatías congénitas: incidencia y herencia. Clin Pediatr Nort Am (ed. esp) 1990;1:23-41.
5. Armengol Rofes AJ. Anomalía de Ebstein de la válvula tricúspide. A propósito de 35 casos. An Esp Pediatr. 1996;44:139-44.
6. Liao PK, Feldt RH. Clínica profile of Ebstein's anomaly. Prog Pediatr Cardiol. 1993;2:16-21.
7. Radford DJ, Graff RF, Neilson GH. Diagnosis and natural history of Ebstein's anomaly. Br Heart J. 1985;54:517.
8. Rodríguez Font E, Viñolas Prat X. Causas de muerte súbita. Problemas a la hora de establecer y clasificar los tipos de muerte. Rev Esp Cardiol. 1999;52:1004-14.
9. Liberthson R. Cardiopatías congénitas en el adulto. En: La práctica de la cardiología. Normas del Massachusetts General Hospital. Eagle KA. 2da. ed. Buenos Aires: Editorial Médica Panamericana; 1991. p. 1183-90.
10. Oscar Gómez JR, Rodríguez EL. Anomalía de Ebstein en el adulto. Hospital "Ángela Iglesia de Llano". Rev Posgrado de la Cátedra de Medicina. 2003;129:11-20.
11. Bernstein D. Ebstein anomaly of the tricuspid valve. In: Kliegman RM, Behrman RE, Jenson HB, Stanton BF, eds. Nelson Textbook of Pediatrics. 19th ed. Philadelphia, PA: Saunders Elsevier; 2011. Chap. 424.7. Actualized: 3/15/2016.
12. Anirban Hom Choudhuri, Rajeev Uppal and Megha Khaitan. Laparoscopic cholecystectomy in a patient with Ebstein's anomaly Anesthetic considerations. Saudi J Anaesth. 2012 Jul-Sep;6(3):301-2.
13. Bengtsson IM, Magnoand R, Wickstrom I. Ebstein´s Anomaly-Anaesthetic Problems. A case report. Br J Anaesth. 1977;49:501.
14. Khatib SK, Tadwalkar GV. Anaesthetic implications of Ebstein's anomaly: A report of two cases. Anaesthesia Pain & Intensive Care. 2012;16(1):60-3.
15. Patanè S. Ebstein's anomaly in adult. Int J Cardiol [On line]. 2008 [citado Dic 2016]. Disponible en: www.elservier.com/locate/ijcard
16. Hennebry TA, Calkins HG, Chandra-Strobos N. Successful interventional treatment of an octogenarian presenting with syncope and Ebstein's anomaly of the tricuspid valve. J Invasive Cardiol. 2002 Jan;14(1):44-7.
17. Suárez-D OH, Vargas-Acero LR, Valderrama-Hernández JA. Anestesia epidural para la cesárea en la anomalía de Ebstein. Rev colomb anestesiol [en línea]. 2011 Apr/July [citado Abr 2016];39(2). Disponible en: http://dx.doi.org/10.5554/rca.v39i2.101. Updated on May 21, 2017.
18. Valdés-Cruz LM, Cayré RO. Diagrama esquemático de la AE. Anomalies of the tricuspid valve and rigth atrium. En: Valdés-Cruz LM, Cayré RO, ed. Echocardiographic diagnosis of congenital heart disease. An embryologic and anatomic approach. Philadelphia, PA: Lippincott-Raven Publishers; 1999. p. 237-42.
Recibido. 15 de mayo de 2017.
Modificado: 8 de junio de 2017.
Aprobado: 5 de julio de 2017.
Yvonne Y. Cárdenas Torres. Instituto Nacional de Oncología y Radiobiología. La Habana, Cuba.
Correo electrónico: yvonnecardenas@infomed.sld.cu