Introducción
La anestesia para el angiofibroma juvenil es un reto para el anestesiólogo, pues en general, se comparte el mismo campo quirúrgico con el cirujano. Esta es una de las intervenciones más complejas dentro de la otorrinolaringología y por muy experimentado que sea el cirujano y el anestesiólogo actuante; el sangramiento incoercible es una causa hipovolemia aguda que se produce en un breve período, lleva al shock hipovolémico y a la muerte de no tratarse adecuadamente.
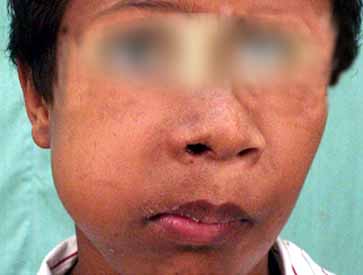
El angiofibroma juvenil es una neoplasia, vasculotumoral agresiva, de histología benigna, con preferencia por el sexo masculino, que se desarrolla en edades prepúberes y púberes. (Fig. 1). Se origina en el agujero esfenopalatino de la nasofaringe y durante su crecimiento ocupa la nasofaringe, la orofaringe, desplaza el velo del paladar, los senos perinasales y espacios faciales, la base del cráneo, tejidos blandos de la cara; a través de los agujeros naturales del cráneo y por compresión ósea.1
La incidencia es de 0,05 % en todos los tumores cráneo-faciales. Aun así, es entre los benignos, el más frecuente de esta región. Lograr una casuística es difícil y requiere de muchos años de dedicación. La posibilidad de invasión al endocráneo es de 10 a 35 % que oscurece el pronóstico de vida y está relacionado proporcionalmente con la juventud del enfermo y la cuantía de las intervenciones quirúrgicas recibidas.
Los principales síntomas que lo caracterizan son epistaxis recurrente y obstrucción nasal con rinorrea. En el examen físico se observa una masa de color rojo púrpura con zonas grises, que ocupa la nasofaringe y que generalmente la ocluye, asimismo en ocasiones puede extenderse a las fosas nasales.2,3,4,5
Los signos que lo identifican son: exoftalmo, enoftalmo, aplanamiento nasal, abultamiento con deformidad de la mejilla y región geniana, escaso desarrollo pondoestatural y de los caracteres sexuales secundarios.6
Por lo antes expuesto, constituye el objetivo de este artículo realizar una actualización sobre la conducta perioperatoria de la anestesia en el angiofibroma juvenil.
Anestesia en el angiofibroma juvenil
El tratamiento de elección es el procedimiento quirúrgico, catalogado dentro de los más complejos del macizo craneofacial. En la literatura no existe una técnica anestésica específica recomendada. La anestesia general orotraqueal es la de elección. Se debe realizar medicación preoperatoria inmediata con midazolam 0,007 mg/Kg más 0,5 mg de sulfato de atropina.7,8,9,10
Siempre es necesario seguir la mayor cantidad de signos vitales posibles con un monitor multiparamétrico como el Nihon Kohden Life Scope modelo OPV 1500K. Dentro de ellos la tensión arterial no invasiva inicialmente (TANI), frecuencia cardiaca (FC), trazado electrocardiográfico, temperatura, diuresis, pulsioximetría y capnografía. También se debe canalizar la vena subclavia derecha para medir la presión venosa central (PVC) y la arterial radial, para medir la presión arterial media (PAM), previo test de Allen.
Una vez realizada la monitorización del paciente se debe proseguir la inducción de la anestesia con propofol (2 a 2,5 mg/kg), lidocaína al 2 % (1,5 a 2 mg/kg) y fentanil 5 µg/kg. Los bloqueadores neuromusculares (BNM) recomendados son vecuronio en dosis de 0,1 mg/kg-1 o rocuronio 0,6 mg/kg-1 para no interferir sobre la FC. Se recomienda realizar el mantenimiento en infusión continua por medio de jeringas perfusoras o bombas de infusión.
Durante el periodo intraoperatorio se deben mantener los parámetros ventilatorios establecidos durante la inducción y garantizar un valor estable de PaCO2 nunca menor de 35 mmHg, valores de PVC entre 10-12 cm H2O, con el objetivo de no introducir sesgos que afectaran diferentes parámetros monitorizados durante la intervención quirúrgica.
En la medida que se adquirió experiencia, se incorporó al procedimiento anestésico determinadas técnicas que influyeron en los resultados que existen en la actualidad, tales como:1,2,3
Hemodilución normovolémica aguda.
Hipotensión arterial inducida farmacológicamente.
Predepósito de la sangre autóloga.
Agentes antifibrinolíticos.
Eritroproyetina.
Angiografia y embolizacion arterial selective.
La transfusión de glóbulos y hemoderivados lleva implícito un gran riesgo,2,4,5,6) por lo que se debe evitar y para ello, se debe asociar a la hemodilución normovolémica.
Hemodilución normovolémica aguda (HNA)
Método que reduce o puede eliminar la necesidad de la transfusión de sangre durante este procedimiento quirúrgico. La HNA se puede hacer con sangre arterial o venosa. La hemodilución puede producir hipovolemia aguda, hipotensión, hipoxia y daño hístico.2,3 También, puede interferir con la tendencia del organismo de aumentar el gasto cardiaco, que es el mecanismo compensatorio primario por reducción del contenido sanguíneo de oxígeno. Finalmente, con una cantidad reducida de hemoglobina (Hb) y la resultante disminución de la disponibilidad de oxígeno, es importante monitorizar la perfusión hística, el cambio del hematocrito (Hcto) y el estado de la volemia.10,11,12,13,14,15,16,17
El procedimiento consiste en cambiar un determinado volumen de sangre por cristaloides (relación 1:3 con el volumen extraído) o coloides (relación 1:1) previo al procedimiento quirúrgico. El objetivo de las soluciones cristaloides es promover la restauración de la presión de llenado cardiaco, sin producir sobrecarga de volumen.
Con relación a los coloides tienen moléculas para las cuales las membranas capilares son relativamente impermeables. Son oncóticamente activas y producen una expansión efectiva con poca pérdida hacia el espacio intersticial. La persistencia en el espacio vascular aumenta la duración de su acción. Se necesita menos volumen para expandir el espacio intravascular. Soluciones de este tipo son el hidroxietil starch, los dextranes y las poligelatinas.11,12,13,14,15,16,17,18
Existen varias soluciones de hidroxietil starch. El más usado es el hetastarch, un polímero conformado por moléculas con un peso molecular que oscila entre 10 000 y 100 000 daltons. Se presenta en soluciones al 6 % con una osmolaridad de 310 mosm y una presión coloido osmótica de 30 mmHg. Su vida media plasmática oscila entre 8 h y 17 días.4,5,6 La mitad de la solución se elimina muy lentamente y buena parte de este porcentaje puede persistir por semanas en el sistema monocito macrófago. El único efecto adverso clínicamente importante es la alteración de la coagulación. Puede disminuir el fibrinógeno, el factor Vlll, el factor de Von Willenbrand, la función plaquetaria, y prolongar el TP y el TPT. Aunque se ha descrito que la coagulopatía aparece con dosis mayores de 20 ml/kg, se puede presentar por efecto idiosincrasia en dosis menores.4,18
Los dextranes son polisacáridos. Los dos más ampliamente usados son el dextrán 70, que tiene un peso molecular promedio de 70 000 daltons y se presenta en soluciones al 6 %, tiene 30 % de retención intravascular después de 24 h y el dextrán 40 tiene un peso molecular de 40 000 dalton, se presenta en soluciones al 10 %. Produce una expansión más corta que el dextrán 70, pero tiene un poder osmótico mayor. EI dextrán es eliminado principalmente por vía renal sin cambios, pero algún porcentaje es captado por el sistema monocito macrófago. Tiene efecto antitrombótico pues puede inhibir la agregación plaquetaria y leucocitaria. El uso de dextrán a altas dosis ha causado sangramiento por lo que se aconseja no usar más de 1000 a 1 500 mL en menos de 24 h. Se ha publicado falla renal con el uso del dextrán 40, que por su rápida excreción renal aumenta la viscosidad urinaria lo que causa obstrucción de los túbulos renales.5,6,7,8,9) Las reacciones anafilácticas se presentan entre 0,03 y 0,07 % y pueden llegar a ser fatales. Se ha documentado alteración de la respuesta inmune a largo plazo. El uso de estas soluciones altera las pruebas cruzadas, debido a que se unen a los antígenos eritrocitarios.1,3,7
Las gelatinas son los preparados coloides más utilizados en nuestro medio. Son soluciones isotónicas con un peso molecular de 35 000 daltons aproximadamente, derivadas de colágeno modificado. Pueden ser almacenados a temperatura ambiente hasta por 5 años y tienen baja incidencia de reacciones anafilácticas. Su vida media es de 2 a 4 h.5,8
Entre las ventajas de los coloides está corregir el déficit de volumen de forma rápida y efectiva y prevenir la presentación de edema pulmonar. Las desventajas son su alto costo, así como los efectos adversos ya nombrados.
Terminada la intervención quirúrgica, se debe reinfundir la sangre autóloga extraída momentos antes del inicio del proceder quirúrgico.7,8,9 Tiene la ventaja que además de los componentes celulares de la sangre, se reinfunden factores de coagulación y algunas otras sustancias que no están presentes o no son funcionales en las transfusiones heterólogas o en los sistemas de autotransfusión intraoperatoria; además, es mucho más barata que la transfusión autóloga preoperatoria y no requiere de semanas de preparación prequirúrgica. El principal riesgo de esta técnica es la coagulopatía dilucional. Hay estudios que muestran que la hemodilución normovolémica no es un factor de riesgo significativamente mayor que otras técnicas de transfusión autóloga para presentar coagulopatías.10
Hipotensión arterial inducida farmacológicamente
La hipotensión arterial inducida farmacológicamente, anestesia hipotensiva, es una técnica utilizada dentro del operatorio que ayuda a minimizar la pérdida de sangre y disminuye la necesidad de transfusión. Su cuidadosa aplicación puede hacerse sin riesgo en la mayoría de los pacientes, que incluye los niños y para una variedad de procedimientos quirúrgicos.18,19,20
Esta técnica supone una disminución controlada de la presión sanguínea y se define como una reducción de la presión sistólica entre 80-90 mmHg. Una definición alternativa es una disminución de la presión arterial media a 50-70 mmHg en un paciente normotenso.18,19,20
Las contraindicaciones de la hipotensión inducida incluyen las que se asocian a la hipoxemia como la enfermedad cardiovascular y anemia severa. Otras enfermedades cardiovasculares, como la insuficiencia cardiaca congestiva e hipertensión mal controlada, excluyen el uso de la anestesia hipotensiva. El aumento de la presión intracraneal y la enfermedad coexistente del sistema nervioso central son contraindicaciones adicionales.18
El anestesiólogo debe estar consciente de las especiales consideraciones fisiológicas durante la hipotensión inducida. Para el sistema nervioso central, la circulación cerebral se debe mantener dentro de un rango para que sea suficiente el oxígeno disponible y entregado al cerebro para impedir la isquemia. El rango de la presión arterial media se debe mantener en niveles entre 50-70 mmHg, aunque otro método para determinar el rango es no reducir la presión arterial más de 30-40 mmHg por debajo de las lecturas iniciales realizadas al paciente.19,20
En el sistema respiratorio, la hipotensión inducida afecta al cambio del gas pulmonar por aumento del espacio muerto alveolar y aumento del shunt intrapulmonar. Por lo tanto, la monitorización frecuente de los gases arteriales en sangre, combinado con la ventilación controlada es necesaria para mantener la normocapnia en el paciente.10,11,12,13,14
En el sistema cardiovascular, durante la hipotensión, el flujo sanguíneo al corazón puede precipitar isquemia en pacientes con función coronaria alterada. Sin embargo, en pacientes con miocardio normal los sucesos isquémicos son infrecuentes.13,14
En el riñón, la hipotensión inducida puede reducir el flujo sanguíneo renal y comprometer la perfusión. La monitorización de la diuresis durante este periodo es necesaria para asegurar un suficiente flujo sanguíneo renal. La evidencia de una adecuada perfusión es una diuresis de 0,5 a 1 mL/kg/h.10,11,12,13,14
La hipotensión intencionada se logra con una variedad de agentes farmacológicos y suplementos no farmacológicos. Aunque hay otras técnicas, los agentes farmacológicos pueden dividirse generalmente en dos categorías: vasodilatadores periféricos y agentes inhalatorios. Los dos vasodilatadores comúnmente utilizados son: nitroprusiato sódico (NPS) y nitroglicerina (NTG).16,17,20
NPS: Actúa al relajar el músculo liso vascular, con un inicio de acción rápido y duración breve. Su influencia primaria está sobre los vasos arteriolares y venosos; pero sin importantes efectos miocárdicos. Se requiere gran cuidado en su administración por su potencia, toxicidad por el cianuro, efectos cardiovasculares e hipotensión de rebote. Dentro de la gama de efectos, la taquicardia puede esperarse y contenerse con beta-bloqueantes en pequeñas dosis.16,17
NTG: La nitroglicerina reduce la presión sanguínea por relajación del músculo liso venoso y como el NPS, tiene un inicio de acción rápido y corta duración. La NTG es menos tóxica que el NPS y tiene menos efecto de rebote que aparece al cesar la perfusión intravenosa (IV); sin embargo, tiene más dificultad para ajustar el nivel de hipotensión porque es menos potente que el NPS para reducir la presión arterial.16,17
En Estados Unidos, se creó en 1996 la Asociación Nacional de Cirugía y Medicina y Sangre (NABMS de sus siglas en inglés National Association of Bloodless Medicine and Surgery), la cual fundamentó el principio de la sangre es costosa, peligrosa y en ocasiones, impredecible.3,4,5,6
En la actualidad, solo la autotransfusión es considerada una alternativa segura a la transfusión de sangre autóloga (TSH).6
Predepósito de la sangre autóloga (PDA)
La primera publicación que habló sobre el método de PDA data de 1921 y desde entonces no ha variado ostensiblemente la metodología utilizada. El paciente realiza las donaciones una o más veces (según el estimado necesario para la operación) durante los días o semanas que preceden a esta. Se deben realizar extracciones de 350 a 400 mL en intervalos de 2 a 7 días. Por lo general, se puede colectar más de 1 L durante los 15 días previos al ingreso. La sangre colectada puede ser almacenada en estado líquido como sangre total o ser separada en sus componentes principales, glóbulos rojos y plasma, que puede congelarse para preservar los factores lábiles de la coagulación. Las células rojas también pueden ser conservadas en estado de congelación. Esta técnica es generalmente usada en pacientes que requieren grandes volúmenes durante la intervención quirúrgica. Es posible colectar las unidades requeridas sin cambios significativos en el estado del paciente, si se mantienen los intervalos recomendados durante las extracciones.12,13,14,15,16
El PDA es una de las técnicas de autotransfusión menos costosas y más efectiva:
Selección de pacientes para PDA: Los criterios de selección no son tan estrictos como para los donantes convencionales, pues es necesario tener en cuenta que el procedimiento debe considerarse parte del tratamiento que recibe para su enfermedad. Antecedentes de enfermedades malignas, hepatitis u otras no descartan al posible donante autólogo.18
Edad: No es un factor limitante si no está asociada con otra contraindicación clínica; sin embargo, en la edad avanzada (sobre los 70 años) y en pacientes de 13 a 19 años, el factor limitante puede estar dado por las condiciones físicas que deben ser evaluadas adecuadamente por el médico.
Peso: Un donante que pese 50 kg o más puede dar de 350 a 400 mL. En los pacientes clínicamente elegibles que pesen menos de 50 kg, las extracciones se podrán hacer a razón de 7 mL/kg de peso corporal cada vez.
Hematócrito: El hematócrito previo a la flebotomía, inicialmente no deberá ser menor que 34 %, esto se chequeará antes de cada extracción y no debe procederse a la sangría si es de 30 % o menos.
Intervalos de donación: Los intervalos deben ser 2 a 3 días. Entre la última donación y la operación, el intervalo no debe ser menor de 72 h.
Determinación del hematocrito: El hematócrito en el rango de 25-30 % proporciona un compromiso óptimo entre contenido de oxígeno y fluidez de la sangre cuando existe una normovolemia y una función cardiovascular aceptable. Existen cambios en la fracción globular, relacionados con el hematocrito, por la ligera disminución que pudiera experimentar después de la extracción, lo cual se repone entre 2 y 5 días más tarde.11,12,13,14,15 La sangría no debe exceder de 350 a 450 mL con un intervalo de donación de 2 a 3 días.
La cantidad de sangre para extraer en la hemodilución es determinada por la siguiente fórmula:
V = EBV x (HCTi - HCTf) / HCTav.
Donde V = cantidad de sangre extraible, EBV = volumen estimado de sangre, HCTi = Hcto inicial, HCTf = Hcto final, y HCTav = promedio de HCTi y HCTf.10,15
Siempre que se utilice este método añadirse suplemento de hierro. La estimulación de la eritropoyesis tras las donaciones (4 a 5 veces la basal) es el principal mecanismo de reposición de la anemia de modo fisiológico en estos procedimientos. El hierro es el elemento indispensable para que esta respuesta sea adecuada. Cada cantidad donada implica la pérdida de 200 mg de hierro. Se recomienda iniciar un tratamiento con hierro de forma oral desde la primera donación o, si es posible desde una semana antes a una dosis como mínimo de 325 mg de sulfato ferroso 3 veces al día, en caso de intolerancia se puede administrar de forma parenteral, y valorar los efectos adversos de estos preparados. El tratamiento se debe prolongar como mínimo hasta un mes posterior a la intervención. Se recomienda en algunos programas una prolongación de varios meses para repleciones con mayor seguridad los depósitos férricos, este tipo de tratamiento depende del sexo, tipo de intervención y número de bolsas extraídas. Algunos programas han demostrado mejor tolerancia al hierro asociándolo al suplemento oral de ácido fólico.
Contraindicaciones
En caso de un incremento en la demanda de oxígeno, (fiebre e hiperventilación) o tratamiento con agentes beta bloqueadores, la respuesta cardiaca a una disminución en los transportadores de oxígeno puede ser insuficiente o bloqueada y presenciarse en pacientes con coagulopatías.5,6 Entre ellas se encuentran:
Angiografia y embolización arterial selectiva
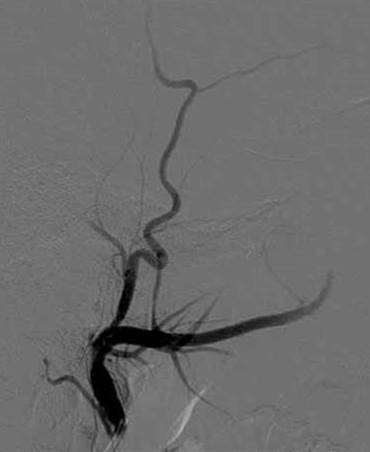
Consiste en la introducción de un medio de contraste al sistema arterial que permite visualizar la red vascular e identificar el sitio sangrante y/o la lesión. La embolización se puede efectuar con diferentes materiales (polivilínico, duramadre, gelfoan). Se debe estudiar la irrigación nasal, es decir, la vascularización proveniente de los sistemas carotídeos externo e interno. Es un procedimiento alternativo con indicaciones precisas debido que se pueden presentar complicaciones en 1-2 % de los pacientes (Figs. 2 y 3).
Está indicado fundamentalmente en el estudio y/o tratamiento de: epistaxis que no ceden con tratamientos habituales (taponamiento nasal, ligadura arterial), tumores vasculares (angiofibroma juvenil, hemangioma), malformaciones arteriovenosas, traumatismos con rotura de arteria y/o formación de pseudoaneurisma, epistaxis posterior a cirugía y telangectasia hemorrágica hereditaria. Pueden ocurrir complicaciones graves principalmente el infarto pulmonar y cerebral. También puede producirse lesiones isquémicas de diversos pares craneanos. Actualmente también se pueden utilizar:
Agentes antifibrinolíticos: Los agentes antifibrinolíticos inhiben la fibrinólisis que podría repermeabilizar un vaso sangrante.12,13,14,15,16 Estos agentes se han utilizado con éxito en el control del sangrado quirúrgico de los órganos que tienen altas concentraciones de factores activadores de plasminógeno (saliva, cerebro, mucosa gástrica y próstata). Son utilizados para evitar el resangrado.19 Dentro de ellos:
Ácido épsilon amino caproico (EACA), ácido tranexámico (TXA) y análogos de la lisina. Muestran buenos resultados al ser administrados de manera profiláctica, pero su eficacia disminuye si se administran después de que se presentan los síntomas del sangrado. No existe evidencia médica que indique que el uso de estos fármacos incremente el riesgo de complicaciones trombóticas. El EACA tiene una efectividad y confiabilidad muy parecida a la de la aprotinina, con un costo tres veces menor, por lo que debe ser preferido como fármaco antifibrinolítico de elección.21,22,23
Aprotinina: Ha mostrado mejorar la hemostasia de pacientes con alteraciones explicadas bien sea por la anticoagulación utilizada o por las alteraciones causadas en la estructura de los receptores plaquetarios con el uso de las máquinas de circulación extracorpórea. Esquemas de administración: uno de dosis alta que consiste en una dosis inicial de 2.000.000 de unidades inactivadoras de kallicreina (KIU) y 500.000 KIU/hr en infusión continua durante la cirugía; y un esquema de dosis baja que se realiza administrando 1.000.000 KIU al inicio de la cirugía y una infusión continua de 250.000 KUI/hr durante la intervención. Algunos artículos concluyen que la efectividad de la aprotinina es mayor que la de los análogos de lisina, disminuye los requerimientos transfusionales y las reintervenciones posoperatorias por sangrado.22,23
Desmopresina (Deamino-D-arginina Vasopresina-DDAVP). Este es un análogo de la vasopresina. El DDAVP ha traído grandes beneficios en el tratamiento de la hemofilia y la enfermedad de Von Willebrand. Es una excelente opción para reducir las pérdidas intraoperatorias de sangre de estos pacientes. La terapia con DDAVP ha mostrado ser efectiva en el tratamiento de pacientes con alteraciones plaquetarias secundarias a enfermedad renal crónica, cirrosis hepática y uso de aspirina, sobretodo en pacientes que se someten a by pass coronario luego de una ingesta crónica de esta. A pesar de que la desmopresina ha mostrado beneficios en el tratamiento de pacientes con alteraciones de la coagulación, no ha mostrado ningún beneficio en pacientes sin coagulopatía de base, tampoco se muestran beneficio de su uso para enfermos con problemas hemorrágicos intra o posoperatorios comparado, con los demostrados beneficios de la aprotinina y los análogos de la licina.23,24,25
Beneficios de la transfusión autóloga
Las ventajas del método son muchas ya que el empleo de su misma sangre excluye el riesgo (aunque remoto en la sangre correctamente estudiada) de transmisión de enfermedades, debida sobre todo al periodo de ventana, que es el tiempo que transcurre entre el momento del contagio de una enfermedad y la posibilidad de su detección con un análisis de sangre.15,16,17,18
También el hecho de emplear la propia sangre previene la sensibilización, es decir, la formación de anticuerpos contra algún elemento de la sangre transfundida que el individuo no reconoce como propia. Esto conlleva a:16,17,18,19,20,21,22,23,24,25
Seguridad del paciente
Menor riesgo de trombosis
Ausencia de transmisión de infección
Ausencia de incompatibilidad sanguínea
Ausencia de problemas inmunológicos
Ahorro financiero
Evita el uso inadecuado de componentes de la sangre
Evita el inadecuado uso de sangre
Disminuye la transfusión de sangre homóloga
Consentimiento del donante
Toda solicitud de donación autóloga ha de ser firmada como aceptación por el donante tras una explicación del procedimiento pormenorizando sus riesgos y ventajas. En caso de donaciones pediátricas o de menores de 18 años el consentimiento ha de ser firmado por los padres o tutor correspondiente. El paciente firmará también el consentimiento para que sus donaciones sean empleadas como homologas en caso de no preciarles para su intervención. Así mismo, si está regulado en el programa para evitar riesgos, el paciente ha de considerar que en caso de encontrarse marcadores serológicos de infectividad en sus unidades, no se continuará con las donaciones y las bolsas serán eliminadas.19
Uso de la eritropoyetina
La eritroproyetina es una hormona humana de producción renal, obtenida mediante técnica de replicación genética. Estimula la médula ósea para incrementar la producción de hematíes. Se puede administrar en dos formas o regímenes: 20) Régimen I. 4 dosis de 600 mg/kg. subcutánea o EV, 2, 3 o una semana antes de la IQ, última dosis el día de la IQ para un total de 2400 mg/kg. Régimen II. 15 dosis EV o subcutánea con 300-500 mg/kg iniciando 9 días antes de la IQ y hasta 4 días después de esta para un total de 4500-7500 mg/kg.
El procedimiento quirúrgico es el tratamiento de elección para los enfermos que padecen esta enfermedad. Por ser un tumor hipervascular que se desarrolla en el macizo craneofacial, en edades jóvenes de la vida, cuya resección se realiza a ciegas con un sangramiento muy elevado, se deben tomar medidas de seguridad pues el pronóstico puede ser sombrío.21
La exéresis quirúrgica del angiofibroma juvenil constituye un verdadero reto para el equipo quirúrgico por lo que se preconiza la embolización preoperatoria, así como asociar en el intraoperatorio la hemodilución y la hipotensión controlada farmacológicamente. El predepósito de sangre autóloga en los pacientes que puedan donar constituye una ventaja.21 Las pautas transfusionales deben considerarse en este tipo de proceder quirúrgico.25
Conclusiones
Se concluye que la exéresis quirúrgica del angiofibroma juvenil es una intervención de alto riesgo. El equipo de trabajo constituye un elemento primordial. La asociación de hipotensión inducida, hemodilución hipovolémica y predepósito de sangre autóloga son los pilares fundamentales para la mejor evolución de estos pacientes.