Introducción
Los pilares de la anestesia general comprenden varios aspectos: hipnosis, amnesia, analgesia, relajación muscular, control sobre el sistema nervioso autónomo y un adecuado cuidado de la homeostasis. Para lograrlos se han empleado históricamente varios agentes farmacológicos desde el éter, óxido nitroso, agentes halogenados, pasando por la anestesia balanceada donde se combina la técnica inhalatoria con un opioide, la anestesia total intravenosa, hasta la anestesia libre de opioides; la cual en los últimos años, surgió en un intento por disminuir los efectos adversos de este grupo farmacológico.
Lograr suplir la función que tienen los opioides potentes en el perioperatorio es un reto farmacológico. Para ello varias drogas con sitios de acción diferentes como ketamina, lidocaína, dexmedetomidina, sulfato de magnesio y otros se usan con buenos resultados y en diferentes combinaciones.1
Distintos protocolos han sido probados con el objetivo de encontrar la sinergia adecuada de esta “bomba farmacológica”. En la mayoría se dosifica basado en dosis por kilogramo de peso, tanto para la dosis de carga como para el mantenimiento, a pesar de que se sabe que diferentes características de los pacientes como: peso, estatura, edad, género, influyen activamente en la cinética del fármaco, y si no se toman en cuenta, las concentraciones plasmáticas finales suelen ser erróneas, se pierde la ventana terapéutica deseada y existe sobre e infra dosificación, además de efectos adversos y complicaciones.2
Los modelos farmacocinéticos consisten en ecuaciones matemáticas basadas en patrones compartimentales. Toman en cuenta diferentes características de los pacientes para calcular volúmenes de distribución, aclaramiento, constantes de transferencia entre compartimientos y tiempos de decremento, con el propósito de predecir y mantener constantes las concentraciones plasmáticas y en sitio efecto. Características como la obesidad hacen que los modelos sean cada vez más complejos para intentar ajustarse a esta particularidad.
A pesar de todo el esfuerzo por crear los mejores modelos de perfusión, el escenario ideal para la administración de fármacos anestésicos consiste en la valoración objetiva del efecto del fármaco mediante la monitorización de profundidad anestésica y del dolor. En los últimos años la preocupación no solo es que el paciente presente un despertar intraoperatorio y desarrolle recuerdos y estrés postraumático sino también el lado opuesto. Es decir, un exceso de hipnosis que provoque las ondas de supresión cerebral relacionadas, según varios estudios, con morbilidad posoperatoria como delirio y disfunción cognitiva; por lo que es menester monitorizar la hipnosis tanto en esta técnica libre de opioides como en cualquier anestesia general.
Diferentes monitores permiten medir dicho efecto a través de las ondas del electroencefalograma. Estas se detectan por electrodos colocados en la frente del paciente y se analizan con el software qCON (índice de nivel de conciencia), que entrega un número y una gráfica sobre los cuales se toman decisiones importantes para guiar la infusión de fármacos.3
La analgesia en el período perioperatorio también debe ser óptima pues su adecuado control influye directamente con el desenlace del paciente, estancia hospitalaria, compensación adecuada de patologías de base y una menor morbilidad. Los monitores de analgesia se encuentran aún en período de desarrollo. Actualmente se dispone de varios métodos, cada uno con sus respectivas controversias pero aportan información valiosa. El monitor qNox interpreta las ondas del electroencefalograma y mediante un análisis emite un valor que indica la probabilidad que tiene el paciente de responder a un estímulo doloroso, información también útil para guiar la infusión de fármacos según los diferentes momentos quirúrgicos.
Por lo antes expuesto el objetivo de la investigación fue describir el caso clínico realizado con la técnica de anestesia libre de opioides.
Presentación del caso
Paciente de género femenino, de 18 años de edad con obesidad grado II a la cual se le realiza una colecistectomía laparoscópica con la técnica anestésica total intravenosa y libre de opioides, guiada por índice de profundidad anestésica qCON y de probabilidad de responder a un estímulo doloroso qNOX (índice de probabilidad de responder a un estímulo doloroso).4,5
Estatura: 150 cm; peso: 85 Kg; Índice de Masa Corporal: 37 Kg/m2. Examen físico y exámenes complementarios dentro de normalidad.
En el preoperatorio inmediato se administra metoclopramida en dosis de 10 mg intravenoso (IV), omeprazol en dosis de 40 mg IV, ketorolaco en dosis de 60 mg IV y dexametasona en dosis de 8 mg IV.
Se monitoriza frecuencia cardíaca, frecuencia respiratoria, tensión arterial no invasiva, temperatura periférica y electrocardiografía continua derivación DII y V5, mediante monitor Dragerinfinity vista. Se emplea en hemisferio izquierdo el monitor Conox de quantium medical®. Mediante el análisis continuo de parámetros electroencefalográficos dicho monitor calcula los siguientes índices: qCON, qNOX, además de electromiografía de los músculos de la cara y un radio de supresión cerebral.
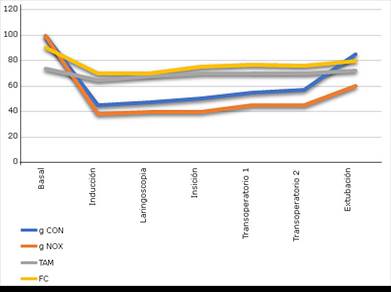
Se describen los signos vitales y parámetros basales (Fig.) los cuales se obtuvieron en diferentes momentos del transoperatorio en: estado basal, inducción anestésica, intubación, incisión quirúrgica, transoperatorio (1 a los 15 min de la incisión; 2 a los 30 min de la incisión), y finalmente al momento de la extubación. La tensión arterial media tuvo una variación entre 65 y 75 mmHg. La frecuencia cardíaca entre 65 y 90 latidos por minuto, el qCon entre 43 y 58 y qNox entre 38 y 45.
Fármacos empleados
Propofol, dilución 20 mg/mL. Modelo farmacocinético de Schinder con peso corregido por ecuación de Servin, mediante jeringuilla perfusora mindray® modo TCI.
Lidocaína, dilución 8 mg/mL. Modelo farmacocinético Kuipers.
Ketamina, dilución 4 mg/mL. Modelo farmacocinético de Clements 250.
Dexmedetomidina, dilución 4 mcg/mL. Modelo farmacocinético de Hannivoort.
Sulfato de magnesio, dilución 40 mg/mL. Infusión en mg/kg/h.
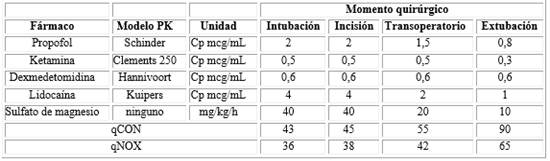
Las concentraciones y dosis empleadas en los diferentes momentos del transoperatorio para los agentes empleados en modo TCI y en modo infusión están descritas se describen en la tabla. Además se empleó rocuronio como relajante muscular en dosis única de 0,6 mg/kg de peso corporal durante la inducción.
Para garantizar el flujo adecuado de las infusiones se abordaron dos accesos venosos periféricos con un catéter venoso calibre 18 G. Las infusiones se colocaron de proximal a distal de menor a mayor flujo respectivamente, minimizando el espacio muerto con un previo cebado. Las variaciones de las concentraciones plasmáticas se realizaron según la monitorización de qCON para mantenerla entre 45 y 55 y el qNOX por debajo de 50. Los datos fueron obtenidos y registrados en los diferentes momentos del transoperatorio previamente descritos: estado basal, inducción anestésica, intubación endotraqueal, incisión a los 15 y 30 min de la incisión y en la extubación.
Las concentraciones plasmáticas de propofol se cambiaron entre 2 mcg/mL en el momento de la intubación hasta 1 mcg/mL en el momento de la extubación. La lidocaína se empleó en una concentración plasmática de 4 mcg/mL en la inducción anestésica, 2 mcg/mL en el transoperatorio y a 1 mcg/mL al momento de la extubación. La dexmedetomidina se mantuvo siempre en 0,6 mcg/ml y la ketamina a 0,5 mcg/mL.
El sulfato de magnesio se infundió a 40 mg/kg/h hasta el momento de la incisión quirúrgica, luego a 20 mg/kg/h hasta el momento de extraer la vesícula biliar y finalmente a 10 mg/kg/h hasta el momento de la extubación. Se realizó también infiltración de puertos de laparoscopia con bupivacaína al 0,25 % 10 mL e irrigación del lecho de la vesícula también con bupivacaina al 0,5 % 10 mL, dosis total de bupivacaína 75 mg.
El proceder quirúrgico concluyó sin datos de relevancia a los 60 min. La recuperación entre la finalización de la cirugía y la extubación fue de 10 min, la cual se efectuó en plano profundo sin tos ni ningún otro evento. No fue necesario emplear reversión de relajante muscular.
La evaluación del dolor fue mediante escala visual análoga (EVA) manifestando 2, 3 y 2 puntos a los 30 min, 60 min y a las 4 h respectivamente. No se emplearon fármacos adicionales para rescate de dolor posoperatorio. La estadía en sala de recuperación posanestésica fue de 4 h y con evolución favorable, un puntaje de 19/20 en la escala de recuperación posanestésica de Aldrete modificada para cirugía ambulatoria. Se indica alta a domicilio.
Discusión
Es necesario conocer el efecto que tienen estos fármacos sobre todo en la estabilidad hemodinámica ya que el propofol, la lidocaína, la dexmedetomidina y el sulfato de magnesio, por diferentes mecanismos contribuyen a la hipotensión y bradicardia. En contraparte la ketamina tiene una función vital pues al presentar en su mecanismo de acción una inhibición de la recaptación de noradrenalina en el receptor presináptico, se contrapone a los mencionados efectos y evita que disminuyan las cifras de tensión arterial y de la frecuencia cardíaca.6 El caso presentado mantuvo cifras de tensión arterial media y de frecuencia cardíaca adecuadas gracias a esta asociación.
Los fenómenos de hiperalgesia o tolerancia aguda han sido investigados durante los últimos años.7,8 Es sabido que la administración de opioides puede generarlos e incrementar las necesidades analgésicas posoperatorias. Se observó que a pesar de no haber empleado opioides ni en el transoperatorio ni en el posoperatorio, la paciente en la valoración de EVA tuvo puntajes por debajo de 3 puntos.
Las náuseas y vómitos son otra complicación común en el perioperatorio, por lo general se valora el riesgo de cada paciente según sus características y tipo de intervención quirúrgica, para con ello instaurar una terapia multimodal capaz de prevenirlos. No obstante, en algunas ocasiones es de difícil tratamiento pues los opioides poseen receptores en el área postrema que actúan como desencadenantes de estos. Es bien conocido que el propofol tiene una función importante porque previene las náuseas y vómitos, y si además se emplea la técnica anestésica libre de opioides es de esperar que esta complicación tenga menor incidencia.9
El hecho de que se tratara de un paciente del género femenino, obesa y con procedimiento quirúrgico por vía laparoscópica aumenta la posibilidad de presentar factores de riesgo como las náuseas y vómitos; sin embargo, el uso de infusión de propofol como la anestesia libre de opioides y la profilaxis farmacológica permitieron que esta paciente no presentará dichas complicaciones.
Los trastornos del sueño son más habituales tras administrar opioides, por lo que la técnica libre de opioides ha sido empleada en casos de narcolepsia y es atractiva desde el punto de vista de la farmacodinamia en casos de apnea obstructiva del sueño, pues los opioides pueden producir depresión respiratoria en el posoperatorio.
La paciente presenta como comorbilidad obesidad grado II la cual puede predisponer a trastornos del sueño como apnea obstructiva y retención de CO2. No obstante, no se evidenciaron este tipo de complicaciones.10
El íleo paralítico posoperatorio en muchas ocasiones se produce luego de una cirugía abdominal, lo que aumenta la estadía hospitalaria. Los mismos opioides por su mecanismo de acción son capaces de inhibir la peristalsis. La manipulación quirúrgica, la hipoperfusión esplácnica, la descarga simpática mediada por el sistema nervioso autónomo como respuesta al estrés y el desequilibrio electrolítico contribuyen también directamente a la aparición de dicha complicación. La lidocaína intravenosa mejora la recuperación gastrointestinal; también tiene acción antinflamatoria, por lo que es capaz de mitigar la hiperalgesia producida por opioides, mejora el dolor posoperatorio, disminuye los requerimientos de otros fármacos anestésicos y se la asocia como neuroprotectora.11
Algunos estudios reportan que la morfina es capaz de incrementar el tamaño tumoral, así como el número de metástasis del cáncer de pulmón debido a que el receptor de crecimiento tumoral del cáncer de pulmón es coactivado por los receptores mu, estos son propios de todos los opioides. En pacientes oncológicos se intenta demostrar mayor supervivencia cuando se evita el uso de opioides, esto con resultados aún no muy claros pero que deberían ser evaluados al momento de elegir si usar o no opioides.12
La dexmedetomidina usada como coadyuvante o agente hipnótico principal contribuye a disminuir el consumo de anestésicos en el transoperatorio, además disminuye los requerimientos posoperatorios de analgesia, relacionándose con menor cronicidad del dolor. Otros efectos como la neuroprotección hacen de este fármaco una alternativa cada vez más importante en el período perioperatorio.13
La ketamina se ha empleado desde hace mucho tiempo y la gran experiencia recolectada ha enseñado a optimizarla, desde el agente anestésico único como fue descrito hace varios años hasta el empleo actual con dosis subanestésicas y guiado por modelos farmacocinéticos.14
Actualmente existen diferentes formas de monitoreo de las respuestas nociceptivas ante el estrés quirúrgico con el fin de mantener a los pacientes en las mejores condiciones analgésicas. La respuesta sistémica al estrés quirúrgico conduce a un peor control del dolor, recuperación tardía, mayor tiempo de estancia hospitalaria e incremento del costo de los servicios sanitarios. Un tratamiento con dosis altas de opioides predispone a un despertar lento, somnolencia, y sobre todo a situaciones de hiperalgesia posoperatoria por opiáceos. Existen dos grupos de monitorización nociceptiva según el origen de la respuesta al estímulo, pueden ser procedentes de cambios en el electroencefalograma o de la respuesta del sistema nervioso autónomo.15
El monitor Conox está equipado con un índice de nocicepción llamado qNOX, que predice la probabilidad de respuesta a un estímulo nocivo durante la cirugía. El qNOX es un índice que emplea una escala de 0 a 99 donde 99 indica alta probabilidad de respuesta al estímulo nocivo; los valores cercanos a cero de este índice significan menor probabilidad de respuesta a los estímulos quirúrgicos. El índice qCON mide el nivel de conciencia con el fin de individualizar el nivel hipnótico en cada paciente. Se han utilizado qCON y qNOX en su sistema de circuito cerrado y se ha demostrado que el circuito cerrado garantiza un mayor porcentaje de pacientes con un rango adecuado de anestesia y, por lo tanto, se reduce el riesgo de despertar por un lado, y por otro lado una mala calidad de nocicepción.
En la paciente, debido a que presenta obesidad, la administración de fármacos es un reto, a pesar de que se emplearon modelos farmacocinéticos que intentan corregir la obesidad y brindar las mejores aproximaciones a las concentraciones plasmáticas reales, el escenario ideal es poseer estos sistemas de retroalimentación donde se valora objetivamente la acción del fármaco.15,16
La anestesia libre de opioides es una alternativa posible, se puede utilizar con seguridad cuando se dispone de monitorización adecuada de hipnosis y analgesia, logrando así optimizar las dosis. Los modelos farmacocinéticos utilizados para realizar este tipo de técnica anestésica predicen con bastante exactitud las concentraciones plasmáticas y con ello se puede reducir los efectos adversos y complicaciones derivadas de su uso. La realización de este primer caso a nivel local abre el panorama para que esta técnica se utilice con más frecuencia y se puedan realizar estudios prospectivos donde se podrá evidenciar con exactitud sus beneficios.