Introducción
La porfiria cutánea tarda (PCT) es una enfermedad relativamente común, con una prevalencia de 1/10 000. Es el resultado de la deficiencia genética de una enzima llamada uroporfirinógeno descarboxilasa, que interviene en la síntesis del grupo hemo que al unirse a la globina formará la hemoglobina para su incorporación al hematíe.1,2 Afecta principalmente a la piel con el desarrollo de ampollas en los lugares expuestos al sol y guarda relación con el hierro y con la hepatopatía por virus C. Estas últimas condiciones, son frecuentes en los pacientes de las unidades de hemodiálisis en Cuba, donde se utiliza el hierro como parte del tratamiento junto a la eritropoyetina para mantener niveles adecuados de hemoglobina y la hepatopatía por virus C afecta a un porciento considerable de esta población de pacientes en hemodiálisis periódica intermitente.1,2 Es por ello que en estos pacientes se ha descrito la llamada pseudoporfiria cutánea tarda, con una clínica similar y con factores patogénicos similares pero donde no se han determinado una anomalía genética que lleve a una disminución de la actividad de la enzima involucrada en esta enfermedad.1,3 Por lo interesante del caso y por el hecho de que en la literatura nacional digital no se encuentra reporte de alguno similar, nos motivamos a su publicación.
Presentación del caso
Paciente masculino, color de piel negra con APP (antecedentes patológicos personales) de HTA (hipertensión arterial) severa desde los 35 años de edad. En marzo del año 2005 ingresa con cuadro clínico de decaimiento, vómitos y orinas espumosas. Se realiza complementarios y los resultados más importantes arrojan una creatinina sérica en 1637 µmol/L, urea en 37,9 mmol/L y el ultrasonido renal describe riñones pequeños, ecogénicos, irregulares y con mala relación córtico medular iniciándose tratamiento de hemodiálisis periódica intermitente. En este mismo año adquiere una hepatopatía por virus C.
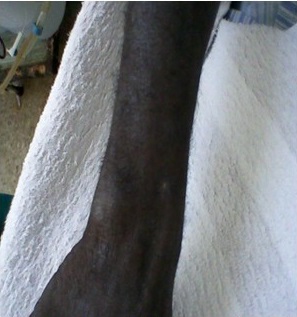
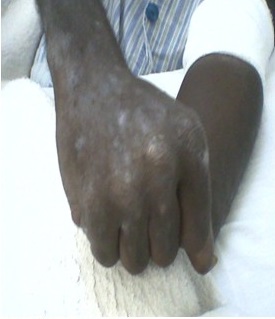
En junio del año 2010 comienza a presentar lesiones ampollares en áreas expuestas al sol (antebrazos, manos y cara). En agosto de 2010 se interconsulta con dermatología por empeoramiento de las lesiones y se recomienda la no exposición al sol, fomentos de agua estéril por 30 minutos 3 veces al día y difenhidramina 25 mg cada 8 horas. El paciente además tomaba ácido fólico 5 mg diarios, carbonato de calcio 3 g diarios y nifedipino 30 mg diarios. Se realiza biopsia de piel y esta describe una dermatitis vesicular subepidérmica con degeneración reticular y vesicular intraepidérmicas, con muy escasos elementos inflamatorios y con cambios hialinos y esclerosis en dermis papilar, los cuales eran compatibles con una PCT. Se le realiza protoporfirina IX en sangre y arrojó un valor de 20,03 µmol/L (VN: 0-59 µmol/L). (Figuras 1 y 2).

Fig. 1 - Lesiones activas. Ampollas en zonas de piel expuesta al sol con un diámetro entre 0,5 1 cm., algunas confluían y que al romper dejaban la piel denudada.

Fig. 2 - Lesiones activas. Ampollas en zonas de piel expuesta al sol con un diámetro entre 0,5 1 cm., algunas confluían y que al romper dejaban la piel denudada.
Se decide asociar como medida terapéutica disminuir la dosis de hierro que se le administraba semanalmente de 100 mg a 50 mg y la estricta y constante protección del sol con el uso de gafas, guantes, mangas largas y gorra. Con estas medidas el paciente tuvo una discreta mejoría.
En noviembre del 2010 se queja de que las lesiones reaparecen en las manos confluyendo y dejando la piel denudada. Se determina hierro sérico y el valor fue de 26,9 µmol/L .Se decidió suspender el hierro endovenoso y subir la dosis de eritropoyetina de 4000 a 8000 unidades semanales, teniendo en cuenta que el hematocrito de junio a noviembre osciló entre 0,39 y 0,37 Vol%.
En enero del año 2011 había mejoría de las lesiones, excepto en las manos, al parecer por poca protección del sol en las mismas. Con un hematocrito en 0,44 a partir de las medidas médicas anteriores se decide además realizar sangrías de 30 cc en cada sesión de hemodiálisis (90 cc semanales de sangre) con el objetivo de contribuir a disminuir los niveles de porfirinas plasmáticas y lograr la mejoría clínica del paciente.
En febrero del año 2011 se realiza hierro sérico y este se encontraba en 13,1 µmol/L con un hematocrito en 0,37, por lo que se mantiene sin el uso de hierro. En marzo de este año 2011 los valores de hematocrito y del hierro sérico se mantenían y las lesiones vesiculares que padecía el paciente desaparecieron. (Figuras 3 y 4).
Discusión
En este paciente el diagnóstico más probable se encontraba entre la PCT y la pseudoporfiria cutánea tarda (pseudo PCT) también denominada dermatosis bulosa3 ya que se presentan manifestaciones clínicas similares, teniendo en cuenta que es un paciente con un tratamiento de hemodiálisis periódica intermitente por una insuficiencia renal crónica en estadio 5. Los medicamentos que consumía no están dentro de los descritos como causantes de lesiones en piel tipo ampollas, ni tampoco como los favorecedores de lesiones en la piel en los pacientes con porfiria cutánea tarda.1
En estos pacientes se incrementan los niveles de porfirinas plasmáticas debido a una pobre depuración de las mismas y al efecto que puede tener la azotemia per se en la actividad de la uroporfirinógeno descarboxilasa (UPD) y el paciente se ve afectado por el efecto tóxico de estas, lo que describe a esta enfermedad como las lesiones en piel que pueden presentar los pacientes bajo régimen de hemodiálisis.3
Hoy día sin embargo y con la existencia de filtros o capilares con una mayor capacidad de depuración, se pueden disminuir de forma considerable los niveles de porfirinas séricas en estos pacientes, no obstante la depuración no es diaria ni constante por lo que podrían mantener niveles que favorecerían la aparición de las manifestaciones cutáneas, además de que las porfirinas se unen a proteínas plasmáticas dificultando su depuración en las sesiones de hemodiálisis.3
Existían además condiciones que favorecieron la aparición de la pseudo PCT y que se han observado en otros casos publicados, como el antecedente de la hepatopatía por virus C y el tratamiento con hierro como parte de la prescripción de los pacientes en hemodiálisis para garantizar niveles adecuados de hierro sérico y una respuesta adecuada de la eritropoyetina.3-5 Por esta razón se tomaron medidas como: suspender el hierro sérico y aumentar la dosis de eritropoyetina para garantizar niveles adecuados de hemoglobina y garantizar la calidad de vida del paciente. Además se decidió realizar flebotomías en una mínima cuantía que contribuyeron a reducir las concentraciones de porfirinas plasmáticas y a la mejoría clínica del paciente.
Al parecer la hemosiderosis secundaria que pueden tener estos pacientes o sencillamente el hierro utilizado podría favorecer la generación de radicales libres de oxígeno que inhibirían la actividad enzimática en el metabolismo de las porfirinas. En el caso de la hepatitis C, esta afectaría al hígado y favorecería la actividad del hierro, se plantea que favorece la depleción del glutatión en el hapatocito y desacopla el hierro del citocromo P450 favoreciendo el incremento de las porfirinas oxidadas y los radicales de oxígeno e inhibiendo la UPD.1,3
El cuadro clínico entre la PCT y la pseudo PCT es similar, la determinación de porfirinas plasmáticas y de la actividad de las enzimas involucradas en la síntesis del grupo hemo ayudan a la diferenciación entre ambas; en este paciente solo se logró la determinación de protoporfirina IX que fue normal. No fue posible en los laboratorios consultados la determinación de otras porfirinas o porfirinas en general que nos ayudaran a diferenciar con exactitud entre PCT y pseudo PCT ya que no es una determinación que se realice con frecuencia en nuestro medio. Se plantea que en la PCT los niveles de porfirinas séricas son muy elevados y en el caso de la pseudo PCT son normales o la elevación es mínima.6,7
En el caso de la PCT se afecta la actividad de la enzima UPD, la cual actúa sobre la porfirina uroporfirinógeno III. La protoporfirina IX (determinada en este paciente) es la última de las porfirinas antes de su conversión en el grupo hemo por la enzima ferroquelatasa, esto quiere decir que su normalidad en sangre no define la existencia o no de una PCT. Esta enfermedad puede presentarse de forma esporádica y la deficiencia enzimática limitarse al hígado, por lo que se puede presentar en la madurez o incluso más tarde.1,2,8,9
En este paciente también se dificultó el diagnóstico al no poder determinar ni cualitativamente ni cuantitativamente las porfirinas en orina ya que el paciente no tenía diuresis debido a su condición de paciente con insuficiencia renal crónica en estadio 5 y bajo régimen de hemodiálisis desde hacía unos 5 años. Tampoco se pudieron determinar en las heces fecales.
Podemos concluir que la diferenciación entre PCT y pseudo PCT puede ser difícil en pacientes en hemodiálisis periódica intermitente y se necesitan de determinaciones de laboratorio que orienten mejor el diagnóstico, no obstante el tratamiento es similar en ambas con una respuesta terapéutica buena.