Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Habanera de Ciencias Médicas
versión On-line ISSN 1729-519X
Rev haban cienc méd v.10 n.2 Ciudad de La Habana abr.-jun. 2011
CIENCIAS BÁSICAS BIOMÉDICAS
Universidad Nacional de Rosario, Argentina
Facultad de Ciencias Bioquímicas y Farmacéuticas de Rosario
El efecto de los agroquímicos en la espermatogénesis
The effect of the agrochemicals in the spermatogenesis
Cecilia Vicenta Paparella1, Adriana Beatriz Pavesi1, Rodolfo Néstor Feldman2, Beatriz Reina Bouvet1
1Guemes 2147. 2000. Rosario, Santa Fe. Argentina. Teléfono: 0341-4470462. E-mail: ceciliapaparella@yahoo.com.ar
1Walt Disney 2124. 2000 Rosario, Santa Fe. Argentina. Teléfono: 0341-4554138. E-mail: apavesi2001@yahoo.com.ar
2Dorrego 543. 2000 Rosario, Santa Fe. Argentina. Teléfono: 0341-4252579. E-mail: rodolfofeldman@gmail.com
1Gabriel Carrasco 1854. 2000 Rosario, Santa Fe. Argentina.Teléfono: 0341-4302317. E-mail: beatrizbouvet@arnet.com.ar
1Área Química Analítica Clínica. Departamento de Bioquímica Clínica. Facultad de Ciencias Bioquímicas y Farmacéuticas de Rosario.
2Servicio de Reproducción. Facultad de Ciencias Médicas de Rosario. Universidad Nacional de Rosario.
RESUMEN
Se relacionó la exposición ocupacional a agroquímicos con parámetros seminales vinculados con la espermatogénesis. En 104 muestras seminales de pacientes con infertilidad idiopática y 20 a 45 años de edad del Servicio de Reproducción Hospital Centenario (Rosario, Argentina), se efectuó espermograma y estudios funcionales según normas OMS (1999). Se agruparon en G1 (n=42) trabajadores expuestos a agroquímicos y G2 (n=62) hombres sin riesgo espermatogénico. La concentración espermática se determinó en cámara de Neubauer, con Papanicolaou se evaluó la concentración de células germinales y la morfología espermática. Se observó en concentración espermática (espermatozoides.106/ml) G1: 21,1±7,1; G2: 41,6±9,2; morfología (% espermatozoides normales) G1: 5,2±1,3; G2: 8,2±3,6 y células germinales.106/ml en G1: 0,91±0,51; G2: 0,32±0,21. La concentración espermática fue menor en G1, las alteraciones morfológicas y células germinales mayores en G1. Estos resultados indican que la exposición a agroquímicos altera la espermatogénesis y es un factor a considerar cuando se estudia infertilidad masculina.
Palabras clave: Agroquímicos, infertilidad masculina, espermatozoides, células germinales, espermatogénesis, disruptores endocrinos.
ABSTRACT
The occupational exposition to agrochemicals was related with sperm parameters linked with spermatogenesis. In 104 semen samples of patients with idiopatic infertility of the Reproduction Service of Centenario Hospital (Rosario, Argentina), sperm study and functional tests according to WHO (1999) have been carried out. Two groups were formed: G1 (n=42) workers exposed to agrochemicals; G2 (n=62) men with no spermatogenic risk. The sperm concentration was determined in Neubauer camera, the concentration of germinal cells and the sperm morphology were evaluated with Papanicolaou. The results were: sperm concentration (spermatozoids 106/ml) G1: 21.1 ± 7.1; G2: 41.6 ± 9.2; morphology (% normal spermatozoids) G1: 5.2 ± 1.3; G2: 8.2 ± 3.6; and germinal cells 106/ml in G1: 0.91 ± 0.51; G2: 0.32 ± 0.21. The sperm concentration was lower in G1, major morphological changes and germinal cells in G1. This results show that the exposition to agrochemicals alters the spermatogenesis, it is a factor to consider in the male infertility.
Key words: Agrochemicals, male infertility, spermatozoid, germinal cells, spermatogenesis, endocrine disruptions.
INTRODUCCIÓN
La contaminación química medioambiental es un problema mundial. Se estima que anualmente se producen e introducen en el mercado alrededor de 2 000 compuestos químicos de síntesis, que al ser liberados al medioambiente pueden interaccionar con los seres vivos y ocasionar daños agudos o crónicos a la salud humana general y, en especial, a la salud reproductiva.1,2
Los contaminantes medioambientales contribuyen a la infertilidad tanto en el hombre como en la mujer. La exposición a diversos contaminantes se asocia con la ocupación laboral, y las principales vías de ingreso al organismo son la piel y la vías respiratoria.3,4,5
Muchas de estas sustancias químicas naturales o sintetizadas por el Hombre y liberadas al Medio Ambiente, se comportan como hormonas alterando la homeostasis normal del sistema endocrino del individuo mediante un desequilibrio en el balance de estrógenos, andrógenos y hormonas tiroideas. 6 Son compuestos persistentes, organohalogenados y bioacumulables que incluyen algunos plaguicidas, sustancias químicas industriales, compuestos de síntesis y algunos metales pesados. Estos compuestos químicos se conocen como alteradores o disruptores endocrinos.7
La Organización Mundial de la Salud define a los disruptores endocrinos como «sustancias exógenas que alteran la función del sistema endocrino y consecuentemente causan efectos adversos sobre la salud de un organismo intacto, de su progenie o de sus poblaciones».8
Por otra parte, el Instituto de Salud y Medio Ambiente Americano constató la presencia medioambiental de sustancias que se comportan como hormonas. Estos compuestos se unen al receptor hormonal o antagonizan su efecto bloqueando al receptor correspondiente; en ambos casos alteran el sistema hormonal.9
Los efectos hormonales de los disruptores endocrinos pueden ser debido a que:10,11
- Mimetizan los efectos de hormonas endógenas.
- Antagonizan la acción normal de las hormonas.
- Alteran el patrón de síntesis y metabolismo de hormonas naturales.
- Modifican los niveles de los receptores hormonales.
Una de las acciones hormonales mejor documentada, atribuible a estos compuestos, es su capacidad de mimetizar o bloquear el efecto de los estrógenos; es decir, la posibilidad de actuar como un estrógeno o un antiestrógeno.12,13
La espermatogénesis es un proceso complejo, controlado por diferentes mecanismos que interactúan de manera variable a lo largo de los sucesivos períodos del desarrollo.14 Este proceso de formación de los gametos masculinos se desarrolla en los túbulos seminíferos del testículo, constituidos por una luz central revestida de epitelio especializado, el cual está formado por dos líneas celulares distintas: las células somáticas de Sertoli y las células germinales o espermatogénicas. Las células de Sertoli se extienden a lo largo de todo el epitelio seminífero, desde la membrana basal hasta la luz del túbulo, acompañando el desarrollo de las células germinales.15 Estas células somáticas intervienen en la regulación de la espermatogénesis enviando señales a las células germinales adyacentes, ya que poseen receptores para la hormona folículo estimulante (FSH) sobre la membrana plasmática y receptores citoplasmáticos para testosterona. El epitelio seminífero es un medio rico en andrógenos, indispensables para la proliferación, diferenciación y maduración espermática. Toda alteración de la función endocrina o exocrina del testículo se refleja en modificaciones morfológicas y/o funcionales del espermatozoide.16,17
MATERIAL Y MÉTODOS
Muestras: Se analizaron 104 muestras de semen provenientes de hombres con infertilidad idiopática, con edades entre 20 y 45 años, quienes asistieron al Servicio de Reproducción del Hospital Provincial Centenario de Rosario durante los meses de febrero de 2009 a marzo de 2010. Se excluyeron muestras de individuos con patología pasada o actual capaz de alterar la calidad seminal, tales como varicocele, criptorquidia, hipospadias, presencia de anticuerpos antiespermáticos, tumores testiculares o malformaciones de glándulas anexas.
Todas las muestras de semen se obtuvieron por masturbación, luego de 3 a 5 días de abstinencia sexual; se realizó el espermograma y los estudios funcionales espermáticos, según normas OMS.18
La población en estudio se dividió en 2 grupos: G1 (n = 42) trabajadores expuestos a agroquímicos desde un tiempo mayor o igual a 2 años y G2
(n = 62) hombres con ocupaciones laborales que no involucran riesgo espermatogénico (comerciantes, docentes, administrativos, empresarios).
Determinaciones
La morfología espermática y la concentración de células germinales (CG) se evaluó con tinción Papanicolaou modificada para semen.18 Esta coloración permite diferenciar claramente las células germinales de otras células presentes en el semen.26
La concentración de espermatozoides se determinó por método subjetivo utilizando la cámara de Neubauer.18
Concentración de células germinales y morfología espermática
Se realizaron dos extendidos con semen entero y con espermatozoides lavados con solución fisiológica estéril. Se contaron 200 espermatozoides clasificándolos según sus características morfológicas, utilizando ocular micrometrado y criterios estrictos.17, 19, 20 En el extendido de semen entero se determinó la concentración de células germinales.18
Valores de referencia
Células germinales: menor o igual a 500.000 células germinales por ml de semen (0,5 x 106 CG/ml), según los resultados obtenidos en muestras seminales de una población de hombres fértiles.21,22
Morfología espermática: mayor o igual a 15 % de espermatozoides con morfología normal.18
Concentración de espermatozoides
Se realizó una solución del semen fresco con el reactivo Mac-Comber y Saunders, según la densidad espermática observada en el examen microscópico directo. Se determinó la concentración espermática en cámara de Neubauer, la cual se realizó por duplicado con la finalidad de obtener un error de conteo aceptablemente bajo.
Valor de referencia
Mayor o igual a 20.000.000 espermatozoides por ml semen (20 x 106 espermatozoides/ml)18
Estudio estadístico
El análisis estadístico de los promedios se realizó mediante la prueba t-Student considerando significativo un valor de probabilidad menor a 0,05 (p<0,05).
RESULTADOS Y DISCUSIÓN
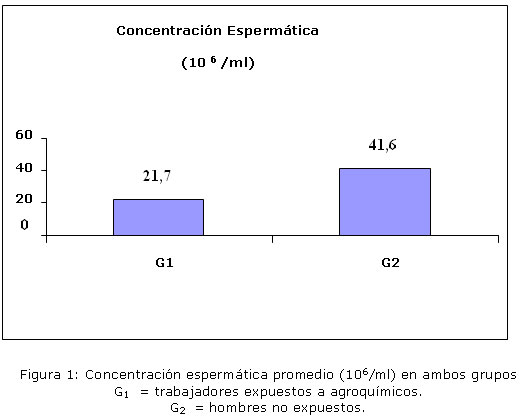
El promedio de concentración espermática en trabajadores expuestos (G1) fue de 21,1 x 106 espermatozoides/ml de semen y en hombres no expuestos a agroquímicos (G2) fue de 41,6 x 106 espermatozoides/ml de semen (Tabla 1).
La comparación de los promedios de la concentración espermática entre G1 y G2 presentó una diferencia estadísticamente significativa (p= 0,0253).
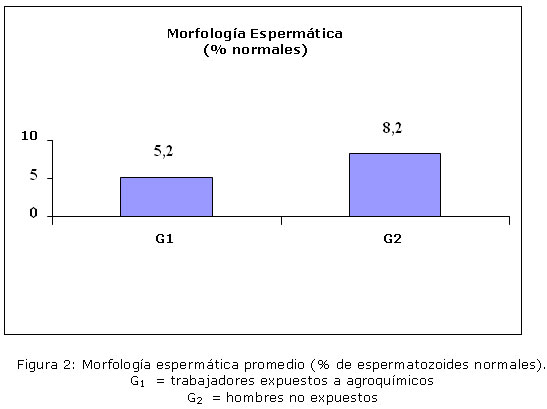
El análisis de la morfología espermática mostró un promedio de espermatozoides morfológicamente normales de 5,2 % en hombres expuestos (G1) y 8,2 % en el grupo no expuestos (G2) (Tabla 1). La comparación de los promedios entre ambos grupos resultó estadísticamente significativa (p=0,0014).
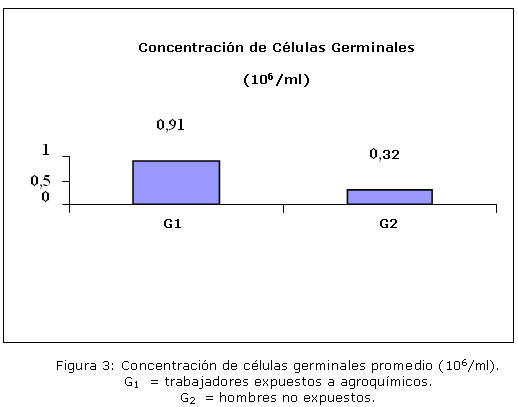
La concentración promedio de células germinales fue de 0,91 x 106 CG / ml en trabajadores expuestos (G1), mientras que en no expuestos (G2) fue de 0,32 x 106 CG / ml (Tabla 1). El análisis estadístico presentó diferencia significativa entre ambos grupos (p=0,0009).
Los plaguicidas son un amplio grupo de sustancias biológicamente activas utilizadas para el control de plagas, pero, además, afectan la salud humana.23,24, 25
Las gónadas son los órganos más vulnerables a los agentes medioambientales físicos y químicos. Estos compuestos químicos, naturales y artificiales se comportan como hormonas femeninas, alterando o inhibiendo el funcionamiento del testículo.26, 27
En los últimos 50 años, se observó una marcada disminución en la concentración espermática; este descenso se debe al desarrollo industrial y a las nuevas sustancias químicas con actividad hormonal liberadas al ambiente. Además en los años 60, se demostró que estos productos químicos de síntesis utilizados para control de plagas agrícolas alteran el equilibrio entre las especies, se acumulan en los organismos vivos y sus efectos se manifiestan de forma tardía e incluso en generaciones posteriores.28
En los pacientes infértiles estudiados, aunque los niveles de concentración de espermatozoides están dentro del rango de referencia en ambos grupos, es menor la concentración espermática en el semen correspondiente al grupo de hombres expuestos a agroquímicos (G1). (Figura 1).
En cuanto a la morfología espermática, si bien está alterada en ambos grupos, la presencia de espermatozoides morfológicamente anormales es mayor en el grupo de trabajadores expuestos (G1), (Figura 2). En el semen de estos hombres se observa, además, un marcado aumento de formas espermáticas inmaduras, lo cual indica detención del proceso espermatogénico. (Figura 3).
La carencia hormonal produce inmadurez en el eyaculado y se manifiesta en la muestra seminal con elevada concentración de células germinales e incremento en las alteraciones morfológicas. (Figuras 2 y 3). 29
Estudios epidemiológicos demostraron que los desórdenes reproductivos se han incrementado durante los últimos 40 años, y se observa una significativa disminución de la concentración espermática, aumento de las alteraciones en el desarrollo del sistema genitourinario asociadas con cáncer testicular e infertilidad. Este deterioro se debe fundamentalmente al cambio en la calidad de vida y el aumento de la exposición a muchas sustancias nocivas para el organismo y, en especial, para la función testicular.30
Los efectos adversos que en la salud humana provoca la contaminación por exposición ocupacional, amerita adoptar medidas preventivas que incluyan un manejo adecuado de estos compuestos en los trabajadores expuestos y la aplicación de las pautas de seguridad sanitaria necesarias para evitar que la población no ocupacionalmente expuesta se contamine con ellos.
CONCLUSIONES
La exposición a agroquímicos altera el proceso de síntesis y maduración de los espermatozoides y se manifiesta en el semen con concentración espermática disminuida, aumento en el porcentaje de espermatozoides con anomalías morfológicas y elevada concentración de células germinales. El deterioro de estos parámetros seminales diminuye la capacidad reproductiva masculina.
El análisis del semen es una herramienta útil para el seguimiento y pronóstico de los riesgos y consecuencias de la exposición laboral o accidental a disruptores endocrinos. La exposición a agroquímicos altera el proceso espermatogénico, razón por la cual consideramos relevante evaluar sus efectos cuando se realiza el estudio integral del hombre infértil.
REFERENCIAS BIBLIOGRÁFICAS
1. Bustos-Obregón E. y Hartley R. Ecotoxicología y daño testicular: contaminación química ambiental. Revisión International Journal of Morphology, 2008; 26(4):833-40.
2. Bustos-Obregón E. y Valenzuela M. Agropesticidas en Andrología: Conceptos básicos y modelo animal. Boletín Informativo de la Sociedad Argentina de Andrología. 1998; 7(1):1-1.
3. Rivas A, Granada A, Jiménez M, Olea F. Exposición humana a disruptores endocrinos. Ecosistemas. Revista científica y técnica de tecnología y medio ambiente. 2004; 13(3): 7-14.
4. Bonde JP, Gwereman A, Ernst E. Identifying environmental risk to male reproductive function by occupational studies. Occup. Environ. Med. 1996; 53 (8):511-19.
5. Gerahard I, Waibel S, Daniel V. Impact of heavy metals on hormonal and immunological factors in woman with repeat miscarriages. Hum. Reprod. Update. 1998; 4 (3):301-9.
6. Miller WR, Sharp RM. Environmental estrogens and human reproductive cancers. Endocrine- related cancer. 1998; 5:69-96.
7. Colborn T. and Clement C. Chemically-induced alterations in sexual and functional development: The wildlife / human connection. Princeton, New Jersey: Princeton Scientific Publishing; 1992, p. 283-288.
8- Sebastián Martín Trossero SM. Disruptores endócrinos: el enemigo silencioso. Rev. Ecociencia y Naturaleza. 2007; 2:20-3.
9. Olea Serrano N, Fernández Cabrera MF, Martín Olmedo P. Conferencia: Estrogens in the Environment. Instituto Nacional de Salud y Medioambiente Americano (NIEHS). Rev. Salud Ambient. 2001;1(1):6-11.
10. Olea Serrano N. COM 706. Disruptores endocrinos: posibles medidas de intervención. La perspectiva europea. Comisión de las Comunidades Europeas. Estrategia comunitaria en materia de alteradores endocrinos. Bruselas. 1999:1-10.
11. Fernández MF, Pedraza V, Olea N. Estrogens in the environment: is there a breast cancer connection? Cancer Journal. 1998; 11:11-7.
12. Olea N, Molina MJ, García-Martin M, Olea-Serrano MF. Modern agricultural practises: The human prince. CommentsToxicol. 1996; 455-74.
13. Olea N, Barba A, Lardelli P, Rivas A, Olea-Serrano MF. Inanvertent exposure to xenoestrogens in children. Toxicol Industrial Health. 1999; 15:151-8.
14. Rey R, Gottlieb S, Copelli S. Regulación de la espermatogénesis de la embriogénesis a la vida adulta. Boletín Informativo de la Sociedad Argentina de Andrología. 2003; 12(2):28-44.
15. Kierszenbaum AL. Histología y Biología celulares. Introducción a la Anatomía Patológica. Elsevier 2º Edición. 2008, p. 569-96.
16. Debeljuk L. Influencia de las células germinales del testículo sobre la función de la célula de Sertoli y la regulación del sistema de retroalimentación negativo. Boletín Informativo de la Sociedad Argentina de Andrología. 2000; 9(2):51-4.
17. Calamera J. y Calamera P. El laboratorio de Andrología como ayuda diagnóstica. CEGIR. Revista de Medicina Reproductiva. 2003; 6 (1):16-26.
18. World Health Organization. Laboratory Manual for the examination of human semen and the semen-cervical mucus interaction. WHO, Cambrigde University Press; 1999.
19. Calamera JC. Morfología espermática para todos. Ediciones científicas. Dr. Montes José. Uruguay: 1999.
20. Kruger T, Acosta A, Simmons K, Swanson J, Malta Janes, Oshninger S. Predictive value of abnormal sperm morphology in Vitro fertilization. Fertil and Steril. 1998; 49(1):112.
21. Gatti V, Bouvet B, Solis E. and cols. Diferenciación de células redondas en semen. Boletín Informativo de la Sociedad Argentina de Andrología.1997; 6: 79.
22. Bouvet B, Brufman A, Gatti V. and cols. Cellular sub-population in semen. Revista Biocell. 2000; 24:164.
23. Perry MJ. Effect of environmental and occupational pesticide exposure on human sperm: a systematic review. Hum. Reprod. Update. 2008;14 (3): 233-42.
24. Bonde JP. Occupational risk to male reproduction. G. Ital. Med. Lav. Ergon. 2002; 24 (2):112-17.
25. Sharpe RM. and Irvine DS. How strong is the evidence of a link between environmental chemical and adverse effects on human reproductive health. British Medical Journal. 2004; 328 (7437): 447-51.
26. Colborn T, Vom Saal FS, Soto AM. Development effects of endocrine disrupting chemicals in wildlife and humans. Environ. Health Perspect. 1993; 101:378-84.
27. Disruptores Endocrinos: Un nuevo riesgo tóxico. Instituto Sindical de Trabajo, Ambiente y Salud (ISTAS). 2000; 1-11.
28. Carlsen E, Giwereman A, Keiding N, Skakkebaek NE. Evidence for decreasing quality of semen during past 50 years. British Medical Journal. 1992; 305:609-13.
29. De La Parra I, Oizerovich S, Escobar ME. Alteraciones del eje reproductivo por enfermedades crónicas o sistémicas, sustancias tóxicas y drogas ilícitas. Rev. Reproducción Humana. 2002; 2 (3):21.
30. Skakkebaek NE. Testicular dysgenesis syndrome.Horm. Res. 2003; 60 (3):49.
Recibido: 9 de diciembre de 2010.
Aprobado 8 de abril de 2011.