Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Habanera de Ciencias Médicas
versión On-line ISSN 1729-519X
Rev haban cienc méd vol.13 no.4 La Habana ago. 2014
CIENCIAS CLÍNICAS Y PATOLÓGICAS
Universidad de Ciencias Médicas de La Habana
Facultad de Ciencias Médicas "Finlay-Albarrán"
Arritmias ventriculares en pacientes con enfermedad renal crónica terminal en hemodiálisis. Monitorización Holter intradialítica
Ventricular arrhythmias in patients with end-stage chronic renal disease on haemodialysis. Intradialytic Holter monitoring
Ana María Suárez ConejerosI, Jorge Marcial Otero MoralesII, Annerys Méndez RosabalIII, Sandra Cruillas MirandaIV, Héctor R. Ayala GómezV, Raydel Argudín SelierVI, Mariana Otero SuárezVII
I Especialista Primer Grado en Medicina Interna. Profesor Auxiliar. FCM "Finlay-Albarrán". e.mail: sconejero@infomed.sld.cu
II Especialista Segundo Grado Medicina Interna. Auxiliar. FCM "Finlay-Albarrán". e.mail: jmotero@infomed.sld.cu
III Especialista Primer Grado en Cardiología. Hospital Clínico-Quirúrgico Docente "Hermanos Ameijeiras".
IV Especialista Primer Grado Medicina Interna. Asistente. FCM "Finlay-Albarrán".
V Residente 3er año de Nefrología. Hospital Clínico-Quirúrgico Docente "Hermanos Ameijeiras"
VIResidente 3er año de Nefrología. FCM "Finlay-Albarrán".
VII Estudiante 5to año de Medicina. FCM "Finlay-Albarrán". e.mail: sconejero@infomed.sld.cu
RESUMEN
Introducción: las arritmias cardíacas son frecuentes en pacientes hemodializados y pueden contribuir a su mortalidad.
Objetivo: estimar la frecuencia de aparición de arritmias ventriculares intradialíticas potencialmente fatales en pacientes con enfermedad renal crónica terminal en hemodiálisis y su asociación con variables clínicas, laboratorio, electrocardiográficas y ecocardiográficas.
Material y Métodos: se investigaron 34 pacientes con enfermedad renal crónica terminal en hemodiálisis de tres hospitales de La Habana. A todos se les realizó ecocardiograma, electrocardiograma, potasio, calcio, urea en sangre. Se monitorizaron con Holter en la primera y segunda diálisis de la semana. Se obtuvieron 68 registros.
Resultados: 36 registros (53%) exhibieron arritmias ventriculares y 32 (47%) no mostraron arritmias; 22 registros (32%) presentaron arritmias ventriculares potencialmente fatales. Los principales factores asociados con significación estadística a arritmias ventriculares potencialmente fatales fueron: edad >45 años, tensión arterial media postdialítica >105 mmHg, e infradesnivel del ST >2 mm. La presencia de hipertrofia ventricular izquierda, la fracción de eyección < 50 %, el tiempo en diálisis >5 años, la existencia de arritmias auriculares y la tensión media arterial predialítica>105 mmHg; se asociaron a arritmias complejas, pero no mostraron significación estadística. Los promedios de edad, tensión arterial media postdialítica, potasio predialítico, duración del QT, grosor del tabique y pared posterior del ventrículo izquierdo, fueron superiores en los casos que registraron arritmias ventriculares complejas o potencialmente fatales.
Conclusiones: la mayoría de los registros obtenidos mediante Holter durante la diálisis exhibieron arritmias ventriculares. Existió un predominio de las arritmias ventriculares potencialmente fatales.
Palabras clave: hemodiálisis, arritmias ventriculares, Enfermedad Renal Crónica Terminal, monitorización holter, electrocardiografía.
ABSTRACT
Introduction: cardiac arrhythmias are frequent in dialysis patients and may contribute to mortality.
Objectives: to estimate the frequency of significant intradialytic ventricular arrhythmias potentially life-threatening in patients with end-stage of chronic renal disease taking hemodialysis (HD) and its association with ventricular arrhythmias and clinical, laboratory, and electrocardiogram and echocardiogram parameters.
Material and Methods: 34 patients with end-stage renal disease on maintenance hemodialysis in three hospitals of Havana were studied. Body weight and blood pressure were recorded before and after HD. Pre dialysis and post dialysis blood samples were taken for estimation of potassium, calcium and urea. Electrocardiogram and echocardiogram were also applied. Holter monitoring was performed the first and second days of dialysis during all HD session. 68 recordings were analyzed. Ventricular arrhythmias were stratified according to the Lown´s classification. Classes 3 and above were taken as complex ventricular arrhythmias.
Results: ventricular arrhythmias during HD were noted in 36 recordings (53%) and 32 recordings did not have any ventricular arrhythmias during HD. In 22 recordings (32%) ventricular arrhythmias were potentially life-threatening. Age >45, mean blood pressure post dialysis >105 mmHg, and ST-segment depression >2mm were statistically significant. Left ventricular hypertrophy, duration of HD >5 years, atria arrhythmias and mean blood pressure pre dialysis >105 mmHg were associated with complex ventricular arrhythmias but they did not show statistical significant.
Conclusions: ventricular arrhythmias were detected in a significant proportion of patients with end-stage renal disease during hemodialysis. Complex ventricular arrhythmias or potentially life-threatening arrhythmias were seen in most of the recordings performed.
Key words: hemodialysis, ventricular arrhythmias, End-Stage Renal Disease, holter monitoring, electrocardiogram.
INTRODUCCIÓN
Los pacientes con enfermedad renal crónica terminal (ERCT) en hemodiálisis exhiben una frecuencia muy elevada de mortalidad de origen cardíaco. 1 Se estima que el fallo cardíaco suele causar la muerte hasta en 43% de los enfermos en hemodiálisis.1 Por otra parte, se estima también que en 61% de estos pacientes la muerte suele estar relacionada con arritmias fatales o paro cardíaco de causa desconocida. 2
Se ha documentado, a través de monitorización con Holter, que los complejos ventriculares prematuros (CVP) son encontrados entre 76 y 100% de los casos y que las arritmias ventriculares complejas se encuentran entre 13% y 36% de estos pacientes. Las arritmias supraventriculares son también comunes y se observan entre 20% y 88% de los casos con ERCT en hemodiálisis.2 La presencia de arritmias potencialmente fatales en pacientes sometidos a hemodiálisis suele estar determinada por varios factores. Desde el punto de vista académico estos factores se pueden diferenciar en dos grupos: los que se relacionan con determinadas condiciones (tanto estructurales como funcionales) presentes en el corazón de estos pacientes que permiten el desarrollo de arritmias cardíacas, es decir, factores que fungen como sustrato arritmogénico; y los que desencadenan o propician las arritmias y que pueden ser definidos como factores disparadores de arritmias.
Entre los principales factores que actúan como sustratos arritmogénicos se suelen incluir fundamentalmente la disfunción ventricular sistólica, la disfunción ventricular diastólica, 3 la hipertrofia ventricular izquierda, 4 la fibrosis cardíaca (miocardiopatía urémica), la enfermedad de arterias coronarias, 5 la disfunción endotelial y la disfunción autonómica. 6 Entre los factores disparadores se destacan principalmente la isquemia aguda inducida por la diálisis, el fallo cardiaco congestivo, los cambios electrolíticos y de volumen durante el proceder dialítico, las alteraciones del intervalo QT y la sobreactividad simpática.
La propia hemodiálisis, por tanto, puede ser considerada potencialmente arritmogénica. La muerte súbita en estos pacientes, parece relacionarse con el período peridialítico, es decir, se presenta con mayor frecuencia en las siguientes 12 horas después de comenzar un tratamiento dialítico o en el período interdialítico largo.7
La presencia de arritmias asociadas al proceder dialítico puede ocurrir independientemente del grado de daño vascular coronario (macro y micro), pues parecen existir otros mecanismos durante la hemodiálisis que causan hipoperfusión miocárdica y determinan la existencia de disfunción ventricular, lo cual aumenta la probabilidad de que aparezcan arritmias peligrosas. En los enfermos con cardiopatía isquémica propiamente, la isquemia cardíaca puede causar una disfunción ventricular izquierda, hecho que puede persistir después del retorno de la perfusión a la normalidad. Esta disfunción prolongada se conoce como stunning o aturdimiento miocárdico.8
En pacientes hemodializados, se ha observado también la persistencia de alteraciones regionales de la contractilidad de la pared ventricular después de pasados 30 minutos de terminar la diálisis, pues durante el proceder se presentan condiciones favorables para el desarrollo de isquemia, por los rápidos cambios de volumen y electrolíticos inducidos por la misma, la cual puede ser subclínica.9 Repetidos episodios de isquemia, pueden llevar a una pérdida irreversible de la función contráctil como puede suceder durante las hemodiálisis tres veces por semana, llevando a un stunning cardíaco repetido, que conduce finalmente a una disfunción crónica del ventrículo izquierdo.
La caída abrupta de los electrolitos durante la diálisis, especialmente de potasio y calcio, también puede comprometer la automaticidad miocárdica, favorecer la aparición de anormalidades en la repolarización ventricular y elevar el riesgo de arritmias. Algunos autores abogan también por evaluar, mediante electrocardiograma (ECG) o monitorización con Holter, los efectos de la diálisis sobre el intervalo QT y la dispersión del QT (QTd), como factores de riesgo para el desarrollo de arritmias malignas. 10 El alargamiento del intervalo QT corregido (QTc) predispone a torsade de pointes, lo cual puede degenerar en episodios de fibrilación ventricular.
La importancia de lo expuesto, aunado a la inexistencia de investigaciones previas en nuestro país que posibiliten establecer la magnitud de la existencia de arritmias potencialmente fatales en el curso del proceder dialítico, es lo que ha motivado la realización de esta investigación.
OBJETIVO
- Estimar la frecuencia de aparición de arritmias ventriculares intradialíticas en un grupo de pacientes con ERCT bajo tratamiento de hemodiálisis.
- Estimar la frecuencia de arritmias ventriculares complejas según la clasificación de Lown (clase 3) y su relación estadística con variables clínicas (edad, peso, tiempo en diálisis, riesgo de enfermedad coronaria, uso de antiarrítmicos y tensión arterial media pre y postdialítica), de laboratorio (urea, potasio y calcio pre y posdiálisis), electrocardiográficas (frecuencia cardiaca, QT, infradesnivel del segmento ST, cambio de voltaje de onda T y arritmias auriculares asociadas) y ecocardiográficas (fracción de eyección, grosor del tabique interventricular y pared posterior del ventrículo izquierdo).
MATERIAL Y MÉTODOS
Se realizó un estudio de casos y controles desde febrero a diciembre de 2012. Se estudiaron 34 pacientes con ERCT, procedentes de tres unidades de hemodiálisis de La Habana, con más de un año de tratamiento de hemodiálisis crónica o regular tres veces a la semana, a través de fístula arteriovenosa, dializados con bicarbonato como tampón del líquido de diálisis.
No se incluyeron pacientes con situaciones clínicas agudas, ni pacientes que no ofrecieran su consentimiento para participar en él.
Los pacientes incluidos fueron evaluados en el curso del primer proceder dialítico de la semana, después del intervalo largo interdialítico (diálisis 1er día/semana) y en la segunda hemodiálisis, después un intervalo corto interdialítico (diálisis 2do día/semana). Todos los pacientes se monitorizaron con un Holter Monitor por el tiempo que duró la sesión dialítica. La monitorización cardíaca comenzó inmediatamente antes del comienzo de la hemodiálisis y el equipo se retiró una vez concluido el proceder. Se utilizó para el análisis del estudio Holter el sistema Excorde 3C (tres canales). Se lograron realizar en total, por medio de la monitorización Holter, 68 registros electrocardiográficos.
Al inicio y término de la diálisis se registró el peso del paciente y la tensión arterial (TA); se le extrajo sangre para hematocrito, potasio (K), calcio (Ca), glicemia y urea. Al término de la diálisis se realizó ECG y se registró el volumen ultrafiltrado (VUF)) durante el proceder dialítico. De cada paciente se recogió información relativa a la edad, sexo, color de la piel, peso seco, talla, tiempo en hemodiálisis, existencia de hipertensión arterial, diabetes mellitus, cardiopatía isquémica (definida como historia de infarto cardíaco antiguo o angina de pecho), insuficiencia arterial periférica y enfermedad cerebrovascular. Se recogieron datos acerca del hábito de fumar, causa de la insuficiencia renal y empleo de medicamentos específicos. También se registró del expediente clínico del enfermo el resultado del ecocardiograma del último año, creatinina y albúmina en sangre y se analizaron los ECG más recientes de los pacientes.
Las arritmias ventriculares fueron estratificadas en 5 clases, según la Clasificación de Lown de las contracciones ventriculares prematuras (CVP), 11 donde se define: clase 0, ausencia de arritmias; clase 1, existencia de CVP aisladas (<30/hr); clase 2, presencia de CVP frecuentes (>30/hr); clase 3, CVP multiformes; clase 4a, CVP pareados; clase 4b, CVP en salvas; y clase 5, Fenómeno de R en T. Las arritmias ventriculares clasificadas como Clases 3, 4 y 5 (Clases 3) se definieron indistintamente como arritmias ventriculares complejas o arritmias potencialmente fatales.
Entre las arritmias auriculares se incluyeron la existencia de extrasistolia auricular, taquicardia supraventricular, fibrilación auricular paroxística y fibrilación auricular crónica.
Los cambios del segmento ST y de voltaje de la onda T, fueron identificados en los registros Holter mediante mediciones manuales. Se definió la existencia de infradesnivel del ST ante la aparición de un infradesnivel de dicho segmento mayor de 2 mm observado en, al menos, 2 canales durante más de 1 minuto. Se consideró la existencia de una reducción del voltaje de la onda T ante una disminución en la altura de dicha onda mayor de 0,5 mv en los tres canales del Holter.
El intervalo QT se mensuró manualmente tanto en los ECG postdialíticos como en el registro continuo del Holter. La mensuración se realizó en el ECG convencional en todas las derivaciones y en el registro Holter en todos los canales. El rango normal del QT se corrigió (QTc) atendiendo a la frecuencia cardíaca por la fórmula de Bazzet .12 Se consideró la existencia de QT largo cuando el QT del paciente excedía 10% del valor estimado del QTc para su frecuencia cardíaca. Se excluyó de la medición del QT un caso con fibrilación auricular crónica.
Se consideró hipertrofia ventricular izquierda (HVI) en los casos en que el tabique interventricular (TIV) o la pared posterior (PP) excedían de 11 mm. Se identificó la existencia de disfunción sistólica en los casos en que la fracción de eyección ventricular (FEV) resultó ser menor de 50% y se aceptó el antecedente de infarto cardíaco antiguo cuando se corroboró la presencia de alteraciones regionales de la contractilidad. La tensión arterial media (TAM) se calculó a partir de la toma de la tensión arterial sistólica y diastólica medida antes de comenzar la diálisis y medida después de terminar la diálisis, según la fórmula:
2 (Presión diastólica) + presión sistólica/ 3.
El análisis estadístico se realizó utilizando el programa SSPS para Windows. Las variables continuas se describen por la media y las desviaciones estándar. Se empleó el Oddss Ratio (OR) y la prueba de Chi Cuadrado para comparar las variables categóricas entre los grupos con arritmias y sin arritmias. Un valor de P <0,05 fue considerado estadísticamente significativo.
RESULTADOS
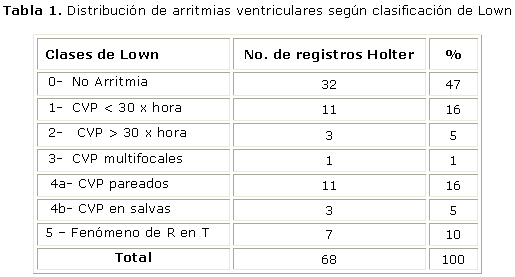
En la Tabla 1, se expone la distribución de las arritmias ventriculares, de acuerdo con la Clasificación de Lown, de los 68 registros electrocardiográficos obtenidos mediante el monitoreo Holter.
En la Tabla 2, se exponen las características de los casos estudiados con la intención de mostrar las particularidades clínicas, hemoquímicas, ecocardiográficas y electrocardiográficas de los pacientes estudiados.
Tabla 2. Características de la población en estudio
| Características | Valores* (n=68**) | Características | Valores* |
| Variables clínicas |
| Hemoquímica |
|
| Edad (años) | 50 (± 18) | Urea prediálisis | 22.3(±5.44) |
| Tiempo en diálisis (años) | 6 (± 5) | Urea postdiálisis | 7.01(±3.05) |
| Riesgo enfermedad | 28(41%) | K prediálisis | 4.61(±1.06) |
| Uso de antiarrítmicos | 18 (26%) | K postdiálisis | 3.11(±0.53) |
| Tensión arterial media prediálisis | 98 (±11) | Ca prediálisis | 0.97 (±0.22) |
| Tensión arterial media postdiálisis | 96 (±12) | Ca postdiálisis | 1.03 (±0.19) |
| Peso postdiálisis | 61(±15) | Hematocrito | 36 (±5) |
| Volumen Ultrafiltrado | 2117(±1021) | Monitorización Holter |
|
| Variables |
| Arritmia auriculares | 24(35%) |
| Fracción de eyección | 58 (±12) | Frecuencia cardíaca | 65 (±12) |
| Tabique interventricular | 14 (±3) | Frecuencia cardíaca | 106 (±20) |
| Pared posterior | 13 (±3) | Intervalo QT (mseg) | 407(±42) |
| Variables electrocardiográficas |
| Intervalo QTc (mseg) | 381(±29) |
| Frecuencia cardíaca | 82(±16) | Intervalo QT largo | 12 (17%) |
| Intervalo QT (mseg) | 362(±34) | Infradesnivel ST | 10 (14%) |
| Intervalo QTc (mseg) | 345 (±28) | Cambio voltaje de la T | 35(51%) |
| Intervalo QT largo | 9 (13%) | Cambios positivos de T | 25(36%) |
| Cambios negativos de T | 10 (14%) |
*Los valores se expresan según el caso en: n (%); media (±DS)
** n representa el numero de registros Holter correspondiente a 34 pacientes
En la Tabla 3, se analiza el comportamiento de diferentes variables cualitativas dicotómicas en dos grupos de pacientes: un primer grupo (1era columna), correspondientes a registros Holter de pacientes que presentaron arritmias ventriculares complejas o potencialmente fatales (Lown 3); y un segundo grupo (2da columna), donde aparecen los registros Holter de pacientes que no presentaron arritmias ventriculares o que presentaron arritmias simples o no potencialmente fatales (Lown <3).
Tabla 3. Comparación entre Clases Lown agrupadas atendiendo a variables cualitativas
| Variables | Registros | Registros | OR | IC | p |
| Datos clínicos | | ||||
| Edad > 45 años | 19 | 19 | 9.0 | 2,32-34,77 | 0.0005 |
| Tiempo en diálisis | 11 | 17 | 1.7 | 0,61- 4,76 | 0.3 |
| Diálisis 1er día/semana | 12 | 22 | 1.3 | 0,47- 3,62 | 0.6 |
| Diálisis 2do día/semana | 10 | 24 | 0.8 | 0,27- 2,11 | 0.6 |
| Riesgo enfermedad | 11 | 17 | 0.6 | 0,61- 4,76 | 0,3 |
| Uso de antiarrítmicos | 5 | 13 | 0.7 | 0,22- 2,44 | 0.6 |
| Arritmias auriculares | 10 | 14 | 1.9 | 0,66- 5,43 | 0.2 |
| Tensión arterial | 6 | 10 | 1.4 | 0,41- 4,35 | 0.6 |
| Tensión arterial | 8 | 6 | 3.8 | 1,12-12,91 | 0.02 |
| Peso postdiálisis | 17 | 15 | 7.0 | 2,17-22,69 | 0.0006 |
| Volumen Ultrafiltrado | 8 | 20 | 0.7 | 0,26-2,11 | 0.5 |
| Hemoquímica | | ||||
| Urea prediálisis | 13 | 14 | 3.3 | 1.14-9.43 | 0.02 |
| Urea postdiálisis | 12 | 10 | 4.3 | 1.44-12.89 | 0.008 |
| K prediálisis | 4 | 8 | 1.1 | 0,28-3,97 | 0.9 |
| K postdiálisis | 11 | 34 | 0.4 | 0,12-1,02 | 0.05 |
| Ca prediálisis | 9 | 14 | 1.6 | 0,55-4,55 | 0.3 |
| Ca postdiálisis | 6 | 12 | 1.1 | 0,33-3,34 | 0.9 |
| Hematocrito < 35 | 9 | 22 | 0.8 | 0,27-2,11 | 0.5 |
| Ecocardiograma | | ||||
| Fracción eyección | 5 | 5 | 2.4 | 0,61-9,41 | 0.1 |
| Tabique interventricular | 20 | 34 | 3.5 | 0,71-17,40 | 0.1 |
| Pared posterior | 18 | 32 | 2.0 | 0,56-6,88 | 0.2 |
| ECG | | ||||
| Frecuencia cardíaca | 5 | 11 | 0.9 | 0,28-3,12 | 0.9 |
| QT largo | 2 | 7 | 0.6 | 0,10-2,93 | 0.4 |
| Holter | | ||||
| Frecuencia | 9 | 23 | 0.7 | 0,24-1,93 | 0.4 |
| Frecuencia | 13 | 25 | 1.2 | 0,43-3,39 | 0.7 |
| QT largo | 4 | 8 | 1.1 | 0,28-3,97 | 0.9 |
| Infradesnivel ST | 7 | 3 | 6.7 | 1,53-29,22 | 0.005 |
| Cambio voltaje | 11 | 24 | 0.91 | 0,33-2,53 | 0.8 |
*Registros electrocardiográficos obtenidos mediante Holter clasificados en clase Lown 3,4 y 5 (arritmias ventriculares complejas).
** Registros electrocardiográficos obtenidos mediante Holter clasificados en clase Lown 0 (no arritmias) y clase Lown 1 y 2 (arritmias ventriculares simples o aisladas).
En la Tabla 4, se presenta el comportamiento de diferentes variables cuantitativas en tres grupos de pacientes: un primer grupo (1era columna) correspondientes a registros Holter de pacientes que no presentaron arritmias ventriculares (Lown 0); un segundo grupo (2da columna), donde aparecen los registros Holter de pacientes que presentaron arritmias ventriculares simples o no potencialmente fatales (Lown 1 y 2); y un 3er grupo donde se presentan arritmias ventriculares complejas o potencialmente fatales (Lown 3).
Tabla 4. Comparación de Clases Lown agrupadas atendiendo a variables cuantitativas
| Variables | Registros | Registros | Registros | Total |
| Clínicas |
| |||
| Edad (años) | 41 (± 17) | 52(± 17) | 63(± 13) | 50 (± 18) |
| Tiempo en diálisis | 6(± 5) | 5 (± 3) | 6(± 5) | 6 (± 5) |
| Peso postdiálisis | 60(± 18) | 59 (± 16) | 65(± 9) | 61(±15) |
| Volumen | 2167 (± 1151) | 2357 (± 969) | 1891(± 872.2) | 2117(±1021) |
| Tensión arterial | 97(± 12) | 100 (± 7) | 98(± 14) | 98 (±11) |
| Tensión arterial | 92(± 12) | 100 (± 10) | 101(± 12) | 96 (±12) |
| Hemoquímica |
| |||
| Urea prediálisis | 22.3(± 5.4) | 20.6 (± 3.8) | 23.4(± 6.3) | 22.3(±5.4) |
| Urea postdiálisis | 7.01(± 3,0) | 6.2 (± 2.5) | 8.19 (± 3.4) | 7.24(±3.1) |
| K prediálisis | 4.51(± 0.95) | 4,61 (± 0.89) | 4.75(± 1.31) | 4.61(±1.06) |
| K postdiálisis | 3.07(± 0,49) | 3,02 (± 0.44) | 3.23(± 0.63) | 3.11(±0.53) |
| Ca prediálisis | 0.97(± 0.18) | 0,99 (± 0.21) | 0.97(± 0.30) | 0.97 (±0.22) |
| Ca postdiálisis | 1.06(± 0.23) | 0,97 (± 0.18) | 1.01(± 0.14) | 1.03 (±0.19) |
| Hematocrito | 36 (± 5) | 35 (± 7) | 36(± 5) | 36 (±5) |
| Albúmina | 42 (± 4) | 39 (± 4) | 43(± 4) | 41(± 4) |
| Ecocardiograma |
| |||
| Fracción de | 59 (± 11) | 59 (± 11) | 56(± 12) | 58 (±12) |
| Tabique interventricular (mm) | 12(± 3) | 15 (± 3) | 15(± 3) | 14 (±3) |
| Pared posterior (mm) | 12 (± 3) | 13 (± 3) | 14(± 2) | 13 (±3) |
| Electrocardiograma |
| |||
| Intervalo QT (mseg) | 359(± 36) | 361 (± 27) | 377(± 33) | 362(±34) |
| Intervalo QTc (mseg) | 343(± 24) | 343 (± 26) | 356(± 34) | 345 (±28) |
| Frecuencia cardiaca (lat/min) | 83 (± 15) | 84 (± 15) | 80(± 19) | 82(±16) |
| Holter |
| |||
| Frecuencia cardíaca | 65 (± 13) | 65 (± 9) | 65(± 13) | 65 (±12) |
| Frecuencia cardiaca máxima (lat/min) | 105(± 21) | 104 (± 12) | 107(± 22) | 106 (±20) |
| Intervalo QT (mseg) | 405 (± 2) | 409 (± 37) | 410(± 48) | 407(±42) |
| Intervalo QTc (mseg) | 381(± 30) | 378 (± 21) | 385(± 31) | 381(±29) |
* Registros electrocardiográficos obtenidos mediante Holter clasificados en clase Lown 0 (no arritmias).
** Registros electrocardiográficos obtenidos mediante Holter clasificados en clase Lown clase Lown 1 y 2 (arritmias ventriculares simples o aisladas).
*** Registros electrocardiográficos obtenidos mediante Holter clasificados en clase Lown 3, 4 y 5 (arritmias ventriculares complejas).
DISCUSIÓN
Se realizaron 68 registros electrocardiográficos intradialíticos a través de monitorización con Holter. En 53% de los registros, se detectó la presencia de arritmias ventriculares y en 32% se identificó la existencia de arritmias ventriculares potencialmente fatales o ventriculares complejas (Clase Lown 3), lo cual coincide con algunos reportes donde se considera que estos trastornos del ritmo cardíaco pueden aparecer hasta en 36% de los pacientes en hemodiálisis. 3 En otros trabajos, las arritmias complejas (Clase Lown 3), son generalmente reportadas hasta en 17% de los pacientes estudiados, pero las variaciones en la incidencia de las mismas parecen depender de las diferencias que se establecen en la terminología para definirlas.13
Se determinó que los pacientes con arritmias ventriculares complejas (Clase Lown 3) tenían promedios de edades superiores (63 ± 13 años), lo cual parece corresponder con mayor comorbilidad y le añade a estos pacientes un riesgo significativo para el desarrollo de arritmias (OR: 9; p<0.05). Hay artículos que han incluido la edad entre los factores predictores de muerte cardiovascular en pacientes en hemodiálisis.14
Aunque no se encontró de forma aislada significación estadística entre el riesgo de padecer enfermedad coronaria y la aparición de arritmias potencialmente fatales (Clase Lown 3), sí creemos que desde el punto de vista clínico esta asociación tiene importancia, ya que para que se produzcan tales arritmias se necesita un sustrato cardíaco arritmogénico, además de factores disparadores que se presentan durante el proceder como los cambios de volumen y electrolitos.
Al relacionar la existencia de arritmias potencialmente fatales con el día de realización de la diálisis se observó que durante la observación intradialítica del 1er día de diálisis de la semana había más probabilidades de aparición de arritmias que el 2do día (OR 1.3) correspondiente a la segunda diálisis de la semana, aunque desde el punto de vista estadístico ello no fue significativo. En nuestra opinión, esta diferencia observada entre ambos días sí tiene significación clínica, dado que en el 1er día de diálisis, después del intervalo largo interdialítico (fin de semana), pueden coexistir diferentes condiciones que propicien trastornos del ritmo cardíaco como mayor sobrecarga de volumen.
La tensión arterial media postdialítica fue mayor en los pacientes que clasificaron en la clase Lown 3 (OR: 3.8; p<0.05), lo cual pudiera ser expresión de la sobreactividad simpática que se desarrolla tempranamente y de manera sostenida a partir de señales aferentes que se originan en los riñones insuficientes de pacientes con ERCT. Probablemente, el propio daño renal sea el activador de esta sobreactividad ya que la misma disminuye después de la nefrectomía bilateral. 15,16
Debemos señalar que, en nuestro estudio, los pacientes con arritmias Clase Lown 3 (arritmias ventricular graves o complejas) tenían un mayor peso postdiálisis (OR: 7 y p<0,05), lo cual interpretamos que puede deberse a la existencia de sobrecarga de volumen en dicho grupo, ya que coincidentemente el grupo que exhibió arritmias más graves (Clase Lown 3) presentó también promedios menores de volumen ultrafiltrado (VUF). Estudios posteriores al aumentar la muestra habrán de evaluar la objetividad de esta relación.
La existencia de arritmias ventriculares complejas (clase Lown 3) se relaciona con mayor probabilidad de tener hipertrofia ventricular izquierda, (OR: 3.5 y 2.0 para TIV y PP, respectivamente). También en este grupo de clase Lown se evidenció que el TIV y la PP tuvieron en promedio mayor grosor. Este hecho si bien no tuvo significación estadística sí le concedemos gran significación clínica. Otros investigadores lo han señalado también.17,18
Los valores de urea obtenidos, antes de someterse a la diálisis (urea prediálisis), fueron más altos en el grupo de pacientes con arritmias ventriculares complejas (clase Lown 3), tanto cuantitativamente, al mostrar promedios mas altos, como cualitativamente (OR >3), y de igual forma se encontraron en este estudio resultados similares para la urea realizada al terminar la diálisis (urea postdiálisis). Este un hecho a destacar clínica y estadísticamente. Resulta obvio que un empeoramiento metabólico aumente la susceptibilidad de estos pacientes a presentar arritmias.
La existencia de 12 registros con QT largo es un dato de interés, pues existen variantes genéticas de síndrome de QT largo y la propia diálisis entonces pudiera favorecer la aparición de arritmias y muerte súbita en pacientes que desconozcan que padecen este trastorno. Recientemente parece considerarse un síndrome de QT largo adquirido durante la diálisis y la hipertrofia del ventrículo izquierdo ha sido asociada a este síndrome.19 Una serie de medicamentos comúnmente usados como los antihistamínicos, antidepresivos, eritromicina, azitromicina, sotalol, entre otros, puede alargar el QT y disparar una taquicardia ventricular polimorfa. En pacientes hemodializados, hay reportes en la literatura, señalando que el Ciprofloxacino alarga el QT sobre todo cuando se asocia a hipocalcemia,20 y predispone a torsade de pointes y se han reportado casos de otros trastornos de la conducción como bloqueos auriculoventriculares durante el tratamiento con Verapamilo, asociado a ligera hipercaliemia en pacientes hemodializados. 21
Se observó también que las arritmias potencialmente fatales se asociaron de forma estadísticamente significativa a infradesnivel del segmento ST (clínicamente silente) en los registros realizados (p<0,05), lo cual ha sido reportado en diferentes trabajos.14 Hay estudios que evidencian que la frecuencia de arritmias ventriculares intradialíticas es mayor cuando existe estenosis significativa de arterias coronarias, situación que suele presentarse en este tipo de pacientes, teniendo en cuenta, la alta prevalencia de diabetes, hipertensión y calcificaciones vasculares, todo lo cual predispone a la cardiopatía isquémica, así como otras condiciones clínicas relacionadas que disminuyen la tolerancia a la isquemia, entre ellas se pueden citar: la anemia, la dislipidemia, la hiperhomocisteinemia y la propia disfunción endotelial.13 Por otra parte, está bien establecido que los tratamientos hemodialíticos intermitentes ejercen efectos hemodinámicos significativos, pues la diálisis puede complicarse con hipotensión intradialítica en 30% de los casos 12,22 e inducir isquemia miocárdica.
Diferentes variables, tales como tiempo en diálisis, primera diálisis de la semana (Diálisis 1er día/semana), TAM predialítica, arritmias auriculares asociadas y niveles de calcio predialítico, al relacionarlas con la existencia arritmias potencialmente fatales exhibieron cocientes de probabilidad (oddss ratio) mayor de 1,3. Sin embargo, la estimación de p no evidenció significación estadística. En nuestra opinión, esta diferencia entre el valor del odds ratio y la p pudiera estar determinada, en primer lugar, por el tamaño de la muestra estudiada.
CONCLUSIONES
La mayoría de los pacientes estudiados presentaron arritmias ventriculares con predominio de las arritmias ventriculares complejas o potencialmente fatales.
Los factores asociados con significación estadística a la existencia de arritmias ventriculares complejas o potencialmente fatales fueron: la edad (>45 años), la urea pre (>25 mmol/l) y postdialítica (>9 mmol/l), la tensión arterial media postdialítica (>105 mmHg), el peso postdiálisis (>60 kg) y el infradesnivel del ST (>2 mm). La presencia de hipertrofia ventricular izquierda, el tiempo en diálisis >5 años, la primera diálisis, la existencia de arritmias auriculares y la tensión media arterial predialítica > 105 mmHg, se asociaron a la existencia de arritmias complejas pero no mostraron significación estadística.
Los promedios de edad, peso postdiálisis, TAM postdialítica, urea pre y postdialítica, potasio predialítico, grosor del TIV y PP, QT en el ECG y en el Holter fueron superiores en los casos que registraron arritmias ventriculares complejas o potencialmente fatales.
REFERENCIAS BIBLIOGRÁFICAS
1. Kanbay M, Afsar B, Goldsmith D, Covic A. Sudden Death in Hemodialysis. An Update. Blood Purif. 2010; 30: 135-145. [Citado Mayo 10]. Disponible en: http://www.karger.com/Article/FullText/320370
2. Bozbas H, Atar I, Yildirir, Ozgul A. Clinical Study. Prevalence and Predictors of Arrhythmia in End Stage Renal Disease Patients on Hemodialysis. Turkey Renal Failure 2007; 29:331_339. [Citado 2013, Mayo 10]. Disponible en: http://informahealthcare.com/doi/abs/10.1080/08860220701191237
3. Quiroga B, Villaverde M, Abad S, Vega A, Reque J, López-Gómez JM. Diastolic Dysfunction and High Levels of New Cardiac Biomarkers as Risk Factors for Cardiovascular Events and Mortality in Hemodialysis Patients. Blood Purif. 2013 Sep 14;36(2): 98-106. [Citado 2013, Octubre 15]. Disponible en: http://www.karger.com/Article/FullText/354080
4. Covic AC, Buimistriuc LD, Green D, Stefan A, Badarau S, Kalra PA. The prognostic value of electrocardiographic estimation of left ventricular hypertrophy in dialysis patients. Ann Noninvasive Electrocardiol. 2013 ;18(2):188-98.
5. Shastri S, Tangri N, Tighiouart H, Beck GJ, Vlagopoulos P<, et al. Predictors of sudden cardiac death: a competing risk approach in the hemodialysis study. Clin J Am Soc Nephrol. 2012 Jan; 7(1):123-30. [Citado 2013, Mayo 10]. Disponible en: http://cjasn.asnjournals.org/content/7/1/123.long
6. Pun PH, Middleton JP. Sudden cardiac death in hemodialysis patients. A comprehensive care approach to reduce risk. Blood Purif. 2012; 33 (1-3):183-9. [Citado 2013, Mayo 10]. Disponible en: http://www.karger.com/Article/FullText/334154
7. Bleyer AJ, Hartman J, Brannon PC, Reeves-Daniel A, Satko SG, Russell G. Characteristics of sudden death in hemodialysis patients. Kidney Int 2006; 69:2268_2273. [Citado 2013, Abril 20]. Disponible en: http://www.nature.com/ki/journal/v69/n12/full/5000446a.html
8. Selby NM, Mcintyre CW. The Acute Cardiac Effects of Dialysis. Seminars in Dialysis 2007; 20: 220_228. [Citado 2013, Febrero 6]. Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1525-139X.2007.00281.x/abstract
9. Middleton JP. Predisposition to Arrhythmias: Electrolytes, Uremic Fibrosis, Other Factors Carolina Seminars in Dialysis 2011; 24 (3): 287-289. [Citado 2013, Mayo 10]. Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1525 -139X.2011.00866.x/abstract
10. Genovesi S, Rossi E, Nava M, Riva H, De Franceschi S, Fabbrini P, et al. A case series of chronic haemodialysis patients: mortality, sudden death, and QT interval. Europace. 2013 Jul; 15(7):1025-33. [Citado 2013, Septiembre 15]. Disponible en: http://europace.oxfordjournals.org/content/15/7/1025.long
11. Lown B, Wolf M. Approaches to sudden death from coronary heart disease. Circulation 1974; 44:130_142. [Citado 2013, Mayo 10]. Disponible en: http://circ.ahajournals.org/content/44/1/130.long
12. Bazzet HC. An analysis of the time-relations of electrocardiograms. Heart. 1920; 7:353-70.
13. Herzog CA, Mangrum JM, Passman R. Sudden cardiac death and dialysis patients. Semin Dial 2008; 21: 300_307. [Citado 2013, Mayo 10]. Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1525-139X.2008.00455.x/abstract
14. Holme I, Fellström BC, Jardin AG, Schmieder RE, Zannad F, Holdaas H. Prognostic model for total mortality in patients with haemodialysis from the Assessments of Survival and Cardiovascular Events (AURORA) study.J Intern Med. 2012 May; 271(5):463-71. [Citado 2013, Mayo 10]. Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2796.2011.02435.x/abstract;jsessionid=22E091471F28445350657B1A8EA4410E.f04t02
15. De Bie MK, Buiten MS, Rabelink TJ, Jukema JW. How to reduce sudden cardiac death in patients with renal failure. Heart. 2012; 98:335-341. [Citado 2013, Mayo 10]. Disponible en: http://heart.bmj.com/content/98/4/335.long
16. Shamseddin MK & Parfrey PS. Sudden cardiac death in chronic kidney disease: epidemiology and prevention. Nat. Rev. Nephro 2011; 7: 145_154. [Citado 2013, Agosto 14]. Disponible en: http://www.nature.com/nrneph/journal/v7/n3/full/nrneph.2010.191.html
17. Burton JO, Korsheed S, Grundy BJ, McIntyreCW. Hemodialysis-induced left ventricular dysfunction is associated with an increase in ventricular arrhythmias. Ren Fail 2008; 30(7):701-709.
18. Green D, Roberts PR. Sudden Cardiac Death in Hemodialysis Patients. An In-Depth Review Am J Kidney Dis. 2011; 57(6):921-929. [Citado 2013, Julio 11]. Disponible en: http://www.ajkd.org/article/S0272-6386%2811%2900595-6/fulltext
19. Valentim B, Pereira A, Coelho P, Pereira T. Study of ventricular electrical systole in patients with end-stage kidney disease on hemodialysis. Arq Bras Cardiol. 2013 Mar; 100(3):261-8. [Citado 2013. Septiembre 12]. Disponible en: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0066-782X2013000300008&lng=en&nrm=iso&tlng=pt
20. Daya SK, Gowda RM, Khan IA. Ciprofloxacin- and hypocalcemia-induced torsade de pointes triggered by hemodialysis. Am J Ther. 2004;11(1):77-9.
21. Letavernier E, Couzi L, Delmas Y, Moreau K, Murcott O, De Précigout V. Verapamil and mild hyperkalemia in hemodialysis patients: a potentially hazardous association. Hemodial Int. 2006;10(2):170-2.
22. McIntyre CW. Effects of hemodialysis on cardiac function. Kidney International. 2009; 76: 371-375. [Citado 2013, Junio 15]. Disponible en: http://www.nature.com/ki/journal/v76/n4/full/ki2009207a.html
Recibido: 21 de octubre de 2013
Aprobado: 3 de junio de 2014