Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Ingeniería Electrónica, Automática y Comunicaciones
versión On-line ISSN 1815-5928
EAC vol.35 no.3 La Habana sep.-dic. 2014
ARTICULO ORIGINAL
Construcción y caracterización de electrodos de Vidrio/ITO/PANI para la medición de pH
Construction and characterization of Glass/ITO/PANI electrodes for pH measurements
Ing. José Alejandro Somoza Chuay, MsC. José Enrique Eirez Izquierdo, Dr. Sonnia Pavoni Oliver, Dr. Eduardo Martín Rodríguez
Centro de Investigaciones en Microelectrónica (CIME), Cujae, La Habana, Cuba. E-mail: josealejandro@electrica.cujae.edu.cu , joseenrique.ei@electrica.cujae.edu.cu , sonnia.pavoni@electrica.cujae.edu.cu , eduardo.martin@electrica.cujae.edu.cu
RESUMEN
Actualmente un gran número de investigaciones están orientadas hacia el empleo de materiales orgánicos en el desarrollo de sensores debido a la sensibilidad que estos materiales presentan ante diversos agentes químicos. La Polyanilina (PANI) es uno de los materiales orgánicos que pueden ser utilizados como elemento sensible. En este trabajo se construyó un electrodo de Vidrio/ITO/PANI con dimensiones de 2.5 cm x 1.5 cm x 0.25 cm mediante la técnica layer by layer (LbL). Se utilizó un canal de medición conformado por el electrodo de trabajo Vidrio/ITO/PANI, un electrodo de referencia de plata/cloruro de plata (Ag/AgCl) y un amplificador de instrumentación INA116. Se utilizó el principio potenciométrico para caracterizar el electrodo construido ante diferentes valores de pH. La respuesta potenciométrica mostró una sensibilidad de -55,12 mV/pH muy cercana a la de un electrodo típico de pH.
Palabras claves: ITO, PANI, pH, electrodos.
ABSTRACT
The electronic properties of organic materials can be changed by the influence of different chemical agents. These changes give the possibility to use these materials in different applications like sensors. One of the organic materials studied as detection layer for this kind of sensors is polyaniline (PANI). In this work a Glass/ITO/PANI electrode of 2.5 cm x 1.5 cm x 0.25 cm was constructed using layer by layer (LbL) technique. The potentiometric response was obtained through an instrumentation amplifier (INA116), using a reference electrode (Ag/AgCl) and a work electrode of Glass/ITO/PANI. Buffer solutions with different pH values were evaluated. As results of electrodes characterization, the sensibility of the potentiometric response was -55,12 mV/pH.
Key words: ITO, PANI, pH, electrodes.
INTRODUCCIÓN
El desarrollo de sensores que detecten señales provenientes de diferentes dominios y las conviertan en señales eléctricas procesables es de suma importancia y actualidad. Los sensores electroquímicos utilizan la electroquímica como herramienta analítica. Por lo general consisten en al menos dos electrodos que se ponen en contacto con una solución electrolítica, donde se encuentran los analitos que se quieren detectar. Según la técnica de análisis que se utilice, los sensores electroquímicos pueden clasificarse en amperométricos, potenciométricos y conductimétricos [1].
En particular la medición y el control del pH tienen una amplia aplicación en áreas de la industria y el diagnóstico médico. El pH de una solución indica cuan ácida o básica es la misma. Cuando un electrodo preparado para medir pH, se pone en contacto con la solución se desarrolla un potencial (E) cuya expresión está dada por la ley de Nernst (E0 es el potencial de equilibrio):
E = E0 0,05916*pH [V]
A lo largo de la evolución de los sensores se ha producido una notable actividad en la búsqueda de materiales para la construcción de electrodos. Se ha reportado el empleo de un material conocido como ITO (indium tin oxide), compuesto por un 90% de In2O3 y 10% de SnO2. El ITO es transparente y conduce la corriente eléctrica [2-5]. Estas dos propiedades han permitido que sus aplicaciones más importantes hasta el momento se hayan concentrado en la fabricación de displays, celdas solares y biosensores [6-12]. En el caso de los biosensores, la presencia del material resalta fundamentalmente en la construcción de sensores de glucosa, detección ¨on chip¨ de microfluidos y para el análisis de electroluminiscencia química [13-15].
El elemento clave de un electrodo para medir pH potenciométricamente es la membrana selectiva al ion H+. Los primeros electrodos, creados hace un siglo aproximadamente, tenían una membrana de vidrio; que permite el paso de iones H+, pero no el de otras especies iónicas. Cuando este electrodo se sumerge en una solución que contiene iones, los del tipo H+ se difunden a través de la membrana hasta que se alcanza un equilibrio entre las concentraciones de la solución externa y la interna del electrodo, de esta manera se produce una acumulación de carga en el interior de la membrana que es proporcional al número de iones H+ presentes en la solución externa. En la literatura se ha reportado el uso de elementos orgánicos para la construcción de membranas, como por ejemplo el Polypirrol [1] y más recientemente la Polyanilina (PANI) [16].
El PANI varía su conductividad eléctrica en dependencia del medio y las condiciones bajo las que sea utilizada. Generalmente se depositan a bajas temperaturas sobre materiales conductores para la fabricación de electrodos. Estos electrodos pueden utilizarse como elemento sensor que pueden estar en contacto directo con los analitos a medir, incluso si estos se encuentran en medio acuoso.
La utilización del ITO en combinación con un material orgánico como el PANI no es nueva. Estos materiales se han utilizado con anterioridad en la construcción de electrodos de trabajo los cuales han sido empleados de maneras diversas [17, 18]. Sin embargo, la utilización de estos electrodos como elemento sensor de pH no está explotada a profundidad y evidencias de esto son las investigaciones que desarrolla la comunidad científica internacional alrededor de este tema [19].
En este trabajo se presenta la fabricación de un electrodo de Vidrio/ITO/PANI utilizando el método Layer by Layer (LbL) [20]. Este método constituye una variante sencilla y muy utilizada para depositar polímeros. Se construyó una celda electroquímica conformada por el electrodo fabricado, un electrodo de referencia de Ag/AgCl y soluciones buffer con diferentes valores de pH. Las variaciones del sistema ante diferentes concentraciones del ion H+ se determinaron potenciométricamente y la respuesta obtenida mostró una sensibilidad de -55,12 mV/pH.
Materiales y métodos
CONSTRUCCIÓN DEL ELECTRODO
Se utilizaron láminas de vidrio de dimensiones 2,5 cm x 1,5 cm x 0,25 cm cubiertas por una de sus caras con una capa de ITO. Se empleó un agitador magnético modelo WILDCAT. Para la construcción de los electrodos se utilizaron 100 ml de agua destilada, 40 ml de Liquinina Sulfonada (LS) y 40 ml de PANI.
Se construyeron tres electrodos de trabajo. La deposición del polímero se llevó a cabo adaptando la técnica Layer by Layer (LbL) y se siguió la metodología siguiente:
· Se introdujo la placa de ITO, durante 3 minutos, en un recipiente que contenía PANI.
· Después se introdujo en un recipiente con agua en agitación durante 20 segundos, de manera que la placa quedó en una posición tangente al flujo de agua.
· Seguidamente se secó la placa con aire.
· Acto seguido, se introdujo la placa en otro recipiente con Liquinina Sulfonada (LS) durante tres minutos. La función de esta etapa es propiciar una mejor adherencia del PANI a la superficie de ITO.
· Después nuevamente se introdujo la lámina en un recipiente con agua limpia durante 20 segundos bajo las mismas condiciones que se explicaron anteriormente.
Este ciclo se repitió 10 veces y una vez concluido se obtuvo una placa de Vidrio/ITO/PANI que se utilizó como electrodo de trabajo. En la Figura 1 que sigue se ilustran las capas del proceso de fabricación del electrodo. En 1(a) se muestra la lámina de Vidrio/ITO, donde el vidrio aparece en blanco y el ITO en azul. En 1(b) se muestra la lámina anterior después de la deposición del polímero PANI representado en color verde.
DISEÑO DEL EXPERIMENTO
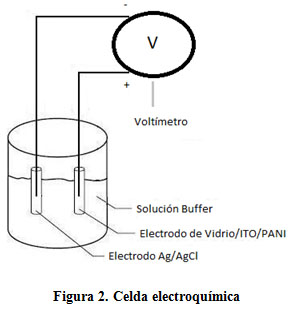
La celda electroquímica para realizar el experimento estuvo formada por tres elementos: el electrodo de Vidrio/ITO/PANI, utilizado como electrodo de trabajo; un electrodo de referencia de Ag/AgCl y como solución electroquímica se prepararon cinco soluciones buffer con pH de 2, 4, 7, 10 y 12. (Figura 2)
Las soluciones buffer se prepararon a partir de agua destilada, hidróxido de sodio (NaOH) y ácido clorhídrico (HCl). La validación del pH de las soluciones se realizó con un medidor de pH del tipo Sartorius PB-20 [21].
Para las mediciones potenciométricas se utilizó un circuito electrónico conformado por un amplificador de instrumentación INA 116P, una tarjeta de adquisición de datos NI-PCI 6014, una fuente de alimentación del tipo AGILENT E3646A y un multímetro del tipo AGILENT 34401. La conexión entre la celda electroquímica y el sistema de medición se realizó de forma tal que el electrodo de trabajo se conectó a la entrada positiva del amplificador de instrumentación y el de referencia a la entrada negativa.
El amplificador de instrumentación, conectado en configuración diferencial, se alimentó con una tensión de +5 V y -5 V. El multímetro se utilizó para comprobar que las fuentes entregaran la tensión de alimentación del amplificador y para validar el funcionamiento de la tarjeta de adquisición de datos. La salida del amplificador fue conectada a una de las entradas analógica de la tarjeta de adquisición de datos y la señal fue procesada mediante una aplicación en LabVIEW 2011. Esta última, es la encargada de tomar cada uno de los valores de la diferencia de tensión de los electrodos, filtrarlos y guardarlos en un fichero en formato Excel. Las muestras fueron tomadas a razón de una muestra por segundo durante cinco minutos, para un total de 300 muestras por cada valor de pH. La Figura 3 muestra el esquema de interconexión de los elementos que conforman el sistema de medición.
Resultados y Discusión
ELECTRODO VIDRIO/ITO/PANI
En la Figura 4 se muestra la lámina de Vidrio/ITO y el electrodo Vidrio/ITO/PANI obtenido luego de la deposición del polímero. Mediante un análisis visual se apreció una buena adherencia del polímero depositado.
ANÁLISIS POTENCIOMÉTRICO
La respuesta potenciométrica para cada uno de los valores de pH analizados se muestra en la Figura 5a. Como puede observarse, para valores de pH de 4, 7 y 10, las variaciones entre la señal tomada en el instante inicial de la medición y el instante final de las mediciones mostraron valores de 0,4%, 0,38% y 0,26% respectivamente. Por su parte, para los pH de 2 y 12 la señal disminuyó en un 2,74 % y 4,2% respectivamente. Teniendo en cuenta que las variaciones de las señales no superan el 5%, se considera que las señales se mantuvieron estables durante los 300 segundos de experimento.
La diferencia de potencial de los electrodos dependió del pH de la solución. Para analizar esta relación se obtuvo una curva de calibración (Figura 5b), donde cada punto corresponde al promedio de las tensiones medidas para los 5 minutos de experimento (300 muestras) y su correspondiente desviación estándar se ha representado con barras paralelas. La curva roja es el resultado del ajuste lineal que mostró un coeficiente de regresión de 0,98078. La sensibilidad, se obtiene a partir de la pendiente, y resultó de -55,12 mV/pH con un error relativo de 7,5 % con respecto al valor teórico de -59.16 mV/pH preestablecido por la ley de Nernst [22].
CONCLUSIONES
En este estudio se construyó un electrodo de Vidrio/ITO/PANI mediante la técnica Layer by Layer.Además, se caracterizó de forma experimental utilizando la técnica potenciométrica el electrodo obtenido con respecto a un electrodo de Ag/AgCl.La respuesta potenciométrica mostró una sensibilidad de -55,12 mV/pH con un error relativo de 7,5 % con respecto al valor teórico de -59.16 mV/pH correspondiente a un comportamiento nernstiano. De esta manera se comprobaron las potencialidades de la combinación del ITO y el PANI como materiales sensibles para la construcción de electrodos de pH.
REFERENCIAS
1. Alegret, S., M.d. Valle, and A. Merkoçi, Sensores electroquímicos. 2004, Bellaterra: Servei de Publications.
2. Manifacier, J., Thin Solid Films 1982.
3. Matveeva, E., Electrochemistry of the Indium-Tin Oxide Electrode in 1 M NaOH Electrolyte. Journal of The Electrochemical Society, 2005. 152 (9): p. H138-H145.
4. Mirkhalaf, F., D. Whittaker, and D.J. Schiffrin, Electrochemistry of ITO and gold electrodes covalently modified with dithizone and the effect of Cu(II) and Pb(II) ions. Journal of Electroanalytical Chemistry, 1998. 452: p. 203213.
5. Tsai, M.-C. and P.-Y. Chen, Voltammetric study and electrochemical detection of hexavalent chromium at gold nanoparticle-electrodeposited indium tin oxide (ITO) electrodes in acidic media. Talanta, 2008. 76: p. 533-539.
6. Bakker, E., Electrochemical sensors. Anal.Chem., 2004. 76(3285).
7. Crawford, G.P., Flexible flat panel displays. 2005: John Wiley and Sons Ltd. .
8. DuBow, J.B. Solar cells of indium tin oxide on silicon. in Electron Devices International Meeting1975.
9. Gardner, T.J., C.D. Frisbie, and M.S. Wrighton, Systems for Orthogonal Self-Assembly of Electroactive Monolayers on Au and ITO: An Approach to Molecular Electronics. J. Am. hem. SOC., 1995. 117: p. 6927-6933.
10. Heller, A. and B. Feldman, Electrochemical Glucose Sensors and Their Applications in Diabetes Management. Chemical Reviews, 2008. 108: p. 2482.
11. Wang, L. and E. Wang, A novel hydrogen peroxide sensor based on horseradish peroxidase immobilized on colloidal Au modified ITO electrode Electrochemistry Communications, 2004. 6: p. 225-229.
12. Yu, D. and K. Kim, Electrochemically Directed Modification of ITO Electrodes and Its Feasibility for the Immunosensor Development Bull. Korean Chem. Soc., 2009. 30(4).
13. Lee, T., H. Cai, and I. Hsing, Characterization of gold nanoparticles in organic or inorganic medium (ethanol/water) fabricated by spark discharge method. Analyst, 2005. 130: p. 364.
14. Pollack, M.G., R.B. Fair, and A.D. Shenderov, Electrowetting-based actuation of liquid droplets for microfluidic applications. Appl. Phys. Lett 2000. 77: p. 1725.
15. Sharma, I.D., et al. Modification And Designing Of Electrodeposited Polyaniline Films For Potential Applications. International Conference on Advances in Condensed and Nano Materials (ICACNM-2011). 2011.
16. MacDiarmid, A.G. and A.J. Epstein, POLYANILINE: SYNTHESIS, CHEMISTRY AND PROCESSING1992. p. TECHNICAL REPORT NO.: 1992-34.
17. Qin, Q. and Y. Guo, Preparation and Characterization of Nano-Polyaniline Film on ITO Conductive Glass by Electrochemical Polymerization. Hindawi Publishing Corporation Journal of Nanomaterials, 2012.
18. Zhu, B.-j., et al. Synthesis and characterization of the PANI/ITO conducting nanocomposites. in Materials Science Forum. 2011.
19. Al-Obeidi, A., et al., ITO/Poly(Aniline)/Sol-Gel Glass: An Optically Transparent, pH-Responsive Substrate for Supported Lipid Bilayers. Hindawi Publishing Corporation Journal of Materials, 2013.
20. Zhao, N., et al., Combining Layer-by-Layer Assembly with Electrodeposition of Silver Aggregates for Fabricating Superhydrophobic Surfaces. Langmuir, 2005. 21: p. 4713-4716.
21. Sartorius Basic Meter PB-20. www.sartorius.us/fileadmin/fm-dam/DDM/Lab.../MAN-PB-20-s.pdf‎ , 2000.
22. Kalantar-Zadeh, K., Sensors: An Introductory Course. 2013, School of Electrical and Computer Engineering. RMIT University: Melbourne, Victoria, Australia.
Recibido: Julio 2014
Aprobado: Septiembre 2014