Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Reumatología
versión On-line ISSN 1817-5996
Rev Cuba Reumatol vol.17 no.2 La Habana mayo.-ago. 2015
ARTÍCULO ORIGINAL DE INVESTIGACIÓN
Indicadores biológicos y de estrés oxidativo en la evolución de pacientes con artritis reumatoide
Biological and oxidative stress markers in the evolution of patients with rheumatoid arthritis
Iliana Sansaricq Coto I, Ela María Céspedes Miranda II, Evelia Juana Molinet Fuertes III, Marisol Peña Sánchez IV
IEspecialista de 1er. Grado en Laboratorio Clínico, Hospital Universitario "General Calixto García". Universidad de Ciencias Médicas de La Habana. La Habana, Cuba.
II MSc. Especialista de 2do. Grado en Bioquímica Clínica. Facultad de Ciencias Médicas "General Calixto García". Universidad de Ciencias Médicas de La Habana. La Habana, Cuba.
III MSc. Especialista 1er. Grado en Reumatología. Hospital Universitario "General Calixto García". Universidad de Ciencias Médicas de La Habana. La Habana, Cuba.
IV MSc. Licenciada en Ciencias Farmacéuticas. Instituto de Neurología y Neurocirugía. Universidad de Ciencias Médicas de La Habana. La Habana, Cuba.
RESUMEN
Introducción: la artritis reumatoide es una enfermedad autoinmune e inflamatoria crónica. En los servicios de reumatología se valora la evolución de los pacientes mediante velocidad de sedimentación globular y Proteína C reactiva. Se ha propuesto que el estrés oxidativo contribuye al daño tisular en las articulaciones.
Objetivo: analizar el leucograma y el daño oxidativo en pacientes con artritis reumatoide en períodos de crisis y remisión.
Método: estudio prospectivo en el que se realizó el conteo global y diferencial de leucocitos, la cuantificación de productos reactivos al ácido tiobarbitúrico, y la actividad de las enzimas superóxido dismutasa y catalasa en 23 pacientes con diagnóstico de artritis reumatoide en periodos de crisis y remisión. Se determinaron además proteína C reactiva, velocidad de sedimentación globular y factor reumatoide.
Resultados: el factor reumatoide fue mayor de 15 U/mL en el 82.61 % de los pacientes. El conteo de neutrófilos fue menor en la etapa de remisión en relación con la etapa activa de la enfermedad (4.21±1.24 vs 5.03±1.51 ×10-9/L; p=0.003), comportamiento similar al conteo global de leucocitos, la velocidad de sedimentación globular y la proteína C reactiva. Resultó relevante la menor actividad catalasa en los pacientes en remisión en relación con el periodo de crisis (445.31±281.87 vs 1046.08±659.77 U×L-1min-1).
Conclusiones: el comportamiento de los neutrófilos en la evolución hacia la remisión del paciente reumatoideo está en correspondencia con la velocidad de sedimentación globular, la proteína C reactiva y la disminución del estado inflamatorio. La actividad catalasa contribuye al desbalance redox y su actividad es consistente con una regulación adaptativa de la enzima para la protección contra el estrés oxidativo.
Palabras clave: artritis reumatoide, conteo diferencial de leucocitos, estrés oxidativo.
ABSTRACT
Introduction: rheumatoid arthritis is an autoimmune and inflammatory disease of unknown cause. In the Rheumatology services, the evolution of the patients is valued by means of erythrocyte sedimentation rate and C-reactive protein. It has been suggested that the oxidative stress contributes to the joint tissue damage.
Objective: to analyze differential leukocyte count and oxidative damage in patients with Rheumatoid Arthritis in crisis and remission periods.
Methods: prospective study in which global and differential leukocytes count, thiobarbituric acid reactive substances as a marker of lipid peroxidation, the superoxide dismutase, as well as the catalase activities were measured in 23 patients during their crisis and remission periods. C-reactive protein, erythrocyte sedimentation rate and rheumatoid factor were measured, too.
Results: rheumatoid factor was over 15 U/ml in the 82.61 % of the patients. A minor neutrophils count was observed in the remission period in relation to the active period of the disease (5.03±1.51 vs. 4.21±1.24 ×10-9/L, p=0.003), as well as the global leukocytes count, the erythrocyte sedimentation rate and the C-reactive protein. It was verified that the catalase activity decreased in remission state in relation to the crisis period (445.31±281.87 vs. 1046.08±659.77 U×L-1min-1).
Conclusions: in the evolution of the rheumatoid arthritis, the neutrophils count is in correspondence with the inflammatory state of the patients. Catalase activity is consistent with the regulation of this enzyme to protect against oxidative stress.
Keywords: rheumatoid arthritis, differential leukocytes count, oxidative stress.
INTRODUCCIÓN
La artritis reumatoide (AR) es una enfermedad inflamatoria, autoinmune, de origen multifactorial y de carácter sistémico, crónico y progresivo, que cursa en brotes y afecta las membranas sinoviales de múltiples articulaciones.1,2 Esta enfermedad está ampliamente distribuida en el mundo, se presenta en todas las razas y empeora con el aumento de la humedad atmosférica.3
Aunque los mecanismos fisiopatológicos son aun desconocidos, las infecciones, los fenómenos de hipersensibilidad y los mecanismos de autoinmunidad, así como la predisposición genética y los factores ambientales, desempeñan un papel importante.4-6
En la artritis reumatoide se produce activación de los leucocitos en el líquido sinovial, con liberación de citoquinas proinflamatorias y radicales libres que inician la inflamación y atraen a otras células inmunológicas al sitio.
Con el transcurso de la enfermedad, estas especies reactivas median la destrucción del cartílago y contribuyen a la sinovitis proliferativa. En particular, la interleuquina 8 podría ser la responsable de atraer neutrófilos, células que liberan también especies reactivas del oxígeno (ERO).7,8
Este incremento de las ERO y de otras especies oxidantes en relación con los sistemas antioxidantes, produce un desbalance en la homeostasis redox y en consecuencia, estrés oxidativo, alteraciones en la relación estructura-función de los diferentes niveles de organización biológica, en la regulación génica y modificación en la señalización celular, mecanismos moleculares básicos a considerar en la fisiopatología de la artritis reumatoide.9,10
No se dispone de un estudio específico para el diagnóstico definitivo y la valoración de la evolución de la enfermedad; sin embargo, en los últimos años los avances en el diagnóstico están relacionados con la detección de autoanticuerpos contra péptidos citrulinados cíclicos y de citoquinas proinflamatorias.11
Hallazgos notorios para los servicios de reumatología nacionales resultan ser leucocitosis y trombocitosis, así como aumento de la velocidad de sedimentación globular en las fases activas de la enfermedad.12
Para Seven y colaboradores, el incremento en los marcadores de oxidación de lípidos, proteínas y ácido desoxirribonucleico, así como el deterioro de las defensas antioxidantes, conforman el papel del estrés oxidativo (EO) en la patogenia de la enfermedad.13 Si este EO condiciona el estado evolutivo de la AR, con remisión de la inflamación, la modificación de los biomarcadores de EO podrían asociarse al estado de la enfermedad.
En este estudio se analizan el conteo diferencial de los leucocitos e indicadores de estrés oxidativo en pacientes con AR en estado activo e inactivo de la enfermedad.
MÉTODOS
Se realizó un estudio analítico, de cohorte y prospectivo con 23 pacientes con diagnóstico de AR activa, procedentes del servicio de reumatología del Hospital Universitario "General Calixto García", en el período de enero del 2012 - enero del 2013. Se incluyeron pacientes entre 35 y 70 años, no obesos, sin hábitos tóxicos, enfermedades autoinmunes, u otra complicación con expresión clínica de la enfermedad, y que no ingirieron suplementos antioxidantes en los dos meses previos al estudio. Una segunda toma de muestra se realizó al paciente en etapa de remisión de la enfermedad.
El diagnóstico de AR (en crisis y en remisión) se definió según el Colegio Americano de Reumatología.14 Se trabajó según las normas establecidas en la convención de Helsinki y el Comité de Ética de la institución aprobó el estudio.
Muestras biológicas: El suero y el plasma se obtuvieron a partir de 10 mL de sangre de la vena cubital de las personas en ayunas de 12 horas.
Procedimientos analíticos: La velocidad de sedimentación globular (VSG) se determinó mediante el método de Westergren, y el conteo global y diferencial de leucocitos mediante un método automatizado multiparamétrico (en el analizador hematológico Abbott). Las células se clasificaron en tres subtipos: linfocitos, neutrófilos y Mid (conteo de monocitos, eosinófilos y basófilos), según los procedimientos analíticos del laboratorio clínico. La proteína C reactiva (PCR) se cuantificó mediante inmunoturbidimetría y para la determinación del factor reumatoide (FR) se utilizó un método cualitativo basado en la aglutinación semicuantitativa con látex.
Los productos reactivos al ácido tiobarbitúrico (PRATB) como indicador de la peroxidación lipídica se cuantificaron según Yagi,15 la actividad de la enzima Cu-Zn superóxido dismutasa (SOD) según Marklund y colaboradores,16 y la actividad de la catalasa (CAT) se realizó mediante la técnica referida por Aebi en 1984.17
Procesamiento y análisis de los datos
El análisis de los resultados se realizó mediante el paquete estadístico SPSS 15.0 para Windows. Se determinó la distribución de frecuencias por sexo y grupos etáreos, así como los estadígrafos de posición de las variables. Al rechazarse la hipótesis de una distribución gaussiana para algunas variables se estimó la diferencia entre los grupos mediante estadística no paramétrica, que incluyó el análisis de dos muestras relacionadas, mediante prueba de Wilcoxon para determinar la modificación de las variables en el tiempo.
RESULTADOS
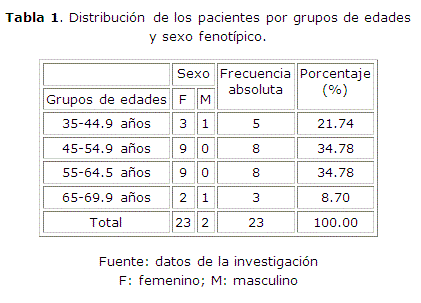
La distribución de los pacientes según la edad y el sexo fenotípico se presenta en la Tabla 1. El 69.56 % de los pacientes se encuentra entre los 45 y los 65 años, con predominio de las mujeres (91.30 %), siendo la edad media de 52.1 ± 8.76 años.
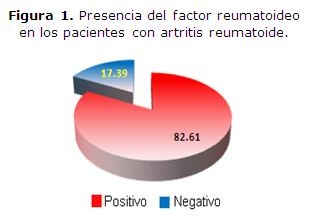
Como se observa en la Figura 1, el factor reumatoideo fue mayor de 15 U/mL en el 82.61 % de los pacientes.
En la Tabla 2 se presentan los estadígrafos de posición de los indicadores biológicos correspondientes a los pacientes en crisis y en remisión. El análisis de las variables revela que los neutrófilos disminuyen en la etapa de remisión en relación con la etapa activa de la enfermedad, comportamiento similar al conteo global de leucocitos, la eritrosedimentación y la PCR.
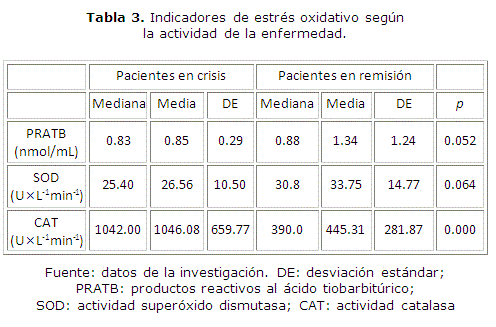
La concentración de productos reactivos al ácido tiobarbitúrico como indicador de la peroxidación lipídica, así como la actividad de las enzimas superóxido dismutasa extracelular y catalasa en etapa de crisis y de remisión de los pacientes se presentan en la tabla 3.
La actividad de ambas enzimas es superior en relación a valores de referencia (1.45 ± 0.50 y 161.00 ± 12.50 U×L-1min-1, respectivamente). Resulta relevante la menor actividad catalasa en los pacientes en remisión en relación con la etapa de crisis de la enfermedad.
DISCUSIÓN
El predominio de mujeres con AR en el estudio (más del 75 %) está en correspondencia con los cambios hormonales que se producen sobre todo en mayores de 45 años, hallazgo que coincide con los reportes de otros autores que refieren que una de las características de la mayoría de las enfermedades autoinmunes es que adultos del sexo femenino son más sensibles a padecerlas.8
Se reconoce la participación de los leucocitos en la patogenia de la enfermedad, al tenerse en cuenta que la AR es el resultado de una compleja interacción entre las células sinoviales y los leucocitos que infiltran desde la circulación. El incremento de estas células cuando es mayor la actividad de la enfermedad y la disminución en etapa de remisión obedece al propio proceso inflamatorio, aunque existen diferencias en los reportes de los niveles de leucocitos y AR. Los resultados que se presentan en relación con esta variable se corresponden con algunos autores. El recuento leucocítico suele resultar normal, aunque puede haber una leucocitosis leve. Roca reporta que los leucocitos aumentan, hasta llegar, durante los brotes, a 15×10-9 y más, con desviación izquierda.18
El FR está presente en el 82.61 % de los pacientes, criterio diagnóstico que distingue seropositivos de seronegativos para la AR.6 La disminución de la VSG y la PCR en etapa de remisión y el incremento en la etapa activa de la enfermedad igualmente está en relación con la propia disminución del proceso inflamatorio, lo que se corresponde con lo que refieren los diferentes autores, quienes reconocen que estos biomarcadores están acelerados cuando existe elevada actividad.8,19,20 De hecho estas determinaciones se utilizan en la práctica clínica para la evaluación de los pacientes.
En el estudio retrospectivo de Yousuf y colaboradores, con 567 pacientes, la VSG estuvo acelerada, mayor o igual a 100 mm/h en el 4.2 % de las realizadas; de las cuales el 15.9 % correspondieron a enfermedades autoinmunes, y un 7.3 % a pacientes con diagnóstico de AR.20 Resultado similar en relación con la eritrosedimentación y con la PCR fue reportado por Stamp en 2012, en 49 pacientes en crisis y 28 con baja actividad de la enfermedad.8 Asimismo, Li y colaboradores, de la universidad de Harbin reconocieron incremento en la PCR en 382 pacientes con diagnóstico de AR.21
El estado inflamatorio de la AR también fundamenta un incremento en la concentración de PRATB en los pacientes con AR en relación con personas saludables (valores de referencia: 0.41±0.37 nmol/mL). Se sabe que en estas condiciones los neutrófilos liberan radical superóxido por la intensa actividad enzimática, en particular de la enzima NADPH oxidasa. La participación del anión superóxido en los mecanismos de la inflamación es reconocida por diversos autores.22 Este anión puede reaccionar con el peróxido de hidrógeno y originar radical hidroxilo; también puede reaccionar con el óxido nítrico, para formar el peroxinitrito. La acción tóxica del radical hidroxilo y del peroxinitrito es aún más potente, lo que favorece la oxidación de los ácidos grasos insaturados presentes en las membranas celulares. El propio mecanismo de la peroxidación lipídica está en relación con la tendencia al incremento de los productos reactivos en etapa de remisión. La formación de productos finales requiere del ataque al ácido graso insaturado por las especies oxidantes, proceso que transita por la formación de hidroperóxidos. En la fase de terminación o descomposición de los hidroperóxidos lipídicos es que aparecen productos finales como aldehídos reactivos, que se detectan en muestras biológicas mediante la determinación de productos reactivos al ácido tiobarbitúrico.23
El grupo de Melguizo y colaboradores realizó un estudio caso control con 65 pacientes con diagnóstico temprano de AR. La determinación de hidroperóxidos lipídicos resultó más específica y sensible que otros marcadores de estrés oxidativo, de manera que este indicador mejoró el diagnóstico temprano de AR, en particular en pacientes con anticuerpos anticitrulinados negativos.24
El incremento en la concentración de PRATB en pacientes con AR activa en relación con personas sanas (valores de referencia) coincide con los resultados que Staron y colaboradores reportan. Este grupo determinó PRATB, glutatión reducido y actividad de las enzimas superóxido dismutasa (SOD), catalasa y glutatión peroxidasa en eritrocitos de 25 pacientes con AR y 35 personas saludables, encontrándose incremento en la peroxidación lipídica y disminución en la actividad SOD.25 Resultados similares fueron reportados por Baskol y colaboradores, al estudiar cincuenta y siete pacientes subagrupados de acuerdo a la actividad de la enfermedad;26 por Ozcan y colaboradores, en un estudio con 22 pacientes con AR,27 por el grupo de Seven, quien encontró incremento en los productos reactivos al ácido tiobarbitúrico y en los hidroperóxidos lipídicos en 20 pacientes con AR,13 y por Hassan en 30 pacientes.28 Vasanthi no encontró diferencias entre pacientes con AR activa e inactiva (estudio transversal), aunque si una tendencia al incremento de estos productos en la AR inactiva.29 La administración de un extracto de granada durante 12 semanas a ocho pacientes con respuesta inadecuada al tratamiento con drogas antirreumáticas inductoras de la remisión, produjo disminución de los síntomas y disminución en la peroxidación lipídica.19
La actividad de ambas enzimas es superior en relación a valores de referencia en respuesta a un incremento en los sustratos oxidantes, como el anión superóxido y el peróxido de hidrógeno. Solo la actividad catalasa resultó menor en los pacientes en remisión en relación con los pacientes en crisis. A su vez la actividad de la catalasa pudiera estar en relación con el conteo de polimorfonucleares, tanto en la etapa de crisis como de remisión. Durante la activación de estas células se libera ácido hipocloroso (HOCl), una especie reactiva de cloro, la cual se forma en presencia de peróxido de hidrógeno por la catálisis de la enzima mieloperoxidasa. Al compartir ambas enzimas el mismo sustrato, se ha sugerido que la catalasa parece regular la actividad de la mieloperoxidasa en los procesos de activación de los polimorfonucleares.30
El peróxido de hidrógeno es el sustrato para la actividad de la catalasa, por lo que en la medida en que ocurre la dismutación del radical superóxido por la SOD, se va incrementando la concentración de peróxido de hidrógeno y en consecuencia la actividad catalasa, sobre todo en altas concentraciones. El peróxido de hidrógeno es una molécula señal, relativamente estable, pequeña y sin carga por lo que puede atravesar fácilmente las membranas biológicas y producir efectos adversos más distantes que otras especies reactivas, además de formar el radical hidroxilo.31
En remisión, la actividad catalasa disminuye, como respuesta a la disminución directa de su sustrato, a pesar de la tendencia al incremento en la actividad SOD. La transformación del peróxido de hidrógeno también se realiza por la glutatión peroxidasa, que mantiene su actividad en presencia de glutatión reducido, el tiol no proteico más abundante a nivel intracelular y principal sistema de defensa frente a las agresiones oxidantes en las células. Por tanto, ambos sistemas se requieren para preservar la función celular cuando hay presencia de peróxido de hidrógeno.
La posibilidad de formación de otras especies radicálicas como el radical hidroxilo a partir del peróxido de hidrógeno, o del peroxinitrito, a partir del anión superóxido y el óxido nítrico, compromete la estructura lipídica y favorecería también la oxidación de ácidos grasos polinsaturados con incremento de los productos reactivos de la peroxidación.
La modificación en la actividad de las enzimas antioxidantes se reporta por diversos autores; sin embargo, los resultados son contradictorios. En algunos estudios se demuestra un descenso en la actividad de las enzimas, mientras que en otros se observa un incremento. En el estudio de Staron se verifica una disminución de la actividad SOD y en los niveles de glutatión reducido en pacientes con AR;25 sin embargo, en el estudio de Mansour en el 2008, se observa un incremento en la actividad de esta enzima, aunque describen la presencia de autoanticuerpos anti-CAT.32 Una elevada actividad catalasa se observó en el líquido sinovial de pacientes reumáticos por Igari,33 mientras que la actividad de la enzima estuvo disminuida en los pacientes del estudio de Staron y colaboradores,25 y del grupo de Cimen.34
La modificación en la actividad de las enzimas está en correspondencia con las concentraciones de sus sustratos y del funcionamiento del sistema redox de las células.
CONCLUSIONES
La disminución en el conteo global y de neutrófilos, así como de la VSG y la PCR en los pacientes en remisión está en correspondencia con la disminución del estado inflamatorio de los pacientes con AR. Aunque predominan los pacientes con leucograma dentro de los valores de referencia, tanto en crisis como en remisión, los neutrófilos constituyen un buen indicador de la evolución hacia la remisión del paciente reumatoideo; en correspondencia con la VSG y la PCR.
La actividad catalasa contribuye al desbalance redox en la AR y la disminución de su actividad en etapa de remisión en relación con la etapa de crisis es consistente con una regulación adaptativa de la enzima para la protección contra el estrés oxidativo.
REFERENCIAS BIBLIOGRÁFICAS
1. arly B, Baktir A, Cebicci M, Dogan Y, Demirbas M, Kurtul S, et al. Predictors of endothelial dysfunction in patients with rheumatoid arthritis. Angiology. 2014;65(9):778-82.
2. Ibn Yacoub Y, Amine B, Laatiris A, Hajjaj-Hassouni N. Rheumatoid factor and antibodies against citrullinated peptides in moroccan patients with rheumatoid arthritis: association with disease parameters and quality of life. Clin Rheumatol. 2012;31(2):329-34.
3. Charles J, Britt H, Pan Y. Rheumatoid arthritis. Aust Fam Physician. 2013;42(11):765.
4. Ogawa M, Matsuda T, Ogata A, Hamasaki T, Kumanogoh A, Toyofuku T, et al. DNA damage in rheumatoid arthritis: an age-dependent increase in the lipid peroxidation-derived DNA adduct, heptanone-etheno-2′-deoxycytidine. Autoimmune Dis. 2013; 2013:183487. Published online 2013 October 7. doi: 10.1155/2013/183487.
5. McInnes IB, Schett G. The pathogenesis of rheumatoid arthritis. N Engl J Med. 2011;365:2205-19.
6. Frisell T, Holmqvist M, Källberg H, Klareskog L, Alfredsson L, Askling J. Familial risks and heritability of rheumatoid arthritis. Role of rheumatoid factor/anti–citrullinated protein antibody status, number and type of affected relatives, sex, and age. Arthritis Rheumatism. 2013;65(11):2773-82.
7. Desai PB, Manjunath S, Kadi S, Chetana K, Vanishree J. Oxidative stress and enzymatic antioxidant status in rheumatoid arthritis: a case control study. Eur Review Med Pharmacol Sci. 2010;14:959-67.
8. Stamp LK, Khalilova I, Tarr JM, Senthilmohan R, Turner R, Haigh RC, et al. Myeloperoxidase and oxidative stress in rheumatoid arthritis. Rheumatology 2012;51:1796-803.
9. Jan Wruck C, Fragoulis A, Gurzynski A, Brandenburg L, Wai Kan Y, Chan K. Role of oxidative stress in rheumatoid arthritis: insights from the Nrf2-knockout mice. Ann Rheum Dis. 2011;70:844-50.
10. Avery SV. Oxidative stress and cell function. En: Laher I (ed). System Biology of free radicals and antioxidants. Vol I Part I. Cap. 4. New York: Ed. Springer-Verlag Berlin Heidelberg; 2014. p. 89-112. doi 10.1007/978-3-642-30018-9_10.
11. González-Álvaro I, Ortiz AM, Seoane IV, García-Vicuña R, Martínez C, Gomariz RP. Biomarkers predicting a need for intensive treatment in patients with early arthritis. Curr Pharm Design. 2015;21:170-81.
12. Smith HS, Smith AR, Seidner P. Painful rheumatoid arthritis. Pain Physician. 2011;14:E427-58.
13. Seven A, Güzel S, Aslan M, Hamuryudan V. Lipid, protein, DNA oxidation and antioxidant status in rheumatoid arthritis. Clin Biochem. 2008;41(7-8):538-43.
14. Arnett FC, Edworthy SM, Bloch DA, McShane DJ, Fries FJ, Cooper NS, et al. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum. 1988;31(3):315-24.
15. Yagi K. Lipid peroxides and human diseases. Chem Phys Lipids. 1987;45:337-51
16. Marklund S, Marklund G. Involvement of the superoxide anion radical in autoxidation of pyrogallol as a convenient assay for superoxide dismutase. Eur J Biochem. 1974;47:469-74.
17. Aebi H. Catalase in vitro. Methods Enzymol. 1984;105:121-6.
18. Roca R. Temas de Medicina Interna. 4ta. Ciudad de La Habana: Ed: Pueblo y Educación; 2002. p. 83-94.
19. Balbir-Gurman A, Fuhrman B, Braun-Moscovici Y, Markovits D, Aviram M. Consumption of pomegranate decreases serum oxidative stress and reduces disease activity in patients with active rheumatoid arthritis: A pilot study. Isr Med Ass J. 2011;13:474-9.
20. Yousuf M, Akhter J, Al-Khairy K, Al-Saadan MA, Bin-Salih S. Extremely elevated erythrocyte sedimentation rate. Etiology at a tertiary care center in Saudi Arabia. Saudi Med J. 2010;31(11):1227-31.
21. Li W, Li H, Song W, Hu Y, Liu Y, Da R. Differential diagnosis of systemic lupus erythematosus and rheumatoid arthritis with complements C3 and C4 and C-reactive protein. Experimental and therapeutic medicine. 2013;6(5):1271-6.
22. Nakamura T, Yamamoto T. Potential of a 70 kDa IL-10-like factor in synovial fluid from rheumatoid arthritis patients to augment superoxide generation by human neutrophils. International Journal of Rheumatic Diseases. 30 Sep 2013. doi: 10.1111/1756-185X.12166.
23. Ayala A, Muñoz MF, Argüelles S. Lipid Peroxidation: Production, metabolism, and signaling mechanisms of malondialdehyde and 4-hydroxy-2-nonenal. Oxid Med Cell Longev. [Internet] 2014 May 8 [citado 10 enero 2015]: doi: 10.1155/2014/360438. Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4066722/pdf/OMCL2014-360438.pdf
24. Melguizo E, Navarro N, Hernández B, Santos K, Arrobas T, Domínguez C, et al. Diagnostic utility of oxidative damage markers for early rheumatoid arthritis in non-smokers and negative anti-CCP patients. An Sist Sanit Navar. 2014;37(1):109-15.
25. Staron A, Mąkosa G, Koter-Michalak M. Oxidative stress in erythrocytes from patients with rheumatoid arthritis. Rheumatol Int. 2012;32(2):331-4.
26. Baskol G, Demir H, Baskol M, Kilic E, Ates F, Karakukcu C, Ustdal M. Investigation of protein oxidation and lipid peroxidation in patients with rheumatoid arthritis. Cell Biochem Funct. 2006;24(4):307-11.
27. Ozkan Y, Yardým-Akaydýn S, Sepici A, Keskin E, Sepici V, Simsek B. Oxidative status in rheumatoid arthritis. Clin Rheumatol. 2007;26:64-8.
28. Hassan SZ, Gheita TA, Kenawy SA, Fahim AT, El-Sorougy IM, Abdou MS. Oxidative stress in systemic lupus erythematosus and rheumatoid arthritis patients: relationship to disease manifestations and activity. Internat J Rheumat Dis. 2011;14:325-31.
29. Vasanthi P, Nalini G, Rajasekhar G. Status of oxidative stress in rheumatoid arthritis. Internat J Rheumatic Dis. 2009;12:2933.
30. Evans WH, Rechcigl M. Factors influencing myeloperoxidase and catalase activities in polymorphonuclear leokocytes. Biochim Biophys Acta. 1967;148:243-50.
31. Veal E, Day A. Hydrogen peroxide as a signaling molecule. Antioxid Redox Signal. 2011;15(1):147-51.
32. Mansour RB, Lassoued S, Gargouri B, El Gaïd A, Attia H, Fakhfakh F. Increased levels of autoantibodies against catalase and superoxide dismutase associated with oxidative stress in patients with rheumatoid arthritis and systemic lupus erythematosus. Scand J Rheumatol. 2008;37:103-8.
33. Igari T, Kaneda H, Houriuchi S, Ono S. A remarkable increase of superoxide dismutase activity in synovial fluid of patient with rheumatoid arthritis. Clin Orthop Relat Res. 1982;162:282-7.
34. Cimen MYB, Cimen OB, Kaçmaz M, Ozturk HS, Yorgancioglu R, Durak I. Oxidant/antioxidant status of the erythrocytes from patients with rheumatoid arthritis. Clin Rheumatol. 2000;19:275-7.
Los autores refieren no tener conflicto de intereses.
Recibido: 18 de febrero de 2015
Aprobado: 19 de marzo de 2015
Publicado: 31 de abril de 2015
Contacto para la correspondencia: Dra. Iliana Sansaricq Coto. E-mail: elaces@infomed.sld.cu
Hospital Universitario "General Calixto García". Universidad y Calle J, Vedado, Plaza de la Revolución, La Habana, Cuba. CP: 10400.