Introducción
El ácido hialurónico (AH) es un polímero lineal con un alto peso molecular. Se sintetiza en los fibroblastos de numerosos tejidos, pero es especialmente abundante en el líquido sinovial, es un infiltrado de plasma que posee función lubricante de las superficies articulares y aporta los nutrientes indispensables al cartílago óseo epifisario. El AH le proporciona su viscosidad al líquido sinovial.1,2Meyer y Palmer fueron los primeros en aislar en 1934 el AH del humor vítreo bovino y darle nombre a este compuesto.3
Durante el envejecimiento de la piel y de los cartílagos, la concentración de AH y su peso molecular promedio tienden a disminuir. Estas modificaciones provocan la pérdida de la elasticidad y la viscosidad de los tejidos, en especial del líquido sinovial.1 La mayor parte del AH que se encuentra en la articulación consta de 12 500 unidades de disacáridos que proporcionan a la molécula un peso de aproximadamente 5 000 kDa. En la osteoartrosis (OA) las concentraciones disminuyen desde la mitad hasta un tercio de su valor normal lo que provoca el empeoramiento de la lubricación de la articulación y hace que el cartílago se vuelva más sensible a las lesiones.4
El concepto de viscosuplementación fue propuesto por Balazs en 1986. Este método consiste en administrar por vía intrarticular inyecciones de soluciones viscoelásticas de hialuronato o sus derivados con el objetivo de restaurar las propiedades elásticas y viscosas del líquido sinovial y así reconstruir la homeostasis alterada en distintas estructuras enfermas como la articulación osteoartrósica.4-6
Estos compuestos suplementarios permanecen en la articulación durante un tiempo, en dependencia de la naturaleza del viscosuplemento y de la fisiopatología del compartimento tisular donde se administre.4,5
La primera vez que se utilizó la inyección intrarticular de hialuronato fue para tratar la artritis de los caballos de carreras. La respuesta resultó satisfactoria por lo que se continuó usando en veterinaria y se siguió investigando sobre sus efectos en humanos.7 Los primeros estudios terapéuticos en humanos en la OA de la rodilla fueron informados por Rydell y Balazs y Peyron y Balazs y varios años después por Weiss y otros. Desde entonces, los estudios han intentado determinar no solo si el hialuronato intraarticular en la OA es una técnica terapéuticamente útil, sino también los tratamiento óptimos, es decir, la frecuencia y el número de inyecciones, y si el peso molecular del hialuronato inyectado es una propiedad importante en su efectividad.5,8,9
El hialuronato utilizado en los tratamientos se extrae normalmente del cordón umbilical, de la cresta de gallo o de cultivos bacterianos.7 En España se comercializan seis productos, cinco de ellos compuestos por hialuronato sódico y uno por hilano G-F 20 (obtenido a partir del AH con mayor peso molecular que el hialuronato). Las marcas comerciales de estos productos son: Adant®, Hyalgan®, Orthovisc®, Ostenil®, Suplasyn® y Synvisc®. Dos de ellos, Adant® y Ostenil®, se obtienen mediante biotecnología, de los cultivos de la bacteria Streptococcus zooepidermicus. Otros tres, Hyalgan®, Orthovisc® y Synvisc®, se obtienen a partir de la cresta de gallo. Y el último, Suplasyn®, se obtiene por fermentación a partir de Streptococcus. El peso molecular de estos productos oscila entre 500 000 daltons (500 kDa) y 6 000 000 daltons (6 000 kDa).10
Debido a que actualmente existe una gran controversia acerca de la eficacia del tratamiento intraarticular con AH, el objetivo de este trabajo es conocer la eficacia de este tratamiento en las enfermedades articulares.
Métodos
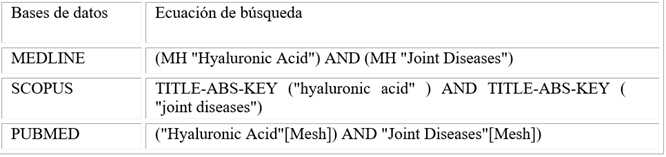
Para realizar este trabajo se ha llevado a cabo una revisión sistematizada de la bibliografía en las siguientes bases de datos: Medline, Scopus y PubMed durante los meses de febrero y marzo de 2018. Los términos empleados en las ecuaciones de búsqueda se basaron en los hallados en los descriptores MeSH: "Hyaluronic Acid" y "Joint Diseases". En la tabla 1 se muestra la ecuación de búsqueda empleada en cada base de datos.
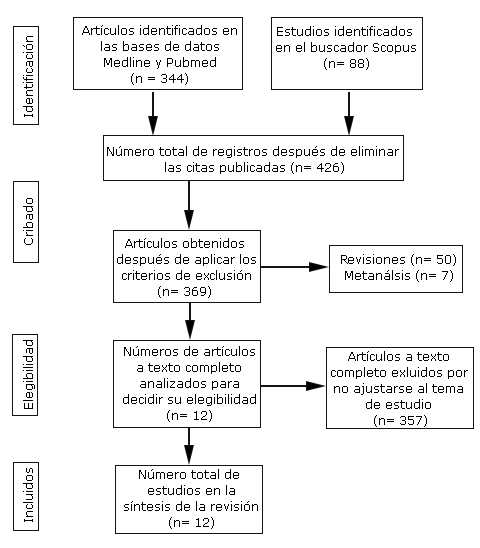
A la hora de seleccionar los artículos, de acuerdo con el objetivo planteado, se consideraron criterios de inclusión los artículos publicados en los últimos 5 años sobre estudios realizados en humanos y se excluyeron las revisiones bibliográficas y metanálisis, duplicados y los estudios que no se ajustaban al objetivo. En la figura 1 se puede observar el desarrollo de la búsqueda y los artículos seleccionados según los criterios anteriormente mencionados.
Resultados
En la tabla 2 se muestra el resumen de los principales los resultados del estudio. A continuación, se realizará el análisis de ellos atendiendo al tipo de estudio, la calidad del estudio, el tipo de muestra (número de participantes, edad, criterios de inclusión y enfermedad), los objetivos, los instrumentos de medida, el compuesto aplicado y los resultados obtenidos.
En relación con el tipo de estudio, se encontraron 8 estudios prospectivos,14,18-20 de los cuales 2 son aleatorios y controlados,12,21 2 aleatorios;15,22 3 ensayos clínicos,13,16,17 un caso control,16 un estudio multicéntrico controlado;13 y un estudio observacional.11
La escala JADAD es un sistema que permite evaluar de manera independiente la calidad metodológica de un estudio y proporciona una puntuación de 0 a 5, donde 0 es baja calidad metodológica y 5 buena calidad.23 Los artículos analizados en esta revisión muestran en general baja calidad metodológica puesto que ocho de ellos11,14,16-20,22 puntúan entre 0 y 1, otro21 obtiene 3 y solo tres de ellos12,13,15 alcanzan 4 o 5. La mitad de ellos,12,13,15,17,21,22 son aleatorios, pero solo tres12,13,15 son métodos a doble ciegas. El hecho de que no exista doble ciegas en los estudios puede sesgar de cierta manera los resultados, ya que la reacción de los pacientes ante el tratamiento al saber qué es lo que se les va a administrar puede ser distinta. El doble ciegas es importante sobre todo en estudios que presentan una valoración subjetiva24 como los analizados en esta revisión.
En cuanto al tamaño de la muestra, se observa demasiada variación en el número de sujetos ya que oscila entre los 20 participantes del estudio de Abate y otros11 y los 1 200 del estudio de Nikose y otros.19 Esta diferencia de pacientes se puede deber a que en el estudio de Abate y otros11 la enfermedad de estudio es el síndrome de choque femoroacetabular, una posible causa de la OA con una incidencia de 14-15 % según algunos estudios;25-27 sin embargo, la enfermedad de estudio de Nikose y otros19 es la OA de rodilla con una incidencia de 50 %.28 Además, la edad de los participantes también varía desde los 18 años hasta los 84, aunque el rango de edad más común13-20,22 es desde los 30-40 a los 70-80 años. La incidencia de este padecimiento aumenta con la edad y afecta al 25-30 % de los adultos en edades comprendidas entre 45 y 63 años y llega al 85 % en los adultos mayores de 60 años.29,30 Con respecto al sexo de los pacientes, la mayoría de las investigaciones incluyó hombres y mujeres, con excepción de 4 estudios11,12,21,22 que no lo especifican. En cuatro de los estudios predominaron las mujeres,13,14,16,20 tres de ellos tienen el mismo número15,17,18 de hombres que de mujeres y solo uno de ellos tiene más hombres en su muestra.19 La predominancia del sexo femenino en la muestra se debe a que esta enfermedad es más común en las mujeres.31,32
Hay que mencionar también los criterios de inclusión, ya que en 5 de los estudios13,15,17,20,22 los sujetos debían presentar OA con un Kellgren- Lawrence grados II o III según los criterios del Colegio Americano de Reumatología; en otros 2 estudios12-14 los sujetos debían tener OA con un Kellgren- Lawrence grados I o II; en otros 2 estudios se indicó la artroscopia;12,21 en el estudio de Abate y otros11 los sujetos tenían que presentar dolor, al menos, hacía 3 meses; en el de Guarda-Nardini y otros16 se incluyeron sujetos con OA crónica diagnosticada por resonancia magnética; en el de Murphy y otros18 los participantes presentaban OA primaria o postraumática; y por último, en el estudio de Nikose y otros19 todos los participantes padecían OA primaria sintomática. Como ya se ha observado en otros artículos,33 no se aprecia ninguna diferencia al aplicar este tratamiento en pacientes con distintos grados de OA, parece ser beneficioso sin importar la gravedad de la enfermedad.
Dentro de esta muestra podemos diferenciar sujetos con diferentes padecimientos como pueden ser: OA de rodilla,13-15,17,19,22 de cadera,17,20 de tobillo,18 o de la ATM;16 el síndrome de choque fémoro-acetabular;11 y con indicación de artroscopia12,21 tanto de rodilla como de muñeca. Los padecimientos más estudiados son la OA de rodilla y de cadera ya que son las articulaciones que soportan el mayor peso y por eso tienen mayor predisposición para padecer este cuadro clínico.34
En relación con el tipo de estudio debemos mencionar también que solo 4 de los 12 estudios cuentan con grupo control (GC).12,14,17,21 En el de Chu-Wen y otros14 el GC eran sujetos sanos y en el de Lùrati y otros17 eran sujetos con OA, en ambos estudios a los sujetos del GC solo se les realizaba seguimiento, no se les administraba ningún tratamiento. En los otros dos estudios,12,21 en el GC se realizó la artroscopia con un anestésico local. Otros 4 estudios establecen una comparación, ya sea entre grupos de edades,22 entre la presencia o no de derrame,16 entre las distintas dosis15 o con solución salina.13 Los cuatro restantes presentan un único grupo de tratamiento.11,18-20
Los instrumentos de medida utilizados fueron similares para todos los estudios, aunque solo 3 de ellos15,19,22 presentaron la misma valoración.
Para la valoración del dolor se usó la escala EVA,11,12,14-16,19-22 el cuestionario WOMAC,12,13,15,19,22) el índice de Lequesne,11,14,17 el cuestionario breve de dolor modificado (BPI II),20 y la escala Mayo Wrist Score (MMWS) modificada.21 Como puede observarse en la tabla, la escala EVA fue el instrumento de medición más común en todos los estudios.
Para valorar de la funcionalidad y la rigidez se aplicó el cuestionario WOMAC.12,13,15,19,22 Para el estado general, el cuestionario de calidad de vida (SF12)12 y la escala de Impresión Clínica Global (CGI).21
En los artículos se observa gran variedad de escalas, algunas de ellas son específicas para evaluar la enfermedad estudiada como el cuestionario de cadera Harris,11,20 el cuestionario FAOS18 para el pie y el tobillo o el cuestionario DASH ("Discapacidad de brazo, hombro y mano").21 Esta diversidad de escalas, todas ellas validadas, es positiva ya que permite medir distintos aspectos, pero por otro lado dificulta la comparación entre unos estudios y otros. Las escalas deberían estandarizarse para así poder realizar un análisis más completo. Cabe mencionar también que todas ellas son escalas subjetivas y sería interesante poder realizar una valoración más objetiva.
Tabla 2 - Principales características de los estudios analizados.
Autores
Muestra
Enfermedad
Instrumentos de medida
Evaluación
Intervención
Resultados
Abate y otros11
20
Síndrome choque fémoro-acetabular
Dolor -EVA
Dolor funcional- LI
Escala cadera -HHS
Consumo AINEs
Al inicio y a los 6 y 12 meses
4 inyecciones al inicio tras 40 días y se repitió a los 6 meses
Elevado peso molecular (32mg/2ml)
Se produjo una disminución significativa del dolor y la discapacidad en ambas escalas. El consumo del medicamento pasó de 3.6 ±2.2 a 1.3 ±1.3 comprimidos.
Anand y otros12
48
24 GE
24 GC
Artroscopia rodilla
Dolor -EVA
Funcionalidad-WOMAC
Calidad de vida- SF-12 medicación de rescate
Previo a la IQ;
a las 2 horas, 1 y 7 días;
3 y 6 semanas después de la IQ
GE-1 inyección 10 ml de AH
GC- 1 inyección bupivacaína
Se encontraron diferencias significativas en el dolor y en la escala WOMAC a las 3 y 6 semanas, al igual que el consumo de analgésicos.
La calidad de vida mejoró significativamente en el GE a partir de las 3 semanas.
Arden y otros13
218
GE- 108
GC-110
OA de rodilla
Funcionalidad - WOMAC
Estado general
Medicación de rescate
Inicio, 2, 4 y 6 semanas
GE- 1 inyección Durolane
60mg/3 ml
GC- 1 inyección 3 ml solución salina
Las puntuaciones del WOMAC fueron mayores para el GE pero sin alcanzar significación estadística. El estado global mostró mejorías significativas a partir de las 4 semanas. El consumo de medicamentos de rescate fue significativamente menor para el GE.
Chu-Wen y otros14
40
GE-25
GC- 15
OA de rodilla
Dolor- EVA
Dolor funcional- LI
Análisis de movimiento con cámaras
Inicio, 1 semana; 3 y 6 meses tras la última inyección
GE- 5 inyecciones de 2,5 ml de AH
Peso molecular 800kDa
GC- ninguna actuación
Se encontraron mejoras estadísticamente significativas en la escala EVA y el IL. Además se observó una mejora significativa en la velocidad de la marcha y la longitud del paso.
Diraçoğlu y otros15
41
G1- 21
G2-20
OA de rodilla
Dolor -EVA
Dolor, rigidez y funcionalidad- WOMAC
Inicio, inmediatamente después, al mes, 3 meses y 6 meses
G1- 1 inyección 4 ml de AH
Peso molecular 1 000-20 900 kDa
G2 -3 inyecciones (1 x semana) de 2,5 ml de AH
Peso molecualr 900-100kDa.
Hubo una mejora estadísticamente significativa en ambos grupos a los 6 meses en todos los parámetros con excepción de la rigidez.
No hubo diferencias significativas comparando ambos grupos entre sí, excepto en la escala EVA a favor del G1.
Guarda-Nardini y otros16
50
OA de la ATM
G1
G2
Dolor y amplitud de movimiento -EVA
Escala limitación funcional
Inicio, final y a los 3 y 6 meses.
G1 y G2- 5 inyecciones
1 ml de AH de peso molecular de 1200 kDa
Ambos grupos mostraron mejoras significativas en todos los parámetros medidos y se mantuvieron a los 6 meses de seguimiento. Sin embargo, las comparaciones entre los grupos no mostraron diferencias significativas en ninguna de las variables.
Lùrati y otros17
109
G1-49
G2- 37
GC-23
OA de cadera y rodilla
Dolor funcional - LI
Inicio y a los 3 meses del tratamiento
G1 - tratamiento estándar
G2- 3 inyecciones de 2 ml de AH de peso molecular de 800-1200 kDa
G3- sanos
A los 3 meses hubo una disminución significativa del dolor funcional en el G2.
Murphy y otros18
50
OA de tobillo
Inestabilidad del tobillo- FAOS
Inicio y a los 6 y 12 meses
3 inyecciones de 2 ml de AH de peso molecular 500-730 kDa cada 2 semanas
Mejora estadísticamente significativa en todos los dominios del cuestionario tras el tratamiento.
Nikose y otros19
1200
OA de rodilla
Dolor y AVD - EVA
Dolor, rigidez y funcionalidad -WOMAC
Inicio, al poner las dosis, a las 3 semanas y a los 3 y 6 meses.
3 inyecciones de 2 ml de AH de alto peso molecular (1 dosis cada 7-10 días)
Mejora estadísticamente significativa en todos los parámetros excepto en la rigidez medida en el cuestionario WOMAC.
Rivera20
207
OA de cadera
Dolor - BPI II y EVA
Cuestionario cadera- HHS
Inicio, a los 3, 6 y 12 meses después.
1 inyección de 3 ml de AH de alto peso molecular 2800 kDa
Hubo una mejora estadísticamente significativa entre el inicio en la escala EVA y el HHS y en la gravedad del dolor, puntuación de impacto y puntuación de impacto general del BPI.
Schütz y Dobner21
140
GE-70
GC-70
Artroscopia de muñeca
Funcionalidad- MMWS
Discapacidad - DASH
Dolor- EVA
Impresión clínica- CGI
Inicio, 3,6,12,y 24 semanas
GE-artroscopia + 2 inyecciones de 2 ml de AH de alto peso molecular (1300 kDa)
GC- artroscopia
Mejora estadísticamente significativa en MMWS en el GE. No se produjo diferencias en el DASH entre los grupos. Mejora en la escala EVA en ambos grupos, pero no entre los grupos. Mejora no significativa en CGI en ambos grupos que fue significativa a las 24 semanas en el GE.
Uçar y otros22
172
G1- 71
G2- 101
OA de rodilla
Dolor -EVA
Dolor, rigidez y funcionalidad -WOMAC
Inicio, 1 mes después de la 3ra inyección y un año después.
G1 (ancianos) y G2 (mediana edad) - 3 inyecciones de 30mg/ 2 ml (1 x semana)
Después de 12 meses se obtuvieron diferencias significativas en la EVA, WOMAC en el G2 con respecto al inicio del tratamiento, excepto en la rigidez. En el G1 no se encontraron estas diferencias.
BPI II - inventario breve del dolor; CDV- calidad de vida; DASH - cuestionario discapacidad brazo, hombro y mano; EVA. Escala analógica visual; FAOS- Foot and Ankle Outcome Scores; GC-grupo control; GE- grupo experimental; HHS- Cuestionario de cadera de Harris; IL- índice de Lequesne; IQ- intervención quirúrgica; MMWS- escala Mayo Wrist score; OA- osteoartrosis; kDa- kilodaltons; WOMAC - Western Ontario and McMaster Universities Osteoarthritis Index.
Las dosis aplicadas en los distintos estudios varían desde 1 única inyección12,13,15,20 hasta 5 inyecciones14,16 en intervalos de una semana. En cinco estudios se aplicaron 3 inyecciones: en tres de ellos 15,17,19 en intervalos de una semana; en otro,18 cada dos semanas y en el de Uçar y otros22 se aplicaron 3 inyecciones consecutivas. Con lo analizado en esta revisión se observa que con una única inyección se consiguen resultados óptimos, por lo que parece ser el tratamiento más efectivo. Estas conclusiones se observan también en el estudio de Monerris y otros.35
En cuanto al compuesto aplicado, la mayoría de los estudios utilizan AH de alto peso molecular, a excepción de dos de ellos,12,22 en los que no se menciona el peso molecular. Este peso varía desde 500 a730 kDa en el estudio de Murphy y otros18 hasta 2 900 kDa en el de Diraçoğlu y otros.15 El peso molecular medio aplicado es 1 000 kDa. Los estudios que aplican una única inyección son los que utilizan los mayores pesos moleculares, 2 800 kDa20 y 2 900 kDa.15) Por otro lado, los pesos moleculares más bajos 500 kDa,18 800 kDa,17 y 860 kDa14 se observan en los estudios que aplican varias dosis. La cantidad aplicada en 6 de los estudios11,17-19,21,22 es 2 ml; en otros dos,14,15 2,5 ml y 3ml,13,20 en el de Anand y otros12 se aplican 10 ml; en el de Diraçoğlu y otros, 4 ml15 y en el de Guarda-Nardini y otros, 1 ml.16
El tiempo de seguimiento de las investigaciones varía de un estudio a otro. Todos ellos realizan un seguimiento a corto plazo. El mayor tiempo de seguimiento es de 12 meses y lo realizan 4 estudios,11,18,20,22 6 meses de seguimiento realizado por 5 estudios.14-16,19,21Anand y otros12 y Arden y otros13 llevan a cabo un seguimiento de 6 semanas y Lùrati y otros,17 de 3 meses. Los resultados positivos se mantuvieron hasta 12 meses,11,18,20,22 aunque los efectos beneficiosos del AH no son permanentes, ya que el AH exógeno es eliminado de la articulación y el problema original continúa existiendo.4 Sería interesante observar qué pasa en esa articulación a lo largo del tiempo y no solo en un periodo de 12 meses, ya que si el cuerpo elimina un compuesto puede deberse a que sea perjudicial para él en cierta medida.
En cuanto a los resultados, todos los estudios llegaron a conclusiones a favor de las inyecciones de AH por vía intrarticular.
En cuanto a las variables estudiadas, todos los autores pretenden valorar la eficacia del AH para aliviar el dolor y mejorar la funcionalidad, a excepción del estudio de Guarda-Nardini y otros.16 que buscan determinar si la eficacia del AH depende de la presencia o no de derrame intrarticular.
Se obtuvo un mejora notable del dolor en todos los estudios en los que se aplicó la escala EVA11,12,14-16,19-22 y el cuestionario breve de dolor modificado (BPI II).20) En el estudio de Schütz y Dobner21 con pacientes sometidos a artroscopia, y en el de Guarda-Nardini y otros,16 con pacientes con y sin derrame, se obtuvieron mejoras considerables en ambos grupos. En el estudio de Uçar y otros22 se apreció una mejora significativa en el grupo de mediana edad (< 65 años) con respecto al de mayor edad; en el de Diraçoğlu y otros15 no se apreciaron diferencias en cuanto al dolor en actividad entre la aplicación de una única inyección y 3 inyecciones; sin embargo, en el dolor en reposo si se obtuvieron mejoras importantes en el grupo con una única inyección. Según Nikose y otros19) se lograron mayores beneficios en los sujetos que presentaban un Kellgren- Lawrence grados I o II. Hay autores4 que concluyen que este tratamiento es más efectivo en la OA con un Kellgren-Lawrence grados I o II, aunque en la mayoría de los artículos de esta revisión, como ya se ha mencionado anteriormente, no se observa diferencia entre los grados de OA ya que se obtienen beneficios sin importar la gravedad, lo cual que quedó demostrado en el trabajo de Fernández y otros.33
En todos los estudios en los que se aplica el índice de Lequesne como instrumento de medida, el dolor funcional disminuyó ostensiblemente.11,14,17 Los sujetos con un promedio de edad entre 45 y 65 años presentaban afectación de rodilla o cadera con un Kellgren- Lawrence grados I, II o III En todos ellos se aplicaron varias dosis de AH.
La funcionalidad y el dolor evaluados con el cuestionario WOMAC mejoraron notablemente en todos los estudios12,13,15,19,22en los que se aplicó. Sin embargo, en cuanto a la rigidez, medida mediante el mismo cuestionario, las mejoras tan solo fueron considerables en dos estudios12,13. En el estudio de Diraçoğlu y otros15 no se observaron diferencias entre la administración de 1 y 3 dosis; en el de Uçar y otros22 esta mejoría solo se obtuvo en el grupo de mediana edad; y en el de Nikose y otros19 los sujetos con un Kellgren- Lawrence I o II alcanzaron mayores beneficios. Todos los pacientes en los que se aplicó esta escala presentaban OA de rodilla. Este cuestionario se aplica en personas con OA de rodilla y cadera.36) La escala de cadera Harris mejoró notablemente en los dos estudios,11,20 en los que se analizó.
En cuanto al uso de medicación, este parámetro solo se valoró en tres estudios.11-13 En dos11,12 de ellos se produjo una disminución del consumo, pero esta solo fue significativa en el de Anand y otros.12 Por su parte, en el de Arden y otros13 el consumo fue estadísticamente mayor. Se desconoce cuál es el motivo de este resultado, ya que la única diferencia que se observa es la enfermedad de estudio, el síndrome de choque femoroacetabular en el de Abate y otros,11 una artroscopia de rodilla en el de Anand y otros12 y una OA de rodilla en el Arden y otros.13 Este dato es fuente de controversia ya que hay autores que muestran que no se producen diferencias en cuanto al uso de medicamentos en la OA de rodilla entre el GC y el GE,37) mientras que otros concluyen que si se produce una disminución en el consumo.38
La calidad de vida, medida mediante el cuestionario S-F 12, y el estado general fueron estudiados por Anand y otros12 y Arden y otros,13 respectivamente, y en ambos parámetros obtuvieron mejorías significativas. Este dato coincide con el estudio de Castellano y Pérez,39 quienes concluyeron que el AH mejora el estado general de los sujetos.
Por último, la velocidad de la marcha y la longitud del paso estudiados por Chu-Wen y otros14 fueron significativamente mejores. También se produjo una mejora significativa en cuanto a la escala Mayo Wrist Score (MMWS), la escala de Impresión Clínica Global (CGI) y en el cuestionario FAOS estudiados los dos primeros por Schütz y Dobner21 y el último, por Muyphy y otros.18 Sin embargo, en el cuestionario DASH, aplicado por Schütz y Dobner,21 estas mejoras no fueron significativas. Estas son variables menos estudiadas por lo que resulta difícil realizar una comparación con otros estudios.
Conclusiones
Las inyecciones de AH por vía intraarticular parecen ser un tratamiento beneficioso en cuanto al alivio del dolor y la mejoría de la funcionalidad, y seguro y efectivo en distintas enfermedades articulares. Sin embargo, no quedan claros los beneficios en cuanto a la rigidez de la articulación, ya que no hay semejanzas en los resultados.
No se han podido esclarecer las dosis y los pesos moleculares más adecuados para el tratamiento por lo que sería interesante realizar futuras investigaciones controladas para poder estipular estos aspectos.
Debería realizarse también un seguimiento a largo plazo para poder valorar durante cuánto tiempo persisten los efectos, o si por el contrario aparecen secuelas.
Estos estudios futuros deberían ser a ciegas y con un grupo control al que se le aplicara un tratamiento placebo para que así los resultados fueran más fiables.