INTRODUCCION
Las Especies Reactivas de Oxígeno (ERO) se definen como especies químicas derivadas del oxígeno con características redox suficientes para ser potencialmente reactivas. (León et al. 2005; Semchyshyn y Lozinska, 2012; Lushchak, 2014; Halliwell y Gutterridge, 2015).
Las ERO se generan continuamente en el organismo a partir de fuentes endógenas y exógenas por lo que constituyen componentes normales de células y tejidos (León et al. 2005; Brandes et al. 2014; Lushchak, 2014; Halliwell y Gutterridge, 2015). Teniendo en cuenta que las ERO tienen una alta reactividad e interaccionan con diversas estructuras celulares como proteínas, lípidos y ácido desoxirribonucleico (ADN) modificando la estructura y función de las mismas (León et al. 2005; Nair et al. 2007); los sistemas biológicos han desarrollado toda una serie de mecanismos de defensa antioxidante para prevenir la formación de estas ERO o disminuir su efecto perjudicial sobre la célula (De Zwart et al. 1999; León et al. 2010; Li et al. 2013; Halliwell y Gutterridge, 2015; Caverzan et al. 2016).
El desbalance entre las sustancias o factores pro-oxidantes y los mecanismos de defensa antioxidantes conlleva al estrés oxidativo (Muller et al. 2007), el cual juega un papel importante en el desarrollo y progresión de diversas patologías (León et al. 2005; Li et al. 2013; Kumar et al. 2015; Mohammad et al. 2016).
Teniendo en cuenta estos antecedentes y como parte de la adopción de estilos de vida más sanos el consumo de suplementos nutricionales antioxidantes ha cobrado auge en las últimas décadas y la evaluación de sustancias con potenciales efectos antioxidantes es un tema de actualidad.
El extracto de semilla de uva (ESU) (Vitis vinifera L.) es un producto natural rico en polifenoles, comúnmente utilizado como suplemento nutricional por sus propiedades antioxidantes. El tratamiento oral con ESU previene el daño hepático inducido en ratas: por isquemia y reperfusión; con tamoxifeno y tetracloruro de carbono (CCl4) (Sehirli et al. 2008; El-Beshbishy et al. 2010; Sharma et al. 2012). Además, ejerce efectos antioxidantes en plasma y en tejido hepático de ratas diabéticas (Chis et al. 2009; Giribabu et al. 2015).
El D-005, extracto lipídico saponificado obtenido del fruto de la palma corojo (Acrocomia crispa), palma endémica de Cuba, de la familia Arecaceae, contiene una mezcla reproducible de ácidos grasos, principalmente oleico, palmítico, laúrico y mirístico mientras el palmitoleico, caprílico, caprico, y esteárico se encuentran en menores concentraciones (González et al. 2015; Sierra et al. 2015).
Diversos estudios han demostrado que los ácidos grasos poliinsaturados tales como el ácido palmítico y el linoleico tienen la capacidad de secuestrar in vitro radicales libres (Chan et al. 1996; Steenkamp et al. 2006). Por otra parte, ha sido descrito los efectos antioxidantes del ácido oleico (Duval et al. 2002). En consonancia con estas evidencias extractos de origen natural que contienen estos ácidos en su composición química poseen propiedades antioxidantes (Chan et al. 1996; Hass et al. 1999; Steenkamp et al. 2006; Wang et al. 2010; Menéndez et al. 2005, 2007; Oyarzábal et al. 2019).
Teniendo en cuenta estos antecedentes, el objetivo de este trabajo es evaluar el efecto del D-005 administrado como dosis orales únicas sobre el incremento de indicadores de estrés oxidativo inducidos por CCl4 en ratas.
MATERIALES Y MÉTODOS
Animales
Se utilizaron ratas Wistar machos (150-250 g de peso corporal) provenientes del CENPALAB (Centro Nacional para la Producción de Animales de Laboratorio, La Habana), las cuales fueron adaptadas durante siete días a las condiciones de laboratorio (temperatura de 20 a 25 ºC, humedad relativa de 60 ± 5 % y ciclos de luz/oscuridad de 12 horas) con libre acceso al agua y la comida.
El manejo de los animales se realizó de acuerdo a las normas establecidas en la “Guía Ética para el Manejo de Animales de Laboratorio” (La Habana, Cuba, 1992) y los principios éticos para el uso de animales de laboratorio recomendados en los lineamientos internacionales y en la República de Cuba, “Principios de las Buenas Prácticas de Laboratorio no Clínico de Seguridad Sanitaria y Medioambiental del Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos 039/2004” (CECMED, 2004); así como los aspectos específicos plasmados en el Manual de Calidad y los Procedimientos Normalizados de Trabajo (PNT) del Centro de Productos Naturales (CPN) perteneciente al Centro Nacional de Investigaciones Científicas (CNIC), La Habana, Cuba. El protocolo del estudio fue revisado y aprobado por el Comité Institucional para el Cuidado y Uso de los Animales de Laboratorio (CICUAL) del CPN.
Administración y dosificación
El D-005 (Lote S-190213) (Laboratorio de Química Farmacéutica, CPN, CNIC, La Habana, Cuba) se preparó en forma de suspensión en Tween-65/H2O (2%) mientras que el ESU (Extracts, Healing & Medicinal Herbs, Australia), utilizada como sustancia de referencia, se disolvió en goma acacia al 1%. Ambos tratamientos se administraron como dosis orales únicas (5 mL/kg).
El CCl4, sustancia inductora del daño hepático y del estrés oxidativo, se preparó en forma de suspensión en aceite de soya (20%) y se administró por vía intraperitoneal (1 mL/kg).
Diseño experimental
Tras culminar la cuarentena, las ratas se distribuyeron aleatoriamente en siete grupos experimentales (10 ratas/grupo): un control negativo tratado oralmente con Tween 65/H2O (2 %) (vehículo) y aceite de soya (intraperitoneal) y seis grupos a los cuales se les indujo el daño mediante la administración de CCl4 (intraperitoneal): un control positivo tratado con vehículo, cuatro con D-005 (5, 25, 50 y 100 mg/kg) y uno con ESU (250 mg/kg).
La administración de los tratamientos se realizó una hora antes de la inducción del daño hepático mediante una inyección intraperitoneal única de CCl4. Transcurridas 18 horas los animales se anestesiaron en atmósfera de halotano para la obtención de las muestras.
Obtención de las muestras
Las muestras de sangre se tomaron de la aorta abdominal y se colectaron en dos tubos: uno con anticoagulante (ácido etilendiaminotetraacético -EDTA-) y otro sin anticoagulante”. Posteriormente, se centrifugaron a 3000 rpm durante 10 min para obtener los sueros y plasmas, los cuales se almacenaron a -20oC hasta su uso para cuantificar la actividad de las enzimas alanino aminotransferasa (ALT) y aspartato aminotransferasa (AST) así como variables oxidativas. Paralelamente, se colectaron muestras del tejido hepático (0,5g) que se homogenizaron en buffer Tris 150 mmol/L a pH 7,4 y se almacenaron a -20ºC hasta su uso.
Se determinaron con el juego de reactivos de la Firma Spinreact. La lectura se realizó a 340 nm, y los valores se reportaron como U/L.
Variables analizadas
Se realizó según la técnica de Ohkawa et al. (1979). Para ello, la mezcla de reacción (plasma u homogenato de hígado) se trató con 0,2 mL de dodecil sulfato de sodio (SDS) (8,1 %), 1,5 mL de ácido acético (20 %, pH 3,5) y 1,5 mL de una solución acuosa de ácido tiobarbitúrico (0,8 %) y se calentó a 95 ºC. Con el objetivo de evitar la producción de peroxidaciones adicionales que pudieran constituir un error en la determinación durante el proceso de calentamiento se adicionó hidroxi tolueno butilado (1 mmol/L) al medio. Después de terminar este paso, las muestras se enfriaron y se les adicionó 5 mL de una mezcla n-butanol:piridina (15:1 v/v). Posteriormente, se agitaron vigorosamente con la ayuda de un vortex, se centrifugaron a 4000 rpm durante 20 min, se tomó la capa orgánica y se leyó su absorbancia a 534 nm en un espectrofotómetro. Para los cálculos de los niveles de SRATB se construyó una curva patrón con MDA bis (dimetil acetal). Los valores de MDA se reportaron como nmol de MDA/mg de proteína.
La concentración de proteína se determinó por el método de Lowry modificado (Marxwell et al. 1978).
Se realizó mediante la técnica descrita por Hu (1994), para lo cual se tomó una alícuota de 200 (L de la muestra (plasma u homogenato de hígado), se le añadió 600 (L de buffer TRIS-EDTA 20 mmol/L pH 8,2, 40 (L de ácido 5,5-ditio-bis- (2-nitrobenzoico) -DTNB- 10 mmol/L y 3,16 mL de etanol absoluto. Se incubó 20 min a temperatura ambiente y posteriormente se centrifugó a 3000 g por 10 min. La absorbancia del sobrenadante se leyó a 412 nm. Se hizo un blanco con DTNB y el total de grupos SH se calculó usando una absortividad de 13,600 cm-1M-1 y se expresó en mmol/L.
Manejo de datos y Análisis Estadístico
Las comparaciones con el control se realizaron mediante la prueba no paramétrica de la U de Mann Whitney. A priori se estableció un nivel de significación (= 0,05. Los análisis estadísticos se realizaron utilizando el paquete comercial Statistic para Windows (Release 6.0; StatSoft, Tulsa, OK, USA).
El análisis de relación dosis/efecto se realizó mediante el método de regresión lineal y correlación utilizando el programa Origin 8.0 (Origin Lab Corporation; USA, Version 8).
RESULTADOS
La Tabla 1 muestra los efectos de la administración de dosis orales únicas de D-005 (5-100 mg/kg) sobre los niveles séricos de las transaminasas (ALT y AST). Los animales del grupo control positivo (con CCl4) alcanzaron valores significativamente superiores con respecto a los animales del grupo control negativo (sin daño). Las dosis de D-005 comprendidas entre 25 y 100 mg/kg redujeron marcada y significativamente la actividad de ambas enzimas, mientras la dosis de 5 mg/kg no produjo efectos significativos sobre estas variables. El efecto fue dependiente de la dosis sobre ALT (r=0,9841 y p=0,015) y AST (r=0,9565 y p=0,043) donde en esta ultima la dosis efectiva media (DE50) fue de 17,6 mg/kg. Por su parte, la sustancia de referencia (ESU; 250 mg/kg) también redujo de modo marcado y significativo las concentraciones de ALT y AST.
Las Tablas 2 y 3 resumen los efectos del D-005 sobre los niveles de MDA y grupos SH en plasma y tejido hepático, respectivamente. El grupo control positivo mostró un incremento significativo sobre ambas variables respecto al grupo control negativo tanto en plasma como en tejido hepático. El D-005 redujo marcada y significativamente los valores de MDA y de grupos SH a las dosis comprendidas entre 25 y 100 mg/kg, si bien la dosis de 5 mg/kg no modificó estos valores. Sin embargo, el efecto sobre MDA en plasma resultó dependiente de la dosis (r=0,9583 y p=0,042) siendo la DE50 =13,2 mg/kg. Por su parte, el ESU (sustancia de referencia) redujo de modo marcado y significativo los niveles de MDA y de grupos SH tanto en plasma como en tejido hepático.
Tabla 1 Efectos del D-005 sobre las concentraciones séricas de las transaminansas
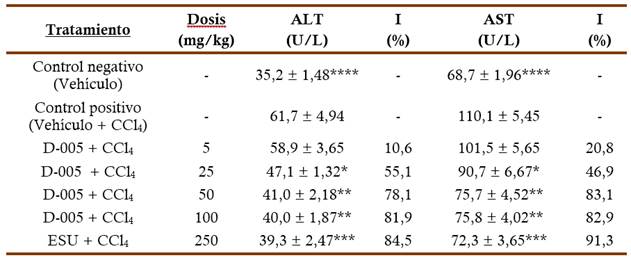
ALT alanino aminotransferasa; AST aspartato aminotransferasa; CCl 4 tetracloruro de carbono; ESU extracto de semilla de uva; I Inhibición Media ( EEM (error estándar de la media) *p<0.05, **p<0.01, ***p<0.001, ****p<0.001. Comparación vs grupo Control Positivo Test de la U de Mann Whitney
Tabla 2 Efectos del D-005 sobre los niveles plasmáticos de MDA y grupos SH

CCl 4 tetracloruro de carbono; ESU extracto de semilla de uva; I Inhibición; MDA malondialdehido; -SH- grupos sulfihidrilos Media ( EEM (error estándar de la media) *p<0.05, **p<0.01, ***p<0.001, ****p<0.001. Comparación vs grupo Control Positivo Test de la U de Mann Whitney.
Tabla 3 Efectos del D-005 sobre los niveles de MDA y grupos SH en homogenato de hígado
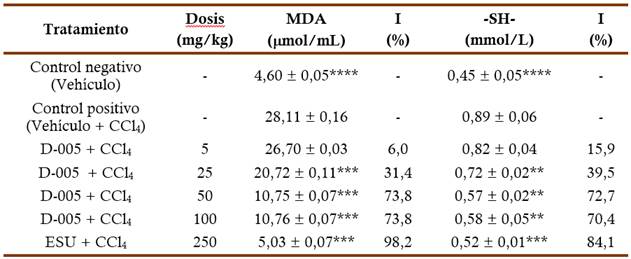
CCl 4 tetracloruro de carbono; ESU extracto de semilla de uva; I Inhibición; MDA malondialdehido; -SH- grupos sulfihidrilos Media ( EEM (error estándar de la media) **p<0.01, ***p<0.001, ****p<0.001. Comparación vs grupo Control Positivo Test de la U de Mann Whitney.
DISCUSION
En este trabajo se evaluaron los efectos del D-005, administrado como dosis orales únicas (5-100 mg/kg), sobre el incremento de marcadores de peroxidación lipídica (MDA) y oxidación proteica (grupos SH) inducidos por CCl4 en ratas.
Como se esperaba el grupo control positivo mostró un aumento significativo en la actividad de las transaminasas séricas, lo que demuestra que hubo un daño a nivel del tejido hepático que afectó su funcionalidad. Además, se incrementaron los niveles de MDA y los grupos SH en plasma y homogenatos de hígado con respecto al grupo control negativo. El incremento de los niveles de MDA y grupos SH observado en este estudio concuerda con reportes previos de la relación entre estas variables y la hepatotoxicidad inducida por CCl4, ya que la generación del radical triclorometil (CCl3 •) el cual reacciona rápidamente con el oxígeno formando el radical peróxido triclorometil (CCl3COO•) es capaz de atacar los ácidos grasos poliinsaturados de las membranas y desencadenar la peroxidación lipidica y/o dañar las proteínas que presentan en su estructura grupos SH (León et al. 2005; Favari et al. 2013). Por este motivo, el empleo del CCl4 como inductor del estrés oxidativo constituye un modelo experimental validado y ampliamente utilizado para evaluar sustancias con posibles efectos antioxidantes (Favari et al. 2013; Adewale et al. 2014; Laouar et al. 2017; Goodla et al. 2019).
Por su parte, el ESU, sustancia de referencia, redujo marcada y significativamente todas las variables analizadas, corroborando así sus efectos antioxidantes y hepatoprotectores demostrados anteriormente. (Belviranli et al. 2015; Hassan et al. 2016; Katsuda et al. 2015; Khazri et al. 2016).
Estos resultados son similares a los reportes de otros autores, y por ello le confieren validez al modelo experimental y a los hallazgos obtenidos en este estudio sobre los efectos del D-005.
El D-005 redujo de modo marcado y significativo el incremento de la actividad de la ALT y AST, inducido por CCl4, siendo 25 mg/kg la dosis mínima efectiva para ambas variables ya que la dosis de 5 mg/kg no produjo efectos significativos. Por su parte, la dosis de 100 mg/kg alcanzó el mayor porcentaje de inhibición (81,9 %) sobre la actividad de la ALT, mientras que el efecto alcanzado sobre la AST con la misma dosis (82,9 %) no fue superior al alcanzado con 50 mg/kg (83,1 % de inhibición) por lo que esta se comportó como la dosis máxima efectiva sobre esta variable. Este resultado demuestra el efecto hepatoprotector del D-005 ante el daño inducido por el CCl4.
De modo similar, el D-005 (5-100 mg/kg) previno de modo marcado y significativo el incremento de los niveles de MDA y grupos SH inducidos por CCl4 en plasma y homogenato de hígado, siendo 25 mg/kg la dosis mínima efectiva ya que 5 mg/kg no produjo efectos significativos sobre estas variables. La dosis de 50 mg/kg alcanzó los mayores porcentajes de inhibición, comportándose como la dosis máxima efectiva.
Los resultados obtenidos sugieren que el D-005 a las dosis ensayadas produce un efecto beneficioso significativo sobre el estrés oxidativo y el daño hepático inducido por CCl4, que pudiera estar dado por el ya conocido efecto antioxidante de los ácidos grasos que están presentes en el D-005, (González et al. 2015; Sierra et al. 2015) como por ejemplo se reporta que los ácidos palmítico, oleico y linoleico, son capaces de secuestrar in vitro los radicales libres e in vivo de inhibir la peroxidación lipídica. (Chan et al. 1996; Steenkamp et al. 2006, Wang et al. 2010; Menéndez et al. 2005, 2007; Oyarzábal et al. 2019)














