1. INTRODUCCIÓN
El biogás es principalmente una combinación de metano y dióxido de carbono producido por la Digestión Anaeróbica (DA) de la materia orgánica. El metano es un componente energético con un alto valor calorífico (~9,4 MJ m3) que puede ser usado en diferentes propósitos como la generación de calor para distintas aplicaciones y la producción de electricidad (British Standards Institution., 2005). Si el biogás es reformado y convertido en biometano, es posible emplearlo como combustible para los vehículos (Deublein y Steinhauser, 2008; Rajendran et al., 2012).
En la (DA) intervienen diversos grupos de bacterias y microorganismos que actúan en sinergia con el metano y el dióxido de carbono. El biogás obtenido ocurre luego de cuatro etapas cruciales tales como la hidrólisis, la acidogénesis, la acetogénesis y por último, la metanogénesis.
En la primera etapa, los sustratos complejos como los carbohidratos, las grasas y las proteínas son hidrolizadas para formar sus respectivos monómeros, como son la glucosa, los ácidos grasos, y aminoácidos. Seguidamente en la acidogénesis, estos monómeros hidrolizados son convertidos en diferentes ácidos grasos volátiles, tales como el ácido propiónico, ácido valérico e iso-valérico, ácido butírico e iso-butírico, y ácido acético.
A continuación, en la tercera etapa (acetogénesis), los ácidos grasos volátiles son convertidos en hidrógeno y dióxido de carbono. Finalmente, en la metanogénesis todos los productos de la acetogénesis son transformados en metano y dióxido de carbono (Álvarez, 2003; Nijaguna, 2006; Rajendran et al., 2013).
La producción de biogás está relacionada directamente por factores tales como la carga orgánica de alimentación (COA), el tiempo de retención hidráulica (TRH), la relación de carbono y nitrógeno, la tasa específica de crecimiento de microorganismos, el pH, amonio, la temperatura y la mezcla en general.
El estudio de estos factores sobre la base experimental, incluyendo el monitoreo de las reacciones metabólicas de las bacterias involucradas en la digestión anaeróbica, se hace costoso y complejo en la actualidad. Sin embargo, estos factores y el metabolismo intermedio en la digestión o fermentación pueden ser interpretados por la ayuda de modelos matemáticos sofisticados.
Los modelos más complejos involucran las inhibiciones desarrolladas acorde a los resultados propuestos por Angelidaki et al., (2000) y Vavilin et al., (1994).
Actualmente, el modelo ADM1 (Anaerobic Digestion Model No. 1) consigue más atención por los especialistas debido a su complejidad y los mecanismos de cinética en las reacciones involucradas (Batstone et al., 2002).
Recientemente, el modelo computacional propuesto por Blesgen y Hass, (2010), fue basado en sub-modelos que incluyen factores biológicos, físico-químicos, aplicados a reactores y plantas. La mayoría de los modelos desarrollados eran teóricos o matemáticos. Sin embargo, otros parámetros del proceso como la COA, el TRH y la termodinámica de las reacciones afectan de manera directa la producción de biogás dejando un área de investigación para estos modelos mencionados.
Los procesos de simulación son bien aceptados por las industrias y centros de investigaciones, por la posibilidad de predecir escenarios reales con exactitud. Los costos de simulación suelen ser inferiores a los ensayos de laboratorios y demás estudios experimentales.
Precisamente, el trabajo tiene como objetivo proponer un modelo de simulación de procesos (MSP) que permita estimar la producción de biogás y monitorear el metabolismo de la digestión anaeróbica (DA), a partir del software ASPEN PLUS V.8, de manera que permita integrarla en un futuro a otros equipos y componentes que conforman una planta industrial.
2. MATERIALES Y MÉTODOS
2.1 Descripción del Modelo
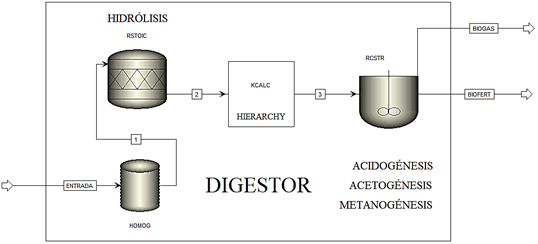
Para el MSP se consideran dos grupos de reacciones para la digestión o fermentación anaeróbica. Estos dos grupos (A y B) dependen de la complejidad de la reacción, definiéndose condiciones específicas para las etapas de la digestión (ver Figura 1).
En la formación de los azúcares, ácidos grasos y alcoholes se consideran reacciones de tipo estequiométrica donde la cinética de la reacción no es relevante. Los productos en dicha etapa dependen de una fracción de conversión para los reactantes.
Para la definición del MSP, se consideran las reacciones estequiométricas (A) que intervienen en la hidrólisis (Tabla 1) evaluadas por Rajendran et al., (2013), para una variación de la fracción de conversión de 0 a 1.
Tabla 1 Reacciones estequiométricas de la hidrólisis
| No | Componente | Reacción de hidrólisis | % Conv. |
|---|---|---|---|
| 1 | Almidón | (C6H12O6)n+H2O→nC6H12O6 | 0,6±0,2 |
| 2 | Celulosa | (C6H12O6)n+H2O→nC6H12O6 | 0,4±0,1 |
| 3 | Hemicelulosa | C5H8O4+H2O→2,5 C2H4O2 | 0,4±0,0 |
| 4 | Hemicelulosa | C5H8O4+H2O→C5H10O5 | 0,6±0,0 |
| 5 | Xilosa | C5H10O5→C5H4O2+3H2O | 0,6±0,0 |
| 6 | Celulosa | C6H12O6+H2O→2C2H6O+2CO2 | 0,4±0,1 |
| 7 | Etanol | 2C2H6O+CO2→2C2H4O2+CH4 | 0,6±0,1 |
| 8 | Proteína Soluble | C13H25O7N3S+6H20→6,5CO2+6,5CH4+3NH3+H2S | 0,5±0,2 |
| 9 | Proteína Insoluble (P.I) | P.I+0,3337H20→0,045C6H14N4O2+0,048C4H7NO4+0,047C4H9NO3+0,172C3H7NO3+0,074C5H9NO4+0,111C5H9NO2+0,25C2H5NO2+0,047C3H7NO2+0,067C3H6NO2S+0,074C5H11NO2+0,07C6H13NO2+0,046C6H13NO2+0,036C9H11NO2 | 0,6±0,1 |
| 10 | Trioleina | C57H104O6+3H20→C3H8O3+3C18H34O2 | 0,5±0,2 |
| 11 | Tripalmato | C51H98O6+8,436H2O→4C3H8O3+2,43C16H34O | 0,5±0,3 |
| 12 | Palmito-Oleina | C37H70O5+4,1H20→2,1C3H8O3+0,9C16H34O+0,9C18H34O2 | 0,6±0,2 |
| 13 | Palmito-Linoleina | C37H68O5+4,1H20→2,2C3H8O3+0,9C16H34O+0,9C18H34O2 | 0,6±0,2 |
Con la separación de las reacciones de hidrólisis se pueden estudiar los efectos del pretratamiento para aumentar la eficiencia del proceso, a partir de la simulación del modelo para diferentes sustratos.
Para el desarrollo de las etapas posteriores de la digestión anaeróbica, las cuales dependen de la cinética en las reacciones (B), se parten de los resultados obtenidos por (Angelidaki et al., 2000; Batstone et al., 2002; Serrano, 2011) (ver Tabla 2).
Tabla 2 Reacciones cinéticas de la degradación de aminoácidos y las etapas acidogénicas, acetogénicas y metanogénicas
| No. | Componente | Reacciones químicas |
|---|---|---|
| Reacciones de degradación de Aminoácidos | ||
| 1 | Glicina | C2H5NO2+H2→C2H4O2+NH3 |
| 2 | Teronina | C4H9NO3+H2→C2H4O2+0,5C4H8O2+NH3 |
| 3 | Histidina | C6H8N3O2+4H2O+0,5H2→CH3NO+C2H4O2+0,5C4H8O2+2NH3+CO2 |
| 4 | Arginina | C6H14N4O+3H2O+H2→0,5C2H4O2+0,5C3H6O2+0,5C5H10O2+4NH3+C02 |
| 5 | Prolina | C5H9NO2+H2O+H2→0,5C2H4O+0,5C3H6O2+0,5C5H10O2+NH3 |
| 6 | Metionina | C5H11NO2S+2H2O→C3H6O2+CO2+NH3+H2+CH4S |
| 7 | Serina | C3H7NO3+H2O→C2H4O2+NH3+CO2+H2 |
| 8 | Treonina | C4H9NO3+H2O→C3H6O2+NH3+H2+CO2 |
| 9 | Ácido-Aspártico | C4H7NO4+2H2O→C2H4O2+NH3+2CO2+2H2 |
| 10 | Ácido - Glutámico | C5H9NO4+H2O→C2H4O2+0,5C4H8O2+NH3+CO2 |
| 11 | Ácido - Glutámico | C5H9NO4+2H2O→2C2H4O2+NH3+CO2+H2 |
| 12 | Histidina | C6H8N3O2+5H2O→CH3NO+2C2H4O2+2NH3+CO2+0,5H2 |
| 13 | Arginina | C6H14N4O2+6H2O→2C2H4O2+4NH3+2CO2+3H2 |
| 14 | Lisina | C6H14N2O2+2H2O→C2H4O2+C4H8O2+2NH3 |
| 15 | Leucina | C6H13NO2+2H2O→C5H10O2+NH3+CO2+2H2 |
| 16 | Isoleucina | C6H13NO2+2H2O→C5H10O2+NH3+CO2+2H2 |
| 17 | Valina | C5H11NO2+2H2O→C4H8O2+NH3+CO2+2H2 |
| 18 | Fenilalanina | C9H11NO2+2H2O→C6H6+C2H4O2+NH3+CO2+H2 |
| 19 | Tirosina | C9H11NO3+2H2O→C6H6O+C2H4O2+NH3+CO2+H2 |
| 20 | Tiptofan | C11H12N2O2+2H2O→C8H7N+C2H4O2+NH3+CO2+H2 |
| 21 | Glicina | C2H5NO2+0,5H2O→0,75C2H4O2+NH3+0,5CO2 |
| 22 | Alanina | C3H7NO2+2H2O→C2H4O2+NH3+CO2+2H2 |
| 23 | Cisteína | C3H6NO2S+2H2O→C2H4O2+NH3+CO2+0,5H2+H2S |
| Reacciones acidogénicas | ||
| 24 | Dextrosa | C6H12O6+0,1115NH3→0,1115C5H7NO2+0,744C2H4O2+0,5C3H6O2+0,4409C4H8O2+0,6909CO2+1,0254H2O |
| 25 | Glicerol | C3H8O3+0,4071NH3+0,0291CO2+0,0005H2→0,04071C5H7NO2+0,94185C3H6O2+1,09308H2O |
| Reacciones acetogénicas | ||
| 26 | Ácido - Oleico | C18H34O2+15,2396H2O+0,2501CO2+0,1701NH3→0,1701C5H7NO2+8,6998C2H4O2+14,4978H2 |
| 27 | Ácido - Propiónico | C3H6O2+0,06198NH3+0,314336H2O→0,06198C5H7NO2+0,9345C2H4O2+0,660412CH4+0,160688CO2+0,0005H2 |
| 28 | Ácido - Isobutírico | C4H8O2+0,0653NH3+0,8038H2O+0,0006H2+0,5543CO2→0,0653C5H7NO2+1,8909C2H4O2+0,446CH4 |
| 29 | Ácido -Isovalérico | C5H10O2+0,0653NH3+0,5543CO2+0,8044H2O→0,0653C5H7NO2+0,8912C2H4O2+C3H6O2+0,4454CH4+0,0006H2 |
| 30 | Ácido - Linoleico | C18H32O2+15,356H2O+0,482CO2+0,1701NH3→0,1701C5H7NO2+8,4402C2H4O2+14,9748H2 |
| 31 | Ácido - Palmítico | C16H34O+15,253H2O+0,482CO2+0,1701NH3→0,1701C5H7NO2+8,4402C2H4O2+14,9748H2 |
| Reacciones metanogénicas | ||
| 32 | Ácido - Acético | C2H4O2+0,022NH3→0,022C5H7NO2+0,945CH4+0,066H2O+0,945CO2 |
| 33 | Hidrógeno | 14,4976H2+3,8334CO2+0,0836NH3→0,0836C5H7NO2+3,4154CH4+7,4996H2O |
En total se definieron diez bloques calculadores que determinaron los parámetros cinéticos correspondientes a la formación de aminoácidos como el glicerol, ácido valérico, acido butírico, ácido propiónico, ácido linoleico, ácido palmírico, ácido oleico, azúcares, así como la metanogénesis acetoclástica e hidrogenotrófica.
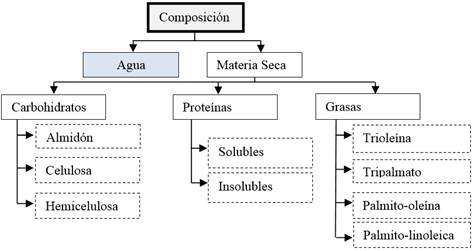
Se considera como materia prima en la etapa de DA, la materia orgánica compuesta por carbohidratos, proteínas y grasas.
Los compuestos que forman los carbohidratos son la celulosa, hemicelulosa y el almidón (ver Figura 2).
Las proteínas a su vez son consideradas en base a la solubilidad. Los componentes grasos desencadenan reacciones importantes en la DA, como son el trioleina, tripalmato, palmito-oleína, y palmito-linoleica.
Para cada bloque calculador los parámetros de inhibición en forma de pH, temperatura, y amonio fueron desarrollados a partir de un algoritmo lógico a partir el modelo ADM1.
Además, en cada entrada (nueva o reciclada), los bloques calculadores determinan los coeficientes de las reacciones ajustándose automáticamente a los parámetros más próximos a la realidad.
2.2 Desarrollo del modelo y operaciones
El proceso de simulación del modelo se desarrolla sobre la base de cuatro etapas para la producción de biogás, tales como la hidrólisis, acidogénesis, acetogénesis y metanogénesis. Estas cuatro etapas describen metabolismos intermedios que parten de la composición de sustratos formados por carbohidratos, proteínas y grasas donde se rompen en monómeros, transformándose finalmente en metano, dióxido de carbono y trazas de gases que se forman en menor cuantía. Las reacciones involucradas en las cuatro etapas fueron obtenidas en investigaciones previas (Andrews, 1968; Angelidaki, et al., 1993; Batstone et al., 2002; Vavilin et al., 1994), y fueron resueltas por Anderson y Bjedov (1996) usando el software MATLAB, pero no incluía la estequiometría de las mismas.
En esta sección, el procedimiento de (paso-por-paso) desarrollado por el modelo se define a continuación. Los compuestos requeridos para la simulación fueron definidos por la base datos del ASPEN PLUS considerando las propiedades físicas de cada elemento, así como la definición de algunos compuestos complejos y sus propiedades. (Wooley y Putsche, 1996).
El modelo termodinámico que se definió y recomendado por la literatura para el proceso en cuestión fue el NRTL (Non-Random Two-Liquid model). Dicho método correlaciona y calcula sobre la base de fracciones molares y coeficientes de actividad para diferentes componentes, facilitando el equilibrio vapor líquido.
En la tabla 3, se describen los modelos seleccionados. Estos reactores permiten desarrollar cada una de las etapas de la digestión, constituyendo ambos en conjunto como un reactor anaeróbico virtual para estimar la producción de biogás (Figura 3).
Todas las condiciones del proceso como los Sólidos Totales (ST), Sólidos Volátiles (SV), razón de flujo, composición másica, temperatura, y TRH del sustrato son definidas a la entrada de los parámetros de la simulación.
Tabla 3 Modelos seleccionados para la simulación
| Etapa | Modelos | Descripción |
|---|---|---|
| Hidrólisis | RSTOIC | Involucra 13 reacciones de conversión considerando la estequiometria |
| Acidogénesis | RCSTR | Involucra 33 reacciones considerando la cinética del proceso a partir del submodelo (ADM1) |
| Acetogénesis | ||
| Metanogénesis |
(RSTOIC, Stoichiometry Reactor; Reactor estequiométrico); (CSTR, Continuous Stirred Tank Reactors, Reactor continuo de tanque agitado)
Para ello, se considera la composición del sustrato porcino empleado por Fujita et al., (1980) la cual representa un 44,06% de carbohidratos, 23% de proteínas, y 4,9% de grasas para un total de 72% de sólidos volátiles. El volumen del reactor empleado es de 30 L con un tiempo de retención hidráulica de 8 días durante el proceso de fermentación (Fujita et al., 1980).
La razón de flujo de la materia orgánica representa la condición inicial del proceso de cálculo comenzando para el bloque de la hidrólisis la formación de monómeros que luego intervienen en las etapas posteriores donde se realiza el cálculo de sus parámetros cinéticos.
Durante la formación de aminoácidos a partir de la acción de monómeros, interviene un bloque calculador que define los parámetros cinéticos para diferentes ácidos grasos volátiles. Posteriormente, dichos ácidos grasos volátiles producen ácido butírico, ácido valérico, y ácido propiónico integrados a sus respectivos bloques calculadores donde finalmente sucede la metanogénesis. Por último, el bloque calculador en la metanogénesis determina los coeficientes para las reacciones acetoclástica e hidrogenotrófica. Como resultado de todas estas reacciones se define la cantidad de metano, dióxido de carbono y demás componentes de la producción de biogás.
En el calculador se asignan diferentes variables como la razón de flujo, la temperatura, parámetros cinéticos iniciales, que se importan de la cantidad de reactantes.
Los resultados del cálculo de los parámetros cinéticos fueron obtenidos por los modelos de estudios previos en la literatura especializada (Andrews, 1968; Angelidaki et al., 2000; Batstone et al., 2002). Para calcular la razón de reacción se emplea la ley de potencia del ASPEN PLUS, la cual incluye una tasa específica de crecimiento para los microorganismos. El pH fue calculado sobre la base del equilibrio químico constante dentro de los bloques calculadores (Angelidaki et al., 2000; Cheng, 2010).
El resultado obtenido en la simulación del proceso se desarrolló por un análisis riguroso del balance de masa y energía, donde la cantidad de biogás y el residual líquido (Bioabono) pueden ser calculados para cada estado de agregación.
2.3. Consideraciones para el análisis de sensibilidad del modelo.
Los factores de sensibilidad a estudiar tratan fundamentalmente sobre los efectos de la variación de la producción de biogás en el tiempo y su dependencia de la composición del sustrato.
Para la investigación se dispone de un solo valor experimental para un TRH definido, motivo por el cual se recurre al desarrollo de un modelo analítico desarrollado por Hashimoto y Chen (1980) válido para evaluar la sensibilidad del MSP. La variación del TRH describe una curva característica para la producción de biogás donde se puede monitorear el crecimiento bacteriano de la digestión anaeróbica.
Por otro lado, los compuestos del sustrato tienen una influencia directa en la producción del biogás y su composición resultante. Para evaluar esta relación se dispone de la composición del sustrato porción determinada por varios autores (Tabla 4).
Tabla 4 Composiciones típicas de sustrato porcino
| Referencia | Composición (Base seca) | |||
|---|---|---|---|---|
| Carbohidratos (%) | Proteínas (%) | Grasas (%) | Cenizas (%) | |
| (Fujita et al., 1980)* | 44,06 | 23 | 4,9 | 28,04 |
| (Cobos, 1988) | 67,39 | 15,87 | 4,69 | 12,05 |
| (Varnero, 1991) | 53,88 | 10,95 | 11,5 | 23,67 |
| (Peaece, 1977) | 56,27 | 23,98 | 7,17 | 12,58 |
*(Composición empleada para la validación del MSP)
Dicha información se inserta al (MSP) para las mismas condiciones de operación empleadas en la validación del modelo.
3. RESULTADOS Y DISCUSIÓN
3.1. Validación del modelo
Los resultados del MSP fueron validados a partir de ensayos de laboratorios realizados por Fujita et al., (1980), mostrando la diferencia entre el reporte de los datos y los calculados.
En la tabla 5 se muestran los resultados del MSP y la diferencia calculada con respecto al valor experimental. La diferencia comprendida corresponde a 0,29% para las condiciones de operación mostradas, evidenciándose una alta precisión de los resultados propuestos. Además de predecir la producción de biogás, el MSP permite analizar la composición del mismo con la finalidad de evaluar el rendimiento de la fermentación en general.
Con el empleo del MSP se puede estimar la producción de biogás y su composición resultante para una variedad de sustratos.
Tabla 5 Resultados del MSP para las condiciones de operación de Fujita et al., (1980)
| Carga orgánica | Experimental Resultado | Simulación Resultado | Error (%) |
|---|---|---|---|
| 230,4 g/d | 269 L/kg | 269,5 L/kg | 0,29 |
Frecuentemente la producción de biogás ocurre con un bajo contenido de metano (CH4), debido a múltiples efectos que inhiben el proceso de fermentación en general. El análisis de la composición del biogás resultante representa una herramienta útil para la concepción y el diseño de plantas industriales.
En la tabla 6 se muestra la composición del biogás producido para las condiciones experimentales realizadas por Fujita et al., (1980) y calculadas por el MSP. Los valores obtenidos de cada compuesto se comparan con rangos típicos propuestos por Deublein (2011) a partir de la literatura especializada.
Esta información tiene gran relevancia con la posibilidad de implementar acciones que contribuyan a una mayor producción de CH4. Además, la concentración de los compuestos secundarios define criterios de diseño para disminuir el deterioro en las instalaciones de los procesos posteriores de una planta.
3.2 Análisis de sensibilidad del modelo
La producción de biogás está estrechamente relacionada con el TRH. El crecimiento de los microorganismos involucrados en la digestión define la tasa de producción de biogás y la degradación gradual del sustrato.
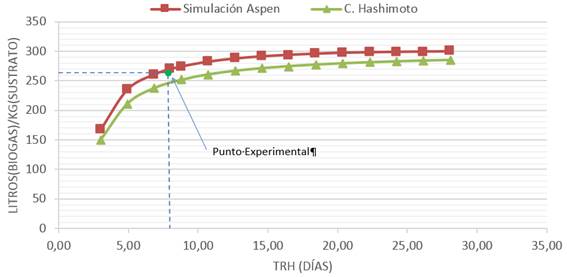
El análisis de sensibilidad se realiza a partir de los valores calculados por el modelo analítico de Hashimoto y Chen (1980) para las condiciones de operación. En la figura 4, se observa el comportamiento en el tiempo de la producción de biogás desarrollados por el (MSP) con respecto al modelo analítico propuesto por Hashimoto y Chen (1980).
El error máximo comprendido entre ambos modelos no supera el 5%, valor aceptado por la literatura ingenieril. De esta manera se ajusta una correlación acertada entre la producción de biogás del (MSP) y el modelo analítico propuesto por (Hashimoto y Chen, 1980) validándose su comportamiento en el tiempo.
Por otro lado, la composición del sustrato representa una condición importante para la producción de biogás. En la figura 5 se establece la relación obtenida mediante la simulación, entre la composición de sustratos definidos por los autores de la tabla 2 y la producción especifica de biogás resultante, así como la cantidad de (CH4) disponible. De esta forma se establecen relaciones importantes como son, la dependencia de la composición del sustrato con respecto a la producción específica de biogás y a la composición de metano obtenido. Para el caso experimental desarrollado por Fujita et al., (1980) la producción específica real es de 269 L/kg(sv) como se observa al inicio de la figura 5.

Figura 5 Comportamiento de la composición del sustrato vs producción específica y contenido de metano
Esto demuestra que los sustratos provenientes de distintas poblaciones porcinas tienen diversas producciones específicas de biogás y un contenido de CH4 específico. Esta relación depende en cierta medida del contenido de lípidos en el sustrato, así como otros factores determinantes. Finalmente, la composición del sustrato tiene una gran influencia en la producción de biogás. Precisamente, se recomienda continuar trabajando en el desarrollo experimental del proceso a partir de diferentes materias primas, de manera que permita perfeccionar la aplicación de los modelos simulados para la producción de biogás.
4. CONCLUSIONES
El (MSP) para la digestión anaeróbica desarrollado en ASPEN PLUS involucró todos los metabolismos intermedios de las fases de la fermentación; el mismo sirve como una biblioteca modelo para la digestión anaeróbica que incluye las reacciones intermedias de cada etapa de la digestión, factores de inhibición y los mecanismos cinéticos de las reacciones.
Al comparar la producción de biogás obtenida por el MSP y el experimental, la diferencia es de un 0,2%, para el sustrato porcino. La composición del biogás resultante de la simulación está dentro de los parámetros promedios definidos por la literatura técnica.
El MSP contribuye al ahorro de tiempo de análisis, dinero y energía para el estudio de nuevos sustratos o cambios en la composición, así como continuar el desarrollo de los mecanismos de DA con el propósito de integrarse a los procesos complejos de una industria real.