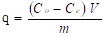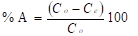INTRODUCCIÓN
Los colorantes han sido utilizados desde tiempos remotos para el teñido de vestiduras. Tienen origen natural ya sea vegetal o animal, aunque actualmente han sido desplazados por los colorantes sintéticos. Su empleo comprende un conjunto de industrias entre las que se incluyen la industria alimentaria, peletera, de cosméticos, papel, plásticos, pigmentos para pinturas, tintas de impresión y por supuesto la industria textil, su mayor consumidora. Como es lógico todas estas industrias vierten un volumen de desechos considerables que pueden causar daños ecológicos, sobre todo por la inhibición de la fotosíntesis; además, estos pueden sufrir una degradación incompleta y generar compuestos más tóxicos, afectando principalmente a los ecosistemas acuáticos (Elizalde y Peláez, 2005).
1.1. Rojo Congo
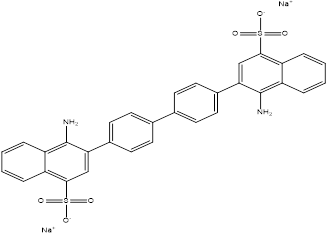
El Rojo Congo es una sal sódica del ácido 3,3'-([1,1'-bifenil]-4,4'-diyl)bis(4-aminonaftalen-1-sulfónico). Colorante diazóico con fórmula C32H22N6Na2O6S2 y de nombre 3,3'-([1,1'-bifenil]-4,4'-diyl)bis(4-aminonaftalen-1-sulfonato) de sodio con masa molar 696,68 g/mol. Es soluble en agua, donde llega a los 25 g/L a 293 K, formando una dispersión coloidal muy estable de color rojo, su solubilidad es mayor en disolventes orgánicos; en disolución acuosa alcanza un pH de 6,7 (10 g/L, 293 K) que se mantiene constante hasta concentraciones de 5 ppm. Es un sólido inodoro con aspecto de polvo rojo-marrón. Presenta importantes propiedades espectrofotométricas es la zona UV-visible con un intenso pico alrededor de los 498 nm en disolución acuosa con un coeficiente de extinción molar cerca de los 45 000 L/(mol•cm), (Merk, 2011).En la Fig. 1 se muestra una de las estructuras resonantes del colorante llamado Rojo Congo.
Fue sintetizado por primera vez en 1883 y rápidamente empleado como colorante directo sin la necesidad de mordiente. Presenta una fuerte afinidad por las fibras de celulosa, aparentemente una asociación no covalente. Sin embargo su empleo en la industria ha disminuido debido principalmente a su tendencia al cambio de coloración y su toxicidad. Se utiliza como indicador debido a su cambio de coloración de azul a rojo en el intervalo de pH de 3,0 a 5,2 (Finar, 1978).
Presenta actividad fluorescente al interactuar con las fibras amiloideas, característica empleada como herramienta de diagnóstico para la amiloidosis. Es utilizado también en bioquímica e histología como preparados de teñidos para microscopía (Potapov y Tatarinchik, 1979).
Está relacionado con la aparición de cáncer y presenta toxicidad para la reproducción, puede ocasionar trastornos durante el embarazo y se sospecha que puede causar daños al feto. Es altamente contaminante para los ecosistemas acuáticos (Jyoti, 2008).
El coco, científicamente llamado Cocos nucífera es una especie única del genero Cocos y pertenece a la familia Areacaceace. La planta que origina al coco, coqueiro tiene una vida perenne y puede alcanzar hasta 30 metros de altura. El coco es un fruto con cáscara dura, formada por el epicarpio, que es la cáscara externa verde y el mesocarpio, más interna que la anterior, formando la parte fibrosa (Vázquez y Torres, 2011).
La cáscara de coco es rica en celulosa y lignina. La primera varía de 35 a 43 % y la segunda de 23 a 43 %. Ambos biopolímeros son eficientes en la remoción de iones y moléculas. Estos constituyentes en combinación confieren la resistencia al fruto de la planta. En el caso del coco verde cerca del 85% corresponde a la cáscara (Silva et al., 2013). Esta investigación tiene como novedad científica encontrar el valor del diferencial del potencial químico presente en el sistema heterogéneo de masa solución de Rojo Congo-polvo de cascara de coco.
El presente artículo tiene como objetivo Determinar el modelo cinético y la isoterma de adsorción correspondiente al sistema heterogéneo, de una solución acuosa del colorante Rojo Congo y polvo de cáscara de coco a las temperaturas de 298 y 323 K.
MATERIALES Y MÉTODOS
2.1. Preparación del adsorbente
El material (cáscara de coco) previamente secada de forma natural al sol y temperatura ambiente, se somete a un tratamiento simple que se describe a continuación: se lavan para eliminar restos de impurezas de gran tamaño; se seca al sol, luego es triturado con un molino de martillo y tamizada la masa en un tamiz vibratorio para seleccionar el tamaño máximo de grano de 0,2 mm de diámetro que se utiliza en el estudio; posteriormente se lava con agua destilada con el objetivo de eliminar la mayor cantidad de iones que puedan ocasionar interferencia y finalmente se seca durante 90 minutos a una temperatura de 423 K para eliminar la mayor cantidad posible de agua.
2.2. Parámetros físicos
La determinación de parámetros físicos permite conocer las características fundamentales desde el punto de vista mecánico del material adsorbente (Prieto et al., 2020). El estudio se lleva a cabo con un tamaño de partícula máximo de 0,2 mm y se determinan los parámetros siguientes: densidad real, densidad aparente, densidad aparente por aprisionamiento, porosidad, compresibilidad, tortuosidad, superficie específica, velocidad de flujo y factor de forma (Prieto y Lestayo, 2017).
2.3. Parámetros químicos
El conocimiento de las propiedades químicas de cierto modo permite predecir el comportamiento adsortivo del sólido. Se destacan los óxidos totales (MO), humedad relativa (Hu), volátiles (V), cenizas (Cen), carbono (%C), hidrógeno (%H), oxígeno (%O), nitrógeno (%N), potasio (K), magnesio (Mg), sodio (Na) y calcio (Ca) (Prieto y Lestayo, 2017).
2.4. Técnica analítica
Se utiliza la espectrofotometría de adsorción molecular para la determinación de la concentración de los colorantes. Esta técnica se fundamenta en que la absorción de energía radiante por una sustancia bajo determinadas condiciones es directamente proporcional a su concentración y a la longitud del camino óptico (Ley de Beer). Es una técnica rápida y sencilla e ideal para la determinación de colorantes. Para esto se determina un máximo de absorción para el colorante y se construye una curva de calibración dentro del rango de concentraciones de trabajo para lo que se utiliza al Espectrofotómetro Ultravioleta Visible Termo-Electron, Modelo GENESIS-6, EE.UU. Todas las concentraciones en el estudio cinético y termodinámico fueron determinadas por esta vía. En la Fig. 2 se muestra la curva de ajuste para la concentración absorbancia de Rojo Congo en solución acuosa a una longitud de onda de 500 nm.
2.5. Proceso de adsorción
Primeramente se someten el material a un proceso de activación en una estufa a 373 K durante 90 minutos. El tamaño de partícula máximo empleado es de 0,2 mm de diámetro, tal y como se especificó en el epígrafe 2.2, las temperaturas de trabajo es de 298 y 323 K y el pH de las soluciones antes y después de cada proceso se mantuvo entre 6,8 y 7,2. Las concentraciones fueron determinadas por espectrofotometría de absorción molecular. Los modelos se ejecutan en forma lineal y se toma como criterio de selección el coeficiente de determinación. Además se calculan los factores siguientes mostrados en la ecuación 1 y 2:
Capacidad de adsorción:
Por ciento de adsorción (% A):
Donde:
q: capacidad de adsorción (mg/g).
C0: concentración inicial del soluto en solución (mg/L).
Ce: concentración de equilibrio del soluto en solución (mg/L).
m: masa del adsorbente (g)
V: volumen de disolución (L)
2.5.1. Cinética de proceso de adsorción
El estudio está dirigido a determinar la capacidad del adsorbente para retener el colorante bajo estudio en el tiempo. Para este estudio se prepararan tres soluciones de 800 mL, luego se puso en contacto con aproximadamente 1 gramo de adsorbente, por el tiempo necesario hasta que la concentración remanente en el seno de la disolución fuese constante, con agitación de 300 rpm en un agitador mecánico. Se toman muestras a intervalos regulares de tiempo, para la determinación de la variación de la concentración con respecto al tiempo de contacto. El empleo de tres soluciones simultáneamente evita pérdidas significativas de volumen y de adsorbente. Lo anterior se realiza a 298 y 323 K. Se calcula la capacidad de adsorción para cada concentración.
Posteriormente se evalúan cada uno de los modelos cinéticos más empleados, y se calculan las constantes asociadas con los modelos con mejor correlación. Las mediciones se hacen por triplicado.
2.5.2. Modelos cinéticos y difusivos empleados
Los modelos cinéticos y difusivos evaluados son los modelos de orden cero (OC), seudoprimer orden (SPO), seudosegundo orden (SSO), Elovich (ME), difusión intrapartícula (DPL), difusión en los poros según Bangham (MB), difusión en la película líquida (DPL) y Difusividad efectiva (De). Además, se determina la energía de activación del proceso difusivo, la variación de entropía y entalpía "aparente" del complejo activado de adsorción, el calor isostérico y el gradiente de potencial químico involucrado en el proceso adsortivo (Foo y Hameed, 2001), (Stoeckli, 2001), (Chun-I ( Li-Hua, 2008), (Eyring et al., 1949), (Prieto y Lestayo, 2017).
2.5.3. Modelos isotérmicos empleados
El estudio está dirigido a comprobar la posibilidad que tiene el adsorbente para remover de la solución el colorante empleado.
Para la realización del estudio termodinámico se prepararan siete disoluciones del colorante bajo estudio a diferentes concentraciones y se ponen en contacto 100 mL de estas con aproximadamente 0,06 gramos del adsorbente, por el tiempo determinado en el estudio cinético hasta alcanzar el equilibrio, con una agitación de 300 rpm. Posteriormente se separaran por filtración y se determina la concentración de equilibrio. Se calculan las capacidades de adsorción para cada disolución concentración a partir de las medias de las concentraciones luego de discriminar los valores erráticos y se determinan qué modelos termodinámicos se ajustan al proceso y las constantes asociadas a los de mejor ajuste. Las mediciones se hacen por triplicado. Se comprueban las isotermas de Langmuir (IL), Freundlich (IF), Toht (IT), Brunauer, Emmett, Teller (BET), Dubinin-Radushkevich (DR), Temkin (IT) y Flory-Huggins (FH) (Prieto y Lestayo, 2017), (Stoeckli, 2001), (Foo y Hameed, 2001), (Chun-I ( Li-Hua, 2008), (Sharma ( Janveja, 2008).
RESULTADOS Y DISCUSIÓN
3.1. Caracterización del adsorbente
Desde el punto de vista físico los parámetros más importantes del adsorbente Polvo de Coco obtenidos se muestran en la Tabla 1:
Tabla 1 Parámetros físicos del adsorbente Polvo de Coco
| Tamaño de partícula (mm) | ≤ 0,2 |
| Densidad aparente (g/cm3) | 0,15 |
| Densidad aparente de por aprisionamiento (g/cm3) | 0,28 |
| Densidad real (g/cm3) | 0,418 |
| Tortuosidad | 1,85 |
| Velocidad de flujo (mg/s) | 0 |
| Factor de forma | 0,4 |
| Porosidad (%) | 63,88 |
| Compresibilidad (%) | 46,64 |
| Superficie específica (m2/g) | 122,32 |
De forma general el material presenta valores de densidad inferiores a otros compuestos, como por ejemplo aquellos de base silícica como el dióxido de silicio (1,87 g/cm3) e incluso el propio silicio (2,53 g/cm3), lo que es de esperar debido a que están constituidos por una estructura básica de diferentes características.
El comportamiento del factor de compresibilidad es elevado, lo que responde a un acomodamiento de los granos al compactarlos.
La porosidad permite evaluar la rugosidad y la capilaridad. El valor es relativamente elevado, la cual posiblemente está relacionada con sus características amorfas.
Las superficies activas, en comparación con arcillas, arcillas calcinadas, cenizas de bagazo de caña de azúcar y zeolitas son elevadas, comparadas con las reportadas para este tipo de materiales (Prieto y Lestayo, 2017). Su velocidad de flujo es nula, lo cual refrenda una morfología de grano muy porosa. En la Tabla 2 se reflejan los valores de parámetros químicos obtenidos del adsorbente Polvo de Coco.
Tabla 2 Parámetros químicos del adsorbente Polvo de Coco
| pH | 7,1 |
| % Óxidos | 98,3 |
| Capacidad de intercambio catiónico | 20 |
| % Humedad | 8,8 |
| % Volátiles | 25,1 |
| % Cenizas | 15,3 |
| % C | 57,2 |
| % O | 37,9 |
| % H | 4,68 |
| % N | 0,2 |
| C/N | 286 |
| K (mg/g) | 5,13 |
| Na (mg/g) | 0,37 |
| Ca (mg/g) | 4,56 |
| Mg (mg/g) | 0,58 |
La solución acuosa del polvo de cáscara de coco tiene un pH= 7,1, lo cual refleja un carácter ácido-base, neutro. Presenta un 8,8 % de humedad, 15,3 % de cenizas y de material volátil 25,1 %. Lo anterior conduce a que el por ciento de carbón fijo sea 50,8. Es de destacar la baja humedad y la alta relación C/N, lo que rubrica la alta presencia de celulosa y lignina.
Los elementos químicos analizados en el polvo son Ca (II), Mg (II), Na (I) y K (I) cuyos valores respectivos se señalan: 4,56 mg/g, 0,58 mg/g, 0,37 mg/g y 5,13 mg/g. Como se aprecia es un material relativamente rico en potasio.
3.2. Resultados del estudio cinético
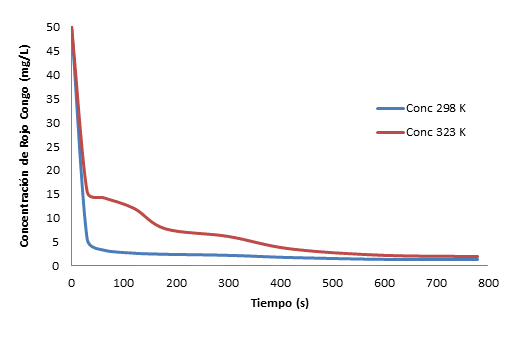
En la Fig. 3 se muestra la dependencia de la concentración de Rojo Congo con el tiempo y para las dos temperaturas de trabajo.
En la Fig. 3 se aprecia que el proceso adsortivo para alcanzar el equilibrio a 298 y 323 K requiere 30 y 400 minutos, respectivamente, donde la capacidad de adsorción son 9,76 mg/g para 298 K y 9,66 mg/g a 323 K. Es necesario señalar que la concentración de equilibrio a 298 K es 1,42 mg/L y 1,90 mg/L a 323 K.
A continuación se muestran los resultados referentes a los modelos cinéticos y difusivos aplicados (Prieto y Lestayo, 2017), (Stoeckli, 2001), (Foo y Hameed, 2001), (Chun-I ( Li-Hua, 2008), (Eyring et al., 1949). En la Tabla 3 se muestran los coeficientes de determinación obtenidos para cada modelo cinético y difusivo aplicado a 298 K y 323 K.
Tabla 3 Coeficientes de determinación para cada modelo aplicado a 298 K y 323 K
|
|
|
|
|---|---|---|
| Orden Cero | 0,815 | 0,980 |
| Seudoprimero | 0,949 | 0,965 |
| Seudosegundo | 0,999 | 0,990 |
| Elovich | 0,923 | 0,963 |
| Difusión intrapartícula | 0,958 | 0,883 |
| Difusión en le película de líquido | 0,814 | 0,968 |
| Bangham | 0,935 | 0,929 |
| Difusividad efectiva | 0,991 | 0,999 |
Como se aprecia el modelo cinético que mejor ajusta es el de seudosegundo orden, lo cual hace presumir un proceso físico de adsorción, cuya constante “aparente” de velocidad de adsorción 1,02 g/(mg•s) y tiempo de vida media t1/2 = 0,1 segundo a 298 K y 0,018 g/(mg•s) para 323 K con un tiempo de vida media t1/2 = 0,08 segundos. Lo anterior muestra la mayor constante “aparente″ de velocidad para la menor temperatura del proceso. Es un hecho que la cáscara de coco contiene celulosa, hidrocarburos aromáticos y alifáticos, alcoholes, aldehídos, cetonas, ácidos alifáticos, ceras, glicéridos y compuestos nitrogenados. Lo anterior presupone una interacción apreciable entre el Rojo Congo y el adsorbente polvo de cáscara de coco (Vázquez y Torres, 2011).
El valor de la capacidad de adsorción del Rojo Congo en solución acuosa es de 9,76 mg/g a 298 K y 9,66 mg/g para la temperatura de 323 K, lo cual hace del polvo de cáscara de coco un buen adsorbente del colorante bajo estudio. Los por cientos de adsorción para las temperaturas de 298 y 323 K son 97,2 y 96,2. Se infiere de este resultado que la mayor adsorción del colorante en el adsorbente ocurre a la menor temperatura.
En cuanto al mecanismo difusivo en base a los coeficientes de determinación se demuestra que la difusión efectiva es fundamental. El coeficiente de difusión efectivo a 298 K es 7,83•10-14 m2/s, valor relativamente bajo para otros tipos de adsorbentes. En este caso se toman como material poroso de comparación zeolita, silicato de calcio, arcilla y ceniza de bagazo de caña de azúcar, cuyos coeficientes de adsorción efectivos son del orden de 10-12 m2/s (Prieto et al., 2016). Para la difusión en la película líquida se sugiere considerarlo con cautela. Es de suponer que el espesor de la película en la interfase, fase líquida/fase sólida en un sistema discontinuo a templa (batch) con agitación a 300 rpm el espesor de la película se haya reducido hasta un límite que el mecanismo predominante que controle el proceso sea el difusivo en el interior del sólido.
El aumento de la temperatura no hace variar el modelo que mejor ajusta a los datos experimentales. En este caso el modelo de seudosegundo orden resulta el más satisfactorio. La constante “aparente” de velocidad de adsorción es 0,018 g/(mg•s). El valor de la capacidad de adsorción es 9,66 mg/g. El tiempo de vida media para esta temperatura es 0,08 segundos, menor que el correspondiente a 298 K que es 0,1 segundo. El valor de la capacidad de adsorción del Rojo Congo en solución acuosa es de 9,66 mg/g, el cual disminuye al aumentar la temperatura. El coeficiente de difusión efectivo es 1,09•10-13 m2/s. Al aplicar la ecuación de Arrhenius al proceso difusivo se establece la energía de activación del proceso de difusión 0,15 kJ/mol, valor relativamente bajo. El valor del factor preexponencial de adsorción Do encontrado es 4,86•10-12 m2/s (Karthikeyan y Sivakumar, 2010).
La causa de la adsorción es el gradiente de potencial químico, el cual es obtenido a partir de las diferencias de las concentraciones finales e iniciales del proceso de adsorción, cuyo valor es de 9,09 kJ/mol, este valor demuestra la efectividad de la adsorción del colorante en el polvo de cáscara de coco.
Un estudio de la energía libre involucrada en los procesos de adsorción manifiestan los valores ΔG298K = -4,13 kJ/mol y ΔG323K = -4,66 kJ/mol. Lo anterior permite obtener ΔH = -3,22 kJ/mol y ΔS = +3,54•10-3 kJ/ (mol•K), esto anterior refrenda un proceso espontáneo, exotérmico y de baja aleatoriedad.
3.3. Isotermas de adsorción
En la Tabla 4 se aprecian los coeficientes de determinación de las isotermas bajo estudio a 298 K y 323 K. Los valores aproximados de los coeficientes de determinación para los modelos de BET y Flory- Huggins hace necesario utilizar otros estadígrafos. La suma del error absoluto permite obtener para BET 0,016 y para Flory- Huggins 0,05. La suma del cuadrado de errores para el BET es 0,00007 y para Flory -Huggins 0,0011. Lo anterior corrobora que el modelo que mejor ajusta es el BET.
Tabla 4 Coeficientes de determinación para cada isoterma a 298 K y 323 K
|
|
|
|
|---|---|---|
| Langmuir | 0,367 | 0,982 |
| Freundlich | 0,491 | 0,789 |
| Toth | 0,268 | 0,860 |
| Dubinin-Raduchkevich | 0,466 | 0,891 |
| BET | 0,972 | 0,997 |
| Redlich | 0,848 | 0,853 |
| Flory-Huggins | 0,968 | 0,982 |
| Temkin | 0,886 | 0,789 |
Para el modelo de BET la constante de equilibrio es de 3,09 y una monocapa de sustrato de 0,60 mg/g. El modelo que mejor ajusta es el modelo de BET, que en este caso la constante de equilibrio toma el valor de 2,3 y la monocapa del sustrato 0,06. Se hace evidente como el aumento de temperatura hace disminuir la constante de equilibrio y el sustrato de la monocapa.
CONCLUSIONES
La cáscara de coco se destaca la elevada porosidad y nivel de compactación. Presenta como bioadsorbente una elevada superficie específica. La composición química muestra una relación C/N elevada, lo cual está condicionado por la presencia de la celulosa y la lignina. Los valores de la capacidad de adsorción son 9,76 y 9,66 mg/g a 298 y 323 K, respectivamente.
El estudio cinético muestra un comportamiento ajustable al modelo de seudosegundo orden y por tanto una adsorción física, la cual está condicionada por la interacción entre los componentes del polvo de cáscara de coco y el colorante Rojo Congo.
El proceso de adsorción en condiciones no isotérmicas refleja un proceso espontáneo, exotérmico y de baja aleatoriedad.
En el estudio de las isotermas de adsorción se pone de manifiesto un ajuste al modelo de BET, una adsorción de multicapas.