Meu SciELO
Serviços Personalizados
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Cubana de Química
versão On-line ISSN 2224-5421
Rev Cub Quim vol.26 no.1 Santiago de Cuba jan.-abr. 2014
ARTICULOS
Nuevo macrociclo tipo amino/amida: sintesis, caracterización y constantes de acidez/basicidad
New Amino/Amide Type Macrocycle: Synthesis, Characterization and Acidity/Basicity Constants
Lic. Yennys Hernández-Molina, Dr.C. Armando Ferrer-Serrano, Lic. Marian Blanco-Ponce
Facultad de Ciencias Naturales, Universidad de Oriente, Santiago de Cuba, Cuba. yhmolina@cnt.uo.edu.cu
RESUMEN
Se sintetizó un nuevo macrociclo tipo amino/amida empleando como reactivos de partida el ácido isoftálico activado con N-hidroxisuccinimida y N,N’-bis(3-aminopropil)-1,3-diaminopropano, a través del método de Alta Dilución. Su estructura fue confirmada por RMN1H, ESI-MS-MS y análisis elemental. Las constantes de acidez/basicidad del compuesto sintetizado fueron determinadas empleando el método potenciométrico, obteniéndose cuatro constantes de basicidad y una de acidez.
Palabras clave: macrociclo, amino/amida, síntesis, basicidad.
ABSTRACTS
A new amine/amide type macrocycle was synthesized using N-hydroxysuccinimide-activated isophtalic acid and N,N’-bis(3-aminopropyl)-1,3-propanediamine as starting compounds, through the High Dilution Method. Its structure was confirmed by 1H NMR, ESI-MS-MS and Elemental Analysis. Acidity/Basicity constants of the synthesized compound were determined by potentiometric titrations, it was determined four basicity constants and one acidity constant.
Keywords: macrocycle, amine/amide, synthesis, basicity.
INTRODUCCIÓN
Los macrociclos han atraído gran atención en consideración a sus interesantes propiedades como ligandos para formar complejos con cationes, aniones y moléculas neutras 1-5. Ellos han encontrado aplicaciones en áreas diversas como la Química Medicinal 6, Analítica 7 y Supramolecular 8-10.
Desde el primer reporte de poliaminas macrocíclicas, un gran número de estrategias han sido desarrolladas para la síntesis de esta clase de compuestos, incluyendo condiciones de alta dilución, el uso de plantillas y de precursores preorganizados conformacionalmente 11-13. Recientemente ha sido desarrollada una metodología para la síntesis de poli(amino/amido) macrociclos a través de la activación por formación de ésteres de N-hidroxisuccinimida 14 que es el procedimiento empleado en este trabajo.
MATERIALES Y MÉTODOS
Procedimientos generales
Todos los reactivos fueron adquiridos comercialmente, excepto el éster del ácido isoftálico con N-hidroxisuccinimida, el que fue sintetizado mediante el procedimiento descrito 14.
Los puntos de fusión fueron medidos en un equipo de temperatura de fusión WRS-2A SENON, las lecturas obtenidas no fueron corregidas. Los espectros de RMN1H, fueron realizados en un espectrómetro RMN Varian de 500 MHz, utilizando DMSO como solvente y TMS como estándar de referencia. Los espectros de masa (ESI-MS-MS) fueron obtenidos con un espectrómetro de masa Micromass Quattro LC (cuadrupolo-hexapolo-cuadrupolo) (Micromass, Manchester, UK) equipado con una interface ortogonal Z-spray para electrospray. Los análisis elementales fueron realizados en un analizador Therno Finnigan EA1112 Series Flash Elemental Analyser con un autosampler líquido y sólido AS 2000.
Las titulaciones potenciométricas fueron llevadas a cabo a 298,1 ± 0,1 K usando NaCl 0,1 mol/dm3 como fuerza iónica. El procedimiento experimental (bureta, potenciómetro, celda, agitador, microordenador, etcétera) ha sido descrito enteramente en otra parte 15. La adquisición de los datos potenciométricos fue realizada a través del programa CrisonCapture.
El electrodo de referencia fue un electrodo Ag–AgCl en solución saturada de KCl. El electrodo de vidrio fue calibrado a través una prueba de concentración hidrogeniónica por titulación de cantidades previamente normalizadas de HCl con soluciones de NaOH libre de CO2 y el punto de equivalencia determinado por el método de Gran 16, 17, que da los potenciales estándares, E°’, y el producto iónico del agua [pKw = 13,78(1)].
El programa HYPERQUAD 18 fue empleado para calcular las constantes de protonación, y el programa de HySS 19 fue usado para obtener los diagramas de distribución de especies. El rango de pH investigado fue 2,0–12,0 y la concentración del compuesto fue de 2,5 · 10-3 mol/dm3. El experimento se realizó por duplicado sin variaciones significativas en los valores de las constantes de protonación. Finalmente, los conjuntos de datos se combinaron y se trataron simultáneamente para dar las constantes de estabilidad finales.
Síntesis del ácido isoftálico activado
Se disuelven ácido isoftálico (5,00 g, 30,1 mmol) y N-hidroxisuccinimida (6,93 g, 60,2 mmol) en THF seco a 0 °C. Al obtener una disolución clara, se añade poco a poco DCC (12,48 g, 60,5 mmol) disuelto en THF anhidro y la disolución resultante se agita a 0-5 °C por 3 h. La diciclohexilurea formada se filtra y el filtrado se concentra hasta sequedad. El producto crudo se recristaliza de 2-propanol para obtener el producto puro. Rendimiento 5,41 g (48 %); T.f. 186-189 ºC; sólido blanco; RMN1H (500 MHz, DMSO-d6): d(ppm) 8,63(1H, s); 8,51(2H, d); 7,94(1H,t), 2,89(8H,m) Exp: C(52,29); N(6,82); H(4,9); Teo: C(53,34); N(7,78), H(3,6).
Síntesis del 2,16,22,36-tetraoxo-3,7,11,15,23,27,31,35-octazatriciclo[37.3.1.117,21]dotetraconta -1(41),17(42),18,20,37,39-hexaeno
En un balón de tres bocas se añaden 100 mL de DME. Por separado en embudos de adición se colocan 0,29 mL (1,42 mmol) de N,N’- bis(3-aminopropil)-1,3-diaminopropano en uno de ellos y en el otro 0,50 g (1,39 mmol) del éster del ácido isoftálico con N-hidroxisuccinimida. Ambos disueltos en DME. Se añade poco a poco (gota a gota) en el seno del disolvente receptor colocado en el balón, bajo agitación constante y en baño de hielo. Inmediatamente aparece una turbidez.
La mezcla se mantiene bajo agitación otras 12 h, luego se separa el sólido por filtración a vacío, se lava con DME y se recristaliza de 2-propanol. Rendimiento 72 %; t.f. 131-132 ºC; sólido blanco; RMN1H (500 MHz, DMSO-d6): d(ppm) 8,67 (2H,s, Ar-H); 8,28 (4H,d, Ar-H); 7,93 (4H,s, amida); 7,51 (2H,s, Ar-H), 3.31 (8H,t, -CH2-amida); 2,18-2,28 (4H,m,-NH-); 1,65 (8H,m, -CH2-); 1,52 (4H,m, -CH2-) ESI-MS-MS(m/z,%): 638,4 (M + 2H+, 6); 419,4 (MW-218,2 + 1, 26); 368,3 (C17H30N5O2+ + MeOH, 42), 335,3 ((M + MeOH + 2H+)/2, 19); 319,4 ((M + 2H+)/2, 11); 304,3 (MW-333,2 + 1, 100); 253,3 ((MW-132,02 + 3)/2, 88); Exp: C(63,23); N(18,34), H(8,56); Teo: C(64,12); N(17,60); H(8,23).
RESULTADOS Y DISCUSIÓN
Dado que la activación de grupos carboxilo para la formación de amidas, empleando N-hidroxisuccinimida como agente activante, se ha reportado 14 con buenos resultados para la obtención de compuestos peptidomiméticos; se decidió emplear esta vía para la síntesis del compuesto macrocíclico presentado en este trabajo.
Primero se realizó la activación del ácido isoftálico con N-hidroxisuccinimida, obteniéndose el éster con un 48 % de rendimiento. La estructura del éster fue confirmada por Análisis Elemental, así como por 1H-NMR. En este último espectro se observan las tres señales correspondientes a los hidrógenos aromáticos a 8,63; 8,51 y 7,94 ppm, respectivamente. Además, la señal correspondiente a los hidrógenos alifáticos del fragmento succinimídico, la cual aparece a 2,89 ppm, coincide con lo reportado para este tipo de compuestos 20.
La macrociclización se realizó, según se muestra en el esquema#1, por reacción del ácido isoftálico activado con N,N’-bis(3-aminopropil)-1,3-diaminopropano en condiciones de alta dilución, empleando el DME como solvente. Se obtuvo un sólido blanco con un rendimiento del 72 %. El producto fue caracterizado por Análisis Elemental, 1H-NMR y ESI-MS-MS.
En el espectro 1H-NMR se observan las señales correspondientes a los hidrógenos aromáticos a d = 8,67; 8,28 y 7,51 ppm, respectivamente. La señal perteneciente a los protones amídicos aparece a 7,93 ppm, en tanto la de los protones de amina secundaria se observa a 2,18 y 2,28 ppm. A 3,31 ppm se observa la señal correspondiente a los protones de grupos metilenos adyacentes a grupos amida y a 1,65 y 1,52 ppm los protones unidos a carbonos alifáticos entre grupos metileno.
La señal correspondiente a los protones de grupos metilenos adyacentes a los nitrógenos amínicos no se observa debido a que coincide con la señal de los protones de los grupos metilo del disolvente DMSO-d6.
En el espectro de masas por electrospray se observan picos correspondientes al macrociclo unido a una molécula de metanol, que es el disolvente empleado para la obtención de dicho espectro, y a fragmentos también unidos a dicha molécula. En este espectro, además, se observa el pico del pseudo-ion molecular a m/z 638,4, que se corresponde con la masa molecular del macrociclo más dos protones, confirmando la estructura del mismo.
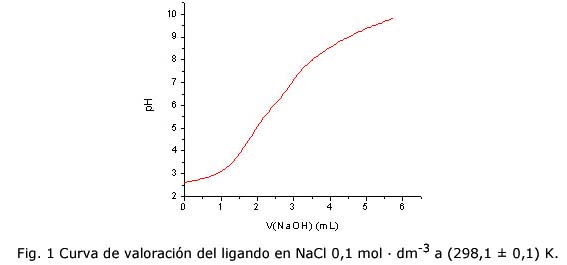
Luego, se determinaron por valoración potenciométrica las constantes de basicidad y acidez del compuesto macrocíclico obtenido, empleando el procedimiento arriba descrito. La figura 1 muestra la curva de valoración obtenida.
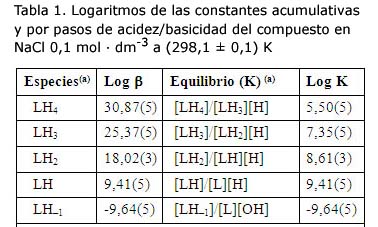
Fueron obtenidas cuatro constantes de basicidad y una de acidez para el rango de pH explorado (2-12), las que se muestran en la tabla 1, correspondiendo las de basicidad a los cuatro grupos amino del compuesto. El valor de la constante obtenida para la primera protonación del ligando se corresponde con otros valores obtenidos para aminas secundarias 21. La disminución en los valores de las constantes sucesivas puede ser racionalizada en base a la repulsión electrostática por la adición sucesiva de cargas positivas a una especie ya cargada positivamente.
En la figura 2 se muestra el diagrama de distribución de especies para el compuesto, observándose que por debajo de pH 5, este se encuentra totalmente protonado, en tanto la especie desprotonada comienza a aparecer por encima de pH 9, aproximadamente.
CONCLUSIONES
La constante de acidez obtenida podría atribuirse a la desprotonación de uno de los grupos amida del compuesto o a la hidrólisis de alguna molécula de agua unida a dichos grupos.
La primera de estas opciones es poco probable, debido a que la desprotonación de un grupo amida es en sí un proceso muy endoergónico, y solo puede tener lugar en medios muy alcalinos, o si esta contribución negativa está más que compensada por una interacción metal-ligando muy exotérmica 22.
BIBLIOGRAFÍA
1. MUNJAL, M.; KUMAR, S.; SHARMA, S. K.; GUPTA, R. "Nickel and Copper Complexes with Few Amide-Based Macrocyclic and Open-Chain Ligands". Inorg. Chim. Acta. 2011, 377, (1), p. 144–154.
2. CONSTABLE, E. C. Coordination Chemistry of Macrocyclic Compounds . New York: Oxford University Press, 1999.
3. HOSSAIN, M. A.; KANG, S. O.; POWELL, D.; BOWMAN JAMES, K. "Anion Receptors: A New Class of Amide/Quaternized Amine Macrocycles and the Chelate Effect". Inorg. Chem. 2003, 42, (5), p. 1397-1399.
4. ALFONSO, I.; BURGUETE, M. I.; GALINDO, F.; LUIS, S. V.; VIGARA, L. "Unraveling the Molecular Recognition of Amino Acid Derivatives by a Pseudopeptidic Macrocycle: ESI-MS, NMR, Fluorescence, and Modeling Studies". J. Org. Chem. 2009, 74, p. 6130–6142.
5. BURGUETE, M. I.; GALINDO, F.; LUIS, S. V.; VIGARA, L. "Ratiometric Fluorescence Sensing of Phenylalanine Derivatives by Synthetic Macrocyclic Receptors". Journal of Photochemistry and Photobiology A: Chemistry. 2010, 209, p. 61–67.
6. KIKUTA, E.; KIMURA, E. "A New Type of Potent Inhibitors of HIV-1 TAR RNA-Tat Peptide Binding by Zinc(II)-Macrocyclic Tetraamine Complexes". J. Am. Chem. Soc. 2001, 123, p. 7911-7912.
7. KHOPAR, S. M. Analytical Chemistry of Macrocyclic and Supramolecular Compounds . Berlin: Springer, 2002.
8. HOSSEINI, M. W.; LEHN, J. M.; MAGGIORA, L. K.; MERTES, B.; MERTES, M. P. "Supramolecular Catalysis in the Hydrolysis of ATP Facilitated by Macrocyclic Polyamines: Mechanistic Studies". J. Am. Chem. Soc. 1987, 109, p. 537-544.
9. HOSSEINI, M. W. "Supramolecular Catalysis of Phosphoryl Anion Transfer Processes". In: Supramolecular Chemistry of Anions . Bianchi, A.; Bowman James, K.; García España, E. (eds). New York: Wiley-VCH, Inc., 1997.
10. ATWOOD, J. L.; STEED, J. W. Encyclopedia of Supramolecular Chemistry . Taylor & Francis Group: 2004; p. 1-872.
11. DIETRICH, B. "Macrocycle Synthesis". In: Encyclopedia of Supramolecular Chemistry . Atwood, J. L.; Steed, J. W. (eds.). Boca Raton: CRC Press, Taylor & Francis Group, 2004, 1, p. 830-844.
12. BRU, M.; ALFONSO, I.; BURGUETE, M. I.; LUIS, S. V. "Efficient Syntheses of New Chiral Peptidomimetic Macrocycles Through a Configurationally Driven Preorganization". Tetrahedron Letters. 2005, 46, p. 7781–7785.
13. ALFONSO, I.; BOLTE, M.; BRU, M.; BURGUETE, M. I.; LUIS, S. V.; RUBIO, J. "Supramolecular Control for the Modular Synthesis of Pseudopeptidic Macrocycles through an Anion-Templated Reaction". J. Am. Chem. Soc. 2008, 130, p. 6137–6144.
14. BECERRIL, J., et al . "Efficient Macrocyclization of U-Turn Preorganized Peptidomimetics: the Role of Intramolecular H-Bond and Solvophobic Effects". J. Am. Chem. Soc. 2003, 125, p. 6677-6686.
15. GARCÍA ESPAÑA, E.; BALLESTER, M. J.; LLORET, F.; MORATAL, J. M.; FAUS, J.; BIANCHI, A. "Low-Spin Six-Coordinate Cobalt(II) Complexes. A Solution Study of tris(violurato)cobaltate(II) ions". J. Chem. Soc., Dalton Trans. 1988, p. 101-104.
16. GRAN, G. "Determination of the Equivalence Point in Potentiometric Titration. Part II". Analyst. 1952, 77, p. 661–671.
17. ROSSOTTI, F. J. C.; ROSSOTTI, H. "Potentiometric Titrations Using Gran Plots. A Textbook Omission". J. Chem. Educ. 1965, 42, (7), p. 375–378.
18. GANS, P.; SABATINI, A.; VACCA, A. "Investigation of Equilibria in Solution. Determination of Equilibrium Constants with the HYPERQUAD Suite of Programs". Talanta. 1996, 43, p. 1739-1753.
19. ADERIGHI, L.; GANS, P.; IENCO, A.; PETERS, D.; SABATINI, A.; VACCA, A. HYSS. Coord. Chem. Rev. 1999, 184, p. 314.
20. GUARDA, L., et al. "Synthesis and Characterization of Bis- and Tos-(4-Carboxybenzoyl)-Alkaneamines". J. Chil. Chem. Soc. 2012, 57, (3), p. 1305-1308.
21. ALGARRA, A. G., et al . "Synthesis, Protonation and CuI I Complexes of Two Novel Isomeric Pentaazacyclophane Ligands: Potentiometric, DFT, Kinetic and AMP Recognition Studies". Eur. J. Inorg. Chem. 2009, p. 62–75.
22. FABBIZZI, L.; LICCHELLI, M.; PALLAVICINI, P.; PARODI, L.; TAGLIETTI, A. "Fluorescent Sensors for and with Transition Metals". In: Transition Metals in Supramolecular Chemistry . Sauvage, J. P. (ed.). New York: John Wiley & Sons, 2008, p. 105.
Recibido: 16/10/2013
Aceptado: 20/11/13
Yennys Hernández-Molina, Facultad de Ciencias Naturales, Universidad de Oriente, Santiago de Cuba, Cuba. yhmolina@cnt.uo.edu.cu