Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Cubana de Química
versión On-line ISSN 2224-5421
Rev Cub Quim vol.26 no.2 Santiago de Cuba may.-ago. 2014
ARTICULOS
Evaluación temporal de la calidad de las aguas del río Los Guaos de Santiago de Cuba
Temporal Evaluation for the Quality of Waters of the Los Guaos River of Santiago de Cuba
Dra. Alina M. Marañón-Reyes, MSc. Norma E. Pérez-Pompa, Lic. Ariamna M. Dip-Gandarilla, Dra. Alina González-Marañón, Dra. Rosa M. Pérez-Silva, Lic. Augusto Ruiz-Estrella
Departamento de Química, Facultad de Ciencias Naturales, Universidad de Oriente, Santiago de Cuba, Cuba, alinapga@cnt.uo.edu.cu; norma@cnt.uo.edu.cu; agm@cnt.uo.edu.cu; rmaria@cebi.uo.edu.cu; augusto@cnt.uo.edu.cu
RESUMEN
La falta de mantenimiento y operaciones no adecuadas, así como un deficiente control y monitoreo de la calidad de las aguas, y la poca introducción de prácticas de producción más limpias por parte de las principales entidades contaminadoras han provocado una gran contaminación de las principales cuencas hidrográficas de Santiago de Cuba. Entre ellas se encuentra el río Los Guaos, que aporta un alto por ciento de carga contaminante a la bahía santiaguera. Resulta de gran interés realizar un estudio de evaluación de la calidad de las aguas de este río, para establecer su calidad y posible uso. Se estudiaron cinco estaciones de monitoreo durante el período enero-abril. Se determinaron 23 parámetros físico-químicos y 2 microbiológicos. Se compararon los resultados con las Normas Cubanas de agua potable, abasto, baño y pesca y se emplearon métodos estadísticos para la evaluación. Según los resultados obtenidos, estas aguas están contaminadas desde casi su nacimiento, lo que invalida su uso sin tratamiento previo. Las mismas se encuentran afectadas por el fenómeno de eutrofización.
Palabras clave: calidad de agua, ecosistema fluvial, Cuba.
ABSTRACT
The lack of maintenance and inadequate operations and poor control and monitoring of water quality, and little introduction of cleaner production practices by major polluting entities have caused great pollution of major river basins Santiago de Cuba. Among them is the river's Guaos, which provides a high percentage of pollutant load to the Bay of Santiago. It is of great interest to conduct a study to evaluate the quality of the waters of this river, to establish their quality and potential use. Five monitoring stations were studied during the period from January to April. 23 physicochemical parameters were determinaro microbiological and 2. The results were compared with the Cuban Standards for drinking water supply, swimming and fishing and statistical methods were used for evaluation. According to the results, these waters are polluted from almost birth, which invalidates their use without treatment. They are affected by eutrophication.
Keywords: quality of water, fluvial ecosystem, Cuba.
INTRODUCCIÓN
La estabilidad de los ecosistemas es constantemente amenazada por la actividad antropogénica. En este sentido, los sistemas acuáticos son receptores de toda clase de desechos que, en su mayoría, son orgánicos. Se detecta, además, la presencia de compuestos tóxicos, considerados agresivos por su persistencia en los sedimentos1.
La cuenca hidrográfica Guaos-Gascón está formada por el río Los Guaos y el río Gascón. El primero se encuentra localizado en la parte oeste de la ciudad de Santiago de Cuba. El mismo presenta una de las cuencas más pequeñas y, a la vez, una de las más contaminadas de la provincia, debido a la influencia del hombre, ya sea por la actividad industrial, agropecuaria, o cotidiana.
El desarrollo acelerado y no sustentable de la cuenca ha modificado la naturalidad del río y ha variado su cauce por problemas de drenaje en las partes bajas. Los asentamientos poblacionales han afectado el entorno natural y se han tomado áreas para establecer cultivos, entre otros2, 3. El río aporta un alto porcentaje de la carga contaminante, fundamentalmente de origen orgánico, a la bahía santiaguera, convirtiendo a este ecosistema en uno de los de mayor fragilidad en el entorno de la ciudad4.
En Cuba existen normas que regulan los criterios de calidad de las aguas según su uso, como los requisitos para agua potable5, agua para abasto6, agua para pesca7 y aguas para baño8. Conociendo las características de las aguas de un río es posible establecer la calidad y el uso correcto de las mismas.
El objetivo de este trabajo es analizar la variación temporal de los indicadores que más afectan la calidad del agua del río Los Guaos, a través de la caracterización físico-química y microbiológica de las mismas.
MÉTODOS EXPERIMENTALES
Descripción del área de estudio
El río los Guaos limita al norte con las estribaciones de la Sierra de Boniato, al sur con la Bahía de Santiago de Cuba, al este con la cuenca del río Gascón y al oeste con la cuenca del río Parada. Presenta una extensión de 11 km y una cuenca de 24,3 km 2 de superficie (figura 1), con relieve entre llano y ondulado.
La zona se caracteriza por un clima tropical seco, con períodos de lluvia aislados y temperatura promedio anual de 29 ºC. En la red fluvial se localizan 16 focos contaminantes de diferentes orígenes, afectando la calidad de sus aguas. Los focos fundamentales son el Centro Genético Porcino, Combinado "Los Guaos" I y II, y el Complejo Industrial "Celia Sánchez Manduley"9. La localización de las estaciones de muestreo se llevó a cabo según la metodología establecida en las Normas Cubanas ISO10-12.
Se realizaron cuatro muestreos comprendidos entre los meses enero-abril del 2011. Se establecieron cinco estaciones de monitoreo a lo largo del río como se observa en la figura 1. Para la ubicación de las mismas se tuvieron en cuenta resultados de estudios anteriores, la localización de fuentes contaminantes, facilidad de acceso y la representatividad13, 14.
Estación 1: ubicada a unos 300 m antes que vierta sus residuales el Centro Genético Porcino. Zona con abundante vegetación en la orilla del río, fondo arenoso-pedregoso, y presencia de vida acuática. En esta estación se evalúa la calidad de una zona aparentemente poco contaminada.
Estación 2: situada a 1 km de la estación 1, en el puente del poblado "El Castillito", después del vertido de las aguas residuales del Centro Genético Porcino; posee malezas en las orillas, fondo arenoso-pedregoso, y presencia de lino.
Estación 3: localizada en el Kilómetro uno y medio del Camino Viejo del Cobre, después que se vierten los desechos de la Cantera Los Guaos I. En esta zona, se observa abundante vegetación en las cercanías y orilla, agua clara, con lino en el fondo y sin existencia de vida acuática.
Estación 4: situada a 150 m de la Carretera de Mar Verde, después que vierte sus residuales el Complejo Industrial "Celia Sánchez Manduley", a 50 m antes de la unión con el río Gascón. En la zona se observa abundante vegetación, aguas turbias, poca presencia de vida acuática y fondo con abundante lino. Los pobladores de la zona la utilizan para baño de animales.
Estación 5: localizada a 600 m de la estación 4 y después de la unión de ambos ríos. La zona presenta abundante vegetación y lino en el fondo; estas aguas se emplean para diversos fines, fundamentalmente, para la fabricación de ladrillos. En las estaciones 2-5 se evaluará la influencia antropogénica.
Toma y conservación de las muestras
La toma y conservación de las muestras se realizó mediante la metodología establecida11, 15. La temperatura se determinó in situ y el oxígeno disuelto se fijó en el campo. Para el análisis de los parámetros físico-químicos se tomaron muestras de agua por duplicado en cada estación, los análisis se realizaron por triplicado. La toma de muestra fue a 30 cm de la superficie de la columna de agua; se emplearon envases de plástico de 1,5 L de capacidad. Los valores de concentración representados para los diferentes parámetros evaluados son el promedio de 24 determinaciones, excepto para los metales pesados que fue de seis determinaciones.
Parámetros físico-químicos y microbiológicos analizados
Los indicadores determinados fueron seleccionados teniendo en cuenta los requisitos de las normas cubanas NC 93-01-105-1987, NCXX (1999), NC 827(2010) y NC93-11 (1986).
• Indicadores físicos y químicos del agua: Temperatura (T) , pH, nitrógeno como nitritos (N-NO2-), nitrógeno como nitratos (N-NO3-), nitrógeno amoniacal (N-NH4+), fósforo en forma fosfatos (P-PO43- ), conductividad eléctrica (ë), sólidos totales (ST), sólidos totales fijos (STF) y volátiles (STV), sólidos sedimentables (SS), oxígeno disuelto (OD), demanda química de oxígeno (DQO), alcalinidad (HCO3- ), sulfato (SO42- ), dureza total (DT), calcio (Ca2+), magnesio (Mg2+), sodio (Na+), potasio (K+), cloruro (Cl-), y los metales pesados según los métodos descritos en el Standard Methods15.
• Como indicador microbiológico se usó la concentración de coliformes termotolerantes o fecales (CF). Las muestras de agua se colectaron en superficie. La preservación de las mismas, se hizo según las especificaciones de la NC-ISO:5667-3 (1994). Se determinó por el método del número más probable (NMP/100 mL).
• Para determinar el nivel de eutrofia se siguió el criterio propuesto por Morris et al. (1988) que considera la relación nitrógeno inorgánico disuelto: fósforo total (Nid: PT), este último como nutriente que limita la productividad del sistema16.
Análisis estadístico: Los resultados experimentales fueron procesados mediante el programa Microsoft Office Excel 2007 con ayuda del Sistema Estadístico STATISTICA Versión 7. Una vez comprobado que los resultados obtenidos no cumplen los criterios de normalidad y homogeneidad, se aplican las pruebas de la estadística inferencial (métodos no paramétricos) y multivariada: Test de Kruskal - Wallis, análisis de correlación R Spearman y Prueba de hipótesis de comparación de medias (prueba U de Mann - Whitney)17.
RESULTADOS Y DISCUSIÓN
Características físico-químicas y microbiológicas de las aguas del río Los Guaos
Una vez analizados los resultados experimentales obtenidos, en cada una de las estaciones de muestreo, se comprueba que los indicadores T, pH, SS, ST, STF, STV, SO4 2- , Na + , K + , HCO3- , Cl- (excepto en las estaciones 4 y 5) y DT pueden considerarse como no contaminantes por encontrarse por debajo de la concentración máxima admisible (CMA), según las NC de agua potable5, para abasto6, para uso pesquero18 y agua para baño8.
La conductividad es una medida del grado de mineralización de las aguas y de la carga iónica presente. Este parámetro a lo largo del río varía entre 562 y 800 µS/cm lo que indica alta salinidad de sus aguas, debido a la presencia de sales inorgánicas19. Al recibir el río las aguas residuales agropecuarias, estación 2, se observa un aumento en el valor de dicho parámetro (tabla 1), que disminuye ligeramente en la estación 3. Estos resultados son similares a los encontrados en estudios anteriores3, 20. Los mayores valores de conductividad se obtienen en la estación 4, debido al vertido de los residuales procedentes del Combinado de Hormigón Los Guaos II y el Complejo Textil "Celia Sánchez Manduley"; una vez que se unen ambos ríos (Guaos y Gascón, estación 5) se produce una ligera disminución, aunque los valores se mantienen elevados debido a que en esta zona se vierten residuales sólidos procedentes de la fabricación de ladrillos.
Tabla 1. Valores medios obtenidos en las diferentes estaciones de monitoreo para los indicadores estudiados
| Parámetro | Estación 1 | Estación 2 | Estación 3 | Estación 4 | Estación 5 |
| T (ºC) | 23 ± 0,90 | 24 ± 0,45 | 24 ± 0,00 | 24 ± 0,45 | 24 ± 0,45 |
| pH (unidades) | 6,8 ± 0,15 | 7,0 ± 0,19 | 6,9 ± 0,51 | 7,1 ± 0,36 | 7,2 ± 0,35 |
| l (µS/cm) | 562 ± 21,90 | 656 ± 27,24 | 605 ± 19,10 | 800 ± 16,89 | 722 ± 11,60 |
| ST (mg/L) | 499 ± 20,00 | 543 ± 24,85 | 525 ± 23,76 | 683 ± 12,66 | 607 ± 26,75 |
| STF (mg/L) | 374 ± 25,32 | 390 ± 35,70 | 388 ± 22,04 | 511 ± 37,75 | 441 ± 17,22 |
| STV (mg/L) | 125 ± 28,57 | 152 ± 34,35 | 136 ± 17,51 | 176 ± 28,79 | 166 ± 29,48 |
| Ca 2+ (mg/L) | 87 ± 4,30 | 90 ± 2,50 | 84 ± 5,07 | 91 ± 2,01 | 80 ± 4,71 |
| Mg 2+ (mg/L) | 23 ± 1,20 | 31 ± 1,47 | 32 ± 0,84 | 38 ± 0,95 | 41 ± 1,15 |
| Na + (mg/L) | 37 ± 2,43 | 36 ± 2,09 | 36 ± 1,30 | 61 ± 1,74 | 50 ± 2,22 |
| K + (mg/L) | 3 ± 0,18 | 16 ± 0,86 | 5 ± 1,06 | 6 ± 0,69 | 6 ± 0,32 |
| Cl - (mg/L) | 136 ± 1,48 | 159 ± 2,30 | 194 ± 1,97 | 278 ± 2,70 | 206 ± 2,47 |
| PO4 3- (mg/L) | 0,04 ± 0,001 | 2,20 ± 0,03 | 0,48 ± 0,002 | 0,35 ± 0,002 | 0,11 ± 0,003 |
Los valores de conductividad de la estación 1 presentan diferencias estadísticamente significativas con las estaciones 2, 4 y 5, y la 3 con la 4 y 5. La conductividad correlacionó positivamente (n = 24; p < 0,05) con Na+ (r2 = 0,600), K+ (r2 = 0,600), Ca2+ (r2 = 0,609), Cl- (r2 = 0,693), SO42- (r2 = 0,784), HCO3- (r2 = 0,789), ST (r2 = 0,972) y STF (r2 = 0,941), estos últimos representan aproximadamente el 74 % de los sólidos totales, lo que indica la prevalencia de compuestos inorgánicos.
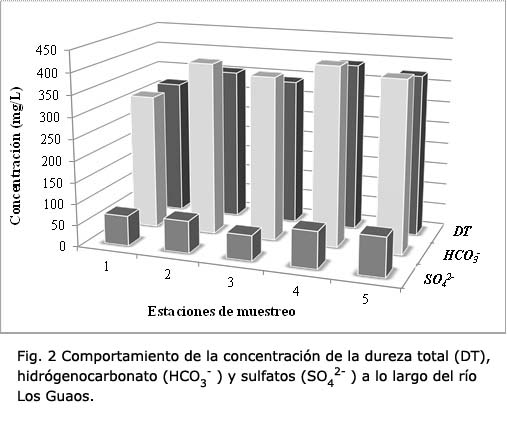
La alcalinidad es un parámetro importante por estar relacionado con la estabilidad del pH, su magnitud depende de la concentración en las aguas de iones carbonato e hidrógenocarbonato lo que se conoce como reserva alcalina o sistema tampón21. En las muestras analizadas prevalece la especie HCO3-, ya que presentan valores de pH inferiores a 8,3. Las concentraciones obtenidas oscilan entre 314 y 416 mg/L, como se observa en la figura 2.
De manera general, según Allende (1976)22, estas aguas se clasifican de alcalinidad muy fuerte y muy contaminada. Este indicador correlacionó positivamente con la l (r2 = 0,789) y la T (r2 = 0,762), e inversamente con el pH (r2 = -0,786).
Los valores de dureza total a lo largo del río varían entre 316 y 391 mg/L (figura 2), encontrándose dentro de la CMA establecida por la NC de agua potable5 400 mg/L). Teniendo en cuenta los elevados valores de alcalinidad, expresados como HCO3- , se puede inferir que la dureza total en todas las estaciones es mayormente bicarbonatada, por lo que se pueden clasificar como aguas con dureza temporal y no sulfatadas19. Existen diferencias estadísticas significativas entre la estación 1 y las estaciones 2, 4 y 5, y la estación 3 con la 4 y 5. Este parámetro correlacionó con el Na + (r2 = 0,761), K + (r2 = 0,761) y los ST (r2 = 0,690).
La presencia de oxígeno disuelto en las aguas es esencial para evaluar los posibles efectos potenciales de algunos agentes contaminantes, así como para sustentar las formas superiores de vida. Las aguas de la estación 1 poseen concentraciones de 6,4 mg/L para un porcentaje de saturación de 74 %, valores que se encuentran por encima de 5 mg/L y 63 % de saturación, recomendados para que la vida acuática aerobia se desarrolle normalmente23, por lo que cumplen con los índices obligatorios para cuerpos de agua dulce de uso pesquero18 y con lo establecido en la NC de abasto6.
Aunque en la estación 2 disminuye ligeramente el porcentaje de saturación de O2), 69 %, la concentración de OD se encuentra dentro de la CMA establecida por las NC (figura 3). Estos resultados se deben a que los residuales del Genético Porcino son tratados biológicamente mediante lagunas de estabilización antes de ser vertidos al río, lo cual permite que disminuya la carga orgánica del residual respecto a estudios realizados anteriormente20.
Aunque en la estación 3 este parámetro disminuye ligeramente, aún se encuentra dentro de los requerimientos establecidos por las normas. En cambio, en la estación 4 se alcanzan valores inferiores a 5 mg/L (19 % de saturación de O2). Según los índices obligatorios establecidos en la NC para uso pesquero18 y la NC de abasto6, estas aguas se clasifican como aguas de mala calidad, lo que puede deberse a que están sometidas a una contaminación industrial continua, a la existencia de abundante vegetación acuática que cubre una gran extensión de la superficie del agua, y a que el intercambio agua-sedimento puede conducir a un descenso en los niveles de OD 24, 25.
En la estación 5, los valores aumentan por la confluencia con el río Gascón, sin embargo se encuentran aún por debajo de la CMA establecida en las NC 93-01-105-1987 (1987) y NC 93-11 (1986). De manera general, por la evaluación de este parámetro, las aguas a lo largo del río se clasifican de calidad entre mala y dudosa.
Los valores de DQO oscilan entre 52 y 415 mg/L como puede observarse en la figura 3. Todas las muestras analizadas se clasifican de mala calidad excepto las de la estación 3 que poseen calidad dudosa, según lo establecido en la NC para uso pesquero18, ello indica que estas aguas poseen un alto contenido de materia orgánica susceptible a oxidarse. Al comparar los valores con la NC de agua para baño8, el valor de este parámetro se encuentra por encima de la CMA en todas las estaciones de monitoreo, por lo que se consideran inadecuadas para dicho uso. El OD y la DQO poseen una fuerte correlación inversa (r2 = -0,981).
Las concentraciones de potasio obtenidas a lo largo del río oscilan entre 3 y 16 mg/L (tabla 1), valores superiores a la CMA para aguas de diversos usos, según normativas internacionales (1 mg/L)23. Los mayores valores se localizan en la estación 2 . Dicho incremento puede deberse a que este punto está situado luego de que el río reciba el vertido de los residuales del Genético Porcino, cuya composición varía en dependencia de la dieta animal que, por lo general, es a base de piensos a los cuales se les adiciona un suplemento dietético compuesto por un núcleo orgánico (vitaminas) y un núcleo mineral que lo conforman sales de los elementos minerales esenciales NO3 - , K + y PO4 3- , entre otros que se consideran mayoritarios2. Existen diferencias significativas entre la estación 1 y la 2, 3 y 4, y la estación 2 con la 3 y 5.
La concentración de iones fosfato varía entre 0,02 y 3,2 mg/L (tabla 1). Las aguas de la estación 1 son de buena calidad, intervalo establecido por la NC de uso pesquero, menor de 0,1 mg/L 18; el resto de las estaciones presentan calidad dudosa (intervalo de la norma para esta clasificación: 0,1-3 mg/L); los mayores valores se obtienen en la estación 2, lo que concuerda con el aporte del residual que se vierte en este punto2. La estación 1, menos contaminada, difiere significativamente de las estaciones 2, 3 y 4, lo que corrobora los resultados planteados anteriormente. La estación 2 difiere de la 1, 4 y 5, en este caso por ser la más contaminada.
Los iones amonio se producen por la descomposición de compuestos orgánicos de nitrógeno, fundamentalmente, como materia proteica, ocurriendo la amonificación20, 26. Este ión está presente a lo largo del río en concentraciones apreciables, por encima de 0,01 mg/L (figura 4). Teniendo en cuenta lo planteado por Perdomo y col. (2001)27, las aguas de este río presentan contaminación fecal en todo su recorrido. Ninguna de las estaciones cumple con lo establecido en la NC de agua potable. Este parámetro correlacionó positivamente con los ST (r2 = 0,756), STF (r2 = 0,903), STV (r2 = 0,597) y N-NO2- (r2 = 0,609), y correlación inversa con N-NO3- (r2 = -0,608).
Los iones nitrato se encuentran en el intervalo de 1,1 a 9,5 mg/L; los mayores valores se presentan en las estaciones 2 y 4, esto puede deberse al vertido de los residuales del Centro Genético Porcino y del Combinado Textil "Celia Sánchez Manduley". En todas las estaciones los valores de concentración de estos iones se encuentran por debajo de la CMA de 45 mg/L y 10 mg/L según la NC de abasto6 y de uso pesquero18, respectivamente. Este parámetro correlaciona de forma inversa con el N-NH4+ (r2 = -0,608), lo que permite inferir que el mismo proviene mayormente de la oxidación del amonio.
En todo el curso de agua los valores de concentración de iones nitrito se encuentran por encima de 0,01 mg/L, CMA establecida por la NC de agua potable5. Las estaciones 1, 3 y 5 presentan las concentraciones más bajas (inferiores a 0,2 mg/L) (figura 4). Según la NC de uso pesquero18 estas aguas se clasifican de buena calidad para la pesca, excepto las estaciones 2 y 4 que son de calidad dudosa. Lo planteado anteriormente se verifica en el test de Kruskal Wallis, donde la estación 1 difiere significativamente de la 2, 4 y 5; y la estación 3 de la 2 y 4. Existe correlación positiva con el K+ y los ST. Como se observa en la figura 4, predomina la contaminación por iones nitrato, excepto la estación 2, lo que indica contaminación albañal no reciente.
El comportamiento de las trazas metálicas en sistemas acuáticos es muy complejo, debido al gran número de posibles interacciones y a los equilibrios con sustancias disueltas y particuladas16. En este trabajo se determinaron los metales Co, Cu, Cr, Sr, Fe, Mn, Pb, Zn, Al, Cd, Ba, Mo y Ni (tabla 2). Las concentraciones de los metales Co, Cu, Cr, Sr, Fe, Mn, Pb y Zn se encuentran por debajo de la CMA según lo establecido en la NC de agua potable5. El resto de los metales estudiados se encuentran por encima de la CMA; esto puede deberse a la mineralización que presenta la cuenca del río como consecuencia de las características geoquímicas de las formaciones geológicas Cobre y Santiago20.
Tabla 2 Valores medios obtenidos en las diferentes estaciones de monitoreo para los metales
| Metales | Estación 1 | Estación 2 | Estación 3 | Estación 4 | Estación 5 |
| Al | 0,227± 0,018 | 0,213± 0,017 | 0,337± 0,016 | 0,320± 0,016 | 0,243± 0,018 |
| Ba | 0,037± 0,005 | 0,057± 0,004 | 0,033± 0,005 | 0,030± 0,005 | 0,040± 0,004 |
| Cd | 0,057± 0,001 | 0,050± 0,001 | 0,050± 0,001 | 0,050± 0,001 | 0,050± 0,001 |
| Co | 0,050± 0,002 | 0,045± 0,002 | 0,045± 0,002 | 0,044± 0,002 | 0,044± 0,002 |
| Cu | 0,163± 0,016 | 0,103± 0,015 | 0,070± 0,012 | 0,077± 0,012 | 0,070± 0,012 |
| Cr | 0,043± 0,002 | 0,043± 0,002 | 0,040± 0,002 | 0,037± 0,001 | 0,040± 0,002 |
| Sr | 0,127± 0,015 | 0,140± 0,017 | 0,163± 0,017 | 0,207± 0,016 | 0,203± 0,017 |
| Fe | 0,160± 0,035 | 0,063± 0,032 | 0,210± 0,035 | 0,217± 0,035 | 0,133± 0,032 |
| Mn | 0,007± 0,008 | 0,063± 0,008 | 0,003± 0,005 | 0,003± 0,001 | 0,017± 0,005 |
| Mo | 0,067± 0,005 | 0,060± 0,005 | 0,060± 0,005 | 0,060± 0,005 | 0,060± 0,005 |
| Ni | 0,050± 0,005 | 0,043± 0,004 | 0,040± 0,004 | 0,043± 0,005 | 0,040± 0,005 |
| Pb | 0,050± 0,003 | 0,050± 0,003 | 0,050± 0,003 | 0,050± 0,003 | 0,047± 0,002 |
| Zn | 0,053± 0,002 | 0,077± 0,004 | 0,040± 0,002 | 0,043± 0,003 | 0,040± 0,003 |
Los parámetros microbiológicos muestran que todas las estaciones de monitoreo presentan valores por encima de 200 NMP/100 mL, valor requerido por la NC aguas para baño8, por lo que estas aguas no están aptas para el contacto directo, ni pueden ser usadas como agua potable5. Las aguas de la estación 1 pueden utilizarse para la pesca18 y para el abasto de la población6.
Nivel de eutrofia en las aguas del río Los Guaos
El abastecimiento excesivo de los nutrientes nitrógeno y fósforo a los cuerpos de agua, provoca que el equilibrio biológico entre la fauna y flora se afecte, lo que da lugar a que algunas especies desaparezcan, mientras otras se desarrollan excesivamente, este fenómeno se conoce como eutrofización16, 28-30. Para determinar el nivel de eutrofia de un cuerpo hídrico es necesario conocer el nutriente límite, para ello se calcula la relación existente entre el N t /P t en todas las muestras analizadas y una vez confirmado que el fósforo es el limitante y considerando el criterio de la OECD (1982) se clasifican las aguas teniendo en cuenta la concentración de fósforo total en µg/L 31.
Los resultados indican que existe un elevado nivel de eutrofización en el río, debido a la entrada de grandes cargas de materia orgánica y de nutrientes de origen terrestre a través de aguas residuales sin tratar adecuadamente. Las aguas de este río se clasifican en la estación 1 como aguas mesotróficas (valores comprendidos entre 10 - 30 µg/L) y las de la estación 5 como aguas eutróficas (35 - 100 µg/L). El grado trófico es más significativo en las estaciones 2-4: presenta valores superiores a 100 µg/L. Estas aguas se clasifican como hipertróficas
Variación temporal de los indicadores físico-químicos y microbiológicos entre 1998 y 2011
Para el análisis de las variaciones temporales se tuvieron en cuenta los resultados obtenidos y los datos históricos que se poseen sobre la evaluación de la calidad de las aguas de este río20. Estos indicadores fueron comparados empleando la prueba de hipótesis de comparación de medias (prueba U de Mann-Whitney ) con un nivel de significación de p £ 0,05. Las variaciones que se producen en los valores de cada parámetro no son estadísticamente significativas. Se aprecia que los valores mínimos y máximos obtenidos en el 2011 se encuentran dentro del intervalo de concentraciones alcanzadas por Pérez y col. (1999)20, como se muestra en la tabla 3.
Tabla 3. Valores obtenidos de algunos de los parámetros analizados en los años 1997 y 2011
| Parámetro | Unidad de medida | Año 1997 | Año 2011 |
| Temperatura | (ºC) | 23 - 24 | 22-25 |
| pH | Unidades | 6,9- 8,4 | 6,2-7,6 |
| Conductividad | (mg/L) | 729 - 1470 | 498-1072 |
| DQO | (mg/L) | 12 - 1455 | 15-600 |
| OD | (mg/L) | 0 - 6,3 | 0,4-7,5 |
| Alcalinidad | (mg/L) | 296 - 995 | 196-514 |
| SO4 2- | (mg/L) | 34 - 140 | 31-111 |
| Ca2+ | (mg/L) | 60 - 91 | 68-98 |
| Mg 2+ | (mg/L) | 19 - 42 | 19-49 |
| Na + | (mg/L) | 44 - 75 | 33-81 |
| K + | (mg/L) | 1 - 43 | 2,3-22 |
| Cl - | (mg/L) | 31 - 59 | 127-345 |
| NO3 - | (mg/L) | 0,8 - 46 | 1,1-9,5 |
| NO 2- | (mg/L) | 0,01 - 2,1 | 0,01-5,2 |
| NH4+ | (mg/L) | 0,02 - 91 | 0,09-16 |
| PO4 3- | (mg/L) | 0,8 - 398 | 0,02-3,2 |
| Coliformes totales | NMP/100mL | 2900-10 6 | 240-10 5 |
| Coliformes fecales | NMP/100mL | 0-10 6 | 9-10 5 |
Aunque la estación 2 se encuentra altamente contaminada en ambos años, en la misma se observa una ligera mejoría luego de que se estableciese el sistema de lagunas de estabilización en el Centro Genético Porcino, lo que se evidencia, en valores más bajos de DQO, nitrato, fosfato y aumento del oxígeno disuelto, aunque este tratamiento no es aún lo suficientemente efectivo. En la estación 4 , por el contrario, los parámetros DQO y amonio aumentan, y disminuye el OD. Estos resultados indican que, aunque han existido algunas variaciones en las concentraciones de los parámetros físico-químicos y microbiológicos, el río mantiene el mismo nivel de contaminación que hace trece años.
CONCLUSIONES
• La caracterización físico-química y microbiológica realizada a las aguas del río Los Guaos evidencia que las mismas están contaminadas, siendo las estaciones 2 y 4 las más afectadas. Estas aguas no son aptas para el uso pesquero, ni pueden ser utilizadas como agua potable (excepto en la estación 1). Para ser destinadas como abasto a la población es necesario realizar un tratamiento especial.
• Todas las estaciones se consideran afectadas por el fenómeno de eutrofización, que resulta más significativo en las estaciones 2-4 (hipertróficas); el fósforo total se tiene en cuenta como nutriente limitante.
• No existen diferencias estadísticamente significativas en la variación temporal de los indicadores, por lo que las aguas del río Los Guaos se mantienen contaminadas desde hace trece años.
BIBLIOGRAFÍA
1. MANAHAN, S. Introducción a la Química Ambiental. España: Editorial Reverté, 2007.
2. ARIAS, T. "Caracterización de algunas de las principales fuente contaminantes de la bahía de Santiago de Cuba y sus consecuencias en el Medio Ambiente". Revista Tecnología Química.2008, VIII, 2, p. 79-89.
3. BOLAÑOS, J. "Estudio de la vulnerabilidad del río Los Guaos y su poder autodepurativo". En:Segundo Seminario Internacional del Agua. Santiago de Cuba, 2004.
4. CITMA. Estrategia Ambiental de Santiago de Cuba (2007-2010). Ministerio de Ciencia Tecnología y Medio Ambiente. Delegación Provincial, Santiago de Cuba, 2008.
5. OFICINA NACIONAL DE NORMALIZACIÓN. Norma Cubana NC 93-02. Agua potable: Requisitos sanitarios y muestreo.Ciudad de La Habana, 1985.
6. OFICINA NACIONAL DE NORMALIZACIÓN. Norma Cubana NC 93-11. Fuentes de abastecimiento de agua: Calidad y protección sanitaria. Ciudad de La Habana, 1986.
7. OFICINA NACIONAL DE NORMALIZACIÓN. Norma Cubana NC 25. Evaluación de los objetos hídricos de uso pesquero: Especificaciones. Ciudad de La Habana, 1999.
8. OFICINA NACIONAL DE NORMALIZACIÓN. Norma Cubana NC 22. Lugares de baño en costas y en masas de aguas interiores: Requisitos higiénico sanitarios. Ciudad de La Habana, 1999.
9. RODRÍGUEZ, N., et al. "Diagnóstico socio ambiental de la Comunidad Cayo Granma". Informe inédito. Universidad de Oriente, 2004.
10. INSTITUTO COLOMBIANO DE NORMAS TÉCNICAS Y CERTIFICACIÓN. Norma Técnica Colombiana NTC-ISO 5667-1. Gestión ambiental. Calidad del agua. Muestreo. Parte 1: Directrices para el diseño de programas y técnicas de muestreo. Bogotá, D.C., 1994.
11. INSTITUTO COLOMBIANO DE NORMAS TÉCNICAS Y CERTIFICACIÓN. Norma Técnica Colombiana NTC-ISO 5667-3. Gestión ambiental. Calidad del agua. Muestreo. Parte 3: Directrices para la preservación y manejo de las muestras. Bogotá, D.C., 1994.
12. INSTITUTO COLOMBIANO DE NORMAS TÉCNICAS Y CERTIFICACIÓN. Norma Técnica Colombiana NTC-ISO 5667-10. Gestión ambiental. Calidad del agua. Muestreo. Parte 10: Guía para el diseño de programas de muestreo. Bogotá, D.C., 1994.
13. GONZÁLEZ, A., et al. "Influencia del cierre de la Mina Grande en la calidad de las aguas del río Cobre de Santiago de Cuba". Revista Cubana de Química.2009, XXI, 2, p. 37-44.
14. PÉREZ, N.; MARAÑÓN, A.; ÁBALOS, A. "Caracterización de las aguas residuales de la Refinería Hermanos Díaz". Revista Cubana de Química. 2004, XVI, 1, p. 53-60.
15. AMERICAN PUBLIC HEALTH ASSOCIATION. APHA. Standard Methods for the Examination of Water and Wastewater. 20 th Edition. USA, 1999.
16. MORENO, D.; QUINTERO, J.; LÓPEZ, A. "Métodos para identificar, diagnosticar y evaluar el grado de eutrofia". Revista Contactos. 2010, 78, p. 25-33.
17. PAULSON, D. S. Applied Statistical Designs for the Research. USA: Editorial Marcel Dekker Inc., 2003.
18. OFICINA NACIONAL DE NORMALIZACIÓN. Norma Cubana NC 93-01-105. Especificaciones y procedimientos para la evaluación de los objetos hídricos de uso pesquero. Ciudad de La Habana, 1987.
19. OROZCO, C., et al. Contaminación Ambiental. Una visión desde la química. Madrid: Pearson Educación, 2002.
20. PÉREZ, N., et al. "Evaluación de la calidad de las aguas del río Los Guaos de la provincia Santiago de Cuba, Cuba". Revista Cubana de Química. 1999, XI, 1, p. 56-61.
21. RIVERA,N. R.; ENCINA, F.; MUÑOZ PEDREROS, A.; MEJÍAS, P. "La Calidad de las Aguas en los Ríos Cautín e Imperial, IX Región-Chile". Información Tecnológica. 2004, 15, 5, p. 89-101.
22. ALLENDE, A. V. Apuntes sobre Química del Agua. La Habana: ISPJAE, 1976.
23. SÁNCHEZ, L. E. "Control de la contaminación de las aguas". Departamento de Ingeniería de Minas. Escuela Politécnica. Universidad de Sao Paulo, 1993.
24. MILÁN, J. A. Estudio del Medio Ambiente. Programa Ambientales Urbano-Territoriales. Nicaragua: Universidad Nacional de Ingeniería, 2004.
25. SPIRO, T. G.; STIGLIANI, W. M. Química Medioambiental. 2ª edición. Pearson Prentice Hall, 2003.
26. VITOUSEK, P. M., et al. "Human Alteration of the Global Nitrogen Cycle: Sources and Consequences". Ecological Applications. 1997, 7, p. 737-750.
27. PERDOMO, C. H.; CASANOVA, O. N.; CIGANDA, V. S. "Contaminación de aguas subterráneas con nitratos y coliformes fecales en el litoral sudeste del Uruguay". Revista Agrociencia. 2001, 1, p. 10-22.
28. ARCE, O. Eutrofización de cuerpos de agua. Química del agua[en línea]. [ref. de 22 de noviembre de 2011]. Disponible en Web: < http://www.fcyt.umss.edu.bo/Eutrofizacion.pdf >.
29. ROMERO, M. "Proceso de eutrofización de afluentes y su prevención por medio de tratamiento de afluentes". Revista Ingeniería Primero. 2010, 17, p. 64-74.
30. QUIRÓS, R. "The Relationship Between Nitrate and Ammonia Concentrations in the Pelagic Zones of Lakes". Revista Limnetica. 2003, 22, p. 37-50.
31. BETANCOURT, C.; SUÁREZ, R.; TOLEDO, L. "Ciclo anual del nitrógeno y el fósforo en el embalse Paso Bonito, Cienfuegos, Cuba". Revista Limnetica.2009, 28, p. 79-90.
Recibido: 05/12/2013
Aceptado: 20/02/2014
Dra. Alina M. Marañón-Reyes. Departamento de Química, Facultad de Ciencias Naturales, Universidad de Oriente, Santiago de Cuba, Cuba, alinapga@cnt.uo.edu.cu