My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Cubana de Química
On-line version ISSN 2224-5421
Rev Cub Quim vol.29 no.3 Santiago de Cuba Sept.-Dec. 2017
ARTICULOS
Evaluación químico analítica y microbiológica de los embalses Chalons y Parada de Santiago de Cuba
Chemical analytical and microbiological assessment of reservoirs Chalons and Parada from Santiago de Cuba
MSc. José Carlos Rodríguez-TitoI, Dra.C. Rosa M. Pérez-SilvaII, Dra. C. Liliana M Gómez-LunaIII, MSc. Inaudis Álvarez- HubertI
IDepartamento de Fundamentos Químicos y Biológicos, Universidad de Oriente, Santiago de Cuba, Cuba, jcrt@uo.edu.cu
IIDirección de Ciencia y Técnica, Universidad de Oriente, Santiago de Cuba, Cuba
IIICentro Nacional de Electromagnetismo Aplicado, Santiago de Cuba, Cuba
RESUMEN
La calidad de los embalses Chalons y Parada se determinó por parámetros químicos físicos y microbiológicos, tomando como referentes los índices obligatorios y complementarios de las Normas Cubanas relacionadas con los principales usos de agua. Para el análisis se seleccionaron 5 puntos de muestreo en cada embalse, en los meses de marzo, mayo, septiembre y noviembre en el período de 2011-2015. Las determinaciones se realizaron in situ y en laboratorio, según las normativas vigentes. Se determinó por el método del número más probable (NMP/100 mL) Coliformes totales y Coliformes fecales. Los resultados infieren que la calidad del agua de los embalses estudiados, desde el punto de vista químico-físico, es adecuada ya que todos los parámetros están dentro de los niveles regulados por las normas cubanas de aguas. Ambos embalses, según estos parámetros, se pueden clasificar como eutróficos, lo cual puede comprometer su calidad desde el punto de vista microbiológico.
Palabras clave: análisis físico-químico, eutrofización, calidad del agua.
ABSTRACT
The quality of Chalons and Parada reservoirs was determined through physical chemical and microbiological parameters, taking as reference the obligatory and complementary indexes of the Cuban Standards related with main uses of water. For the analysis, 5 sampling points were selected in each reservoir, in March, May, September and November between 2011-2015. The determinations were made in situ and in laboratory, according to the current regulations. The totals Coliforms and fecal Coliforms were determined by the most probable number method (MPN/100 mL). The results concluded that the water quality of the reservoirs studied, from the physical chemical point of view, is adequate since all the parameters are within the levels regulated by the Cuban water standards. However, both reservoirs, according to these parameters, can be classified as eutrophic, which can compromise its quality from the microbiological point of view.
Keywords: physico chemical analysis, eutrophication, water quality.
INTRODUCCIÓN
Los recursos hídricos en Cuba se caracterizan por una distribución no uniforme en todo el país, además de que sus magnitudes varían considerablemente en algunas regiones en las que, por lo general, los mayores de estos recursos, se encuentran en zonas con menor demanda de agua y, por el contrario, en las zonas con mayor densidad poblacional y de considerable desarrollo industrial y agrícola, esos recursos son escasos [1].
El problema más crítico del país actualmente, no es solo el agotamiento cuantitativo, sino el cualitativo de los recursos hídricos, dada por la contaminación de las aguas superficiales y subterráneas por residuales domésticos e industriales, y por la intrusión salina debido a la sobreexplotación de cuencas subterráneas [1]. Es por tanto que, en Cuba, la vigilancia de los cuerpos hídricos se viene fomentando de manera creciente, debido al interés de la conservación de este preciado líquido.
En la provincia de Santiago de Cuba existen un total de 11 embalses de abasto de agua, de ellos Chalons y Parada son utilizados solo en casos extremos y en época de seca. En los últimos años, la región oriental sufre una intensa sequía, que puede haber generado cambios en la calidad del agua de estos embalses cercanos a la ciudad de Santiago de Cuba y que son utilizados en la red de abasto de cerca de medio millón de habitantes, así como para uso de la zona industrial.
MATERIALES Y MÉTODOS
Se realizaron muestreos en 5 puntos de los embalses Chalons y Parada, en los meses de marzo, mayo, septiembre y noviembre en el período de 2011-2015. Los puntos de muestreo coincidieron con el de la Red Cal, así como otros distribuidos en zonas donde la accesibilidad no constituía un problema. En todos los casos se determinaron las coordenadas satelitales utilizando la tecnología GPS (tabla 1).
TABLA 1. COORDENADAS SATELITALES DE LOS PUNTOS DE MUESTREO DE LOS EMBALSES CHALONS Y PARADA
| EMBALSE CHALONS | ||||
| 1 | 2 | 3 | 4 | 5 |
| N 20° 4' 6'' O 75° 48' 48'' | N 20° 4' 17'' O 75° 48' 52'' | N 20° 4' 19'' O 75° 48' 52'' | N 20° 4' 19.' O 75° 48' 58'' | N 20° 4' 27'' O 75° 48' 49'' |
| EMBALSE PARADA | ||||
| 1 | 2 | 3 | 4 | 5 |
| N 20° 1' 40'' O 75° 54' 8'' | N 20° 1' 41'' O 75° 53' 59'' | N 20° 1' 50'' O 75° 53' 47'' | N 20° 2' 4'' O 75° 53' 47'' | N 20° 2' 9'' O 75° 54' 0'' |
Procedimiento para la toma de muestras de agua
Se tomaron muestras por triplicado, de 15 a 30 cm de la columna de agua en cada uno de los puntos de muestreo de los embalses Chalons y Parada entre 8:00-10:00 am [2].
Determinación de parámetros físico-químicos y microbiológicos del agua
Se realizaron determinaciones in situ como temperatura, pH, conductividad (µS.cm-1), oxígeno disuelto (mg.L-1) utilizando el sensor multiparamétrico YSI ProDSS. En laboratorio se realizó determinación química de cloruros (mg.L-1), amonio (mg.L-1), (nitritos (mg.L-1), dureza total (mg.L-1), calcio (mg.L-1), magnesio (mg.L-1), sodio (mg.L-1), sulfatos (mg.L-1), fosfatos (mg.L-1), demanda química oxígeno (DQO) (mg.L-1) [3, 4].
Metodología para realizar la determinación de Coliformes Totales y Fecales
Ambos parámetros se determinaron por el método del número más probable (NMP/100mL). El mismo se basa en el enriquecimiento de las muestras de agua con caldo lactosado y la posterior verificación de los tubos de enriquecimiento positivo en caldo bilis verde brillante, incubado a 35-37 °C durante 24–48 h para coliformes totales e incubados a 44,5±0,2 °C (en baño termostatado) durante 24 h para coliformes fecales [5].
Análisis estadístico
Los resultados experimentales fueron procesados utilizando Statgraphics Centurion. Versión 16.1.03. Para hacer comparaciones múltiples de los parámetros de estudio entre los embalses, los años, los meses y los puntos de muestreo y determinar la existencia o no de diferencias estadísticas con un nivel de significación de p < 0,05 se realizó la Prueba de Tukey HSD.
RESULTADOS Y DISCUSIÓN
Los criterios de características del agua permiten establecer las normas de calidad. Las mismas son los requerimientos máximos que deben cumplirse para un determinado hecho, si alguno de esos requerimientos no se cumple, entonces el agua es inservible y será necesario algún tratamiento especialmente diseñado para obtener los niveles recomendados. Atendiendo a esto, en Cuba existen Normas que reglamentan los criterios de calidad de las aguas según su uso, como son las que regulan los requisitos para: agua potable, agua para abasto, agua para pesca [8-10]; las cuales fueron utilizadas en este trabajo, para el análisis de la calidad de las aguas de los embalses Chalons y Parada de la provincia de Santiago de Cuba.
A continuación, se hace un análisis de las características de los embalses según los parámetros físicos, químicos y microbiológicos establecidos por estas normativas cubanas.
Temperatura
La temperatura se comportó, en un rango de 23–26 °C en ambos embalses en los meses de noviembre y marzo de cada año, mientras que en mayo y septiembre los valores medios se comportaron algo más elevados (25-28 °C). Estos niveles no representan valores importantes de contaminación térmica, pero si ideales para el crecimiento de microorganismos que pueden resultar peligrosos para seres humanos y animales [6, 7].
pH y Alcalinidad
En el embalse Chalons, los valores medios de pH obtenido variaron desde 7,08 hasta 8,16 y en el embalse Parada desde 7,14 hasta 7,91, observándose que no existen diferencias significativas entre los valores de ambos embalses con una tendencia al aumento ligero desde el 2011 al 2015. Al comparar estos valores con las normas cubanas de abasto, uso pesquero y agua potable todos se encuentran por dentro del rango permisible [8-10].
En ambos embalses los niveles de alcalinidad se mantienen en valores que no tienen diferencias significativas, aunque Chalons posee niveles de alcalinidad ligeramente superiores (173,71±4,61 mg.L-1) que los de Parada (169,27±11,15 mg.L-1). Estos resultados coinciden con lo planteado por algunos autores que en aguas con valores de pH inferiores a 8,3 la especie dominante es el bicarbonato, variando su concentración entre 50 y 400 mg.L-1 [11, 12].
Conductividad
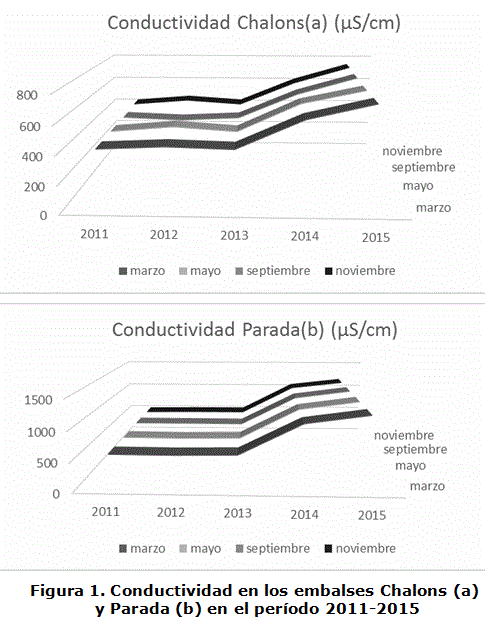
En las NC que se emplean para la evaluación del agua en Cuba, la conductividad no está considerada; en ambos embalses, se mantiene estable con pequeñas desviaciones durante 2011 al 2013, a partir del 2014 aparece un aumento desproporcionado de estos valores, obteniéndose los máximos valores en el 2015. Esto se correlaciona con el aumento de iones que forman sales iónicas (cloruro, sodio y sulfato) (figura 1).
Aunque en las normas evaluadas no se condicionan valores de conductividad para evaluar la calidad del agua, en la literatura algunos autores han planteado que los valores normales de este parámetro en aguas dulces comprenden el rango de 100 a 2 000 µS/cm [4].
Durante todo el período de estudio existen diferencias significativas entre los valores medios de conductividad de ambos embalses. Los valores promedio de los años 2014 y 2015, difieren significativamente con los de los 3 primeros años para cada embalse (p<0,05), siendo muy superiores, lo cual puede ser atribuido a los bajos niveles de agua en ambos embalses, en estos dos últimos años, debido a intensa sequía en la zona Oriental de Cuba, así como por la intrusión salina; siendo más marcado en el embalse Parada, por estar situado cercano a la Bahía de Santiago de Cuba.
Dureza total
La dureza total del embalse Chalons se mantiene estable durante todo el estudio, entre 257 y 283 mg.L-1 y no hay variaciones con diferencias significativas entre las muestras tomadas durante los 5 años, en los meses de estudio (marzo, mayo, septiembre, diciembre), es destacable que existen diferencias significativas (p<0,05) al compararlos con el Embalse Parada, lo cual puede estar influenciado por los residuos de diferentes fábricas de ladrillos y residuales del poblado Boniato, así como, del centro penitenciario de similar nombre que llegan establemente a través de escorrentías y de los ríos El Cocal y Dejao (figura 2).
En el embalse Parada, en todos los años durante el mes de noviembre, aparece una disminución de los valores de Dureza Total (figura 2), siendo el valor medio en este mes de 169,55 mg.L-1. Mientras que en los restantes meses fueron significativamente diferentes, superiores a los 200 mg.L-1, evidenciándose una inestabilidad durante todo el estudio, lo cual puede estar provocado entre otros aspectos, por las variaciones de diferentes iones, además de la marcada influencia del Poblado El Cobre, ya que a través del Río Cobre llegan a dicho embalse residuales de origen antropogénico por diversas fuentes contaminantes [13].
Calcio y Magnesio
Estos dos elementos son fundamentales en los niveles de dureza total de los cuerpos de agua, por lo que el comportamiento estable y con niveles superiores en el embalse Chalons se justifica por una proporción más cercana a la unidad entre las concentraciones medias de Ca2+ y Mg2+ en este embalse (Ca2+ =42,34 mg.L-1 y Mg2+ =32,77 mg.L-1) con respecto a Parada que presentó valores medios en general (Ca2+ =46,29 mg.L-1 y Mg2+ =22,89 mg.L-1) (tabla 2).
Sodio
El Na+ es un elemento relativamente abundante, apareciendo en las aguas en forma de sales diversas (cloruros, sulfatos y silicatos). Dada la alta solubilidad de las sales de Na+, en muchas aguas es el catión más frecuente después del Ca2+, en algunos embalses superando las concentraciones de Mg2+, como ocurre en el embalse Parada (Na + =39,71 mg.L-1) mientras que en Chalons (Na+ =27,31 mg.L-1). Durante todo el estudio los valores medios de las concentraciones de Na+ son inferiores a las de Mg2+.
En el embalse Chalons los valores medios de las concentraciones son inferiores durante todo el estudio a los del embalse Parada, presentando diferencias significativas siempre; en ambos embalses hay un aporte de este ión en los niveles de conductividad obtenidos (tabla 2).
TABLA 2. CONCENTRACIONES DE CATIONES Y ANIONES DE LOS EMBALSES cHALONS Y PARADA (2011-2015)
| EMBALSE CHALONS | |||||
|
| 2011 | 2012 | 2013 | 2014 | 2015 |
| Sodio | |||||
| Marzo | 27,15±0,53 | 24,80±2,12 | 27,82±0,51 | 26,59±1,05 | 30,19±1,24 |
| Mayo | 25,84±1,59 | 25,33±1,70 | 27,66±1,73 | 26,28±2,71 | 28,23±4,84 |
| Septiembre | 27,87±1,36 | 27,15±1,22 | 28,59±0,94 | 27,87±1,75 | 29,86±1,83 |
| Noviembre | 27,47±0,73 | 27,26±1,39 | 24,55±1,86 | 26,42±2,54 | 28,36±2,50 |
| Calcio | |||||
| Marzo | 43,33±7,71 | 43,63±5,08 | 39,60±4,20 | 38,22±2,43 | 42,03±3,49 |
| Mayo | 44,23±5,65 | 44,22±5,27 | 45,12±4,86 | 39,48±4,16 | 41,90±4,62 |
| Septiembre | 42,85±6,22 | 42,76±1,25 | 42,38±3,61 | 37,96±1,02 | 48,25±2,73 |
| Noviembre | 44,22±1,32 | 43,87±2,81 | 46,23±3,06 | 37,20±2,51 | 39,41±1,67 |
| Magnesio | |||||
| Marzo | 31,24±5,25 | 30,64±2,08 | 31,04±3,86 | 32,03±2,44 | 36,48±1,82 |
| Mayo | 31,41±4,88 | 30,90±4,77 | 31,58±1,52 | 32,88±3,70 | 35,34±1,51 |
| Septiembre | 30,52±3,15 | 30,45±2,71 | 29,81±3,97 | 35,52±1,39 | 36,00±1,87 |
| Noviembre | 31,89±6,14 | 30,47±2,92 | 32,54±4,48 | 35,25±3,03 | 39,33±3,35 |
| Cloruros | |||||
| Marzo | 42,6135±6,48 | 37,85±5,52 | 47,358±0,87 | 42,60±3,00 | 49,61±2,75 |
| Mayo | 43,476±5,06 | 44,82±0,99 | 47,818±0,9 | 42,038±2,94 | 46,46±0,80 |
| Septiembre | 42,714±4,23 | 43,99±0,69 | 39,968±7,8 | 42,224±3,41 | 46,266±2,25 |
| Noviembre | 43,322±6,01 | 43,11±6,09 | 45,31±2,18 | 43,91±0,88 | 44,824±5,15 |
| Sulfatos | |||||
| Marzo | 29,96±3,65 | 29,72±4,77 | 30,57±7,21 | 30,08±4,47 | 30,71±5,73 |
| Mayo | 30,22±4,27 | 29,30±6,80 | 30,41±1,85 | 29,97±3,60 | 29,86±2,73 |
| Septiembre | 30,71±3,01 | 29,66±6,61 | 30,91±3,28 | 30,43±3,09 | 35,68±4,13 |
| Noviembre | 29,21±4,07 | 29,52±5,47 | 28,28±2,82 | 29,00±2,88 | 28,34±3,38 |
| EMBALSE PARADA | |||||
|
| 2011 | 2012 | 2013 | 2014 | 2015 |
| Sodio | |||||
| Marzo | 37,36±5,42 | 37,392,46± | 37,51±1,77 | 37,42±2,05 | 41,42±5,15 |
| Mayo | 37,43±3,39 | 36,41±2,48 | 37,36±4,60 | 37,40±4,41 | 50,08±4,18 |
| Septiembre | 37,21±6,46 | 37,52±3,75 | 38,33±6,23 | 37,31±2,41 | 48,73±2,63 |
| Noviembre | 37,41±5,10 | 38,96±5,58 | 39,32±3,46 | 41,93±4,31 | 47,73±6,20 |
| Calcio | |||||
| Marzo | 43,64±2,27 | 43,74±3,12 | 43,39±6,16 | 46,45±2,04 | 49,73±2,53 |
| Mayo | 43,21±6,41 | 43,77±3,55 | 43,74±4,04 | 46,22±7,01 | 51,42±3,85 |
| Septiembre | 43,54±4,12 | 44,32±4,48 | 43,61±3,39 | 46,59±7,46 | 56,61±3,79 |
| Noviembre | 41,44±5,13 | 43,62±4,65 | 44,32±3,05 | 49,69±4,36 | 56,70±2,11 |
| Magnesio | |||||
| Marzo | 21,03±1,97 | 20,68±3,78 | 20,94±1,77 | 21,94±4,16 | 26,77±2,81 |
| Mayo | 20,94±2,64 | 21,38±2,60 | 20,68±2,10 | 22,37±3,59 | 25,22±3,82 |
| Septiembre | 21,74±2,58 | 21,67±1,85 | 20,92±3,58 | 25,95±2,51 | 26,58±4,86 |
| Noviembre | 22,39±2,70 | 20,92±2,93 | 21,67±3,32 | 26,03±4,43 | 27,91±2,49 |
| Cloruros | |||||
| Marzo | 74,50±3,91 | 70,94±2,66 | 76,69±4,33 | 84,04±4,48 | 85,08±4,14 |
| Mayo | 73,66±6,41 | 74,83±3,17 | 70,94±5,52 | 82,87±2,25 | 85,90±3,47 |
| Septiembre | 70,04±2,83 | 75,88±3,21 | 70,76±3,85 | 82,23±2,36 | 83,32±3,24 |
| Noviembre | 74,01±2,84 | 70,76±3,22 | 75,88±6,93 | 83,55±2,67 | 85,37±2,74 |
| Sulfatos | |||||
| Marzo | 54,47±3,05 | 53,79±3,80 | 54,62±3,64 | 57,52±1,60 | 58,77±6,47 |
| Mayo | 47,91±3,35 | 51,66±2,89 | 53,03±4,44 | 57,69±4,89 | 56,11±6,92 |
| Septiembre | 52,07±4,77 | 58,07±3,29 | 52,04±4,00 | 57,38±2,11 | 67,83±6,65 |
| Noviembre | 47,16±4,44 | 59,20±5,44 | 53,23±2,57 | 57,08±4,55 | 67,96±8,47 |
Sulfatos
Por lo general, en las aguas superficiales la presencia de este ión prevalece con respecto a los otros compuestos del azufre, que solo suelen aparecer debido a la contaminación por aguas residuales que provoca la oxidación bacteriana de sulfuros [14].
Existen diferencias significativas (p<0,05) entre los valores medios de sulfatos en los embalses durante todo el estudio, destacándose que en el embalse Parada durante los años 2014 y 2015, se obtuvieron concentraciones que difieren significativamente con el primer año de estudio, lo que explica el aumento de la conductividad en estos dos últimos años en este embalse y con el aumento del ión sodio, como parte del Na2SO4, compuesto muy común y soluble, teniendo en cuenta los altos niveles de Sodio presentes en dicho embalse (tabla 2).
Cloruros
La presencia de este ión en las aguas naturales se atribuye a la disolución de depósitos minerales, a contaminación proveniente de diversos afluentes de la actividad industrial y riego agrícola. Las concentraciones de cloruros en Chalons varían desde 37,85 mg.L-1 hasta 49,61 mg.L-1 y en Parada entre 70,04 mg.L-1 y 85,37 mg.L-1 (tabla 2). En ambos embalses se encuentran dentro de los niveles permisibles por las Normas Cubanas de guas para abasto, uso pesquero y agua potable [8, 9, 15].
Existen diferencias significativas entre los niveles de cloruros de ambos embalses (p<0,05) siendo muy superiores en Parada, lo cual puede estar dado por diversos factores, según lo planteado por diferentes autores, de que el agua de lluvia puede ser una fuente importante de ión cloruro, especialmente en zonas próximas a la costa, disminuyendo rápidamente tierra adentro [16, 17]. A veces puede presentarse un incremento esporádico del contenido de cloruros como consecuencia de contaminaciones domésticas, en particular procedentes de la orina del hombre y de los animales, que contiene por término medio 5,00 g.L-1 de ión cloruro [18]. En dos de los puntos de muestreo del embalse Parada (puntos 4 y 5) hay pequeñas comunidades, que poseen cría de ganado ovino-caprino, porcino y vacuno. Así como sucede en la conductividad, existen diferencias significativas entre los valores medios de cloruros del embalse Parada de los últimos dos años de la investigación y los primeros años, existiendo una correlación directa entre los niveles de conductividad, sulfato y cloruro (tabla 2).
Es conocido que los iones cloruros, fosfatos y nitritos son indicadores típicos de contaminación residual doméstica vertida a un cauce natural. Esto, además, puede servir de señal de alerta acerca de la probabilidad de que el agua presente contaminación también de carácter microbiológico patógeno no deseable [19].
Sólidos Totales Disueltos (STD)
Tanto los sólidos totales disueltos, como la conductividad informan sobre el contenido salino de un cuerpo de agua, los mismos pueden ser orgánicos y/o inorgánicos, provenientes de diferentes actividades domésticas, comerciales e industriales.
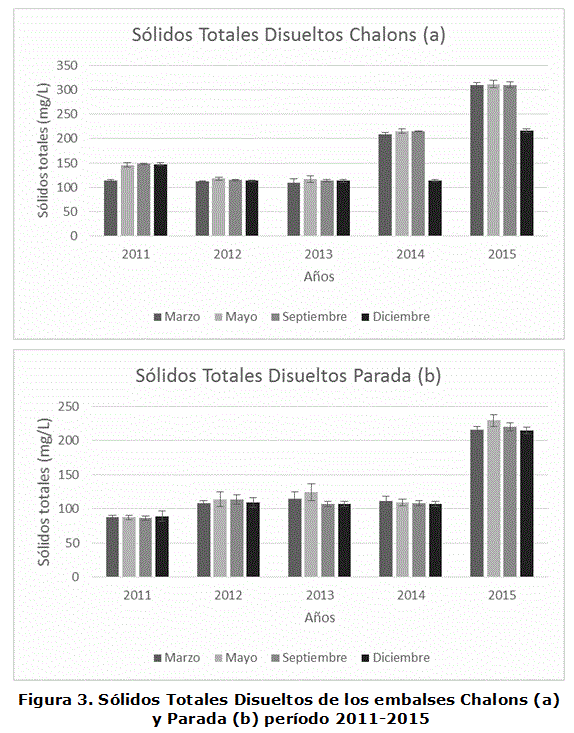
Los STD en el embalse Chalons se mantienen sin diferencias significativas (p<0,05), con valores alrededor de 100 y 150 mg.L-1, durante los años 2011-2013. A partir del 2014 hay un aumento significativo en estos niveles, superando los 200 y 300 mg.L-1, lo cual es mucho más marcado en el 2015, lo que se corresponde con el aumento de los iones y la conductividad. Este comportamiento anómalo es significativamente diferente en el año 2015 (figura 3).
En el embalse Parada existe una estabilidad en los valores de Sólidos Totales Disueltos durante el período 2011-2014, con valores que oscilan entre 86 y 114 mg.L-1. En cambio, en el año 2015, al igual que en el embalse Chalons, los valores de sólidos totales disueltos fueron superiores y estadísticamente diferentes a los años anteriores, lo cual puede justificarse porque ambos embalses presentaron niveles de agua crítico, debido a la intensa sequía que padece la zona. Esto provocó que varios iones, incluidos los que tienen su influencia en el aumento de los sólidos totales, se encontraran en niveles significativamente diferentes y superiores a los de años anteriores.
Al comparar los niveles máximos permisibles de las Normas Cubanas para aguas de abasto, de uso pesquero y potable con los resultados obtenidos, las aguas de ambos embalses pueden clasificarse como aguas de buena calidad, ya que a partir de 1 g.L-1 es que puede verse afectada la calidad del embalse [8-10, 15].
Amonio, nitritos y fosfatos
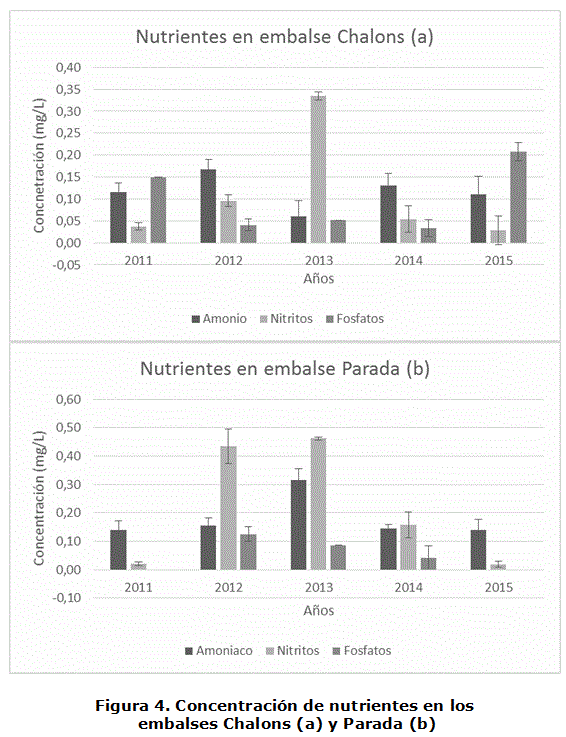
En el embalse Chalons (figura 4), las determinaciones de amonio y nitritos dieron como resultado que generalmente los niveles de amonio fueron superiores que los de nitrito, salvo en el año 2013 (NO2 =0,34 mg.L-1), donde hubo una ligera contaminación fecal, provocada por el trasiego de animales y baños de animales que habitan en la comunidad aledaña a este embalse en los días cercanos al muestreo, demostrando que los iones amonio se oxidaron rápidamente a nitrito siendo significativamente diferentes a los otros años del estudio [4, 20].
En Parada (figura 4), los años 2012 y 2013 mostraron valores más elevados de nitritos (0,43 y 0,46 mg.L-1). La concentración de este ión en las aguas superficiales es baja, pero pueden apreciarse ocasionalmente concentraciones inesperadamente altas, debido a la contaminación industrial y aguas residuales domésticas que van disminuyendo, hasta llegar en el 2015 a un valor similar al encontrado al inicio del estudio [4, 20].
Al evaluar los resultados de las determinaciones físico-químicas, según los valores de P total, las aguas de ambos embalses clasificarían como hipereutróficos, sin embargo, al evaluar la concentración de N total son oligotróficos y según las concentraciones de los STD, clasifican como eutróficos [21]. En estudios anteriores estos embalses fueron clasificados como oligotróficas [2, 19].
Con el objetivo fundamental de prevenir el fenómeno de la eutrofización cultural en los ecosistemas acuáticos, investigadores y organismos sugieren o establecen una serie de criterios de calidad del agua con relación a la carga de nutrientes [22]. Según esto, plantean que a niveles superiores a 760 µg NTotal/L y 40 µg PTotal/L pueden resultar en eutrofización de ríos y lagos en muchas regiones. Además, la agencia europea para el medioambiente [23] considera que, en general, una concentración de nitrógeno total al menos diez veces superior a la concentración de fósforo total (la cual no debería exceder el rango 10-25 µg PTotal/L) puede prevenir la proliferación de cianobacterias fijadoras de nitrógeno en ríos y lagos.
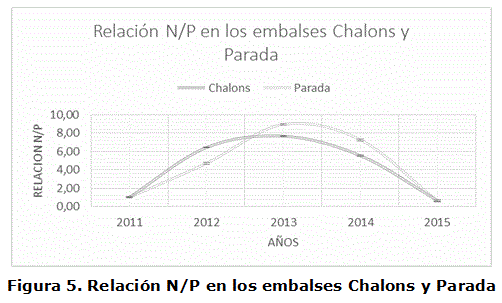
Sin embargo, cuando se evaluó la relación Nitrógeno/Fósforo (N/P) en los embalses Chalons y Parada, se observó que en 2011 y 2015 la relación es muy cercana a la unidad no existiendo diferencias significativa entre ellas, lo cual constituye un aumento de la concentración de fósforo, en forma de fosfato, lo cual favorecería una rápida proliferación de cianobacterias fijadoras de nitrógeno en los embalses, limitando el crecimiento de otras especies de fitoplancton y provocando una disminución de la calidad del agua en dicho ecosistema (figura 5) [24, 25].
Oxígeno disuelto y Demanda Química de Oxígeno
Los valores medios en los embalses correspondientes al oxígeno disuelto en todos los puntos de monitoreo, cumplen con el índice obligatorio para cuerpos de agua dulce de uso pesquero y con lo establecido en la Norma Cubana de Abasto (>5 mg.L -1), clasificándose como aguas de buena calidad [8, 10].
En el período de estudio, en ambos embalses, los valores medios de la DQO oscilan en un intervalo de 19,0 y 21,5 mg.L-1, clasificándose las aguas de calidad dudosa según lo estipulado en la NC:25-99 (15-30 mg.L-1). Esto indica presencia de materia orgánica susceptible a oxidarse, en la mayoría de los casos hasta CO2 y H2O (figura 6) [26].
El OD en ambos embalses se encuentra dentro de los valores establecidos por las Normas Cubanas [9, 10], lo cual sugiere que las aguas tienen buena calidad. Entre ambos embalses y durante todo el estudio los valores no presentan diferencias estadísticas, mientras que en los valores de la DQO entre ambos embalses si existen diferencias significativas (p<0,05).
Análisis microbiológico. Coliformes fecales y totales
En el embalse Chalons, solo en el punto 2 de muestreo, en el año 2013, se obtuvo presencia de Colifomes totales (240 NMP/100 mL) cercano al límite permisible y 12 NMP/100 mL de Colifomes fecales, lo cual pudo estar vinculado a la cercanía de una cría considerable de ganado ovino-caprino que consumían agua de la orilla cercana a ese punto de muestreo, resultado que sustenta lo obtenido en la determinación de iones nitritos (NO2 =0,34 mg.L-1).
En el embalse Parada se obtuvo, en los puntos de muestreo 4 y 5 durante los años 2012 y 2013, un comportamiento similar, debido también, a la cercanía de una pequeña comunidad donde mantenían la cría de animales domésticos (NO2 =0,43 mg.L-1 a 0,46 mg.L-1). No obstante, estos parámetros en ambos embalses se encuentran dentro de lo establecido por las normas cubanas vigentes. A partir del 2014 los resultados fueron de ausencia en todos los puntos, siendo uno de los aspectos positivos a esta disminución, las medidas tomadas en la comunidad por razones de salud, según fue comunicado por algunos pobladores [8-10, 15].
CONCLUSIONES
La calidad del agua de los embalses Chalons y Parada desde el punto de vista químico físico es adecuada ya que todos los parámetros están dentro de los niveles regulados por la Norma Cubana de aguas para abasto, aguas para baño, aguas para pesca y agua potable. Sin embargo, ambos embalses según estos parámetros químicos, se pueden clasificar como eutróficas, lo cual puede comprometer su calidad desde el punto de vista microbiológico.
REFERENCIAS BIBLIOGRÁFICAS
1. BATISTA SILVA, J. L. "Utilización actual de los recursos hídricos y calidad ambiental". Mapping. 2002, 76, 88-94.
2. GÓMEZ LUNA, L. M.; ÁLAMO, B.; RODRÍGUEZ TITO, J. C. "Riesgo de contaminación con cianobacterias en tres embalses de agua de Santiago de Cuba". Medisan. 2010, 14(2).
3. MARAÑÓN REYES, A. et al. "Evaluación temporal de la calidad de las aguas del río Los Guaos de Santiago de Cuba". Revista Cubana de Química. 2015, 26(2), 115-125.
4. SARDIÑAS, P. O. et al. "Evaluación físico-química y microbiológica del agua de la presa El Cacao (Cotorro, Cuba)". Hig. Sanid. Ambient. 2006, 6, 202-206.
5. Oficina Nacional de Normalización, "Microbiología del aguaDetección y enumeración de coliformesTécnica del Número Más Probable (NMP)". NC:1095, 2015, La Habana, Cuba.
6. LÜRLING, M. et al . "Comparison of cyanobacterial and green algal growth rates at different temperatures". Freshwater Biology. 2013, 58(3), 552-559.
7. DE SENERPONT, D. et al. "Plankton dynamics under different climatic conditions in space and time". Freshwater Biology. 2013, 58(3), 463-482.
8. Oficina Nacional de Normalización, "Evaluación de los objetos hídricos de uso pesquero". NC:25, 1999, La Habana, Cuba.
9. Oficina Nacional de Normalización, "Agua Potable-Requisitos sanitarios". NC:827, La Habana, Cuba, 2012.
10. Oficina Nacional de Normalización, "Higiene comunal-fuentes de abastecimiento de agua-calidad y protección sanitaria". NC:1021, La Habana, Cuba, 2014.
11. BAIRD, C. Química ambiental. 2da ed. España: Reverté, 2001.
12. FONTANA, L. et al. "The eutrophication history of a tropical water supply reservoir in Brazil". Journal of Paleolimnology. 2014, 51(1), 29-43.
13. GONZÁLEZ, A. et al. "Composición de las aguas del río cobre de la provincia de Santiago de Cuba en la zona de la mina grande". Revista Cubana de Química. 2005, 17(3), 71-76.
14. PATINO, R. et al. "Long-term trend analysis of reservoir water quality and quantity at the landscape scale in two major river basins of Texas, USA". Land and Reservoir Management. 2016, 31(3), 254-279.
15. Oficina Nacional de Normalización "Lugares de baño en costas y en masas de agua interiores. Requisitos Higiénicos Sanitarios". NC:22, La Habana, Cuba, 1999.
16. LOPEZ ARCHILLA, A. I. et al. "Temporal variation of phytoplankton in two neighbouring Mediterranean shallow lakes in Donana National Park (Spain)". Limnetica. 2012, 31(2), 289-304.
17. BARCELÓ, D.; LÓPEZ, M. J. Contaminación y calidad química del agua: el problema de los contaminantes emergentes. Jornadas de presentación de resultados: el estado ecológico de las masas de agua. Panel científico-técnico de seguimiento de la política de aguas, Sevilla, 2008.
18. CATALAN, J. et al. "The roles of food and water in the bioaccumulation of organochlorine compounds in high mountain lake fish". Environmental Science & Technology. 2004, 38(16), 4269-4275.
19. GOMEZ, L.; ÁLVAREZ, I.; RODRÍGUEZ, J. C. "CUBA: Toxic cyanobacteria risk assessment, research and management". En CHORUS, I. "Current approaches to Cyanotoxin risk assessment, risk management and regulations in different countries" Federal Environment Agency (Umweltbundesamt), 2012, pp. 40-48.
20. CAMARGO, J. A.; ALONSO, A. "Contaminación por nitrógeno inorgánico en los ecosistemas acuáticos: problemas medioambientales, criterios de calidad del agua, e implicaciones del cambio climático". Ecosistemas. 2007, 16(2), 98-110.
21. JORGENSEN, S. E.; JOHNSEN, I. B. Principles of environmental science and technology. vol. 14. Elsevier, 2011.
22. Environmental Protection Agency "National recommended water quality criteria". EPA US: Washington, DC, 2006.
23. LIU, Y. et al. "Global phosphorus flows and environmental impacts from a consumption perspective". Journal of Industrial Ecology. 2008, 12(2), 229-247.
24. CHISLOCK, M. F.; SHARP, K. L.; WILSON, A. E. "Cylindrospermopsis raciborskii dominates under very low and high nitrogen-to-phosphorus ratios". Water Research. 2014, 49, 207-214.
25. HORVATH, H. et al. "Contribution of nitrogen fixation to the external nitrogen load of a water quality control reservoir (Kis-Balaton Water Protection System, Hungary)". Hydrobiologia. 2013, 702(1), 255-265.
26. CHELLAPPA, N. T.; BORBA, J. M.; ROCHA, O. "Phytoplankton community and physical-chemical characteristics of water in the public reservoir of Cruzeta, RN, Brazil". Brazilian Journal of Biology. 2008, 68(3), 477-494.
Recibido: 25/11/2016
Aceptado: 3/05/2017
MSc. José Carlos Rodríguez-Tito, Departamento de Fundamentos Químicos y Biológicos, Universidad de Oriente, Santiago de Cuba, Cuba, jcrt@uo.edu.cu