Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Tecnología Química
versión On-line ISSN 2224-6185
RTQ vol.31 no.1 Santiago de Cuba ene.-abr. 2011
ARTÍCULO ORIGINAL
OBTENCIÓN DE SULFURO DE COBRE Y MEJORA DE LA CALIDAD DEL SULFURO MIXTO DE NI + CO
OBTAINING COPPER SULFUR AND IMPROVING THE NI + CO MIXED SULFURITY QUALITY
MSc. Katia Rodríguez-Viamonte, Lic. Omar Lobaina-Eduardo, Lic. María Elena Prieto-Breffe
Centro de Investigaciones del Níquel, Moa, Cuba. krodriguez@cil.moa.minbas.cu
RESUMEN
Se presentan los resultados obtenidos del estudio a escala piloto de la separación de cobre en forma de sulfuro como proceso previo a la precipitación del sulfuro mixto de Ni + Co, utilizando como agente precipitante el hidrosulfuro de amonio. El estudio experimental se realizó en una instalación existente en la Mini – Refinería de Níquel y Cobalto del Centro de Investigaciones del Níquel. Se efectuó un diseño de experimentos 32 con 2 réplicas, para un total de 27 experimentos, utilizando el programa profesional STATGRAPHICS 5.1, en el que se consideraron como variables independientes: temperatura y consumo de reactivo precipitante. Se obtuvieron eficiencias de precipitación de cobre superiores al 98 % mientras que las de cobalto y níquel resultaron inferiores a 14 % y 2 % respectivamente, estos resultados se lograron a 313 K y 5 – 6 de reactivo precipitante (cantidad estequiométrica). El sólido producto de estas pruebas presentó en su composición un contenido de cobre de 14 – 21 % que lo convierte en un producto comercializable, mientras que el contenido de níquel no sobrepasa el 17 %. Se obtuvieron los modelos estadísticos matemáticos que describen el comportamiento de la eficiencia de precipitación de cobre, cobalto y níquel. La precipitación de sulfuro mixto se efectuó a 313 K y 3 veces el consumo de reactivo precipitante necesario. Se obtuvo un producto de mejor calidad, con 0,13 % de cobre, lo que facilita su comercialización y posterior refinación.
Palabras claves: sulfuro de cobre, sulfuro de ni+co, calidad sulfuro mixto.
ABSTRACT
The document contains the results of a pilot test on copper separation in the form of copper sulfide prior to the precipitation of Ni+Co mixed sulfides using ammonia hydrosulfide as a precipitation reagent. The investigation was conducted at the nickel and cobalt Mini-Refinery belonging to the Nickel Research Center. The selected test design was 32 plus 2 repetitions for a total of 27 test runs. The Statgraphics software (version 5.1) was used to assist on the investigation. Temperature and consumption of precipitation reagent were considered as independent variables. The resulting copper precipitation efficiency was above 98% while cobalt and nickel precipitation efficiencies were below 14 % and 2 % respectively. These results were achieved at 313K and 5-6 stoichiometric of precipitation reagent. The copper content of the product solids was 14-21%, which makes this product marketable, while nickel content remained below 17%. Mathematical statistical models describing precipitation efficiency trends for copper, cobalt and nickel were generated. Mixed sulfides precipitation was carried out at 313 K and precipitation reagent consumption requirements (stoichiometric) tripled. The quality of the resulting product was better (0,13 % copper) which favors marketing and refining.
Keywords: cooper sulfide, ni+co sulfide, quality mixed sulfide.
INTRODUCCIÓN
Entre las principales prioridades de la Industria Cubana del Níquel está la mejora de sus productos finales, uno de los cuales es el sulfuro de Ni + Co que se obtiene en las plantas de Lixiviación carbonato-amoniacal (Empresas Comandante Ernesto Che Guevara y Comandante René Ramos Latour).
En la actualidad el proceso de obtención del sulfuro se efectúa con dificultades que afectan su comercialización y el posible desarrollo y diversificación de la industria cubana del níquel y el cobalto. Entre estas dificultades se tiene que la obtención del sulfuro de Ni+Co (con una composición promedio de 22 % de níquel, 8 % de cobalto y 1,4 % de cobre) en las referidas empresas no ha garantizado la obtención de un producto que contenga cobre en cantidades comercializables (10 %), lo que provoca que este elemento constituya una impureza en el sulfuro de Ni + Co, no obteniéndose ingresos económicos por la venta del mismo. Aproximadamente se pierden 200 t /año.
En el presente trabajo se estudia a escala piloto el comportamiento de la separación del cobre en forma de sulfuro a partir de los licores carbonato–amoniacales, con la finalidad de mejorar la calidad de los sulfuros mixtos de Ni + Co que se obtienen en la actualidad en nuestras empresas productoras.
FUNDAMENTACION TEORICA
Proceso de precipitación de sulfuros en forma de combinaciones poco solubles
La teoría de los procesos metalúrgicos permite caracterizar las transformaciones físico químicas que tienen lugar en los procesos de precipitación de sulfuros en forma de combinaciones poco solubles y analizar la influencia de los factores en el desarrollo de estos.
El proceso de precipitación es el resultado de una reacción química, la cual se caracteriza por la aparición de un sólido en el seno de un líquido, al adicionar un reactivo o agente precipitante, formando un producto insoluble con alguno de los iones de la solución.
En la precipitación de sulfuros metálicos como sustancias poco solubles, se establece un equilibrio de disolución-precipitación entre el sólido precipitado y sus iones en disolución, el cual se presenta a continuación:
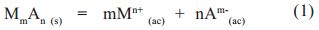
La característica termodinámica principal de estos equilibrios [6] es la constante del producto de solubilidad (Kps) que representa el producto de la actividad de sus iones para la disolución exactamente saturada; para la ecuación (1) la Kps queda expresada como:

Para el caso de disoluciones diluidas, se cumple que γ(M) y γ(A) = 1 por lo que la relación (1.1) se transforma en:
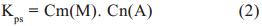
Para que ocurra la precipitación de una sustancia, la solución debe saturarse de esta y cuantitativamente debe cumplirse que: [6]

La Kps es una constante para cada sustancia y depende directamente de la temperatura.
Al analizar la solubilidad de estas sustancias hay que tener presente la influencia de varios factores; por ejemplo el pH, la fuerza iónica, la hidrólisis de aniones de ácidos débiles, de ligandos ajenos formadores de complejos, etcétera. [3]
Los sulfuros de metales pesados como: níquel, cobalto, cobre, hierro, manganeso, cinc y otros son poco solubles. Al precipitar estos iones metálicos en forma de sulfuros hay que tener presente los siguientes equilibrios:
1 Equilibrio de disociación del sulfuro, que viene representado por la siguiente ecuación de reacción:
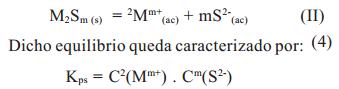
2 Equilibrio de ionización del sulfuro de hidrógeno. En las disoluciones acuosas se comporta como un ácido diprótico que se disocia en:

Por último, combinando las relaciones 1.4 y 1.7 se puede determinar entre otros aspectos, el pH de precipitación del sulfuro y la C(S2-) y C(Mm+) mínima necesaria para que ocurra la precipitación, para las condiciones dadas.
Un aspecto importante a tener en cuenta en la precipitación de sulfuros, es que conociendo el pH de precipitación y su correspondiente valor de la Kpsse puede valorar si es posible realizar una precipitación selectiva de los sulfuros.
En el caso de los sulfuros de níquel, cobalto y cobre, los valores de la Kps, son los siguientes:
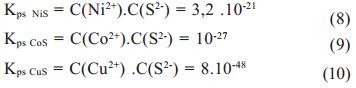
A partir de dichos valores y relacionando las expresiones anteriores, se observa que las concentraciones de los metales en equilibrio con sus sulfuros estarán relacionadas entre sí como se muestra a continuación:
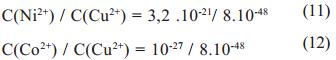
Lo cual significa que existe poca posibilidad de llevar a cabo en condiciones normales una precipitación selectiva (totalmente) de níquel, cobre y cobalto.
En medio amoniacal, la situación puede cambiar al introducir el criterio de inestabilidad de los complejos amoniacales de dichos elementos dado por el valor de la constante de estabilidad de los mismos a 298 K. [6, 4]
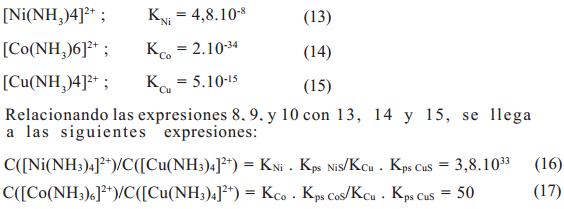
Esto indica a su vez, la poca probabilidad de poder efectuar en condiciones normales y en medio amoniacal, una precipitación selectiva del cobalto, ya que conjuntamente con este sulfuro, precipita cobre y níquel, aunque en menor proporción.
Se ha reportado [3] que en los sulfuros amoniacales las formas que predominan desde el punto de vista estructural son el β-CoS y el α-NiS. Los sulfuros de cobre son más estables que los β-CoS y α-NiS, ya que los iones de cobre en disolución se intercambian con iones níquel y cobalto precipitados en forma de sulfuros, pasando los últimos a disolución y precipitando el cobre como sulfuro.
Se plantea además [1] que la disminución de la temperatura favorece las reacciones de precipitación del níquel y el cobalto al igual que la de intercambio entre ambos metales, mientras que desfavorece la reacción de reducción del cobalto (III) a cobalto (II)
METODOS UTILIZADOS Y CONDICIONES EXPERIMENTALES
Caracterización de materias primas
Se utilizó un licor producto obtenido en pruebas realizadas en la planta piloto del Centro de Investigaciones del Níquel con mineral del yacimiento Yagrumaje norte, del cual se tomó una muestra y se envió al laboratorio para su caracterización. Ver a continuación la tabla 1.
Tabla 1
Composición química del licor carbonato amoniacal utilizado en las pruebas de precipitación de sulfuros (g/L)
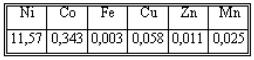
El agente precipitante usado fue el NH4HS, este se utiliza en las empresas productoras para la precipitación de cobalto. La muestra usada en la investigación fue tomada en un periodo de estabilidad operacional con el objetivo de garantizar su representatividad, la concentración usada fue de 150 g/L.
Instalación para precipitación de sulfuros
Para el desarrollo de las pruebas se utilizó una instalación piloto, formada por un tanque de almacenaje de licor producto de 50 m3 de capacidad, un reactor convencional con agitación provisto de deflectores, camisa de calentamiento y medición de temperatura, con una capacidad de trabajo de 1,5 m3, sedimentador, filtro prensa y tanques de almacenaje del licor purificado de cobre. Para la adición del reactivo precipitante se utilizó una bomba dosificadora con variación de velocidad, cuya descarga fue introducida en el reactor a través de un orificio que posee en su parte superior. La camisa de calentamiento del reactor estaba acoplada a la línea de vapor, regulándose la temperatura manualmente para lograr mantener la misma en el valor necesario para cada corrida.
Técnica experimental
Se vierte el licor objeto de estudio en el reactor, se pone en funcionamiento el sistema de agitación y se abre la válvula de vapor, manualmente se controla la temperatura correspondiente a cada experimento, se introduce en el reactor la descarga de la bomba dosificadora y con un flujo constante, comienza la adición del mismo durante 5 min, se detiene la agitación y el contenido del reactor se descarga mediante una bomba al sedimentador, se deja reposar durante 10 min, luego de transcurrido este tiempo la pulpa es bombeada hasta el filtro prensa previamente preparado para su filtración, durante la cual se toma la muestra de licor, se descarga el filtro, el sólido es lavado con agua amoniacal y puesto a secar en la estufa a 333 K, luego se toma la muestra y se envía al laboratorio para su caracterización.
Análisis químico
Los análisis químicos de los elementos metálicos en los licores amoniacales y en los sólidos fueron realizados por espectrofotometría de absorción atómica, siguiendo la metodología existente en las normas de análisis del laboratorio analítico del Centro de Investigaciones del Níquel.
Diseño de experimentos
En la investigación se consideraron como los factores influyentes en la eficiencia de precipitación de sulfuro los siguientes: consumo de reactivo precipitante, temperatura.
Con el propósito de determinar el efecto sobre la eficiencia de precipitación del sulfuro de cobre, cobalto y níquel de estos factores, se realizó un diseño experimental factorial multinivel 32 con dos réplicas para un total de 27 experimentos ordenados en tres bloques utilizando el programa profesional STATGRAPHICS versión 5.1.
Variables independientes:
- Consumo reactivo precipitante
- Temperatura
Variables dependientes:
- Eficiencia de precipitación de cobre
- Eficiencia de precipitación de cobalto
- Eficiencia de precipitación de níquel
Ver a continuación la tabla 2.
Tabla 2
Niveles de las variables en el diseño experimental

Precipitación de sulfuro de Ni + Co a partir de los licores descobrados
El licor purificado de cobre obtenido bajo las condiciones experimentales que arrojaron los mejores resultados de eficiencia de precipitación de este elemento, fueron utilizados luego para precipitar cobalto y comprobar de esta forma que el mismo queda libre de cobre. Para ello fueron utilizadas la misma instalación y técnica experimental que para la precipitación de sulfuro de cobre.
La cantidad de reactivo utilizada fue de 3 veces el estequiométrico necesario y con una temperatura de 313 K correspondiendo con las condiciones bajo las cuales se lleva a cabo este proceso en las plantas productoras.
DISCUSION DE RESULTADOS
En la tabla 3 se muestran los resultados promedios de las eficiencias de precipitación calculados para cada corrida, así como la composición de los sólidos obtenidos en las mismas.
Tabla 3
Promedios de las eficiencias de precipitación de Cu, Co y Ni y composición del sólido obtenido
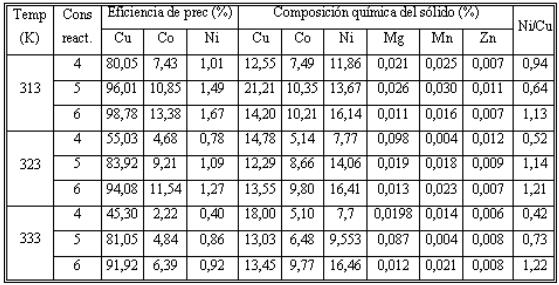
Según los resultados obtenidos de eficiencia de precipitación de cobre, cobalto y níquel, reflejados en la tabla 3, con el aumento del consumo de reactivo precipitante, para los tres elementos estudiados la misma aumenta, lo que además se refleja en los gráficos que se muestran a continuación.
Observando la posición que ocupan las curvas de eficiencia de precipitación de los metales analizados en dichos gráficos, a medida que aumenta la temperatura, el proceso de precipitación del cobalto y níquel se desfavorece, por lo que las eficiencias de precipitación disminuyen. Se comprueba que el proceso de precipitación del cobre tiene el mismo comportamiento con la temperatura que el níquel y el cobalto.
Ver a continuación los gráficos 1, 2 y 3.
Observando y comparando los valores de eficiencia de precipitación de los tres elementos, (tabla 3) y además como se conoce de la literatura [5], los valores de las constantes del producto de solubilidad del cobre, cobalto y níquel disminuyen en ese orden, existe la posibilidad de llevar a cabo bajo las condiciones experimentales a las que se realizó el trabajo, una precipitación selectiva de sulfuro de cobre con respecto al sulfuro mixto de Ni + Co.
Si analizamos la composición de los sólidos obtenidos así como la relación Ni/Cu que se muestran en la tabla 3, nos daremos cuenta que todos presentan características aceptables para ser comercializados, se observa además que no existe una relación directa entre la composición del sólido y la eficiencia de precipitación de los elementos, el contenido de cobre se mantiene alrededor de 15 % llegando hasta valores de 21 %, mientras que el
contenido de níquel no sobrepasa el 17 %, para obtener relaciones Ni/Cu de alrededor de 1.
En el licor producto, el elemento de mayor concentración es el níquel, es por esto que el sulfuro de níquel tiende a precipitar en mayores cantidades que las esperadas bajo las condiciones de equilibrio, debido a que como se sabe, la constante del producto de solubilidad depende de la concentración de los iones en solución [2] y al haber níquel en mayor cantidad se alcanza más rápidamente el equilibrio que da lugar a la formación del sulfuro.
En el proceso de precipitación de cobre, al igual que en el de precipitación de cobalto, resulta beneficioso precipitar la menor cantidad de níquel posible, debido a que el precio del níquel es mayor en el sínter que en el sulfuro, por lo que se tendrían menos pérdidas por concepto de venta de este metal, en cuanto al cobalto su precio es similar en ambos sulfuros, por esta razón, que el cobalto se encuentre en un sulfuro u otro no influye en las ganancias a obtener por su venta. Por todo lo anterior, y teniendo en cuenta las eficiencias de precipitación de cada uno de los elementos se concluye que las condiciones más favorables para llevar a cabo la separación del cobre del licor producto son 313 K de temperatura y 5 - 6 de consumo de reactivo precipitante (cantidad estequiométrica), ya que es con estas condiciones con las cuales se logra una combinación de alta eficiencia de precipitación de cobre y baja eficiencia de precipitación de níquel y cobalto.
Análisis estadístico de los resultados
Los resultados estadísticos obtenidos y analizados por el programa profesional STATGRAPHICS versión 5,1, muestran que ambas variables independientes tienen influencia significativa en las variables dependientes ya que las barras que representan al estequiométrico o consumo de reactivo precipitante y a la temperatura respectivamente, sobrepasan la línea de influencia, lo que queda demostrado en el gráfico 4 donde se presenta la carta estandarizada de Pareto para cada uno de los metales de interés, se observa que el aumento del consumo de reactivo precipitante afecta a las eficiencias de precipitación de cada elemento positivamente, mientras que con el incremento de la temperatura disminuyen.
En los casos del cobre y el cobalto, el consumo de reactivo precipitante ejerce mayor influencia que la temperatura, ocurriendo lo contrario con el níquel.
Ver a continuación los gráficos 4 y 5.
La interacción de las variables y su efecto sobre la eficiencia de precipitación para cada elemento se muestra en el gráfico 5, se observa que en el caso del cobre, en el menor nivel del estequiométrico, la variación de la eficiencia de precipitación es mayor en comparación con el mayor nivel de esta variable independiente y con los dos elementos restantes en ambos niveles, se aprecia además que para todos los casos, el mayor valor de eficiencia de precipitación se alcanza con la combinación de menor valor de temperatura y mayor valor de estequiométrico o consumo de reactivo precipitante.
A continuación se muestran los modelos matemáticos obtenidos que describen el comportamiento de la eficiencia de precipitación de cada uno de los elementos de interés así como el coeficiente de regresión correspondiente.
Modelo matemático obtenido para la eficiencia de precipitación de cobre (Ver aquí)
Modelo matemático obtenido para la eficiencia de precipitación de cobalto (Ver aquí)
Modelo matemático obtenido para la eficiencia de precipitación de níquel (Ver aquí)
El valor del coeficiente de regresión obtenido para cada uno de los modelos se encuentra por encima de 90 %, lo que quiere decir que los modelos ajustados explican más del 90 % de la variabilidad de la eficiencia de precipitación de cada elemento.
Precipitación de sulfuro de Ni + Co a partir de los licores descobrados
El sólido obtenido en esta prueba fue analizado en el laboratorio y a continuación se muestran los resultados. Ver a continuación la tabla 4.
Tabla 4
Composición química del sulfuro mixto de Ni + Co
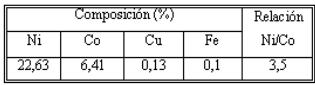
Como se puede apreciar, el contenido de cobre en el sulfuro mixto de Ni + Co es muy pequeño, prácticamente insignificante.
CONCLUSIONES
1. Es posible realizar la separación del cobre en forma de sulfuro del licor producto del proceso de lixiviación carbonato amoniacal previo a la precipitación del sulfuro mixto de Ni + Co, lo que permite obtener un subproducto de cobre con posibilidades de ser comercializado.
2. Las condiciones más favorables para efectuar dicha operación son a 313 K de temperatura y utilizando 5–6 de consumo de reactivo precipitante (cantidad estequiométrica). El sulfuro de cobre así obtenido presenta en su composición entre 14 y 21 % de cobre y no más de 17 % de níquel, para una relación níquel/ cobre de alrededor de 1.
3. Se logra mejorar la calidad del sulfuro mixto de Ni + Co obtenido a partir de licores descobrados, disminuyendo el contenido de cobre de 1,38 % a 0,13 %.
BIBLIOGRAFIA
1. GARRIDO, M. Precipitación de sulfuros de cobalto y níquel a partir de soluciones carbonato amoniacales. Tesis en opción al título de Doctor en Ciencias Técnicas. Instituto Superior Minero Metalúrgico, Moa, 2003.
2. GUERÁSIMOV, J. Curso de química física. Editorial Mir. Moscú. 1971.
3. RODRIGUEZ, Y. Estudio del proceso de precipitación de metales en forma de sustancias poco solubles durante el tratamiento del licor amoniacal C1 de la Empresa "Ernesto Che Guevara" con el residual agua del cooler de la empresa Moa Nickel S.A. Trabajo de diploma, Instituto Superior Minero Metalúrgico, Moa, 1995.
4. SARDUY, C. et al. Estudio de la purificación de lossulfuros de níquel más cobalto. Trabajo de diploma, Instituto Superior Minero Metalúrgico, Moa, 1988.
5. WEAST, R. and ASTLE, M. Handbook of chemistry and physics. 61 edición, CRC, Press, Inc, 1981.
6. ZELIKMAN, A. et al., Teoría de los procesos hidrometalúrgicos. Moscú. 1982.
Recibido: Julio de 2010
Aprobado: Diciembre de 2010
MSc. Katia Rodríguez-Viamonte. Centro de Investigaciones del Níquel, Moa, Cuba. krodriguez@cil.moa.minbas.cu














