Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Tecnología Química
versión On-line ISSN 2224-6185
RTQ vol.33 no.1 Santiago de Cuba ene.-abr. 2013
ARTÍCULO ORIGINAL
Aplicación de la velocidad de aeración para la lixiviación amoniacal de Ni y Co a escala industrial
Application of Aeration Rate for Ammonia Leaching of Ni and Co at Preliminary Industrial Scale
Ing. María Elena Magaña-Haynes, MSc. Armando Rojas-Vargas
Centro de Investigaciones del Níquel (CEDINIQ), Moa, Cuba. mmagana@sn.moa.minbas.cu
RESUMEN
Se estudió la lixiviación carbonato amoniacal aplicando velocidades de aereación para disminuir las pérdidas de níquel y fundamentalmente de cobalto. El sistema está compuesto por 5 reactores en serie. Se midió el Potencial Redox (E0x) para indicar el curso de la lixiviación con un pH-mV de electrodos combinados Pt-calomel. Se calculó la velocidad de aeración (m3/t min), al aplicar un programa de computación, para un tiempo de retención calculado entre 100 y 128 min. El contenido de níquel, cobalto y hierro en el mineral fue de 1,09 %, 0,120 % y 44,96 % respectivamente. La modificación de la velocidad de aeración ejerció un cambio apreciable en la lixiviación de los metales, mientras que para el Ni las pérdidas alcanzaron un máximo de 1,7 %, para el cobalto fue de un 7,4 %.
Palabras clave: lixiviación amoniacal, potencial redox, aeración.
ABSTRACT
The ammonia-ammonium carbonate leaching was studied applying several aeration speed to diminish the nickel losses and fundamentally, of cobalt. The system is composed by 5 reactors in series. The Redox Potential (ORP) was measured to indicate the course of the leaching with a pHmV of combined electrodes Pt-calomel. The aeration speed was calculated applying a computer program, for a time of retention calculated between 100 y 128 min. The content of nickel, cobalt and iron in the mineral was 1,09 %, 0,120 % and 44,96 % respectively. The modification of the aeration speed exercised a valuable change in the leaching of the metals, while that for the nickel the losses reached a maximum of 1,7 %, for the cobalt it was 7,4 %.
Keywords: ammonia leaching, redox potential, aeration.
INTRODUCCIÓN
El presente trabajo posee campo de acción en el proceso de extracción de níquel y cobalto por la tecnología carbonato amoniacal, en la etapa de lixiviación. El mineral laterítico previamente reducido en los hornos de reducción, se mezcla con el licor carbonato amoniacal a una densidad de 1 140-1 150 kg/m3 y temperatura entre 40-42 0C en los tanques de contacto y se lixivia en reactores cilíndricos con agitación y alimentación de aire.
La literatura consultada [1, 5, 6] coincide que la reacción química principal durante la lixiviación de minerales lateríticos se representa por (1), con fuerte dependencia de la temperatura y de la calidad del licor de lixiviación en cuanto a concentración de amoníaco y dióxido de carbono.
Los factores que inciden sobre las pérdidas de níquel y cobalto en la lixiviación han sido explicadas en la literatura [2-4] como son: pérdidas por hidrólisis, pérdidas con los oxihidróxidos de hierro (OHH) y por pasivación de la superficie de las ferroaleaciones con el oxigeno, tiosultafo y cobalto (III); además se han dado recomendaciones para minimizarlas, como es la aplicación del potencial redox [1] como indicador de la marcha de la lixiviación para establecer los flujos de aire.
El ión [S2O3]2- ejerce una acción reductora sobre el níquel y fundamentalmente cobalto [3, 4] precipitándolos en forma de sulfuros, en magnitud que depende de la concentración de dicho ión en el licor amoniacal y de la concentración de cobalto (III), el Co (III) conjuntamente con el oxígeno ejercen acción oxidante, resultando reacciones competitivas. En el caso del níquel puede ocurrir la disolución del sulfuro. El [S2O3]2- ejerce una acción oxidante sobre el hierro (II) e incrementa su velocidad de lixiviación aportando ambos un potencial más negativo en correspondencia con el incremento de la concentración de [S2O3]2-. A la vez, realiza una acción reductora sobre los hidroxocomplejos (OHH) de Fe (II) reflejándose en un incremento del contenido de magnetita en el precipitado y favorece la lixiviación del Ni y el Co al disminuir la constante de velocidad de reacción de primer orden de oxihidrólisis del hierro, con fuerte dependencia de la concentración de hierro inicial y además, de la velocidad de aeración.
La extracción potencial de níquel y cobalto que es posible lograr en la lixiviación se determina por el método "QT", el cual permite determinar los índices de eficiencia de recuperación de los metales. Se han realizado estudios [8, 10] para identificar la calidad del mineral reducido en dependencia del Potencial Redox inicial [E0x, t=0] y aplicar un flujo de aire especificado, para maximizar el extractable de cobalto sin afectar el extractable de níquel en la QT. Los resultados fueron verificados en [9].
En [8] se realizaron ensayos para determinar la resultante de velocidad de reacción de oxihidrólisis del hierro de orden cero y primer orden, al lixiviar mineral reducido (MR) de diferente calidad, a diferentes flujos de aire y obtuvieron tres zonas (Z) de Potencial Redox (E0x) donde localizar las pérdidas con los oxihidróxidos, entre los potenciales: [E0x, t=0], [E0x, r] y [E0x, máx. ZII] para cada MR y propusieron alternativas para la regulación de la aeración. El Potencial Redox [E0x] es una función de la concentración de hierro (II) disuelto y de tiosulfato en el licor QT.
En el caso del proceso industrial, a la variación de la calidad del mineral reducido, se agregan con respeto al método QT, otros factores que inciden sobre la lixiviación del níquel, cobalto y además, del hierro como son: calidad del licor (concentración de amoníaco y dióxido de carbono, cobalto, iones SxOyZ) y temperatura de la pulpa.
El objetivo del presente trabajo es estudiar la lixiviación carbonato amoniacal aplicando velocidades de aeración para disminuir las pérdidas de níquel y fundamentalmente de cobalto, incluyendo los resultados obtenidos de la evaluación industrial de la medición del Potencial Redox y su interacción con las extracciones de níquel, cobalto y la calidad del licor.
FUNDAMENTACIÓN TEÓRICA
La lixiviación carbonato amoniacal se puede representar como un proceso electroquímico por las siguientes reacciones de electrodo:
Procesos anódicos:
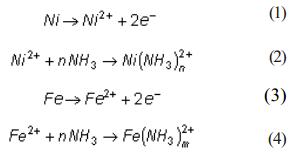
Procesos catódicos:
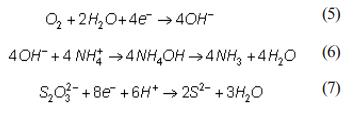
La Ecuación de Nernst expresa la relación cuantitativa entre el potencial redox (E0x) estándar de un par redox determinado, su potencial observado y la proporción de concentraciones entre donador de electrones y aceptor. Plantea Nerst:

Metodología e instalación experimental
La pulpa de mineral laterítico preparada en los tanques de contacto se bombea hasta un distribuidor de cinco líneas y descarga por gravedad hasta la caja alimentadora de interés para este trabajo. La caja alimentadora divide el flujo de pulpa hacia dos sistemas (B y C), compuesto cada uno por cinco reactores cilíndricos de base plana, en serie y con agitación, operan a una ligera presión de vacío como se describe en [7]. La Supervisión del Proceso se realiza mediante el Sistema de Supervisión y Control de Procesos Tecnológicos (SCADA) EROS, sistema ampliamente validado en industrias cubanas.
Para la caracterización del mineral y del licor carbonato amoniacal, se aplican métodos volumétricos, gravimétricos y Espectrofotometría de Absorción Atómica. El potencial se midió con un pHmetro-mV con electrodo combinado PlatinoCalomel, aplicando procedimiento descrito por Rojas [8], seguidamente de tomar la muestra.
Se estableció un flujo de aire diferente para cada sistema (B y C) e igual para todos los reactores de la serie, en dependencia de la potencia de agitación y la dosis de aire (m3 de aire/t. de mineral reducido) normada para la primera etapa de lixiviación. Las muestras se tomaron a la salida del Tanque de Contacto, en la caja alimentadora y en la descarga de cada reactor transcurrido el tiempo de retención y a los siguientes 15 min, para un total de 44 corridas. El licor a la salida del tanque de contacto y en la descarga de cada reactor se caracterizó en cuanto a concentración de níquel, cobalto, amoníaco, dióxido de carbono, azufre, tiosulfato, hierro (II) y se determinó su Potencial Redox [E0x, t = 0] y temperatura.
Se aplicó un programa computacional para estimar el balance de licores, pulpa, calcular el perfil de densidad y de concentración de amoníaco según las condiciones de operación, estimar el tiempo de retención, calcular el flujo de aire y la velocidad de aeración (r) G(m3/(t. min.) reportada por Chang [2].
La extracción de níquel y cobalto se calculó según la ecuación (9), se expresó en fracción (a) a y mediante el modelo (10) para reacción química.

RESULTADOS Y DISCUSIÓN
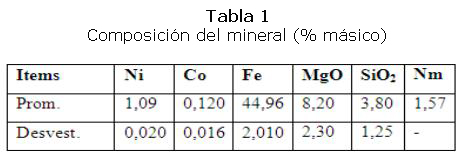
La composición fundamental del mineral alimentado a los hornos de reducción se muestra en la tabla 1, en su contenido de níquel, cobalto, hierro, magnesio, silicio y número de mineral (Nm).
La relación r- NH3/CO2 en el licor de lixiviación fue desfavorable, incrementó el gradiente de concentración de amoníaco en los reactores y afectó las extracciones, se recomienda operar en el rango de 1,5 < NH3/CO2 < 1,8; la concentración de la pulpa fue inadecuada y de cobalto, conforme e inferior a [Co] < 0,2 g/L. Ver tabla 2.
Período sin pérdidas intensas de níquel ni cobalto
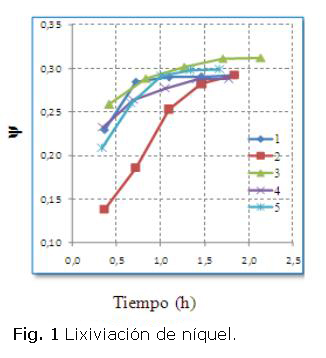
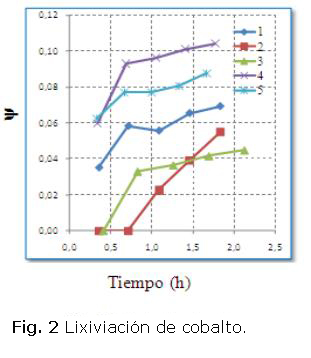
Las corridas experimentales sin pérdidas intensas de níquel ni cobalto se caracterizaron por: relación rNH3/CO2 < 1,95; r- Ni/S = 1,90 +/- 0,14 (prom. +/- desvest.); Potencial Redox en la descarga del 1er. reactor más negativo que -484 mV y en el 2do., tan negativo como -198 mV. En la tabla 3 se muestran las velocidades de aeración aplicadas en cada reactor y en la figura 1 y figura 2, el comportamiento de la lixiviación de níquel y cobalto para 5 corridas experimentales. No se tuvo una correspondencia entre la mayor extracción de níquel y de cobalto. En el caso de las pruebas P2 y P3, puede observarse que no hubo extracción de cobalto sino hasta la descarga del 3ro y 2do reactor respectivamente.
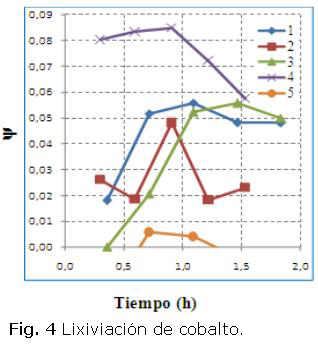
Estudios a escala de banco [4] aplicando la ecuación de Jander  , han mostrado la formación de zonas donde se interrumpe la regularidad del incremento de la lixiviación del níquel con decrecimiento de sus máximos debido a la coprecipitación de Ni con los óxido - hidróxidos de hierro y en la última (zona No. 3) ocurre la expulsión del metal, comportamiento no observado manteniendo los valores referidos de Potencial Redox para la lixiviación en la industria, como se muestra en la figura 1. En el caso de la lixiviación del cobalto, se pueden observar (P1) decrecimiento del máximo y posterior expulsión, al aplicar = 1,78 (m3/(t. min).
, han mostrado la formación de zonas donde se interrumpe la regularidad del incremento de la lixiviación del níquel con decrecimiento de sus máximos debido a la coprecipitación de Ni con los óxido - hidróxidos de hierro y en la última (zona No. 3) ocurre la expulsión del metal, comportamiento no observado manteniendo los valores referidos de Potencial Redox para la lixiviación en la industria, como se muestra en la figura 1. En el caso de la lixiviación del cobalto, se pueden observar (P1) decrecimiento del máximo y posterior expulsión, al aplicar = 1,78 (m3/(t. min).
Se analizó la oxidación del ión tiosulfato [S2O3]2-, ajustándolo a una reacción de primer orden con R2 > 0,92 entre el 1er. y 3er. reactor con constante de velocidad de reacción entre 6,2 · 10-3 < K < 9,6 · 10-3 (1/min) pero, no aportó correlación importante para el análisis de los resultados.
Período de pérdidas intensas de cobalto
Las corridas experimentales con pérdida intensas de cobalto se caracterizaron por: baja carbonatación del licor de lixiviación 1,95 < r- NH3/CO2 < 2,12; rNi/S = 2,04 +/- 0,14 (prom. +/- desvest.) y Potencial Redox más positivo que sin pérdidas intensas.
En la tabla 4 se muestran las velocidades de aeración aplicadas a cada reactor, para 6 corridas.
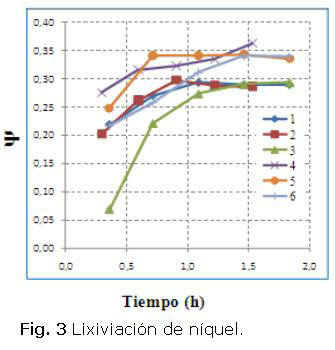
Como se refleja en la figura 3, la extracción de níquel decreció del máximo en un 1,70 % (P2), donde se aplicó (G)= 2,7 en el primer reactor y para el resto de las corridas, inferiores a 0,5 %, mientras que en la figura 4 para el cobalto fue de un 7,4 % (P2). En las pruebas P5 y P6 no hubo extracción de cobalto, coincidió con licor menos carbonatado y a la vez, con la mayor r- Ni/S =2,21. Se recomienda tomar muestras en el último reactor, para determinar la máxima extracción QT e incluir en el análisis. Consideramos que fenómenos como cortocircuitos hidráulicos o canalizaciones y zonas muertas estancadas son aspectos para examinar.
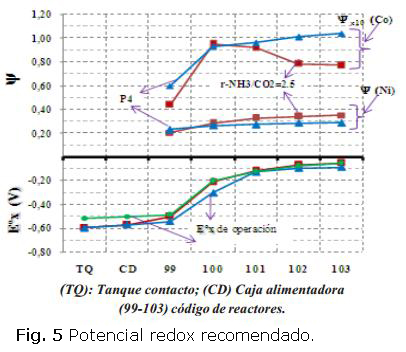
En la figura 5 se muestra correspondiente a la lixiviación de níquel (Ni) y para el cobalto (Co), de la Prueba (P4) sin coprecipitación (figura 2). Comparativamente, se muestran los resultados de la lixiviación en relación con r-NH3/CO2=2,5 (cuadrados rojos), donde, no obstante de mantener el potencial redox (E0x) en el rango recomendado, hubo coprecipitación de cobalto y no de níquel. Este resultado se corroboró con 4 corridas experimentales. No deben compararse las extracciones entre las corridas porque estas no dependen solo de la calidad del licor y de la aeración, sino también de la calidad del mineral reducido determinando el extractable potencial.
Puede observarse en la figura 5 que al ponerse en contacto el mineral reducido y el licor carbonato amoniacal (TQ), el potencial alcanzó los valores más negativos debido a la acción de los iones oxidantes y obtención de la mayor concentración de hierro (II), así como de iones de azufre insaturados tales como tiosulfato y politionatos a partir del azufre presente en el mineral reducido. A la descarga de los reactores del sistema de lixiviación, la diferencia de E0x entre el 1er. reactor (99) y el 2do. (100) fue en el rango -286 < dE0x < -243 mV, en posteriores estudios se podrán investigar nuevos rangos. Al término de la aeración, el potencial alcanzó valores entre -85 < E0x < -26 mV. Se ha de destacar que el tiempo de retención calculado para las pruebas estudiadas fue entre 100 y 128 min, entre los 5 eactores.
Los resultados indicaron que E0x no permite pronosticar por sí solo las extracciones en lixiviación de Ni y Co, aunque para el método QT de determinación del extractable potencial, se han obtenido correlaciones para rangos de calidad de mineral reducido [8].
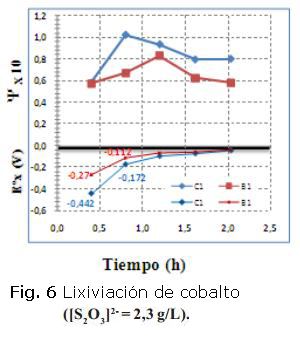
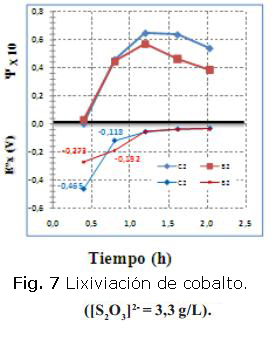
Para las corridas experimentales realizadas en paralelo en las series (B y C), se obtuvo mayor extracción de cobalto en aquella donde se logró el potencial más negativo, como se muestra en dos casos en las figuras 6 y 7. En el eje negativo de la ordenada se refleja el potencial redox (Volt) y en el positivo, en función del tiempo de retención calculado.
CONCLUSIONES
Tras aplicar diferentes velocidades de aeración en la lixiviación carbonato amoniacal de Ni y Co a escala industrial, se llegaron a las siguientes conclusiones:
1. La aplicación de la velocidad de aeración produce un cambio efectivo en la lixiviación del níquel y fundamentalmente del cobalto, en el proceso industrial.
2. Mientras que las extracciones de níquel decrecieron de su máximo hasta un 1,7 %, para el cobalto decreció hasta un 7,4 %.
3. Para la calidad del mineral y licor investigado, operar a un Potencial Redox en la descarga del 1er reactor más negativo que -484 mV y en el 2do, tan negativo como -198 mV, disminuye las pérdidas de los metales con los oxihidróxidos de hierro (OHH) y por pasivación, siendo la caída de potencial redox en el intervalo -286 < dE0x < -243 mV.
4. A una relación r-NH3/CO2 superior a 2,5, el cobalto aún presenta pérdidas intensas no obstante de operar bajo los potenciales recomendados.
BIBLIOGRAFÍA
1. CHANG, C. A. R., BOBKOVSKI, A. G., et-al. "Estudio de las particularidades estructurales y composición de fase de los productos de la hidrólisis de los iones de hierro a partir de licores carbonato-amoniacales", en Tsvetnie Metally. No.9. Págs. 30-34, 1995.
2. CHANG C. A. R., et-al. "Cinética de la lixiviación carbonato - amoniacal del mineral laterítico reducido industrialmente bajo aireación diferenciada", en Revista Minería y Geología, Vol. XV, No. 3, Págs. 23 - 29, 1998.
3. CHANG C. A.; ROJAS-VARGAS, A. "La lixiviación del Proceso CARON: síntesis del conocimiento para su perfeccionamiento industrial". Revista Tecnología Química. Vol. XXIX, No. 1, 2009.
4. CHANG C. A.; ROJAS-VARGAS, A. "La lixiviación del Proceso CARON: síntesis del conocimiento para su perfeccionamiento industrial". Revista Tecnología Química. Vol. XXIX, No. 2, 2009.
5. DOBROJOTOV, G.. N. "Composición sustancial de las mezclas carbonato - amoniacales", en Izv. Vuzov. Zvetnaya Metallurgia,No. 6. Págs.71 - 75, 1986.
6. GRIGORIEVA K.I., VAILLANT H.H., et-al.: "Solubilidad del Níquel y Cobalto (II) en medios carbonatoamoniacales", en Izv. Vuzov Zvetnaya Metallurgia, N1. Págs. 37-41,1987.
7. ROJAS A.V.; GARCÍA-PÉREZ, A. "Análisis de la curva de distribución del tiempo de residencia en un sistema de lixiviación". Revista Tecnología Química. Vol. XXX, No. 1, 2010.
8. ROJAS A.V.; MAGANA M.E. "Intensificación del lixiviado de cobalto en el proceso de lixiviación amoniacal". CEDINIQ. Nicaro. 2005.
9. MAGANA, M. E.; ROJAS-VARGAS, A. "Intensificación del lixiviado de cobalto en el proceso de lixiviación amoniacal (II)". CEDINIQ. Nicaro. 2011.
10.TAVÍO, G. G.; ROJAS-VARGAS, A. "Procesamiento en el horno Selas y posterior lixiviación de muestras del mineral de Pinares de Mayarí". CEDINIQ Nicaro. 2006.
Recibido: Mayo de 2012
Aprobado: Noviembre de 2012
Ing. María Elena Magaña-Haynes. Centro de Investigaciones del Níquel (CEDINIQ), Moa, Cuba. mmagana@sn.moa.minbas.cu