Mi SciELO
Servicios Personalizados
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Tecnología Química
versión On-line ISSN 2224-6185
RTQ vol.38 no.1 Santiago de Cuba ene.-abr. 2018
ARTÍCULO ORIGINAL
Sistematización de aspectos teóricos sobre las tecnologías de producción de biogás a escala industrial
Systematization of theoretical aspects on full scale anaerobic digestion technologies
Dr. C. Ernesto L. Barrera-Cardoso, ernestol@uniss.edu.cu, Lic. Annerys Carabeo-Pérez, Lic. Leyanet Odales-Bernal, Dr. C. Luz M. Contreras-Velázquez, MSc. Lisbet López-González
Centro de Estudio de Energía y Procesos Industriales (CEEPI). Dirección de Investigaciones Aplicadas. Universidad de Sancti-Spíritus José Martí Pérez
RESUMEN
El desarrollo de la producción de biogás a escala industrial en Cuba ha estado limitado en gran medida por el desconocimiento de las alternativas tecnológicas existentes. En el presente trabajo se sistematizan aspectos teóricos de las tecnologías de producción de biogás a escala industrial, teniendo en cuenta cinco etapas básicas: el pretratamiento de los sustratos; la digestión anaerobia; el post-tratamiento de los efluentes; la purificación del biogás; y la generación de energía. A partir de las alternativas consideradas se podrían tratar residuales de altos (= 15 %) y bajos contenidos de sólidos (= 15 %) y residuales complejos (altos contenidos de lignina), al mismo tiempo que se podría generar energía como electricidad, calor o combustible motor.
Palabras clave: producción de biogás, escala industrial, aspectos tecnológicos, residuales biodegradables.
ABSTRACT
In Cuba, the development of biogas production at the full scale has been limited by lack of knowledge about the existing technologies. In this paper the theoretical aspects of biogas production technologies at the full scale are systematized, taking into account five basic steps: pretreatment of substrates; anaerobic digestion; post-treatment of effluents; biogas purification; and power generation. Biodegradable wastes with high (= 15%) and low solids contents (= 15%), as well as complex (high levels of lignin) could be treated with the alternatives described, producing energy as electricity, heat or combustible.
Keywords: biogas production, full scale, technological aspects, biodegradable wastes.
INTRODUCCIÓN
La digestión anaerobia o producción de biogás a escala industrial constituye una alternativa energética renovable que ha sido muy difundida a nivel mundial /1/. Existe una amplia gama de tecnologías de digestión anaerobia que pueden ser utilizadas para cada tipo de sustrato. Estas plantas deben incluir al menos cinco etapas básicas /2/: 1) el pretratamiento de los sustratos; 2) la digestión anaerobia; 3) el post-tratamiento de los efluentes; 4) la purificación del biogás; y 5) la generación de energía en sistemas combinados de producción de electricidad y calor (CHP, por sus siglas en inglés). Estas tecnologías difieren en cuanto a sus costos de inversión, sus parámetros de operación (p.ej.: eficiencia de remoción de DQO, productividad volumétrica) y sus impactos ambientales /3-6/, por lo cual deben ser seleccionadas cuidadosamente en función del contexto al que se quiera aplicar. Por ejemplo, en Brasil, Salomon y Lora /7/, reportaron dentro de los principales obstáculos de la producción de biogás la necesidad de conocer las tecnologías de digestión anaerobia existentes. En Cuba, especialistas de la producción de biogás concordaron, durante el ¨XI Taller Nacional de Biogás¨, en que la comercialización de paquetes tecnológicos y las escasas oportunidades de negocio habían impedido el desarrollo exitoso del biogás a escala industrial. Es por ello que conocer las características técnicas de las plantas actuales para la producción de biogás, incluyendo las alternativas para cada etapa del proceso, se convierte en una necesidad para el sector industrial cubano. Este artículo sistematiza aspectos teóricos sobre las tecnologías existentes para la producción de biogás a escala industrial teniendo en cuenta su aplicabilidad para:
1) el tratamiento de residuales con características diversas en cuanto a biodegradabilidad y contenido de sólidos totales.
2) la generación de energía en forma de electricidad, calor y combustible motor.
Fundamentación teórica
Pretratamiento de los sustratos
En general todas las biomasas que contengan carbohidratos, proteínas, grasas y celulosa como componentes principales, pueden ser empleados como sustratos para la producción de biogás. Inicialmente, las impurezas (p. ej.: piedra, arena, vidrios, plásticos, etcétera) contenidas en los residuales biodegradables deben ser removidas para favorecer el proceso de digestión anaerobia (p. ej.: reduciendo fundamentalmente la formación de espumas y las obstrucciones). En otros casos los residuales biodegradables requieren de un tratamiento (pretratamiento) que mejore su degradación en la etapa posterior (digestión anaerobia). El objetivo de la etapa de pretratamiento es modificar la estructura de los materiales complejos (generalmente lignocelulósicos), con la disminución del grado de polimerización, el debilitamiento de los enlaces de la lignina con los carbohidratos y el incremento del área superficial, favoreciendo de este modo la biodegradabilidad de los sustratos complejos /2, 8/. Estos pretratamientos pueden clasificarse en físicos, químicos o biológicos.
Pre tratamiento físico
El pretratamiento físico es muy común en las aplicaciones industriales. Dentro de los pretratamientos físicos se reportan los pretratamientos mecánicos y térmicos /8/.
El pretratamiento mecánico puede llevar, en algunos casos, a la disminución del tamaño de los sólidos presentes en el residuo y en otros a la destrucción de las células. La técnica de reducción de tamaño incrementa el acceso de los microorganismos, debido a la ruptura de grandes estructuras a cadenas más cortas, de ahí que por esta vía se pueda esperar un mejoramiento del proceso de digestión anaerobia /8/. En este proceso el gasto energético para la operación es directamente proporcional al tamaño de las partículas requerido, el cuál ha sido reportado entre 1 y 4 mm /9/.
El pretratamiento térmico conduce a una mejora en la eficiencia del proceso de digestión (= 30 %) /9/. Típicamente, el proceso ocurre a temperaturas de entre 135 y 220 ºC, presiones por encima de los 10 bar y tiempos de retención de algunas horas /9/. Los requerimientos excesivos de energía para el calentamiento y enfriamiento del residual han sido reportados como una de las limitaciones de estos métodos /8/. Sin embargo, estos pueden ser económicamente factibles cuando se ejecutan utilizando el calor regenerado en el proceso /9/.
Pretratamiento Químico
El pretratamiento químico puede ser empleado para el tratamiento de materiales lignocelulósicos (p. ej.: cachaza, bagazo y residuales de la producción de granos). Muchas veces los pretratamientos químicos son empleados de manera combinada con los térmicos. Es común el uso de ácidos (p. ej.: clorhídrico y sulfúrico) o soluciones alcalinas de hidróxido de sodio y potasio. Los tiempos de retención son considerados cortos (algunas horas) comparados con los de los reactores anaerobios y como resultado se obtiene un sustrato de mayor biodegradabilidad. Las principales desventajas de este método son la baja eficiencia energética y el incremento en los costos de operación por el uso de aditivos químicos que muchas veces no justifican la construcción de una planta a escala industrial. Por tal motivo estos pretratamientos son aplicados mayormente en aplicaciones industriales que permitan aprovechar los residuales de otros procesos (aditivos químicos y calor) /9/.
Pretratamiento Biológico
Los procesos biológicos también pueden ser empleados para el pretratamiento de los sustratos. Diversos estudios han sido reportados para el pretratamiento de residuos lignocelulósicos, con el empleo e inoculación de enzimas específicas (p. ej.: celulosa, proteasa y carbohidrasas) capaces de hidrolizar este tipo de material /8, 9/. Como inconveniente principal se reporta la necesidad de una etapa previa que garantice el ataque enzimático. De ahí que esta alternativa pudiera utilizarse después de uno de los pretratamientos abordados anteriormente.
Digestión anaerobia
Esta etapa es considerada la más importante dentro del proceso bajo estudio, pues es el momento en el que se produce el gas combustible, los bioabonos y se reduce la carga contaminante del residual /2/. La misma tiene por objeto descomponer el material orgánico en un digestor hermético, sin oxígeno molecular, prosiguiendo el proceso hasta que se produzca metano, dióxido de carbono y otros gases. El proceso es una suma de reacciones bioquímicas provocadas por el cultivo de una mezcla de bacterias.
El desarrollo de la tecnología de digestión anaerobia ha estado encaminada, de forma general, al diseño de digestores capaces de cumplir con requerimientos básicos como: altas tasas de carga orgánica continuas, tiempos de retención hidráulicos cortos para minimizar el volumen de reactor y maximizar la producción de metano /10/.
Las diferencias en las tecnologías se basan fundamentalmente en el diseño del reactor anaerobio y se clasifican de acuerdo a los parámetros operacionales como: el contenido de sólidos en la alimentación (húmeda y en seco), las etapas del proceso (una etapa o multietapas), el régimen de alimentación (discontinuo o continuo) y la temperatura de operación (mesofílico o termofílico) /11-13/. Otras clasificaciones incluyen aspectos como el tamaño de la planta y la aplicación de la tecnología /14/.
Cuando la alimentación se caracteriza por un alto contenido de sólidos, mayor de un 15 %, se considera el proceso de digestión anaerobia en estado seco y cuando está entre 0,5-15 % se trata de digestión húmeda o de líquidos.
Varias configuraciones de reactores se han desarrollado para el tratamiento de residuos en general, entre ellos: el reactor de tanque completamente mezclado (CSTR), el reactor de lodo granular expandido (EGSB), el reactor anaerobio de película fija, el reactor anaerobio de flujo ascendente con manto de lodos (UASB). Por sus ventajas el CSTR, el UASB y el EGSB han sido los más utilizados /15/.
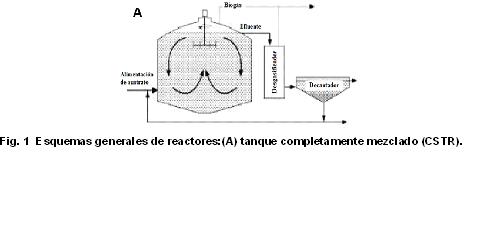
Reactores de tanque completamente mezclado (CSTR)
El reactor CSTR (figura 1A) es sencillo de operar, aunque menos eficaz en cuanto a calidad del efluente en comparación con otras tecnologías. Sus limitaciones se enmarcan en retener las bacterias que catalizan el proceso dentro del reactor y en la pérdida de materia particulada no degrada por corto circuitos /16/. Ha sido usado en el tratamiento de lodos de depuradoras, excretas de animales, residuos industriales /17/ y es actualmente el de mayor aplicación en la degradación de cultivos energéticos como único sustrato o en codigestión /12/. Estos reactores operan de forma continua, ya sea en régimen de temperatura mesofílico o termofílico. Dentro de sus principales parámetros de operación están las cargas orgánicas volumétricas que oscilan alrededor de los 3 kg de solidos volátiles por m 3 de reactor por día, alcanzando productividades de biogás de entre 1,5 y 2,0 m 3 de biogás por m3 de reactor por día /18/. A pesar de esto, la recirculación parcial de biomasa desde el decantador (figura 1A) ha posibilitado el incremento, hasta cuatro veces, de la carga orgánica volumétrica y de la producción de biogás en plantas industriales (p. ej.: la compañía alemana BKW). Así mismo, estas plantas recirculan parte del efluente líquido ( 30 %) evitando el consumo de agua para la dilución de los sustratos y simulando la digestión en seco.
Reactores de flujo ascendente con manto de lodo (UASB)
Los reactores de flujo ascendente con manto de lodo (UASB por sus siglas en inglés), se caracterizan por el desarrollo de los microorganismos en forma de gránulos. Los reactores UASB son considerados como el diseño de preferencia para dar tratamiento a los residuales diluidos /19/.
En estos reactores el sustrato es alimentado por el fondo y circula de forma ascendente a través de la cama de lodos donde se encuentran los gránulos (Figura 1B). La formación del lodo granular es una condición necesaria para el logro de una operación satisfactoria, donde la eficiencia del reactor depende en gran medida de la concentración de biomasa activa y de las cargas orgánicas alimentadas al reactor. Cuando estos reactores alcanzan la condición de estado estacionario se puede observar una cama densa de este lodo granular en el fondo. Encima de esta cama de lodo se forma una zona consistente en finas partículas suspendidas, conocidas como el manto de lodos, y seguido de esta se observa una zona clara que constituye la zona de sedimentación.
Los reactores UASB pueden asimilar como promedio cargas orgánicas de 10 kg de DQO por m3 de reactor por día, con tiempos hidráulicos de retención de 24 h /20-25/. En la mayoría de los casos estos reactores remueven aproximadamente el 80% de la DQO alimentada /20-25/, por tal motivo se requiere de una etapa posterior de tratamiento que garantice las normas de vertimiento de DQO /26/. Las velocidades de ascenso garantizan la formación del lodo granular, por lo que se recomiendan valores de entre 0,1 y 1,0 m/h /27/. De esta forma los reactores UASB (operando a temperaturas mesofílicas) pueden producir entre 4 y 5 m 3 de biogás por m3 de reactor al día /25/ /22/ /20/. Para la operación de estos reactores es recomendable el uso de residuales líquidos de bajos contenidos de sólidos suspendidos (= 0,5 g/L) /28/, ya que estos pueden deteriorar los agregados microbianos, formar espuma y ocasionar, la sobrecarga del reactor /29/.
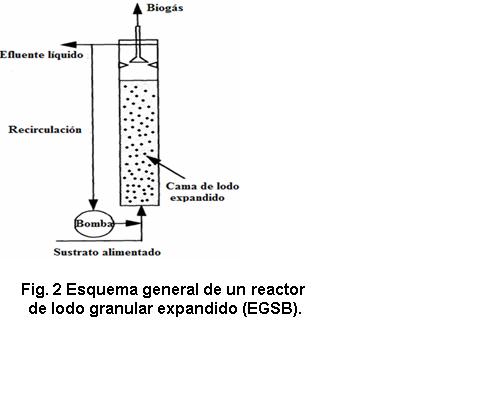
Reactores de lodo granular expandido (EGSB)
Los reactores de lodo granular expandido (EGSB por sus siglas en inglés) (figura 2), son considerados como una evolución de los reactores UASB. La existencia de espacios muertos en los reactores UASB ha sido reportada entre el 7 y el 41 % /30/. Para reducir estos espacios los reactores UASB fueron modificados, recirculando parte del efluente para expandir la cama de lodo /31/. Esta transformación dio origen a los reactores EGSB.
Este tipo de reactor puede alcanzar mayores volúmenes activos y mayores velocidades de ascenso debido al uso de altas relaciones de recirculación (recirculación/alimentación). Esto origina una expansión de la cama del lodo granular, un mejor contacto entre los microorganismos y el sustrato y una reducción de los espacios muertos con respecto a los UASB /31/. Estos reactores tienen como desventaja la baja eficiencia de remoción de sólidos suspendidos lo cual incrementa la necesidad de utilizar etapas de post-tratamiento para el efluente líquido obtenido. Las cargas orgánicas que pueden alcanzar son muy altas ( 40 kg de DQO por m 3 de reactor por día), de igual forma superan a los reactores UASB en las velocidades de ascenso (4 - 10 m/h), las productividades volumétricas (5,0 – 6,5 m 3 biogás/m 3 reactor por día) y las eficiencias de remoción (90 – 98 %), siendo muy bajos los tiempos de retención hidráulica (2 - 7 h) /29, 32, 33/ /34, 35/.
Post-tratamiento de los efluentes
Una vez que los sustratos han sido digeridos se hace necesario un tratamiento adicional a los efluentes del reactor. Existen varias posibilidades para la utilización del digestato líquido o sólido, el más común es su uso como fertilizante. Cuando se utilizan sustratos diluidos (1 – 5 % (w/w), sólidos totales) en la etapa de digestión anaerobia, el digestato es usualmente bombeado para su aplicación a los suelos (fertirriego). Sin embargo en algunas ocasiones es necesario su almacenamiento para su estabilización y mineralización, para lo cual puede ser utilizado un sistema de lagunas /9/.
Cuando se utilizan sustratos sólidos (concentración de sólidos totales entre 20-30 %) en la etapa de digestión anaerobia, el digestato es mecánicamente deshidratado por medio de centrifugas y filtros prensa y luego las fracciones líquidas y sólidas son utilizadas independientemente. El digestato sólido, una vez deshidratado, puede ser utilizado directamente como fertilizante o estabilizado mediante el compostaje. La fracción líquida separada puede ser utilizada en la preparación de los sustratos como agua de dilución aunque se debe prestar mucha atención al posible incremento en concentración de sales y otros compuestos inhibitorios que afectan el proceso de digestión anaerobia. Es por ello que solo un porciento de la fracción líquida es usada en la preparación de los sustratos y el resto es tratado como agua residual /9/.
Purificación del biogás
Existe un gran número de tecnologías que han sido desarrolladas para la purificación del biogás. Cada tipo de tecnología tiene sus ventajas y desventajas y poseen una factibilidad técnica y económica demostrada /36/. La mejor alternativa desde el punto de vista económico va a depender en gran medida de la calidad requerida en el biogás purificado (que está en función de su uso final), de la operación del proceso de digestión anaerobia y del tipo de sustrato empleado /36, 37/. En Alemania, el biogás es utilizado en sistemas combinados de producción de calor y electricidad (CHP, por sus siglas en inglés) después de remover el sulfuro de hidrógeno y el agua presente. Sin embargo, para el uso del biogás como combustible motor o para su inyección a la red los requerimientos de calidad suelen ser muy superiores /37/.
En general, los principales compuestos que pueden requerir su eliminación del biogás en sistemas de purificación son el H 2 S, el NH 3 , el CO 2 y el H 2 O /37/. Algunas recomendaciones sobre el tipo de purificación a emplear en cada caso fueron reportadas por Abatzoglou y Boivin /38/. En primer lugar, la remoción del sulfuro de hidrógeno y el agua es obligatoria para cualquier utilización del biogás. En segundo lugar, la presencia del amoníaco causa un ligero incremento de las emisiones de (NOx) y finalmente, la remoción del dióxido de carbono no es obligatoria (origen es biogénico por lo que no es considerado como un contaminante). Existen un gran número de tecnologías disponibles para la remoción del CO 2 y el H 2 S contenido en el biogás.
Remoción del sulfuro de hidrógeno
El sulfuro de hidrógeno (H 2 S) puede ser removido en el interior del digestor por métodos biológicos utilizando microorganismos de la familia de los Thiobacillus o los Sulfolobus (micro-oxigenación) o dosificando cloruro de hierro al interior del digestor /39-41/. Aunque este método es muy empleado tiene la desventaja de que el azufre elemental formado se puede reconvertir en H 2 S y por esta razón los procesos externos son recomendados /42/. El H 2 S puede ser removido de conjunto con el CO 2 utilizando scrubbers con agua, mientras que otros sistemas como el sistema de absorción por variación de presión (PSA por sus siglas en inglés) utiliza carbón activado para eliminar el H 2 S. El método biológico, que emplea microorganismos de la familia de los Thiobacillus, ha sido comúnmente recomendado como proceso externo, mientras que otros diseños se utilizan para purificar el biogás obtenido cuando se utilizan sustratos de alto contenido de azufre (p. ej.: vinazas); entre ellos la absorción en soluciones de quelatos de hierro y la absorción en soluciones de sulfatos de hierro /43/.
Remoción de H 2 S por oxidación biológica con adición de oxígeno
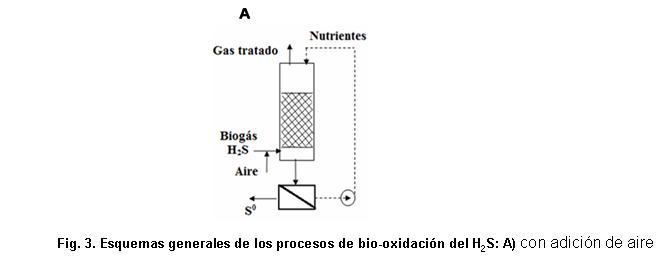
La oxidación biológica con adición de aire puede llevarse a cabo en los llamados biofiltros de goteo que contienen en su interior una columna empacada para la inmovilización de los microorganismos /36/. Estas tecnologías utilizan especies quimiotróficas /38/. Específicamente, Thiobacillus sp. ha sido ampliamente utilizado ya que tienen la habilidad de crecer bajo condiciones extremas (p. ej.: deficiencia de oxígeno y bajos valores de pH) /44/. Estas bacterias quimiotróficas pueden utilizar el dioxígeno como electrón aceptor u otro electrón aceptor (p. ej.: nitratos) en condiciones anaerobias /44/, aunque la mayoría de los reactores utilizan la respiración aerobia /45/. Este proceso consiste en la adición de oxígeno del aire y nutrientes de manera continua o discontinua (figura 3A).
En este proceso, el biogás sin tratar se mezcla con el aire en la entrada del biofiltro, pasa a través de la columna empacada y se pone en contacto con los microorganismos, al mismo tiempo que se alimenta la solución que contiene los nutrientes /36/. Estos microorganismos oxidan el H 2 S con el oxígeno molecular y convierten el compuesto indeseado en agua y azufre elemental (S0), bajo condiciones limitadas de oxígeno /38, 44/. El azufre elemental es separado en un filtro o sedimentador y puede ser empleado como bio-fertilizante. Cuando se alimenta un exceso de oxígeno la reacción produce ácido sulfúrico, lo cual genera la acidificación del medio /38, 44/.
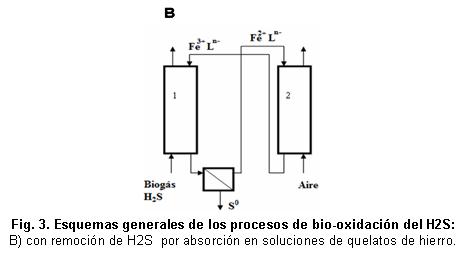
Remoción de H 2 S por absorción en soluciones de quelatos de hierro
La remoción de H 2 S por absorción en soluciones de quelatos de hierro se lleva a cabo en procesos como el Sulferox and Lo-Cat. Estos procesos se basan en la oxidación del H 2 S a azufre elemental por medio de la adición de aire y con la ayuda de un compuesto (quelato de hierro) que sea fácilmente oxidado por el aire atmosférico y fácilmente reducido por el H 2 S /46/. El esquema general de este proceso se muestra en la Figura 3B, donde la solución absorbente contiene el complejo de hierro Fe 3+ L n- (L es el ligando orgánico y n es su carga), el cual oxida al H 2 S a azufre elemental (S0), reduciendo el Fe 3 +L n- a Fe 2 +L n (reactor 1) /47-50/. El complejo de hierro es posteriormente regenerado en el reactor 2 mediante la adición de aire y el azufre elemental es separado en un filtro o sedimentador /47-50/. El proceso puede transcurrir a temperaturas mesofílicas (35 ºC ± 2) y es recomendado cuando las concentraciones de H 2 S en el biogás oscilan entre 20 000 - 30 000 ppmv /43/. En el mismo se hace necesaria la adición de compuestos químicos para evitar la degradación del ligando orgánico, el cual se transforma en ácido iminoacético /3/.
Remoción de H 2 S por absorción en soluciones acuosas de hierro
Este proceso ha sido reconocido como un proceso ventajoso respecto a la absorción en quelatos de hierro, fundamentalmente por no necesitar la adición de compuestos químicos para su operación, por su bajos costos de operación y por la rapidez con que ocurren las reacciones /51, 52/. El esquema general de este proceso es muy similar al anterior (figura 3B). En la primera etapa del proceso (reactor 1) ocurre la absorción física con reacción química del H 2 S en las soluciones acuosas de hierro (comúnmente sulfato de hierro III), seguida por la oxidación bioquímica de los iones ferrosos (reactor 2) que se forman por acción de microorganismos de la familia de los Thiobacillus ferrooxidantes en condiciones aerobias /38, 51-53/. El azufre elemental es separado también en un filtro o sedimentador.
El pH óptimo para la operación del proceso es 2, de esta forma se puede facilitar la ocurrencia de la reacción en el reactor 1, lo cual no afecta a los microorganismos que se encargan de la regeneración del sulfato de hierro III en el reactor 2, ya que los mismos pueden crecer a pH de entre 1 y 6, prefiriendo las condiciones de temperatura mesofílicas /38/.
Remoción del dióxido de carbono
La remoción del CO 2 puede llevarse a cabo por absorción en agua, por absorción en soluciones de aminas y por adsorción por variación de presión (PSA por sus siglas en inglés) /36, 54/.
Absorción en agua
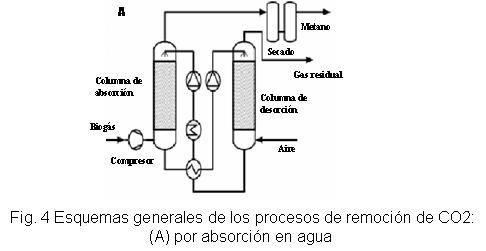
La absorción del CO 2 en agua se favorece a bajas temperaturas y altas presiones. El proceso se lleva a cabo en scrubbers mediante la recirculación de agua a presión, que constituye el líquido lavador, donde queda atrapado el CO 2 . Durante el paso del biogás por el scrubber, el CO 2 se disuelve con mayor facilidad que el CH 4 , debido a su alta solubilidad en el agua /36/. Por tal motivo, el agua de lavado abandona la columna de absorción saturada en dióxido de carbono, siendo transferida a un tanque de flasheo donde se reduce la presión bruscamente y se libera la mayor parte del gas. El agua es entonces enviada a una columna de desorción donde se pone en contacto, en contracorriente, con aire para eliminar el CO 2 remanente. Finalmente, el agua se envía nuevamente a la columna de absorción y así el proceso se repite continuamente (figura 4A) /36/.
Las limitaciones de este método radican en que los componentes del aire, oxígeno y nitrógeno, se disuelven en el agua durante el proceso de desorción, siendo posteriormente transferidos a la corriente de metano limpio. Al mismo tiempo el metano se satura en agua durante el proceso, por lo cual es siempre necesario el secado del gas utilizando scrubbers de etilenglicol /36/.
La aplicación de esta tecnología se recomienda para proyectos de escala piloto e industrial; en los que el metano obtenido pueda ser utilizado sin la necesidad de una etapa posterior de compresión y cuando las cantidades de nitrógeno y oxígeno en la corriente de metano sean tolerables para los requerimientos de la etapa de generación de energía /36/.
Absorción en soluciones de aminas
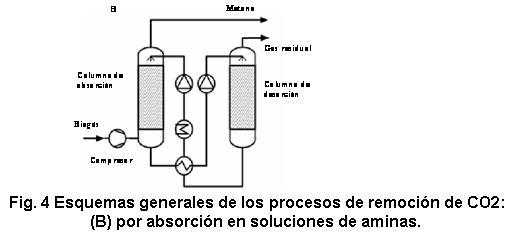
La absorción química se caracteriza por una absorción física del componente gaseoso indeseado en el líquido de lavado, seguida por una reacción química entre ambos componentes que ocurre dentro de la fase líquida. Como resultado, la unión entre ambos componentes se hace mucho más fuerte que en la operación con agua y la capacidad de carga del scrubber es varias veces mayor. La reacción es muy selectiva y la cantidad de metano absorbida en el líquido es muy pequeña lo cual resulta en una alta recuperación de metano durante la operación (figura 4B). La presión de trabajo de este proceso es muy baja (respecto a la de los scrubbers con agua) debido a la gran afinidad del CO 2 a los solventes típicamente empleados (soluciones acuosas de mono-etanolamina, di-etanolamina y metil-di-etanolamina) /36/.
La alta selectividad de las aminas se torna en una dificultad durante la regeneración de la solución de lavado. Típicamente se requieren elevados gastos energéticos en la columna de desorción que son suministrados en forma de calor. En esta columna de desorción, la solución que contiene a las aminas es calentada hasta cerca de los 160 ºC donde la mayor parte del CO 2 es liberado como gas de alta pureza. Una pequeña parte del líquido de lavado se pierde por evaporación en la corriente de metano, por la cual tiene que ser reemplazado frecuentemente /36/.
Adsorción por variación de presión (PSA)
La separación de los gases por adsorción se basa en los diferentes comportamientos de los gases de una mezcla al ser adsorbidos en la superficie de un sólido bajo presiones elevadas. El carbón activado y los tamices moleculares (zeolitas) son usualmente empleados como material adsorbente en este tipo de proceso ya que tienen la capacidad de adsorber el CO 2 del biogás y enriquecer su contenido de metano /36/. Luego de la adsorción a altas presiones el material adsorbente es regenerado mediante la reducción gradual de la presión y la recirculación de biogás o metano. El gas residual (fundamentalmente CO 2 ) es liberado durante este último paso del proceso. Seguidamente, la presión comienza a incrementarse de nuevo mediante la alimentación de biogás o metano al sistema hasta que el adsorbedor esté listo para recomenzar el proceso (figura 5) /36/.
A escala industrial estas plantas utilizan cuatro, seis o nueve adsorbedores en paralelo y en diferentes posiciones dentro de esta secuencia para así lograr una operación continua (figura 5) /36/. Durante la etapa de descompresión la composición del gas residual va cambiando en el tiempo debido a que el metano adsorbido es liberado en ese momento; por lo cual el gas residual es recirculado en ese entonces hacia la corriente de biogás que se alimenta al sistema /36/. Al final de la operación el gas residual puede ser liberado a la atmósfera. Los contenidos de agua y sulfuro de hidrógeno en el biogás deben ser eliminados previos a esta etapa del proceso ya que ambos afectan irreversiblemente la capacidad adsorbente de este material.
En sentido general el método es aplicable cuando se quiere obtener una corriente de metano con 95-99% de pureza, para plantas de escala piloto e industrial y cuando el metano pueda ser utilizado directamente a la presión de salida del sistema /36/.
Generación de electricidad y calor
Motores de combustión interna
Los motores de combustión interna son sistemas combinados de generación de electricidad y calor que pueden ser alimentados utilizando el biogás como combustible. Las características de diferentes tipos de motores ha sido reportada en la literatura /55/. Por ejemplo, las eficiencias eléctricas y térmicas son de 39 y 38 %, respectivamente, para motores con una potencia de 2,8 MW /55, 56/. A estos motores el biogás es comúnmente alimentado con una fracción de metano del 60 % /56/. Durante la operación, el calor recuperado del enfriamiento de los motores, aceites y gases de combustión puede ser empleado para producir agua caliente a 100 ºC /56/. Los gases de la combustión abandonan la chimenea a temperaturas superiores a los 150 ºC para evitar la corrosión de sus componentes /56/. Los requerimientos de sulfuro de hidrógeno en el biogás deben ser inferiores de 250 ppmv para evitar la corrosión del motor /41/.
Turbinas de gas
Este tipo de tecnología también ha sido empleada para la producción combinada de electricidad y calor /56/. En turbinas de 5.6 MW de potencia se reportan eficiencias eléctricas y térmicas de 29 y 44% respectivamente /56/. El biogás con un 60% de metano es también alimentado a las turbinas de gas /56/. Los gases de escape de la combustión alcanzan temperaturas de alrededor de 500 °C y pueden ser recuperados en una caldera para la producción de vapor de alta calidad /55/. Se recomienda que los gases exhaustos abandonen la caldera recuperadora a temperaturas de 150 °C para evitar la corrosión de los componentes del sistema /55, 56/.
Sistemas combinados de calderas y turbinas de vapor
Los sistemas combinados turbina-generador de vapor pueden utilizar diferentes tipos de combustibles, entre ellos el biogás /55/. Las turbinas de vapor de 0,5 MWeléctrico poseen eficiencias térmicas y eléctricas de 7,3 and 84,2 % respectivamente /55/. En estos sistemas se puede alimentar, al generador de vapor, biogás con 60 % de metano al igual que en los motores de combustión interna y en las turbinas de gas /56/. Sin embargo, se ha reportado que ellos pueden admitir mayores concentraciones de sulfuro de hidrógeno en el biogás (= 1000 ppmv). Los gases de escape de la combustión alcanzan temperaturas de alrededor de los 380 °C y pueden ser recuperados en una caldera o economizador para la producción de vapor de alta calidad /55/. Se recomienda también que los gases exhaustos abandonen el economizador a temperaturas de 150 °C para evitar la corrosión de los componentes del sistema /55, 56/.
CONCLUSIONES
Las tecnologías producción de biogás difieren en cuanto a sus costos de inversión, sus parámetros de operación y sus impactos ambientales. Para aplicar estas tecnologías a escala industrial es necesario tener en cuenta las cinco etapas básicas del proceso: el pretratamiento de los sustratos; la digestión anaerobia; el post-tratamiento de los efluentes; la purificación del biogás; y la generación de energía en sistemas combinados de producción de electricidad y calor. Con las alternativas consideradas se podrían tratar residuales de altos (= 15%) y bajos contenidos de sólidos (= 15%) y residuales complejos (altos contenidos de lignina), al mismo tiempo que se podría generar energía como electricidad, calor o combustible motor. Aspectos referentes a sus parámetros de operación y principios de funcionamiento han sido discutidos, siendo aún necesaria la profundización en aspectos económicos y ambientales.
BIBLIOGRAFÍA
1. ALBURQUERQUE J.A, A. ROLDÁN, "Agricultural use of digestate for horticultural crop production and improvement of soil properties", European Journal of Agronomy Vol 43 2012. p. 119-128.
2. KARELLAS, BOUKIS, KONTOPOULOS, "Development of an investment decision tool for biogas production from agricultural waste", Renewable and Sustainable Energy Reviews. Vol 14, p. 2010 1273-1282.
3. BARRERA, "Anaerobic digestion of a very high strength and sulfate-rich vinasse: from experiments to modeling and sustainability assessment", Gent University, 2014.
4. SALOMON, SILVA LORA, ROCHA, ALMAZÁN DEL OLMO, "Cost calculations for biogas from vinasse biodigestion and its energy utilization", Sugar Industry.Vol 136 , 2011,p. 217 - 223.
5. ROCHA, LORA, VENTURINI, ESCOBAR, SANTOS, MOURA, "Use of the life cycle assessment (LCA) for comparison of the environmental performance of four alternatives for the treatment and disposal of bioethanol stillage", International Sugar Journal. Vol.112, 2010,p 611 - 622.
6. BARRERA, ROSA, SPANJERS, ROMERO, MEESTER, DEWULF, "A comparative assessment of anaerobic digestion power plants as alternative to lagoons for vinasse treatment: life cycle assessment and exergy analysis", Journal of Cleaner Production. Vol.113. 2016, p 459-471.
7. SALOMON, SILVA, "Estimate of the electric energy generating potential for different sources of biogas in Brazil", Biomass Bioenergy. Vol. 33, 2009, p. 1101-1107.
8. LÓPEZ-TORRES, "Procedimiento de pretratamiento para mejorar la digestión anaerobia de residuos sólidos". Tesis doctoral. Ciudad de La Habana. Cuba", 2000.
9. ZUPANCIC, GRILC, "Anaerobic Treatment and Biogas Production from Organic Waste", Management of Organic Waste. 2012.
10. WARD, J., HOLLIMAN, JONES, "Optimization of the anaerobic digestion of agricultural resources", Bioresource Technology 2008. 7928-7940.
11. ANGELIDAKI, ELLEGAARD, AHRING, "Application of the anaerobic digestion process", Biomethanation II Berlín: Springer. 2003.
12. BRAUN, WEILAND, A., "Biogas from Energy Crop Digestion. IEA Bioenergy. Task 37 - Energy from Biogas and Landfill Gas.", Disponible en: http://www.biogasmax.eu/media/iea_1_biogas_energy_crop__007962900_1434_30032010.pdf/ 2010.
13. LI, STEPHEN, Z., "Solid-state anaerobic digestión for methane production from organic waste", Renewable and Sustainable Energy Reviews. 2011, p. 821-826.
14. HEIERMANN, BUDDE, SUÁREZ, "Anaerobic digestion fundamentals and implementation in Germany. Ponencia presentada en la 1ra Conferencia Científica Internacional de la UNISS, Yayabociencia 2011. Sancti Spíritus, Cuba", 2011.
15. CONTRERAS, Digestión anaerobia de residuos de la agroindustria arrocera cubana para la producción de biogás. Informe inédito. Ingeniería Química, UCLV, 2014.
16. KAPARAJU, "Bioethanol, biohydrogen and biogas production from wheat straw in a biorefinery concept", Bioresource technology. Vol.100, 2009. p. 2562-2568.
17. CHÁVEZ-VAZQUEZ, BAGLEY, "Evaluation of the performance of different anaerobic digestion technology for solid waste treatment", Disponible en: http://agrienvarchive.ca/bioenergy/download/an_dig_u_toronto_2000.pdf/ 2010.
18. LINKE, MÄHNERT, "Biogasgewinnung aus Rindergülle und nachwachsenden Rohstoffen", Agrartechnische Forschung.Vol 5. 2005. p. 125-132.
19. FRANKIN, "Full-scale experiences with anaerobic treatment of industrial wastewater", Wat. Sci. Tech. 44 2001 1-6.
20. KAPARAJU, SERRANO, ANGELIDAKI, "Optimization of biogas production from wheat straw stillage in UASB reactor", Applied Energy.Vol. 87. 2010, p. 3779-3783.
21. SOUZA, FUZARO, POLEGATO, "Thermophilic anaerobic-digestion of vinasse in pilot-plant UASB reactor", Wat. Sci. Tech. Vol.25. 1992, 213-222.
22. RAMOS, OBAYA, VALDÉS, VILLA, ENG, "Granulation of digested sewage-sludge in mesophilic uasb reactors treating distillery waste-waters from sugar-cane molasses", Acta Biotechnologica. Vol. 14. 1994, p. 283-292.
23. INCE, KOLUKIRIK, OZ, INCE, "Comparative evaluation of full-scale UASB reactors treating alcohol distillery wastewaters in terms of performance and methanogenic activity", Journal of Chemical Technology and Biotechnology. Vol. 80, 2005, p. 138–144
24. CHINNARAJ, VENKOBA RAO, "Implementation of an UASB anaerobic digester at bagasse-based pulp and paper industry", Biomass Bioenergy 30 2006 273-277.
25. MOLETTA, "Winery and distillery wastewater treatment by anaerobic digestion", Wat. Sci. Tech. 51 2005 137-144.
26. DIAMANTIS, AIVASIDIS, "Two-stage UASB design enables activated-sludge free treatment of easily biodegradable wastewater", Bioprocess. Biosyst. Eng. 33 2010 287-292.
27. SARAVANAN, SREEKRISHNAN, "Modelling anaerobic biofilm reactors--A review", J Environ Manag 81 2006 1-18.
28. OBAYA, VALDÉS, PÉREZ, CARMOUSE, BONACHEA, LLANES, ROJAS, "Tratamiento combinado de las vinazas de destilería y residuales azucareros en reactores UASB", Tecnología del agua 249/Junio 2004 78-85.
29. SEGHEZZO, ZEEMAN, VAN LIER, HAMELERS, LETTINGA, "A review: The anaerobic treatment of sewage in UASB and EGSB reactors", Bioresour Technol 65 1998 175-190.
30. PEÑA, MARA, AVELLA, "Dispersion and treatment performance analysis of an UASB reactor under different hydraulic loading rates", Water Res 40 2006 445-452.
31. BHATTACHARYYA, SINGH, "Understanding the Mixing Pattern in an Anaerobic Expanded Granular Sludge Bed Reactor: Effect of Liquid Recirculation", J Environ Eng 136 2010 576-584.
32. ZOUTBERG, DEBEEN, "The Biobed(R) EGSB (expanded granular sludge bed) system covers shortcomings of the upflow anaerobic sludge blanket reactor in the chemical industry", Wat. Sci. Tech. 35 1997 183-188.
33. NICOLELLA, VAN LOOSDRECHT, HEIJNEN, "Wastewater treatment with particulate biofilm reactors", Journal of Biotechnology 80 2000 1-33.
34. ZOUTBERG, FRANKIN, "Anaerobic treatment of chemical and brewery waste water with a new type of anaerobic reactor; The Biobed(R) EGSB reactor", Wat. Sci. Tech. 34 1996 375-381.
35. VANDERLA ST, LETTINGA, "Anaerobic treatment of domestic sewage under moderate climatic conditions using upflow reactors at increased superficial velocities", Wat. Sci. Tech. 25 1992 167-178.
36. RD-TPES, "Biogas to biomethane technology review. Vienna University of Technology (Austria), Institute of Chemical Engineering. Research Divison Thermal Process Engineering and Simulation", 2012.
37. WEILAND, "Biomass Digestion in Agriculture: A Successful Pathway for the Energy Production andWaste Treatment in Germany", Eng. Life Sci. 6 2006 302 - 309.
38. ABATZOGLOU, BOIVIN, "A review of biogas purification processes", Biofuels Bioproducts and Biorefining 3 2009 42-71.
39. SCHNEIDER, "Grundlegende Untersuchungen zur effektiven, kostengünstigen Entfernung von Schwefelwasserstoff aus Biogas – Biogasanlagen: Anforderungen zur Luftreinhaltung, Bayerisches Landesamt für Umweltschutz, Augsburg", 2002 25–41.
40. VAN DER ZEE, VILLAVERDE, GARCÍA, FDZ.-POLANCO, "Sulfide removal by moderate oxygenation of anaerobic sludge environments", Bioresource Technology 98 2007 518-524.
41. WEILAND, "Biogas production: current state and perspectives", Applied Microbiology and Biotechnology.Vol 85. 2010, p 849-860.
42. NAEGELE, LINDNER, MERKLE, LEMMER, JUNGBLUTH, BOGENRIEDER, "Effects of temperature, pH and O2 on the removal of hydrogen sulfide from biogas by external biological desulfurization in a full scale fixed-bed trickling bioreactor (FBTB)", Int J Agric & Biol. Vol 6. 2013, p. 69 - 81.
43. BARRERA, SPANJERS, DEWULF, ROMERO, ROSA, "The sulfur chain in biogas production from sulfate-rich liquid substrates: a review on dynamic modeling with vinasse as model substrate", Journal of Chemical Technology and Biotechnology.Vol. 88 2013 1405–1420.
44. SYED, SOREANU, FALLETTA, BÉLAND, "Removal of hydrogen sulfide from gas streams using biological processes - A review", Canadian Biosystems Engineering 48 2006 2.1-2.14.
45. DEVINNY, RAMESH, "A phenomenological review of biofilter models", Chemical Engineering Journal 113 2005 187-196.
46. LENS, HULSHOFF POL, Environmental Technologies to treat sulfur pollution, IWA Publishing, London, 2000.
47. WUBS, BEENACKERS, "Kinetics of H2S absorption into aqueous ferric solutions of EDTA and HEDTA", American Institute of Chemical Engineers Journal 40 1994 433-444.
48. WUBS, BEENACKERS, "Kinetics of the oxidation of ferrous chelates of EDTA and HEDTA in aqueous-solution", Industrial and Engineering Chemistry Research 32 1993 2580-2594.
49. DEMMINK, BEENACKERS, "Gas Desulfurization with Ferric Chelates of EDTA and HEDTA: New Model for the Oxidative Absorption of Hydrogen Sulfide", Industrial and Engineering Chemistry Research 37 1998 1444-1453.
50. DEMMINK, BEENACKERS, "Oxidation of ferrous nitrilotriacetic acid with oxygen: A model for oxygen mass transfer parallel to reaction kinetics", Industrial and Engineering Chemistry Reserach 36 1997 1989-2005.
51. PAGELLA, DE FAVERI, "H2S gas treatment by iron bioprocess", Chemical Engineering Science 55 2000 2185-2194.
52. MESA, ANDRADES, MACÍAS, CANTERO, "Biological oxidation of ferrous iron: study of bioreactor efficiency", Journal of Chemical Technology and Biotechnology 79 2004 163-170.
53. EBRAHIMI, KLEEREBEZEM, VAN LOOSDRECHT, HEIJNEN, "Kinetics of the reactive absorption of hydrogen sulfide into aqueous ferric sulfate solutions", Chemical Engineering Science 58 2003 417-427.
54. WELLINGER, LINBERG, Biogas Upgrading and Utilization - IEA Bioenergy Task 24. International Energy Association, Paris, France, Available at: http://wellowgate.co.uk/biogas/Scrubbing.pdf 2000, pp. [Accessed on 25th June, 2014].
55. U.S-EPA., Catalag of CHP technologies. Combined Heat and Power Partnership, Available at: http://www.epa.gov/chp/documents/catalog_chptech_full.pdf , 2008, pp. [Accessed on 14th May, 2014].
56. WISER, SCHETTLER, WILLIS, Evaluation of Combined Heat and Power Technologies for Wastewater Facilities, Available at: http://www.cwwga.org/documentlibrary/121_EvaluationCHPTechnologiespreliminary%5B1%5D.pdf 2010, pp. [Accessed on 25th June, 2014].
Recibido: Septiembre 2017
Aprobado: Diciembre 2017
Dr. C. Ernesto L. Barrera-Cardoso, ernestol@uniss.edu.cu; Centro de Estudio de Energía y Procesos Industriales (CEEPI). Dirección de Investigaciones Aplicadas. Universidad de Sancti-Spíritus José Martí Pérez