Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Tecnología Química
versión On-line ISSN 2224-6185
RTQ vol.38 no.3 Santiago de Cuba set.-dic. 2018
ARTICULO ORIGINAL
Balances de masa y calores de reacción para evaluar la extracción de vanadio a partir de catalizadores agotados en el proceso de obtención de ácido sulfúrico
Mass balances and reaction heats to evaluate the vanadium extraction from spent catalysts of sulfuric acid production process
Dr. Lorenzo Perdomo-González 1 , DrC. Rafael Quintana-Puchol 2 , Dr. Manuel Rodríguez-Pérez 1 , Dr. Amado Cruz-Crespo 1 , Dr. Carlos R. Gómez-Pérez 1 ,
1 Centro de Investigaciones de Soldadura, UCLV, 2 Departamento Licenciatura Química, UCLV lperdomo@uclv.edu.cu
Resumen
Para la obtención de ácido sulfúrico por el método de contacto se utilizan catalizadores con más de 4 % de vanadio, los cuales salen de servicio una vez agotados, siendo necesario su almacenamiento. Por otro lado, la cascarilla de laminación se genera durante el proceso de laminación en caliente, constituyendo aproximadamente el 2 % del acero producido. La combinación adecuada de estos dos residuos industriales puede ser aprovechada para la extracción del vanadio de los catalizadores mediante aluminotermia. Los resultados del procesamiento de estos residuales industriales pueden ser evaluados mediante la realización de balances de masa y la determinación de los calores de reacción de la reacciones redox que ocurren. Esta comprobación constituye el principal objetivo del presente trabajo. Como resultado se obtiene que pueden procesarse mezclas de cascarilla de laminación - catalizador en proporciones desde 1 / 0,25 hasta 1 / 1,5, obteniéndose aleaciones con contenidos de vanadio entre 0,6 y 2,69 % y de silicio de 8,9 a 23,12 %. De la determinación de los calores de reacción de las mezclas se obtuvo que para todas las mezclas evaluadas la cantidad de calor generada por unidad de masa supera la barrera de 550 cal/g.
Palabras clave : aluminotermia, cascarilla de laminación, catalizador de vanadio agotado, balance de masa, calor de reacción
Abstract
Obtaining sulfuric acid by the contact method requires the use of catalysts with more than 4 % vanadium, which leave service once spent, requiring storage. On the other hand, the mill scale is generated during the hot rolling process, constituting approximately 2 % of the processed steel. The appropriate combination of these two industrial wastes can be exploited for the extraction of vanadium from the catalysts by the aluminothermic method. The results of the processing of these wastes can be evaluated by means of mass balances and the determination of the heats of the redox reactions involved. This analysis is the main objective of this work. As a result it is obtained that the mixtures of mill scale - catalyst can be processed in proportions from 1 / 0.25 to 1 / 1.5, obtaining alloys with vanadium and silicon contents between 0.6 and 2.69 % and silicon 8.9 and 23.12%, respectively. By means of determination of the reaction heats of the mixtures it was obtained that the amount of heat generated per mass unit exceeds the 550 cal / g barrier, for all the evaluated mixtures.
Key words : aluminothermy , mill scale, spent vanadium catalyst, mass balance, reaction heat
INTRODUCCION
Para la producción de ácido sulfúrico por el método de contacto se utilizan catalizadores de pentóxido de vanadio [1 - 3], los que una vez agotados se convierten en residuos industriales constituyendo un problema medioambiental [3 - 5].
En Cuba, el Ministerio de Ciencia, Tecnología y Medio Ambiente ha establecido regulaciones sobre el manejo de estos residuos, obligando a las empresas a tomar medidas en este sentido, tal es el caso de la resolución No. 87/99 [6]. Esta resolución en su artículo 5 del capítulo 4 ( DEL MANEJO DE DESECHOS PELIGROSOS) señala: Las entidades generadoras de desechos peligrosos procurarán su recuperación y reciclaje, ya sea por sus propios medios o a través de las entidades especializadas correspondientes. Por otro lado, en su artículo 10 plantea que el CITMA en coordinación con las unidades exigirá y controlará la realización de acciones encaminadas a garantizar que los generadores de desechos peligrosos u otros desechos, adopten cuantas medidas resulten pertinentes para garantizar procesos de producción limpia que reduzcan la generación de residuos, procurando al máximo el reciclaje y otras acciones para la disposición final adecuada de los desechos peligrosos y otros desechos.
De aquí que una alternativa para reducir estos problemas ambientales y evitar el almacenamiento indefinido de los catalizadores agotados puede ser la extracción de los elementos metálicos, para su posterior utilización.
El vanadio presente en los catalizadores agotados de la producción de ácido sulfúrico puede ser recuperado, lo cual en muchas ocasiones es realizado por el mismo fabricante del catalizador [2]. Cuando estos productos salen del proceso, como residuos industriales, contienen más de un 4 % de vanadio [4, 5, 7].
Existen varios reportes relacionados con la recuperación del vanadio y otros metales presentes en catalizadores agotados, utilizándose para ello tanto métodos hidro-metalúrgicos como piro-metalúrgicos [4, 5, 7, 8].
La producción de metales y aleaciones, mediante aluminotermia ha sido ampliamente estudiada, utilizándose fundamentalmente para la obtención de aleaciones de muy bajo contenido de carbono, tal es el caso de la producción de ferrocromo extra bajo en carbono [9, 10].
La elección de esta tecnología se fundamenta, sobre todo, en la simplicidad de la técnica y el bajo costo de inversión requerido . La reacción de los óxidos con el aluminio, puede ser representada por la ecuación general siguiente [9]:
2/y M x O y + 4/3 Al = 2x/y M + 2/3 Al 2 O 3 , donde MxOy representa el óxido, libre o combinado, reducible en el mineral o concentrado.
Una limitante para el uso de la reacción aluminotérmica, en la obtención de metales a partir de minerales, está relacionada con la ley del mineral, siendo necesario en muchos casos el uso de óxidos de alto grado de pureza o la adición de sales ricas en oxígeno para garantizar el desarrollo de las reacciones de oxidación-reducción de manera autosostenida [11, 12].
La cascarilla de laminación es una mezcla de óxidos de hierro II y III, con pequeñas cantidades de hierro metálico y otras impurezas que se producen durante el proceso de laminación en caliente del acero, generándose alrededor del 2 % del acero producido [13, 14, 15].
Una alternativa para el uso de la tecnología aluminotérmica utilizando minerales o residuales de baja pureza, es su combinación con otros de alta pureza, de forma tal que se logre conformar una carga capaz de generar la energía mínima necesaria para el inicio, autosostenibilidad del proceso y la adecuada separación metal – escoria [16, 17].
Mezclas de cascarilla de laminación con catalizadores agotados de la producción de ácido sulfúrico, utilizando aluminio como reductor, pueden ser procesadas mediante aluminotermia si se logran las proporciones requeridas en las mezclas, recuperándose el vanadio contenido en el catalizador en forma de aleación de FeSiV [17]. De aquí que, la evaluación de la extracción del vanadio presente en los catalizadores agotados de la producción de ácido sulfúrico, a partir de la realización de balances de masa y la determinación del calor de reacción de las reacciones redox a desarrollarse de manera autosostenida, constituye el objetivo del presente trabajo.
MATERIALES Y MÉTODOS
Materias primas . Preparación
Las materias primas usadas para la confección de las mezclas pirometalúrgicas son: cascarilla de laminación, viruta de aluminio y catalizador agotado, cuya composición química se muestra en la tabla 1. La cascarilla de laminación se genera en la empresa Acinox-Tunas de Las Tunas, l as virutas de aluminio proceden de las operaciones de maquinado en la Industria Nacional Productora de Utensilios Domésticos (INPUD), de Santa Clara y el catalizador agotado de la producción de ácido sulfúrico en la Empresa Pedro Soto Alba de Moa [17].
Los materiales, en las proporciones requeridas, son mixturados en un mezclador rotatorio durante aproximadamente 30 minutos. Las mezclas son calentadas en una estufa a una temperatura entre 270 ºC y 300 ºC , durante 40 min aproximadamente, con el objetivo de eliminar la humedad presente y facilitar su procesamiento pirometalúrgico.
El procesamiento de las cargas se realiza en un crisol de grafito de 2,2 L de capacidad, de fondo cónico con un orificio en el fondo para facilitar la extracción de los productos, iniciándose la reacción mediante un chispazo con arco eléctrico. La figura 1 muestra la secuencia de trabajo [17].
Balances de masa
Se prepararon 7 mezclas (cargas), una formada por cascarilla y aluminio, tomada como patrón de referencia (0) y las 6 restantes conformadas por cascarilla, aluminio y catalizador, según se muestra en la tabla 2 [17].
Tabla 2. Cargas de las mezclas pirometalúrgicas a procesar mediante aluminotermia
| Componente
| Carga 0 | Carga 1 | Carga 2 | Carga 3 | Carga 4 | Carga 5 | Carga 6 |
| Cascarilla (g) | 100 | 100 | 100 | 100 | 100 | 100 | 100 |
| Catalizador (g) | 0 | 25 | 50 | 75 | 100 | 125 | 150 |
La cantidad de aluminio se adicionó de acuerdo a la estequiometria de las reacciones químicas fundamentales que ocurren durante el proceso.
Los balances de masa se realizan a partir de la aplicación del principio de Conservación de la Masa [18], según muestra la ecuación general:
Acumulación = Entrada – Salida + Generación – Consumo (I)
Para realizar los balances de masa se consideró que todo el hierro presente en la cascarilla de laminación está en forma de Fe 2 O 3 y que el 100 % del óxido de hierro y de la sílice se reducen durante el procesamiento. En la distribución de productos, se asume que el 10 % del azufre pasa al metal, el 30 % a la escoria y el 60 % a los gases, tomando como referencia la distribución de este elemento para la obtención de ferrocromo alto carbono [11] y que el cinc se volatiliza re-oxidándose en la fase vapor [19]. El balance de masa para cada una de las cargas pirometalúrgicas evaluadas se muestra en la tabla 3.
Determinación de los calores de reacción
Los calores de reacción (?H reacción ) se determinan para cada una de las reacciones químicas tomadas en consideración (ver tabla 4) utilizando la expresión II y los datos de la tabla 5. Los resultados de su determinación para cada una de las reacciones se muestran en la tabla 6.
? H reacción = S n ?F prod - S n ?F reacc (II)
Tabla 4. Reacciones químicas fundamentales del procesamiento aluminotérmico de catalizadores agotados
| No de reacción | Reacción |
| 1 | Fe 2 O 3 + 2Al ? 2Fe + Al 2 O 3 (III) |
| 2 | 3V 2 O 5 + 10Al ? 6V + 5Al 2 O 3 (IV) |
| 3 | 3SiO 2 + 4Al ? 3Si + 2Al 2 O 3 (V) |
| 4 | 3MnO + 2Al ? 3Mn + Al 2 O 3 (VI) |
| 5 | Fe 2 O 3 + 3Mg ? 2Fe + 3MgO (VII) |
Tabla 5. Calores de formación de los óxidos a 298 ºC en kcal/mol [20]
| Óxido | Fe 2 O 3 | V 2 O 5 | SiO 2 | MnO | Al 2 O 3 | MgO |
| ?Hf 298 | -198.5 | -373 | -203.35 | -92,04 | -399.09 | -143,84 |
La cantidad total de calor generado (Q total ) por unidad de masa (g) de cada una de las mezclas se determina de la relación entre la cantidad total de calor generada por las reacciones químicas ( Q i ) que se encuentran involucradas en la mezcla y la masa total de carga a procesar (M total ). Los datos para cada una de las reacciones son tomados del balance de masa mostrado en la tabla 3.
Tabla 6. Calores de reacción ( Q total ) para cada una de las cargas pirometalúrgicas
| Reacción | Carga 0 | Carga 1 | Carga 2 | Carga 3 | Carga 4 | Carga 5 | Carga 6 | ||
| 1 | -125062,9 | -125424,5 | -125784,6 | -126147,1 | -126509,6 | -126870,5 | -127231,3 | ||
| 2 | 0 | -2247,3 | -4494,6 | -6741,9 | -8989,2 | -11236,5 | -13483,8 | ||
| 3 | 0 | -11387,1 | -22774,2 |
| -45548,4 | -56935,5 | -68322,5 | ||
| 4 | 0 | -21,6 | -43,3 | -64,9 | -86,6 | -108,2 | -129,9 | ||
| 5 | -355,4 | -434,0 | -514,6 | -592,3 | -669,9 | -749,5 | -829,2 | ||
| S (cal/mol) | -125418,2 | -139514,5 | -153611,2 | -167707,5 | -181803,7 | -195900,2 | -209996,8 | ||
| Q total (cal/g) | -918,1 | -822,1 | -756,7 | -710,6 | -675,9 | -648,2 | -626,1 |
RESULTADOS Y DISCUSIÓN
La cascarilla de laminación se genera de forma inevitable durante el proceso de laminación en caliente del acero, constituyendo una fuente potencial de óxido de hierro, la cual tiene usos limitados en la industria cubana [21], a pesar de que en el país existen dos grandes empresa metalúrgicas que generan continuamente este residual (Antillana de Acero y Acinox-Tunas).
Los elevados contenidos de hierro, en sus diferentes fases del sistema Fe-O, presentes en la cascarilla de laminación [16, 22, 23], convierten a este residual en una fuente permanente de materia prima con las características adecuadas como comburente para la obtención de aleaciones de hierro mediante procedimiento aluminotérmico.
Por otro lado, de acuerdo con la composición química reportada, el catalizador de vanadio (envenenado) está constituido en un 61,99 % por los óxidos de silicio, aluminio, hierro, magnesio, calcio, sodio, potasio, vanadio y manganeso, siendo los óxidos de silicio, hierro, vanadio y manganeso potencialmente factibles de reducir, mediante procesamiento pirometalúrgico. Además contiene azufre, responsable principal de su envenenamiento, y agua adsorbida y absorbida. La composición química de este residual (ver Tabla 1) permite determinar que del 61,99 % de estos hipotéticos óxidos el 50,7 % pueden ser reducidos a metal, lo cual representa el 81,8 % del total de los óxidos reportados [17].
A partir de la composición química de la cascarilla de laminación y del catalizador agotado pueden prepararse mezclas, en diferentes proporciones, de estos dos residuos industriales para su procesamiento mediante aluminotermia, donde la proporción de uno respecto al otro en la mezcla dependerá fundamentalmente de la cantidad de calor por unidad de masa que sea capaz de generar la misma.
En la tabla 7 se resumen los resultados del procesamiento aluminotérmico de todas las cargas, en cuanto a cantidad de metal y escoria para cada colada, reportándose los datos teóricos determinados a partir del balance de masa y los reales obtenidos del procesamiento pirometalúrgico. Este comportamiento puede ser observado en la figura. 2.
Tabla 7 . Resultados de los balances de masa y del procesamiento metalúrgico para cada una de las cargas
| Carga | Producto | Masa teórica (g) | Masa real generada (g) | Promedio (g) | Rendimiento* (%) | |
| Colada 1 | Colada 2 | |||||
| 0 | metal | 72,6 | 66 | - | 66 | 90,9 |
| escoria | 63,8 | 39 | - | 39 | 61,1 | |
| 1 | metal | 79,7 | 56,7 | 68,8 | 62,8 | 78,8 |
| escoria | 81,2 | 81,75 | 78,5 | 80,1 | 98,6 | |
| 2 | metal | 87,0 | 75 | 71,9 | 73,45 | 84,4 |
| escoria | 98,6 | 102,5 | 104,5 | 103,5 | 105,0 | |
| 3 | metal | 94,0 | 69,5 | 74,4 | 71,9 | 76,5 |
| escoria | 116,0 | 120,4 | 127,9 | 124,5 | 107,3 | |
| 4 | metal | 100,9 | 75,3 | 80,5 | 77,9 | 77,2 |
| escoria | 133,4 | 146,3 | 145,4 | 145,8 | 109,3 | |
| 5 | metal | 108,1 | 73,5 | 77,5 | 75,5 | 69,8 |
| escoria | 150,9 | 171,3 | 165 | 168,1 | 111,4 | |
| 6 | metal | 115,3 | - | 85,75 | 85,75 | 74,4 |
| escoria | 168,3 | - | 187,5 | 187,5 | 111,4 | |
* El rendimiento se determina a partir de la relación entre la masa real obtenida y la teórica obtenida del balance de masa.
En la figura 2 se aprecia que la cantidad de producto (teórica y real) para cada una de las cargas mantiene la misma tendencia, observándose que la cantidad real de metal se mantiene por debajo de la cantidad teórica prevista en los balances de masa, no siendo de la misma manera en el caso de las escorias donde a medida en que aumenta la cantidad de catalizador en la mezcla aumenta la cantidad de escoria real con relación a la teórica.
En la tabla 7 puede observarse que el rendimiento metálico para la carga 0 es del 91 %, apreciándose que este tiende a disminuir cuando se introduce el catalizador en la mezcla, variando entre el 70 y 84 %, aunque no se observa una tendencia regular de este indicador. En el caso de la escoria, el rendimiento para la carga 0, fue del 61 %, apreciándose que para el resto de las mezclas, este parámetro va aumentando a medida en que aumenta el contenido de catalizador en la mezcla, alcanzando un 111 % para la mezcla 6. Estos valores de rendimientos por encima de 100 % con relación al teórico se deben a que no se logra el grado de reducción de los óxidos metálicos asumido en los balances de masa, por tanto, el rendimiento metálico es inferior al previsto y el de escoria superior. Este comportamiento es lógico ya que en los procesos metalúrgicos no se logra el 100 % de recuperación de los elementos metálicos.
Por otro lado, el balance permitió determinar la composición química teórica de todos los productos generados durante el proceso (metal, escoria y gases).
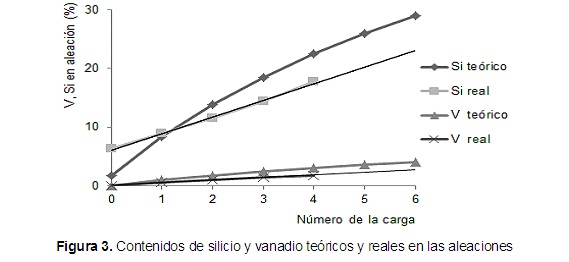
En la tabla 8 se muestra la composición química teórica de la aleación y en la tabla 9 la real, no reportándose la composición de las aleaciones 5 y 6 debido a que la alta fragilidad de las aleaciones impidió la preparación de las muestras para el análisis químico mediante espectroscopia de emisión atómica. En la figura 3 se muestran los contenidos de silicio y vanadio real y teórico para cada una de las cargas.
Tabla 8. Composición química teórica de las aleaciones (en % masa)
| Composición | Carga | ||||||
| 0 | 1 | 2 | 3 | 4 | 5 | 6 | |
| Si | 1,76 | 8,34 | 13,82 | 18,51 | 22,55 | 26,02 | 29,06 |
| Fe | 96,62 | 88,40 | 81,34 | 75,60 | 70,66 | 66,23 | 62,36 |
| Mn | 0,15 | 0,20 | 0,25 | 0,29 | 0,32 | 0,35 | 0,37 |
| Cu | 1,26 | 1,40 | 1,52 | 1,62 | 1,71 | 1,79 | 1,85 |
| V | 0,00 | 0,98 | 1,80 | 2,51 | 3,11 | 3,63 | 4,08 |
| S | 0,00 | 0,29 | 0,53 | 0,74 | 0,92 | 1,07 | 1,21 |
| Al | 0,21 | 0,38 | 0,73 | 0,73 | 0,74 | 0,91 | 1,06 |
Tabla 9. Composición química real de las aleaciones analizadas (en % masa)
| Composición | Carga | ||||
| 0 | 1 | 2 | 3 | 4 | |
| V | 0,01 | 0,60 | 0,98 | 1,43 | 1,76 |
| Si | 6,33 | 8,90 | 11,5 | 14,5 | 17,7 |
| Al | 1,44 | 0,32 | 1,19 | 2,11 | 4,15 |
| C | 0,13 | 0,49 | 0,62 | 0,63 | 0,78 |
| Cr | 0,16 | 0,24 | 0,26 | 0,31 | 0,32 |
| Mo | 0,06 | 0,41 | 0,50 | 0,53 | 0,61 |
| Mn | 0,57 | 0,53 | 0,44 | 0,47 | 0,46 |
| P | 0,02 | 0,04 | 0,04 | 0,05 | 0,05 |
| S | 0,04 | 0,16 | 0,07 | 0,07 | 0,21 |
| Cu | 1,15 | 2,04 | 2,22 | 2,38 | 2,35 |
| Ni | 0,44 | 0,44 | 0,10 | 0,10 | 0,08 |
| Ti | 0,04 | 0,04 | 0,04 | 0,04 | 0,04 |
| Nb | 0,00 | 0,02 | 0,02 | 0,02 | 0,02 |
| W | 0,04 | 0,10 | 0,11 | 0,10 | 0,11 |
| S Total | 10,43 | 14,33 | 18,09 | 22,74 | 28,64 |
En la tabla 9 se puede observar que la carga patrón está formada por un 10,43 % de elementos de aleación, incrementándose la presencia de estos elementos en las aleaciones obtenidas en la medida en que aumenta la presencia de catalizador en la carga desde 14,33 hasta 28,64 %, apreciándose un incremento en la cantidad de vanadio recuperada.
Al comparar la composición química teórica (tabla 8) con la composición real (tabla 9), se puede observar que existe correspondencia entre los resultados previstos a partir de los balances de masa y los reales obtenidos.
El contenido de vanadio en las aleaciones obtenidas va aumentando desde 0,6 % para la carga 1 hasta un 1,76 % para la carga 4, observándose que la diferencia entre la cantidad prevista y la obtenida va a ir aumentando desde 0,38 hasta 1,35 %. En el caso del silicio se observa un comportamiento bastante similar al del vanadio, obteniéndose diferencias entre los contenidos previstos y reales desde 0,56 % hasta 4,85 % (ver figura 3).
El comportamiento de los contenidos de vanadio y silicio real en las aleaciones analizadas permite determinar las ecuaciones que describen las curvas mostradas en la figura 3 para cada uno de los elementos señalados.
V real = 0,433x + 0,09, R² = 0,9903 (VIII)
Si real =2,834x + 6,118, R² = 0,9975 (IX)
Como se observa , ambos modelos, tienen un ajuste superior al 99 %, por lo que pueden ser usados para estimar los contenidos de V y Si en las aleaciones 5 y 6, las que no fue posible analizar químicamente, obteniéndose los resultados mostrados en la tabla 10.
Tabla 10. Composición másica de vanadio y silicio estimado en las aleaciones 5 y 6 (en % masa)
| Carga | V | Si |
| 5 | 2,26 | 20,23 |
| 6 | 2,69 | 23,12 |
Este análisis permite predecir que las aleaciones de FeSiV obtenidas de las mezclas 5 y 6 deben contener 2,26 y 2,69 % de vanadio respectivamente, manteniéndose estos valores por debajo de los contenidos previstos en los balances de masa, lo que coincide con los resultados anteriores.
El contenido de aluminio en las aleaciones obtenidas fue superior al valor previsto en los balances de masa, aumentando la diferencia en la medida en que se incrementa la cantidad de catalizador, lo cual evidencia que el aluminio no fue capaz de reducir todos los óxidos reducibles que componen las mezclas, quedando presente en la aleación.
En azufre en las diferentes aleaciones fue variable, obteniéndose valores de 0,07 % para las mezclas 2 y 3, 0,16 % para la mezcla 1 y 0,21 para la 4, lo cual evidencia que no hay un comportamiento estable en este sentido, en todos los casos el valor fue superior al de la mezcla patrón (0). Este comportamiento pudiera estar relacionado con el tiempo de precalentamiento de la mezcla en el horno, la temperatura de inicio de la reacción y por el tiempo de interacción entre la carga caliente y el medio exterior, todo lo cual puede favorecer la eliminación del azufre presente en el catalizador. Debe destacarse que para todas las cargas el contenido de azufre fue inferior al previsto en los balances de masa, lo cual favorece la calidad de las aleaciones para el desarrollo de consumibles de soldadura y evidencia la posibilidad de eliminar la mayor parte de este perjudicial elemento en operaciones previas al procesamiento aluminotérmico.
Todas las aleaciones obtenidas pueden ser utilizadas en la elaboración de cargas de aleación de consumibles de soldadura, debiéndose destacar que en el caso de las aleaciones 5 y 6 donde la alta fragilidad impidió su caracterización se favorece de manera considerable su trituración, abaratando la preparación del consumible ya que en estas aplicaciones las ferroaleaciones se utilizan en forma de polvos (de 0,1 y 0,15 mm) [24, 25].
En cuanto a los resultados de la determinación de los calores de reacción, en la tabla 6 se puede observar que en todos los casos la cantidad de calor generada se encuentra por encima de 550 cal/g lo que favorece el proceso y permite que la reacción se auto sostenga, según criterios preestablecidos en la literatura [12]. No obstante a esto, se plantea que las escorias generadas en estos procesos son muy viscosas, por lo que se recomienda incrementar la cantidad de calor hasta valores entre 620 – 680 cal/g [12] , razón por la cual se decidió no continuar incrementando la cantidad de catalizador en la mezcla, de forma tal que se lograra mantener la adecuada separación entre el metal y la escoria.
De manera general se observó que al disminuir la cantidad de calor generada por unidad de masa, tiende a disminuir la cantidad de metal y a aumentar la de escoria producida, lo cual puede estar relacionado con una disminución de la eficiencia de las reacciones de oxidación-reducción, siendo posible observar esta tendencia en las tablas 6 y 7.
Esta disminución de la cantidad de calor por unidad de masa también puede provocar que quede metal atrapado en la escoria, debido al aumento de su viscosidad en la medida en que disminuye la temperatura, favoreciendo la pérdida de metal y afectando la calidad de las escorias.
Por tanto, al obtenerse para la mezcla 6 una cantidad de calor por unidad de masa de 626,1 cal/g, queda establecida la cantidad máxima de catalizador a incorporar a la mezcla (1 parte de cascarilla por cada 1,5 partes de catalizador), proporción que permitió el desarrollo de las reacciones redox de manera autosostenida y la adecuada separación metal escoria .
Las aleaciones obtenidas han sido evaluadas en el desarrollo de electrodos tubulares revestidos con resultados satisfactorios [26].
Conclusiones
1. Los balances de masa realizados a partir de la composición química de cada uno de los componentes de las cargas, permiten hacer una valoración previa de los resultados del procesamiento pirometalúrgico de las mezclas, cascarilla de laminación/catalizador, obteniéndose que los rendimientos reales de metal tienden a disminuir con relación al valor teórico en la medida en que aumenta la proporción de catalizador en la mezcla y los de escoria tienden a aumentar.
2. El alto contenido de hierro, en forma de óxidos de hierro, presente en la cascarilla de laminación permitió formular mezclas con los catalizadores agotados de la fabricación de ácido sulfúrico para su procesamiento aluminotérmico en función de recuperar los elementos metálicos contenidos en ambos residuales, donde la relación máxima cascarilla catalizador quedó limitada a la proporción 1/1,5 debido a que la cantidad de calor por unidad de masa que genera la carga conformada es de 626 cal/g .
3. El procesamiento pirometalúrgico de las mezclas, cascarilla de laminación con catalizador agotado, en las relaciones desde 1/0,25 hasta 1/1,5, adicionándole aluminio en relaciones estequimétricas, permitió obtener aleaciones de hierro con contenidos de elementos de aleación desde 14,33 hasta 28,64 %, donde se destacan los contenidos de vanadio entre 0,6 y 2,69 % y de silicio de 8,9 y 23,12 %, todas utilizables en la fabricación de cargas de aleación de consumibles de soldadura.
4. La estrategia de combinar los resultados potenciales de los balances de masa y los calores de reacción para cada una de las cargas, permitió evaluar la factibilidad de realización del proceso, donde las diferencias entre los resultados reales y los teóricos fueron aumentando a medida que aumentó la proporción de catalizador en la mezcla, debido a que disminuye la cantidad de calor generada por unidad de masa disminuyendo la eficiencia del proceso.
BIBLIOGRAFÍA
1. PERNETT, Leda, et al. Modelamiento y simulación de un reactor catalítico para la oxidación de SO 2 a SO 3 , utilizando V 2 O 5 como catalizador. Prospect. 2016, vol 14, núm. 1, Enero - Junio, p. 39-46.
2. Serie Guías Técnicas de aplicación de BREF´s en la Comunidad Autónoma del País Vasco. Fabricación de Ácido Sulfúrico. IHOBE – Sociedad Pública de Gestión Ambiental. Nº 1 – Octubre 2006. Depósito legal: BI-xxx-06. https://dokupdf.com/downloadFile/5a01ff3cd64ab2b9bd8a8086
3. MOUSA, Khalid, et al. Study on Vanadium Recovery from Spent Catalyst Used in the Manufacture of Sulfuric Acid. Iraqi Journal of Chemical and Petroleum Engineering. 2010, vol 11, núm. 2, p. 49-54.
4. GARCÍA, Diego, et al. Leaching of vanadium from sulphuric acid manufacture spent catalysts. Rev. Metalurgia. 2001, vol 37, núm. 1, p. 18-23.
5. CALDERÓN, Hugo, et al. Recovery of Vanadium from Acid and Basic Leach Solutions of Spent Vanadium Pentoxide Catalysts. Journal of Geological Resource and Engineering. 2015, 4, p. 213-218.
6. CUBA. Resolución No. 87/99, 21 octubre de 1999. Ministerio de Ciencia Tecnología y Medio Ambiente. 1999. http://www.sld.cu/galerias/pdf/sitios/insat/r-87-1999-citma.pdf
7. MORALES, Félix. Obtención de carga aleante para consumibles de soldadura utilizando residual catalítico y cromita cubana. Tesis Doctoral, Facultad de Metalurgia, ISMM de Moa. Cuba. 2005.
https://repoedum.ismm.edu.cu/files/original/d3e4ab7a1813645932fdefa5ef0c35b4.pdf
8. MIYAUCHI, Akihiko, et al. Production of Metallic Vanadium by Preform Reduction Process . Materials Transactions. 2010, vol 51, núm. 6, p. 1102 - 1108 .
9. EISSA, M.M., et al. The aluminothermic production of extra low carbon ferrochromium from low grade chromite ore. INFACON XII. The Twelfth International Ferroalloys Congress. Sustainable Future. Helsinki, Finland, 2010, p 431-438. ISBN 978-952-92-7341-6 (electronic)
10. WENZEL, B., et Al. Aluminothermic reduction of Cr 2 O 3 contained in the ash of thermally treated leather waste. Brazilian Journal of Chemical Engineering. 2013, vol 30, núm. 01, p. 141 – 154.
11. ARANGURENT, F., Mallol, A. Siderurgia. Madrid, Ed. Dorssat S.A., 1963, 612 p.
12. RISS, A., Khodorovsky, Y. Production of ferroalloys. Moscow, Ed. Foreign languages publishing house. 1975, 278 p.
13. DEVES, Bruno. et al. Study on reducing and melting behavior of mill scale/petroleum coke blend. Tecnol. Metal. Mater. Miner. 2013, vol 10, núm. 4, p. 365-374 .
14. GABALLAH, N.M. et al. Production of iron from mill scale industrial waste via hydrogen. Open Journal of Ino rganic Non-Metallic Materials. 2013, núm. 3, p. 23-28.
15. COVCEVICH, Mauricio. et al. Characterization and Reduction Behavior of Mill Scale. ISIJ International. 2011, vol. 51, no. 7, p. 1072–1079.
16. PERDOMO-GONZÁLEZ, Lorenzo, et al. Obtención simultánea de ferromanganeso y materiales abrasivos por reducción aluminotérmica usando pirolusita sin tostación previa y residuos sólidos industriales. Minería y Geología. 2015, vol 31, núm. 2, p. 95-112.
17. PERDOMO-GONZÁLEZ, Lorenzo, et al. Recuperación del vanadio de los residuos catalíticos de la producción de ácido sulfúrico mediante aluminotermia. Centro Azúcar, 2016, Vol. 43, Núm. 2, p. 43-56.
18. CASTELLANOS, Jesús, et al. Balances de masa y energía métodos clásicos y técnicas no convencionales. Editorial Samuel Feijoo, 2001, Santa Clara, Cuba, 167 p. ISBN: 959-250-014-2.
19. DVORÁK, Petr, et at. Zinc Recovery from Flue Dust. Journal of the Polish Mineral Engineering Society. Inzynieria Mineralna, Styczen, Czerwiec, 2017, January – June, p. 195-199.
20. PERRY, R. H & Green, D.W. Perry?s Chemical Engineers Handbook. Seventh edition. Mc Graw Hill. USA. 1999, p. 2-187 a 2-195. IS BN 0-07-049841-5.
21. FERNÁNDEZ, Lourdes, et al. Reciclaje y reutilización de desechos en la industria cubana. II Convención Internacional de las Industrias, CUBAINDUSTRIAS 2016, Palacio de las Convenciones de La Habana. Cuba. 2016. ISSN 1607-6281.
22. EL-HUSSINY, N. et al. Recycling of Mill Scale in Sintering Process. Science of Sintering. Central Metallurgical Research and Development Institute (CMRDI). 2011, vol. 43, p. 21-31.
23. SEOK-HEUM, Baek, et al. Optimization of process parameters for recycling of mill scale using Taguchi experimenal design. Journa l of Mechanical Science and Technology. 2010, vol 24, núm. 10, p. 2127-2134.
24. FERNÁNDEZ, Alfonso, et al. Caracterización de depósitos obtenidos con electrodos tubulares revestidos para el recargue de medios de labranza sometidos a desgaste abrasivo en el sector azucarero. Centro azúcar. 2014, vol. 41 núm . 2, abril-junio, p. 1-11.
25. CRUZ-CRESPO, Amado, et al. Efecto sobre la dilución de la granulometría de la ferroaleación en el alma de electrodos tubulares revestidos bajo la influencia de la composición del revestimiento. Soldag. insp. 2011, vol 16, núm. 1, Jan/Mar, p. 079-085.
26. ARAÑÓ, José. Estudio de la estructura y la resistencia al desgaste abrasivo del metal depositado con electrodos tubulares base; Fe-Si-V-C, Fe-Cr-Mn-C, y Fe-Cr-MnV-C. Tesis de Maestría. Facultad de Ingeniería Mecánica e Industrial. Universidad Central Marta Abreu de Las Villas, Cuba, 2016.
Recibido: Marzo 2018
Aprobado:Julio 2018
Dr. Lorenzo Perdomo-González. Centro de Investigaciones de Soldadura, UCLV