INTRODUCCIÓN
El equino es una especie poliéstrica estacional, fototrópica positiva; así, en países de cuatro estaciones la época reproductiva se manifiesta a fines de primavera y durante el verano (Cintora, 2005). Sin embargo, en latitudes cercanas al plano ecuatorial hay poca variación estacional en cuanto a horas luz, llegando la yegua a ser considerada como una especie poliéstrica anual; por lo que, se pueden aparear en cualquier época del año (Ramírez et al., 2010). Por lo tanto, el control del ciclo estral y la ovulación en la yegua es un aspecto del manejo reproductivo que debe investigarse más a profundidad (dos Reis et al., 2020).
Los agentes farmacológicos que se usan actualmente para controlar el ciclo estral en la yegua son los mismos que se utilizan en el bovino, estos protocolos algunas veces son aplicados de idéntica manera, sin considerar las diferencias existentes entre las especies. Así, desde la década de 1970 para el control individual del ciclo estral de la yegua se utilizan agentes luteolíticos (prostaglandinas PG) por su simpleza en la administración (Rosa et al., 2022). Sin embargo, a diferencia de la hembra bovina, la yegua presenta una fase lúteal corta y generalmente con una sola onda folicular; de allí que los programas basados en el acortamiento del ciclo con prostaglandinas suelen tener un alto índice de fracasos, esto vinculado principal al tamaño del folículo ovulatorio al momento de la aplicación de la dosis luteolítica de PG (Andrade et al., 2011).
Además, el uso cada vez más frecuente de la inseminación artificial en esta especie hace necesario recurrir al control farmacológico grupal del ciclo sexual. En este contexto, se han venido probando varios protocolos que incluyen la administración de progesterona o progestágenos sintéticos por varias vías de aplicación como la oral, intramuscular (Oliveira et al., 2018), subcutánea (Handler et al., 2007), esponjas y dispositivos intravaginales impregnados de progesterona (Macan et al., 2021).
La estrategia del uso de progestágenos consiste en alargar artificialmente la fase lútea por un lapso superior a la duración de un cuerpo lúteo normal. El bloqueo del eje hipotálamo-hipofisiario ejercido por el progestágeno exógeno inhibe la liberación de hormona luteinizante (LH) durante el tratamiento e impide la manifestación del comportamiento estral. Con la terminación brusca del tratamiento se produce un efecto similar a la luteólisis, por lo que la mayoría de las hembras entran en celo generalmente en el tercer día post retiro del implante (Polasek et al., 2017). Sin embargo, el tratamiento solo con progestágenos no inhibe la liberación de hormona folículo estimulante (Bollwein et al., 2004) desde la adenohipófisis, razón por la cual continúa el desarrollo folicular.
Por tal motivo, se viene investigando la utilización de altas concentraciones iniciales de progesterona, combinados con estrógeno (dos Reis et al., 2020), lo cual es absorbido a través de la mucosa vaginal, provocando efectos inhibitorios sobre la liberación de LH y FSH, respectivamente, cuyo efecto práctico es provocar la atresia del folículo dominante y la aparición de una nueva onda folicular que va a permitir contar con un folículo preovulatorio viable (Segabinazzi et al., 2021).
Por lo antes expuesto, en el presente trabajo se propuso evaluar el efecto del Benzoato de estradiol combinado con un implante intravaginal de progesterona sobre la sincronización del celo y la ovulación en yeguas criadas en el trópico alto en el plano ecuatorial.
MATERIALES Y MÉTODOS
Animales y granja
Se utilizaron en el experimento 24 yeguas criollas dedicadas a la actividad física de turismo, edad entre 4-8 años, condición corporal entre 3-3,5 en escala de 1-5 (Henneke et al., 1983). pertenecientes a dos haciendas de la provincia del Pichincha, ubicadas sobre los 2900 msnm, temperatura entre 10-20 ºC.
Previo al experimento los animales fueron examinados mediante ecografía transrectal y determinados como cíclicos. La alimentación de las yeguas se basó en pastura, balanceado comercial y sales minerales. Durante la realización del estudio se tuvo presente la normativa del código sanitario para animales terrestres, capítulo 7,8 “Utilización de animales en la investigación y educación”, de la Organización Mundial de Sanidad Animal (OIE, 2016).
Diseño experimental
Las yeguas fueron distribuidas aleatoriamente en dos tratamientos: T1 (n=12) este grupo recibió 10 mg Benzoato de estradiol (Grafoleón®; Life, Quito, Ecuador), aplicado vía intramuscular (IM) y T2 (n=12) 25 mg de Benzoato de estradiol. En los dos tratamientos adicionalmente se colocó un dispositivo intravaginal de liberación de progesterona (Sincrogest®; 1 g de progesterona; Ourofino, Quito, Ecuador) y una dosis (125mcg) de Cloprostenol sódico (Estrumate, MDS, quito, Ecuador) el día 0 del protocolo.
La valoración del folículo dominante (FD) luego de la aplicación de los tratamientos, se realizó mediante ecografía transrectal (Aloka, Prosoun 2, Japón) con una sonda lineal de 7,5 MHz cada 48h (08:00), hasta que se observó un nuevo grupo de folículos de 9 mm (Fase de reclutamiento). El tamaño del FD (mm) se determinó mediante la fórmula ancho por largo/2. Además, a partir del día 0 del protocolo cada 48 horas se colectaron 10 ML de sangre de la vena coccígea (08:00) en tubos sin anticoagulante. Las muestras fueron centrifugaron a 3000 gravedades durante 20 min y el suero sobrenadante fue congelado a -20 °C hasta la valoración del estradiol (Steranti Research, UK). La determinación hormonal fue realizada mediante radioinmunoensayo. El rango de la curva estándar para el estradiol varió entre 5 a 400 pg/ML, sensibilidad de 5,2 pg/ML, coeficiente de variación intra-ensayo de 8,1%.
El día que se observó un nuevo grupo de folículos de 9 mm se consideró como día del inicio de la nueva onda folicular.
El implante de progesterona fue retirado cuando el folículo preovulatorio (FPO) de la nueva onda folicular llegó a medir 35 mm. Luego se procedió a realizar ecografía transrectal cada 12 horas, con la finalidad de observar el momento que el FPO desapareció, considerando este el momento de la ovulación.
Estadística
Se utilizó el programa SPSS versión 25®. Se comprobó la normalidad de los datos con la prueba de Shapiro-Wilk. El efecto de los tratamientos sobre las variables comportamiento del FD (tamaño), niveles de estradiol y el momento del reinicio de la onda folicular, las cuales se distribuyeron normalmente, fueron analizados mediante la prueba de T Student. En segunda instancia se organizaron subgrupos de animales en base al día de reinicio de la onda folicular en el tratamiento 1 (T1_4d y T1_6d) y tratamiento 2 (T2_4d y T2_10d) y se analizó su influencia sobre las variables comportamiento del FD, tamaño del FPO, día del retiro del implante y día de la ovulación; mediante análisis de varianza simple y para la comparación de medias se utilizó la prueba de Tukey al 5%.
RESULTADOS Y DISCUSIÓN
El tamaño medio del FD a día 0 en T1 fue de 26,1 ± 2,73 mm, valor similar al encontrado en T2 (24,3 ± 3,54 mm; P>0,05). Los valores medios del tamaño del FD en ambos tratamientos fueron similares hasta el día 4 (Fig. 1; panel A), y a partir de este día, el tamaño del FD fue decreciendo en T1; sin embargo, en T2 el FD incremento su tamaño hasta el día 8, y luego inició el proceso de atresia. Estas particularidades generaron que el reinicio de la onda folicular se produjera en momentos diferentes entre tratamientos; así, para T1 el reinicio de la onda folicular en promedio se produjo en el día 5, siendo menor a T2 (P<0,05), el cual reinició al día 8 (Panel B; Fig. 1).
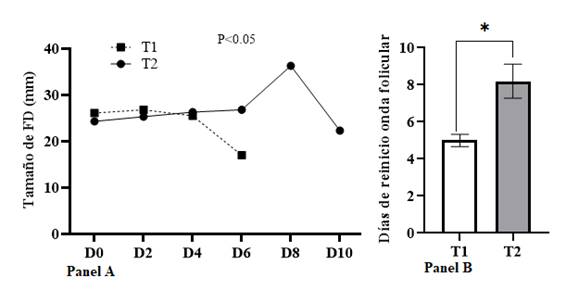
Fig. 1 Comportamiento del folículo dominante (FD) en los tratamientos T1=10 mg de BE y T2=25 mg de BE en forma general (Panel A). Valores medios del día del reinicio de la onda folicular en los tratamientos 1 y 2 (Panel B).
Los resultados obtenidos en el presente trabajo corroboran la evidencia científica existente, sobre el uso de la progesterona asociada a estrógenos como inhibidor del desarrollo folicular, esto por acción supresora en la secreción de FSH; lo cual produce reinicio de una nueva onda folicular en yeguas (Andrade et al., 2011). Sin embargo, la progesterona por sí sola no tiene efecto inhibitorio en la secreción de FSH, por lo tanto, es necesario combinar con estrógenos para producir dicho efecto (Segabinazzi et al., 2021). Esta combinación permitió en el presente estudio la aparición de un nuevo grupo de folículos de 9mm, momento en el cual se consideró como día del reinicio de la nueva onda folicular como lo describen Andrade et al. (2011).
Al valorar la concentración de estradiol (E2) en el día 0 previo a la aplicación del tratamiento se observaron niveles similares en T1 (54,5 ± 7,80 pg/ML) y T2 (68,8 ± 6,21 pg/ML; P>0,05); sin embargo, al día 2 post-tratamiento los niveles de T2 fueron más altos (113,2 ± 6,93 pg/ML) que los de T1 (78,5 ± 11,50 pg/ML), con diferencia entre grupos (P<0,05), igual que en el día 4 (Fig. 2).

Fig. 2 Niveles de estradiol en los tratamientos T1=10 mg de BE y T2=25 mg de BE, luego de la aplicación de los tratamientos. Prueba de T de Studen.
Se considera que la mayor concentración de estradiol en el segundo tratamiento en los días 2 y 4 del experimento está relacionado con la dosis de BE aplicado el día 0 del protocolo (25 mg) en T2. Esto basado en la farmacodinamia del producto que describe que luego de la aplicación vía intramuscular del BE este aumenta y mantiene niveles comparables con yeguas cíclicas (Silva et al., 2017).
Valores medios del reinicio de la onda folicular, tamaño del folículo dominante y niveles de estrógenos en los subgrupos de los tratamientos 1 y 2
Al analizar la sincronía del reinicio de la nueva onda folicular al aplicar BE y progesterona en los dos tratamientos; en T 1 (n=10), la aparición de un nuevo pool de folículos de 9 mm se produjo en el 50% de yeguas (n=5) a los cuatro y dos días después (día 6) en los cinco animales restantes (50%) del grupo. Estos resultados nos permiten determinar una ventana de 48 horas entre los dos grupos (T1_4d y T1_6d) de animales del tratamiento 1. En el tratamiento 2 el reinicio de la onda folicular se evidenció al cuarto dia en tres yeguas (30%; T2_4d) y las siete yeguas restantes en el día 10 (70%; T2_10d). lo que demuestra que la aplicación de 10 mg de BE proporciona mayor homogeneidad en el reinicio de la onda folicular en comparación con el tratamiento que recibió 25 mg de BE (Fig. 3).

Fig. 3 Número de animales que reiniciaron la onda folicular en los días 4 (T1_4d) y 6 (T1_6d) en el tratamiento 1 y en los días 4 (T2_4d) y 10 (T2_10d) en el tratamiento 2, luego de la aplicación del protocolo.
El reinicio de la nueva onda folicular, estuvo íntimamente relacionado con el tamaño del FD al inicio del protocolo. Así cuando, el animal presentó un FD menor a 25 mm y recibió 10 mg de BE (T1_4d; 21,8 ± 3,18 mm), la atresia del FD se produjo a los cuatro días posterior a la aplicación del protocolo. Sin embargo, cuando el FD alcanzó un tamaño >30 mm (T1_6d; 30,4 ± 3,74 mm) a pesar de que recibió 10 mg de BE la atresia se produjo 48 horas más tarde (día 6) en relación al subgrupo T1_4d.
Esta particularidad está relacionada al hecho de que el crecimiento del FD después del proceso de selección (en yeguas 22 mm) es menos dependiente de la FSH, cuya concentración se mantiene en niveles basales, debido a la producción de estrógenos e inhibina que genera una retroalimentación negativa en la hipófisis; la cual permite mantener concentraciones mínimas basales de FSH esenciales para la supervivencia del FD (Andrade et al., 2011).
Las yeguas que recibieron 25 mg de BE (T2), de igual manera presentaron dos subgrupos T2_4d (24,0 ± 9,74 mm) y T2_10d (24,4 ± 3,65 mm) con tamaños similares del FD; sin embargo, el tiempo trascurrido posterior a la aplicación del BE para atresia del FD fue diferente con una ventana de tiempo de 144 horas (6 días); por lo tanto, se considera que las yeguas del subgrupo T2_4d respondieron al protocolo de sincronización y las del subgrupo T2_10d no respondieron y el reinicio de onda se produjo luego de la atresia fisiológica del FD (Fig. 4).
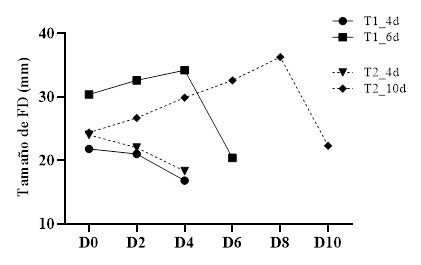
Fig. 4 Comportamiento del folículo dominante (FD), en los animales que reiniciaron la onda folicular en los días 4 (T1_4d) y 6 (T1_6d) en el tratamiento 1 y en los días 4 (T2_4d) y 10 (T2_10d) en el tratamiento 2, luego de la aplicación del protocolo.
Comportamiento del folículo preovulatorio
El comportamiento del folículo preovulatorio (FPO) se valoró de acuerdo al día de reinicio de la onda folicular. En los animales que se reinició la onda folicular a los cuatro días (T1_4d y T2_4d), el FPO alcanzó un tamaño igual o mayor a 35 mm a los nueve días posteriores al reinicio de onda folicular. Sin embargo, en los grupos en los que el reinicio fue a los seis y 10 días posteriores a la aplicación del BE (T1_6d y T2_10d), el FD requirió más tiempo para alcanzar el tamaño de 35 mm (13 días) en promedio (Fig. 5).
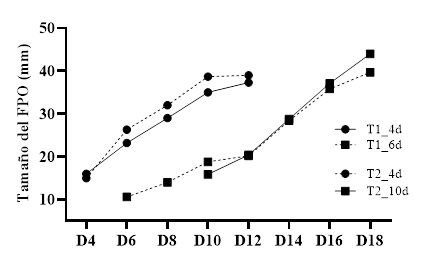
Fig. 5 Comportamiento del folículo preovulatorio (FPO), en los animales que reiniciaron la onda folicular en los días 4 (T1_4d) y 6 (T1_6d) en el tratamiento 1 y en los días 4 (T2_4d) y 10 (T2_10d) en el tratamiento 2.
Día de retiro del implante de liberación de progesterona
El retiro del implante de progesterona se realizó una vez que el FPO alcanzó los 35 mm de tamaño (Larocca et al., 2006). En el tratamiento 1 (T1_4d) a los 11,2 ± 0,49 días y 16,4 ± 0,98 (T1_6d) días. En el tratamiento 2 (T2_4d) se realizó a los 10,0 ± 1,15 días y 15,7 ± 0,52 (T2_10d) días (Fig. 6). Estos resultados evidenciaron que el día de retiro del implante de los animales de T1_4d fue similar al de T2_4d (P>0,05); sin embargo, ambos difieren de los tratamientos T1_6d y T2_10d (P<0,05)., los cuales a su vez no difieren entre sí (P>0,05).
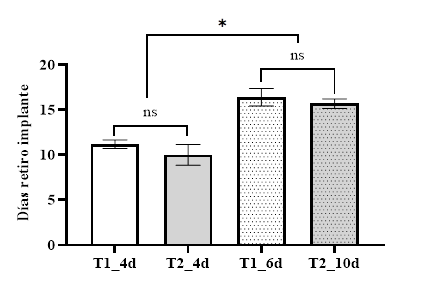
Fig. 6 Día del retiro del implante de liberación de progesterona, en los animales que reiniciaron la onda folicular en los días 4 (T1_4d) y 6 (T1_6d) en el tratamiento 1 y en los días 4 (T2_4d) y 10 (T2_10d) en el tratamiento 2.
Los días necesarios para el retiro del implante luego del reinicio de la onda folicular observados, son mayores a lo descrito por Larocca et al. (2006), quienes organizaron a las yeguas en dos grupos; en el primer colocaron un dispositivo intravaginal con 1,38 g de progesterona y aplicaron 25 mg de BE IM, y el segundo grupo recibió un implante con 1,0 g de progesterona y 25 mg IM de BE, se necesitaron seis y siete días respectivamente para que el FPO alcancara los 35 mm. Esta diferencia puede estar relacionada con la cantidad de progesterona que administraron Larocca et al. (2006).
Días y horas de ovulación
Es un suceso que ocurre a las 24-48 horas antes de finalizar el celo (dos Reis et al., 2020), este suceso se produce tras el aumento de LH, lo cual desencadena una serie de eventos que comprometen la integridad del tejido ovárico, siendo la interacción de péptidos vasoactivos, prostaglandinas y esteroides los principales actores en la cascada de la ovulación. (Andrade et al., 2011).
El día de ovulación en T1_4d fue a los 13,2 ± 0,49 días y a los 19,2 ± 0,48 días (T1_6d) y en T2_4d fue a los 12,6 ± 0,67 días y a los 19,1 ± 0,40 días (T2_10d) (Fig. 7: Panel A). En cuanto a las horas de ovulación fue a los 50,4 ± 2,40 horas (T1_4d) y a los 57,6 ± 0,98 horas (T1_6d); para T2_4d fue a los 52,0 ± 0,0 horas y a los 63,4 ± 2,21 horas (T2_10d) (Fig. 7: Panel B). En animales de T1 que reiniciaron la onda folicular a los cuatro y seis días, asi como, para aquellos de T2 que reiniciaron su onda folicular a los cuatro días, no hubo diferencia estadística. Sin embargo, al comparar estos tres grupos con T2_10 d se observó diferencia en las horas de ovulación (P<0,05).

Fig. 7 Día de ovulación de los animales que reiniciaron la onda folicular en los días 4 (T1_4d) y 6 (T1_6d) en el tratamiento 1 y en los días 4 (T2_4d) y 10 (T2_10d) en el tratamiento 2 (Panel A). Horas promedio de ovulación de los animales que reiniciaron la onda folicular en los días 4 (T1_4d) y 6 (T1_6d) en el tratamiento 1 y en los días 4 (T2_4d) y 10 (T2_10d) en el tratamiento 2 (Panel B).
El tiempo de ovulación en nuestro estudio ocurrió 2,4 días después de retirar el implante de progesterona en yeguas tratadas con 10 mg de BE, a diferencia del tratamiento a base de 25 mg de BE donde el valor medio de ovulación fue de tres días posterior al retiro del implante de progesterona (P>0,05). Nuestros resultados están por debajo de los 6-8 días reportados por Larocca et al. (2006) y a los observados por Macan et al. (2021), quienes determinaron que la ovulación ocurre a los 6,5 días después de retirado el dispositivo intravaginal en yeguas.
CONCLUSIONES
La combinación de un implante de progesterona con una dosis de 10 mg de Benzoato de estradiol mejoró la sincronización del celo y la ovulación en yeguas. Sin embargo, con dosis de BE más alta (25 mg) la eficiencia de la sincronización del celo disminuye, a pesar de que sigue existiendo ovulación














