Introducción
La necesidad de rediseñar los modelos ecosistémicos existentes, de manera que estos permitan entender las consecuencias de las actividades humanas en el marco de la complejidad que realmente caracteriza a los ecosistemas, es un tema al que recientemente se le ha prestado mucha atención. En este sentido, es la diversidad de interacciones lo primero que se pierde en respuesta al cambio global, mucho antes de que empiecen siquiera a detectarse cambios en la biodiversidad (Ochoa, 2017).
Los bosques nublados de montaña del trópico son considerados ecosistemas muy frágiles, porque juegan un papel hidrológico y ecológico Armenteras et al., (2015) y la Organización de las Naciones Unidas para la Agricultura y la Alimentación (FAO, 2016), señalan que la conversión de bosque nativo a espacios agrícolas se establece como el factor de mayor impacto sobre la mayoría de los ecosistemas terrestres, porque disminuye la superficie de hábitats naturales, constituyéndose en una amenaza para la biodiversidad. Así mismo, la remoción de la cobertura vegetal natural y el aprovechamiento desmedido de los recursos naturales han intensificado los procesos de desertificación de los suelos.
La agricultura de montaña ha logrado subsistir manteniendo prácticas ancestrales que corresponden a enfoques agroecológicos, lo que ha permitido generar una agricultura sustentable, debido a la baja dependencia de insumos externos y a la mitigación de los efectos ocasionados por la Revolución Verde en el medio ambiente, circunstancias que tienen efectos en la conservación de los suelos, el agua y la biodiversidad (Acuña y Marchant, 2016). Las técnicas agroecológicas aseguran un uso sostenible de los recursos naturales, el cuidado del ambiente y las personas, permiten que se pueda garantizar la alimentación de cada familia a largo plazo. Una de las prácticas enmarcadas dentro de este contexto es el empleo de una gran diversidad de microorganismos, dentro de los cuales están hongos y bacterias, mezclados en diferentes sustratos orgánicos para ser utilizados en la agricultura y en la ganadería (Peña et al., 2019).
Entre los microrganismos se destacan las micorrizas, que son asociaciones mutualistas entre los hongos del suelo y raíces de las plantas. En esta simbiosis, el hongo cubre sus demandas de carbono e incrementa la absorción de agua y minerales en la planta, tomando principalmente elementos de lenta difusión tales como fósforo, zinc y cobre (Bonilla y Alarcón, 2015; Medina-García, 2016; Pérez et al., 2019), favoreciendo su crecimiento y contribuyendo a la estructuración de las comunidades vegetales, la sostenibilidad, la funcionalidad y mantenimiento de ecosistemas naturales, incluyendo los degradados, siendo útiles para la naturaleza y el hombre (Garzón, 2016; Bañuelos et al., 2017; Lattuada et al., 2019).
El bosque de Huamantanga, ubicado en Jaén, Perú, es muy diverso por su tipo de vegetación, flora y fauna, y como todos los bosques, también está expuesto a la tala y cambio de uso de suelo. Dentro de las especies emblemáticas y de mayor importancia para los pobladores, por su potencial maderable, está Retrophyllum rospigliossi Pilger, conocida comúnmente como "romerillo macho"; sin embargo, su regeneración natural es escasa debido a que un alto porcentaje de semillas es atacado por insectos (coleópteros), incidiendo en una baja existencia de árboles semilleros; por otro lado, existe una alteración de su hábitat natural debido a la extracción de madera de las zonas altas de Jaén y a pesar de haberse realizado una propagación vegetativa, los resultados son mínimos, de igual manera se observa en un tipo de reproducción sexual.
La problemática antes mencionada, unido a la inexistencia de un protocolo de manejo forestal, hace que no se pueda usar R. rospigliossi Pilger en un programa de reforestación, a pesar de su alto valor económico. De ahí la importancia de conocer las características de la asociación micorrízica de esta especie vegetal en su hábitat, pues son precisamente: la presencia de hongos micorriza arbuscular (HMA) y el nivel de micorrización, dos de las variables que se tienen en cuenta para el desarrollo de técnicas culturales en programas de reforestación. Esta investigación se plantea como objetivo: Caracterizar la colonización de micorrizas en Retrophyllum rospigliossi Pilger en las categorías de Brinzal, Latizal y Fustal.
Materiales y métodos
Trabajo de campo. Georreferenciación
Los lugares de muestreo se localizaron mediante imágenes satelitales, con el empleo de un drone y el software Agisoft PhotoScan, en las áreas donde se ubicaron las tres categorías de desarrollo (Brinzal, Latizal y Fustal) de los rodales de R. rospigliosii.
Se estudiaron muestras de suelo que extraídas a una profundidad de 10 a 20 cm de la rizósfera de R. rospigliosii en las categorías Brinzal (ejemplares de hasta un metro de altura), Latizal (de 8 a 20 m de atura y de 10 a 30 cm de diámetro) y Fustal (supera los 20 m de altura y entre 30 y 50 cm de diámetro). Las parcelas muestreadas se identificaron por el nombre de los caseríos más cercanos: Sport Piura (San José del Alto), Nuevo Jerusalén, Guayaquil, San Luis del Nuevo Retiro I y San Luis del Nuevo Retiro II, del distrito de Jaén, región Cajamarca, Perú (Figura 1).
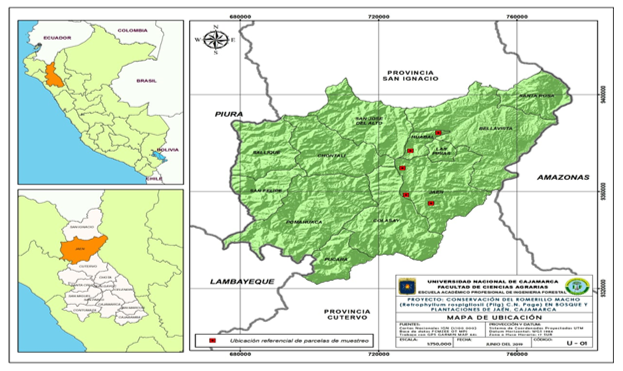 Fuente: Universidad Nacional de Cajamarca.
Fuente: Universidad Nacional de Cajamarca.Fig. 1. - Ubicación de localidades con mayor ocurrencia de las tres categorías de R. rospigliosii Pilger en la provincia de Jaén
Por cada lugar y categoría se tomaron tres muestras de suelo de un kg cada una, garantizando la presencia de raicillas con una longitud mínima de 1cm. Las muestras fueron procesadas antes de las 24 horas de colectadas, en caso contrario, se mantuvieron en refrigeración a 10 °C.
Trabajo de labaratorio
Tinción de raíces
La tinción de raíces se realizó de acuerdo a la metodología propuesta por Philips y Hayman (1970) de la siguiente manera: se tomaron las raíces más finas (menores a 1 mm de diámetro), para facilitar la penetración de los reactivos. Las raíces se colocaron en placas pequeñas de vidrio para que puedan extenderse y no queden apretadas, luego se adicionó KOH al 10 % durante 30 minutos para ablandar el tejido. Seguidamente se sometió a "baño de María" (90 °C) durante 10 minutos. Las raíces fueron lavadas utilizando un tamiz adecuado para evitar pérdidas durante el enjuague. Posteriormente las muestras fueron cubiertas con una solución fresca de KOH al 10 % y H2O2 al 10 % combinado en proporción de 1:1 (V/V), por un tiempo de 15 minutos y finalmente las raíces fueron lavadas con agua corriente. Para corregir el pH se añadió una solución de HCl al 1N durante 15 minutos, luego se decantó el HCl sin lavar y se agregó el azul de Tripano al 0.05 % colocando después las raíces a "baño de María" por 15 minutos. Se retiró el colorante, se lavó con agua destilada, se dejó reposar por 12 horas para eliminar el exceso de colorante y proceder a su observación al microscopio compuesto binocular marca Olympus CX21.
Cuantificación del porcentaje de colonización
Se tomaron 10 segmentos de raíces de 1 cm de largo cada uno y se ubicaron en la lámina portaobjetos de forma paralela, se efectuó la observación de las estructuras fúngicas en el microscopio compuesto con los objetivos desde 10X hasta 40X, utilizando la técnica de determinación de colonización por campos de infección, en el cual se realizaron barridos de cada segmento de raíz. Se registró la presencia de estructuras típicas de los HMA: hifas, esporas, vesículas y arbúsculos.
Para determinar el porcentaje de colonización de cada muestra se utilizó la fórmula propuesta por Sieverding (1983) (Ecuación 1).
La frecuencia de colonización radicular se determinó considerando los segmentos colonizados y no colonizados. Se obtuvo la relación total de segmentos colonizados (aquellos en los que se detectó la presencia de arbúsculos y vesículas), con respecto a los segmentos totales evaluados. Se utilizó el mismo procedimiento para evaluar la presencia de hifas, vesículas y arbúsculos, la que fue expresada en porcentaje.
B. Densidad de esporas
Las muestras se trabajaron siguiendo la metodología propuesta por Sieverding (1983), contando las esporas que se observan en los tejidos coloreados con azul de Tripano.
C. Separación de esporas de hongos micorrízicos en suelos rizosféricos
Las muestras de suelo obtenidas en cada punto de muestreo se homogenizaron individualmente quitando todo material grueso (raíces, piedras y terrones); luego se tomaron muestras de 100 g que fueron colocadas en un vaso de precipitado de 500 ml de capacidad, agregándose 400 ml de agua destilada y se agitó por 10 minutos. Se filtró a través de un juego tamices de 4 000, 500, 250, 125 y 63 µm (ordenados verticalmente en forma descendente); se repitió el procedimiento dos veces. El contenido del tamiz de 63 µm se vertió en una placa Petri que luego se puso a secar a temperatura ambiente (28 a 30 °C).
D. Centrifugación, decantación y extracción para concentrar las esporas
De la muestra de suelo tamizado y seco, se pesó 1 g que fue depositado en tubos de centrífuga, adicionando 15 ml de solución de sacarosa al 70 %, luego se centrifugó a 2 500 rpm durante 10 minutos. Posteriormente se retiraron los tubos de la centrífuga, cuidando de no romper la interfase agua-sacarosa. Con la ayuda de una pipeta de 30 cm, se recorrió toda la superficie de la interfase, la cual se filtró en papel Watman N° 4 con ayuda de un embudo, se lavó con agua destilada para eliminar la sacarosa y se observaron las esporas en el papel de filtro; este se colocó en el microscopio compuesto, se hizo un recorrido en forma de zigzag contando las esporas utilizando los objetivos de 10X y 40X.
E. Identificación
Para la identificación de las esporas, se analizaron sus características morfológicas (forma, tamaño, color, textura de la superficie, tipo de hifa de soporte y procedencia); para lo cual se colocaron en láminas portaobjetos que tenían en el centro una cuadricula con divisiones igual a 0,01 mm. Se observaron con el objetivo de 40X en el microscopio compuesto binocular marca Olympus CX21. La descripción de las esporas se utilizó en la identificación taxonómica hasta el nivel de género con el apoyo de claves y descripciones actualizadas por Guerrero y Hodson (1988).
F. Análisis estadístico
A los datos obtenidos, una vez comprobado que cumplían los supuestos de normalidad, se les aplicó el análisis de varianza (ANOVA) para determinar la presencia de diferencias estadísticas entre los porcentajes de colonización y para cada uno de los porcentajes de las estructuras fúngicas observadas (hifas, esporas, vesículas, arbúsculos). En cada caso se realizaron dos ANOVA, uno para comparar los resultados entre las parcelas muestreadas y otro para la comparación entre los estados de desarrollo. En los casos en que se detectó diferencia significativa (P ˂ 0,05), se aplicó la prueba T para comparar por pares de elementos (parcelas o estado de desarrollo), a partir de todas las combinaciones posibles, con el propósito de determinar, según el caso, entre qué parcelas o estados del desarrollo se encontraba dicha diferencia. En todos los casos se empleó el programa estadístico SPSS versión 26.0.
Resultados y discusión
El estudio de las diferentes estructuras de HMA en la rizósfera de R. rospigliosii, donde la biomasa microbiana es hasta 10 veces mayor que en el suelo (Bonilla y Alarcón, 2015), evidenció la presencia de hifas, esporas, vesículas y arbúsculos en las tres categorías analizadas.
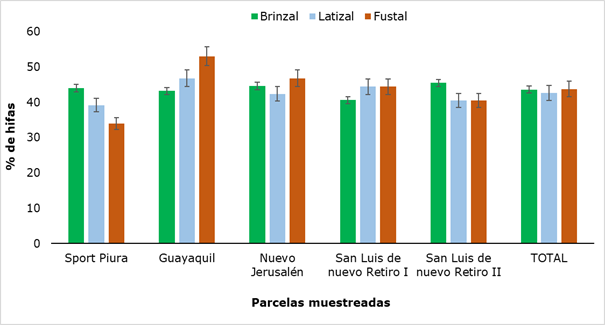
El porcentaje de hifas encontrado en las tres categorías evaluadas (Figura 2), no arrojó diferencias significativas (P ≥ 0,05).
La presencia de hifas osciló entre 34 % y 53 %, ambos valores obtenidos en árboles adultos. Resultados similares fueron informados por Gómez (2019), al realizar el estudio de micorrizas arbusculares en tres sistemas de uso de suelo, determinando un porcentaje de colonización por hifas de un 66% a partir de muestras tomadas a una profundidad de 10 cm. Se infiere así, que la presencia de hifas en todos los sectores y las leves variaciones entre los lugares, puede ser debido al tipo de suelo, pues el bosque Huamantanga presenta una textura muy variada, encontrándose entre franco arenoso hasta arcilloso (UNC, 2019).
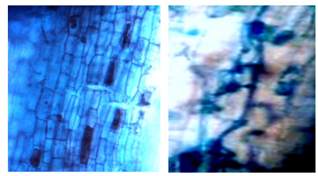
La presencia de hifas de diferente grosor encontradas en las raicillas de la rizósfera de R. rospigliosii(Figura 3) se clasificaron como tipo París y Arum, con formación de suficientes rulos de los cuales se originan los arbúsculos, y presentar hifas intercelulares y arbúsculos intracelulares. Los resultados obtenidos son similares a los de Parra-Rivero et al. (2018) al presentar los tipos de hifa presentes en la colonización por HMA de los sistemas radicales de dos leguminosas arbóreas, observando dos tipos morfológicos simultáneos: Arum y Paris, siendo la primera de mayor frecuencia con hifas gruesas con estructura en H, que recorren paralelos a la superficie radical de manera intercelular y forma arbúsculos laterales intracelulares; la segunda, es de hifa gruesa intracelular que forman circunvoluciones.
La presencia de hifas Paris y Arum en la colonización micorrízica arbuscular, está determinada por la interacción entre el genotipo de la planta y el genotipo del hongo micorrízico de la planta hospedante, sin embargo, el establecimiento de la asociación micorrízica en condiciones naturales puede considerarse como multicausal (Santillana y Toro, 2018). Otros autores mencionan que, siguiendo la clasificación de los tipos de colonización de HMA propuesta, corresponde al tipo denominado Intermedite I, el que se caracteriza por la presencia de arbúsculos intracelulares formados a partir de hifas intercelulares e hifas intracelulares informando por primera vez la presencia de esta relación en los bosques templados del hemisferio sur, de esta manera se valora que las hifas encontradas en la presente investigación, son características correspondientes a una micorriza arbúscula (Cottet y Messuti, 2017).
La densidad de esporas encontradas después del tamizaje de los suelos se muestra en la Figura 4, en la que se puede apreciar que la menor cantidad de esporas se obtuvo en la categoría Brinzal en la parcela Guayaquil (30.8 %) y el valor máximo se obtuvo en este mismo lugar de muestreo en la categoría Fustal (57.6 %), encontrándose una diferencia significativa estadísticamente al comparar los resultados entre las tres categorías analizadas, precisamente entre Brinzal y Fustal.
Los valores obtenidos difieren cuantitativamente de los resultados informados por Peña y López (2018), quienes al evaluar la presencia de esporas de hongos micorrízicos arbusculares en cinco estados sucesionales del bosque altoandino colombiano detectaron entre 4 y 20 esporas g-1; sin embargo, los mayores valores en el número de esporas fueron encontrados en el estado sucesional maduro, lo que corrobora el valor máximo obtenido en la categoría Fustal de la presente investigación.
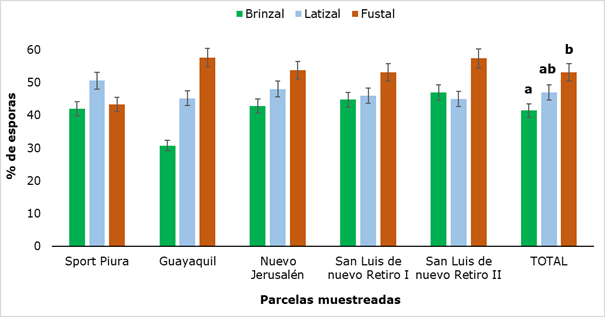 Letras diferentes muestran que hubo diferencias significativas (P ˂ 0,05) entre los estados de desarrollo analizados
Letras diferentes muestran que hubo diferencias significativas (P ˂ 0,05) entre los estados de desarrollo analizadosFig. 4. - Porentaje de esporas en suelo rizosférico de R. rospigliosii
Las esporas micorrízicas del suelo son las más grandes (entre 145 y 800 µm), con colores que varían desde el hialino y amarillo pálido hasta el marrón, rojizo y negro. Las paredes de las esporas (lisas u ornamentadas), el tamaño y la ontogenia de las esporas, forman una base para la identificación de estos hongos. Estas características son de gran utilidad para la identificación taxonómica de los HMA, lo que permitió en esta investigación identificar tres géneros de HMA: Glomus, Entrophosora y Acaulospora, tal y como se observa en la Figura 5.
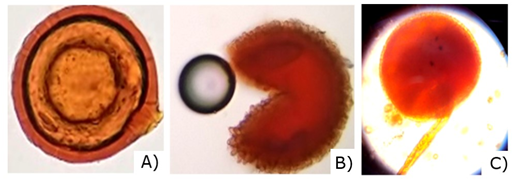
Fig. 5. - Esporas encontradas en la rizósfera de R. rospigliosii Pilger. A) Glomus sp., B) Entrophosora sp., C) Acaulospora sp
Al evaluar la presencia de vesículas en las raicillas (Figura 6) se encontró que esta estructura estaba presente en todas las parcelas muestreadas y los valores oscilaron entre 35 % (categoría Fustal en Guayaquil) y 51,4 % (categoría Brinzal en Sport Piura). De manera general, los mayores valores se encontraron en la categoría Brinzal, la que mostró diferencia significativa con la categoría Latizal. Resultados similares fueron encontrados por García et al., (2004) en una investigación con ocho especies forestales en la selva altoandina, informando valores máximos de 51,7 % de vesículas.
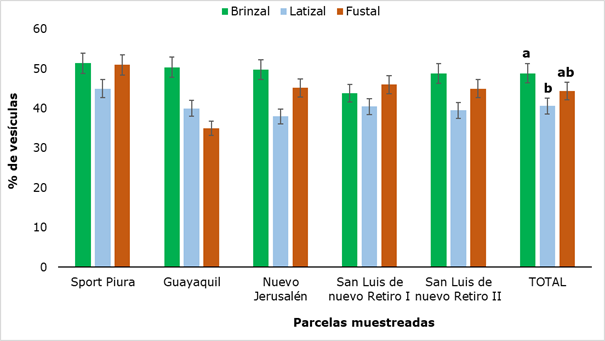 Letras diferentes muestran que hubo diferencias significativas (P ˂ 0,05) entre los estados de desarrollo analizados.
Letras diferentes muestran que hubo diferencias significativas (P ˂ 0,05) entre los estados de desarrollo analizados.Fig. 6. - Porcentaje de vesículas presentes en suelo rizosférico de R. rospigliosii
Estas porciones de hifas (vesículas) que forman algunos géneros de HMA, se encuentran presentes intercelularmente en la corteza de la raíz y se consideran reservorios de nutrientes para el hongo (Figura 7). Esta simbiosis entre el HMA y la planta se conoce como vesículo-arbuscular (VA) por la presencia de vesículas y arbúsculos; como no todas las especies de hongos desarrollan vesículas, en la actualidad se les conoce como micorriza arbuscular (Camarena-Gutiérrez, 2012).
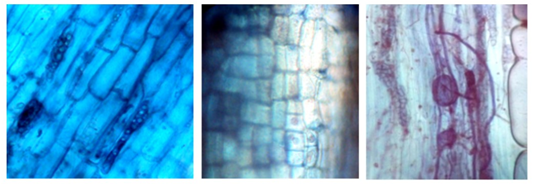
Fig. 7. - Vesículas en la categoría Brinzal coloreado con azul de Tripano en R. rospigliosii, observadas a 40X
El proceso de infección o colonización ocurre inicialmente con el crecimiento del hongo en el suelo y el contacto físico con la raíz. Entonces, ocurre un intercambio de información que permite que el hongo crezca entre las células de la raíz y colonice el tejido vegetal. En algunos lugares, la hifa ingresa a la pared celular y se divide intensamente, pero no rompe la membrana plasmática. Esta estructura ramificada es denominada arbúsculo y se reconoce como un órgano de intercambio de metabolismo entre parejas (Ortiz-Acevedo et al., 2015).
El comportamiento de la presencia de arbúsculos, en las valoraciones expuestas en la presente investigación, fue diferente al de las otras estructuras analizadas (hifas, esporas y vesículas), pues no se detectó en todas las parcelas, y en algunas no se registró en las tres categorías evaluadas (Figura 8).
Como puede apreciarse en la Figura 8, en San Luis de Nuevo Retiro II no se encontraron arbúsculos y en San Luis de Nuevo Retiro I sí se detectaron, en las tres categorías evaluadas. En el resto de las parcelas muestreadas hay presencia de arbúsculos, pero no en todas las categorías, de ahí que se aprecien diferencias estadísticamente significativas entre los resultados obtenidos para cada sitio de muestro. Los valores oscilaron entre un mínimo de 0,6 % y un máximo de 2,0 %, el primero en las categorías de Latizal y Fustal y el segundo en la categoría Brinzal. En la Figura 9, se muestran algunos arbúsculos encontrados en esta última categoría.
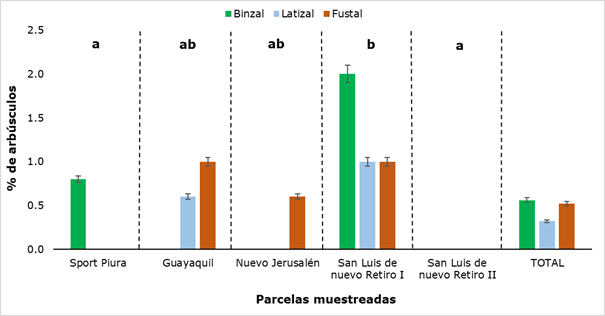 Letras diferentes muestran diferencias significativas (P ˂ 0,05) entre las parcelas muestreadas.
Letras diferentes muestran diferencias significativas (P ˂ 0,05) entre las parcelas muestreadas.Fig. 8. - Porcentaje de arbúsculos detectados en los diferentes sectores y categorías de R. rospigliosii
Los resultados evidencian un bajo porcentaje de arbúsculos, al compararlos con otras investigaciones, como las realizadas por Parra-Rivero et al., (2018) y Rivera et al., (2016), quienes informan valores altos para esta estructura (entre 31 % y 90 %), al estudiar la colonización de HMA en plantas arbóreas. Esta diferencia en la presencia de estructuras colonizantes tipo arbúsculos, puede deberse a que estos tienen una vida efímera (4-15 días) y siempre terminan por ser digeridos por la planta hospedadora (Rivera et al., 2016; Pérez et al., 2016).
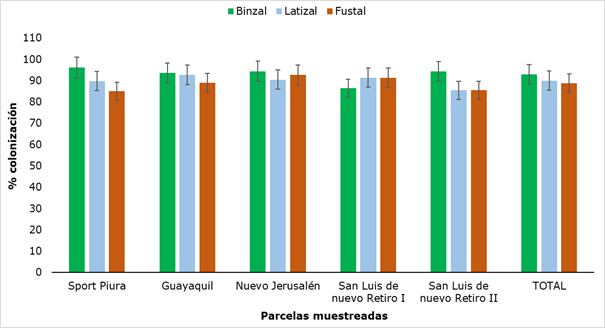
Los resultados de la colonización por HMA en Retrophyllum rospigliosii Pilger se muestran en la Figura 10, en la que se puede apreciar que el valor mínimo obtenido fue de 85 % (Fustal) y el máximo fue de 96,2 % (Brinzal).
Los valores obtenidos para la colonización no mostraron diferencias significativas al analizar las parcelas muestreadas ni al comparar las tres categorías. Si bien estos valores no tienen un patrón estandarizado de comparación, pues la variabilidad de la colonización micorrízica está asociada al tipo de especie vegetal y su edad fisiológica (Belezaca et al., 2020), si constituyen valores muy altos de colonización, lo que unido a la presencia de las estructuras micorrízicas en todas las categorías, permite afirmar que hay cierto grado de dependencia entre la planta y el HMA, elemento de gran importancia debido a que, en la simbiosis micorrízica, el hongo permite el incremento en la adquisición de nutrientes, principalmente de aquellos de escasa movilidad en el suelo, como el fósforo, al mismo tiempo que la planta proporciona compuestos carbonados para el crecimiento del hongo (Flores y Cuenca, 2004).
Este elemento cobra mayor importancia en la presente investigación porque en el bosque de Humantanga, según lo informado por UNC (2019), el fósforo se encuentra en un nivel bajo (8,11 ppm), teniendo en cuenta los rangos interpretativos mencionados por Andrades y Martínez (2014). En este caso, la actividad fúngica asociada a la planta genera un sistema de beneficio mutuo, pues los HMA modifican la morfología de las raicillas, dándole a la planta una mejor capacidad para alcanzar el agua y disolver los nutrientes, pudiendo resolver el problema del agotamiento inminente del stock de fosfato y otros elementos como, nitrógeno, zinc, cobre, hierro, potasio, calcio y magnesio (en algunos casos los nutrientes pueden controlar el desarrollo o iniciar la simbiosis), también puede causar un cambio en la absorción de más nutrientes al mismo tiempo y permiten la inducción de las defensas del hospedero para mejorar la nutrición Uc et al., 2019; (Piliarová et al., 2019).
Conclusiones
En todas las categorías de crecimiento de los rodales de Retrophyllum rospigliosii Pilger analizadas en la investigación, se encontraron estructuras típicas de los HMA (hifas, esporas, vesículas y arbúsculos), lo que indica que este es una especie vegetal que hace simbiosis con micorrizas arbusculares.
Los géneros de hongos determinados en las tres categorías Brinsal, Latizal y Fustal de R. rospigliosii Pilger, según la morfología de las esporas, corresponden a Glomus, Entrophospora y Acaulospora.
Los altos porcientos de colonización de los HMA en R. rospigliosii Pilger y su presencia en las tres categorías de desarrollo, permiten afirmar que esta relación simbiótica es importante en el desarrollo del romerillo macho en el bosque de Huamantanga, garantizando una buena absorción de fósforo, además de los otros beneficios que derivan de esta interacción hongo-planta.
Estos resultados contribuyen al conocimiento de esta colonización micorrízica, lo que permite valorar el empleo de los HMA en el desarrollo de técnicas culturales en programas de reforestación de R. rospigliosii Pilger, especie forestal declarada como especie vulnerable.
Agradecimientos
Los autores expresamos un especial agradecimiento al Centro de Estudios para el Perfeccionamiento de la Educación Superior (CEPES), de la Universidad de La Habana, Cuba y a la Consultora Educativa Especializada (CEES) de Perú, por la asesoría brindada en la elaboración del presente artículo científico.











 texto en
texto en