INTRODUCCIÓN
En el siglo XXI, antes de 2019, se conocen dos epidemias provocadas por coronavirus que son causa de un síndrome respiratorio agudo severo que inducían dificultad respiratoria grave y tasas elevadas de mortalidad entre los individuos afectados. En 2002 apareció en Guangdong, China, una nueva variante de coronavirus causante de una enfermedad respiratoria más grave que recibió el nombre de síndrome respiratorio agudo severo por coronavirus (SARS-CoV, por sus siglas en inglés) y que causó una epidemia global con 8 096 casos confirmados en alrededor de 25 países. En 2012 apareció el MERS-CoV, que causó cuadros de infección respiratoria de mayor letalidad que el SARS-CoV y que afectaba la función renal; se le llamó síndrome respiratorio de Medio Oriente por coronavirus (MERS-CoV, por sus siglas en inglés) porque surgió en esa región. Se estima que el 35% de las personas contagiadas murieron. El 80% de los casos ocurrieron en Arabia Saudita, su disipación pudo contenerse porque el contagio entre humanos fue apenas de 5%. La epidemia por el nuevo coronavirus de 2019 (SARS-CoV-2) fue informada en diciembre en Wuhan, China, y progresó a pandemia asociada a unas altas morbilidad y mortalidad; fue declarada por la Organización Mundial de la Salud (OMS) el 11 de marzo de 2020. El SARS-CoV-2 está relacionado genéticamente con el SARS-CoV.1,2 Hasta el momento en que se culmina el artículo las cifras globales acumuladas informan 110,7 millones de casos y más de 2,4 millones de muertes desde el inicio de la pandemia. Estados Unidos es el país más afectado, con un acumulado de 27 702 074 casos y 491 894 fallecidos, seguido de La India, con 10 991 651 contagios y 156 302 muertes.3 Cuba presenta un acumulado de 43 484 casos confirmados y 291 fallecidos.3,4
Un pequeño número de casos con la enfermedad por coronavirus 2019 (COVID-19, por sus siglas en inglés) ha sido descrito hasta la fecha en niños y, en comparación con los casos diagnosticados en adultos, tiene un espectro clínico limitado, según datos aportados por estudios realizados en China y otros países que refieren que la evolución de la enfermedad es menos severa en los infantes en relación a los adultos.5,6 En tal sentido se ha documentado que los niños, aún siendo casos leves, pueden ser una importante fuente de transmisión del virus, con una tasa de infección entre sus contactos, de un 7,4% en los niños menores de 10 años, similar a la media de la población adulta, con un 7,9%. Se ha detectado, además, que pueden excretar virus fundamentalmente en heces durante un tiempo prolongado, incluso un mes, y que pueden tener altas cargas virales en secreciones respiratorias.6
Con la extensión de la pandemia hacia Europa, y posteriormente a América, se observa que la situación de la población infantil es similar. Todavía existe preocupación por los bebés y los niños inmunodeprimidos o que tienen otras afecciones subyacentes como enfermedad pulmonar crónica (asma) o enfermedad cardiovascular.6
La incidencia acumulada de pacientes con COVID-19 en el grupo de cero a 19 años en América Latina y El Caribe varió de 0,91 a 88,34 por 100 000 habitantes. Los países con mayor incidencia acumulada fueron Chile, Panamá y Perú. La letalidad de cero a 19 años tuvo un rango de cero a 9,09% y los países con registro de muertes fueron Brasil, Colombia, Ecuador, El Salvador, Haití, México, Perú y República Dominicana.7
Cifras oficiales informan que en Cuba, hasta el 30 de septiembre de 2020, han enfermado un total de 618 pacientes en edad pediátrica (hasta los 18 años), que representan entre un 10 y un 12% del total; los más afectados son los que se encuentran en las edades de 15 a 18 años. Cuba no informa fallecimientos por esta causa en edades pediátricas.8
Los elementos anteriormente explicados fundamentan la necesidad de incrementar los conocimientos sobre la situación actual de la enfermedad con la búsqueda activa de complicaciones presentes o no en la población pediátrica. El conocimiento de este estudio contribuye a diseñar e implementar estrategias en la fase aguda que minimicen el impacto que puede tener la enfermedad sobre los niños afectados. Este trabajo tiene como objetivo describir los aspectos clínicos, de laboratorio y el tratamiento de la COVID-19 en la población pediátrica atendida en el Hospital Militar Clínico Quirúrgico “Comandante Manuel Fajardo Rivero” de la Provincia de Villa Clara.
MÉTODOS
Se realizó un estudio descriptivo de cohorte transversal en pacientes diagnosticados con COVID-19 atendidos en el Hospital Militar Clínico Quirúrgico “Comandante Manuel Fajardo Rivero” de la Ciudad de Santa Clara, Provincia de Villa Clara, en el período comprendido de marzo a octubre de 2020. Fueron seleccionados 43 pacientes por muestreo no probabilístico intencional para conformar el grupo de estudio que cumplió con los criterios siguientes:
Criterios de inclusión:
Pacientes con diagnóstico de COVID-19
Pacientes con documentos que disponían de los datos necesarios para el estudio.
Criterios de exclusión:
Las variables del estudio fueron á edad, el sexo, la raza, el estado de los pacientes al ingreso, los síntomas y los signos, los complementarios, la radiografía de tórax y el tratamiento.
Los datos obtenidos fueron compilados en una base de datos en el procesador de cálculos Excel y posteriormente procesados con el software estadístico SPSS versión 22.0 para Windows según el tipo de variable y los resultados expresados en tablas y gráficos para su mejor comprensión.
El estudio se realizó respetando lo establecido por la Asamblea Médica Mundial en Helsinki 20039 y las regulaciones del Centro de Investigaciones Médicas de Cuba y fue revisado y aprobado por el Comité Científico Institucional y por el Comité de Ética para la investigación de la institución implicada que dictaminaron el cumplimiento de los principios éticos.
RESULTADOS
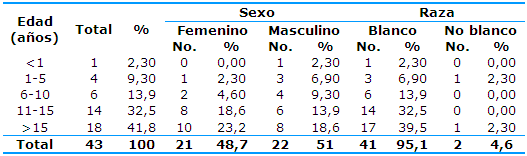
En la Tabla 1 se muestra un total de 43 pacientes positivos a la COVID-19: 21 correspondieron al sexo femenino y 22 al masculino y predominaron el grupo de edad de mayores de 15 años (41,8%) y la raza blanca (95,1%).
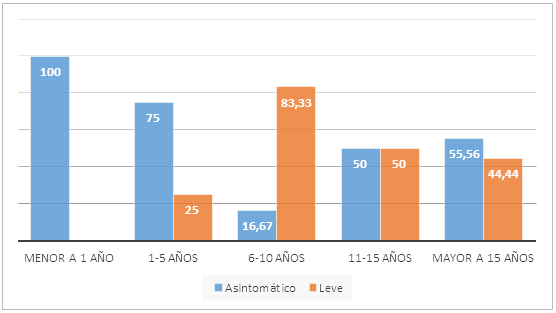
En cuanto al estado de los pacientes al momento del ingreso 22 fueron asintomáticos, principalmente entre los pertenecientes a los grupos de edades de 11 y 18 años. El resto presentó síntomas leves, que fueron más frecuentes en los pacientes en las edades comprendidas entre 6 y 10 años (Figura 1).
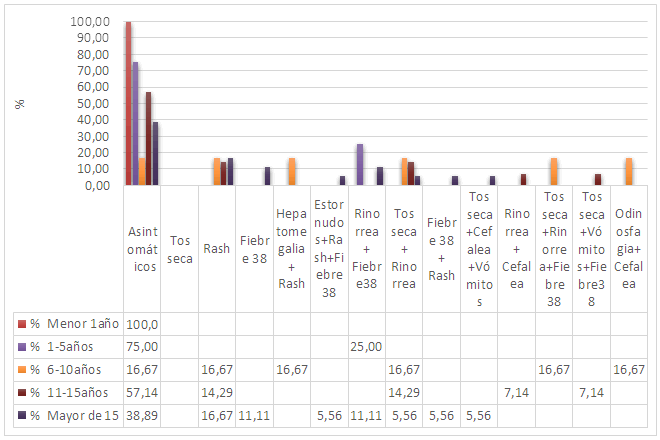
Cursaron la enfermedad de forma asintomática 20 pacientes. En los pacientes que presentaron síntomas y signos se destacaron, por orden de aparición, el rash, las tos seca+rinorrea y la fiebre 38°C+rinorrea (Figura 2).
En la Figura 3 se muestra la evolución de los complementarios sanguíneos realizados a los pacientes al momento del ingreso (34 presentaron resultados normales y 9 linfopenia ligera). Al evolutivo de 72 horas predominó la leucopenia ligera en 17 de los pacientes, seguida de un equilibrio en cuanto a lactato deshidrogenasa (LDH) elevada y creatinina elevada en 4; el grupo más afectado fue el de los mayores de 15 años. Al egreso 23 pacientes presentaron complementarios normales y 17 solo leucopenia ligera.
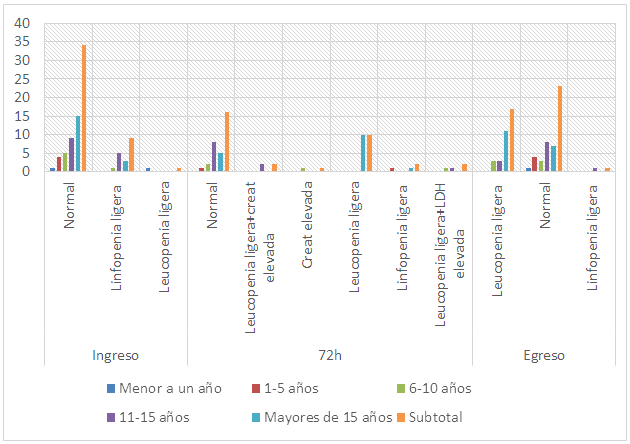
Figura 3 Resultados de los complementarios sanguíneos realizados a los pacientes positivos a la COVID-19 al ingreso, evolutivo a las 72 horas y al egreso
A los 43 pacientes se les realizaron radiografías de tórax, solo dos presentaron alteraciones: un menor de un año que cursó la enfermedad con infiltrado inflamatorio bilateral y un adolescente mayor de 15 años con opacidad en vidrio esmerilado en base derecha. Al egreso la totalidad de las radiografías evolutivas se encontraban normales.
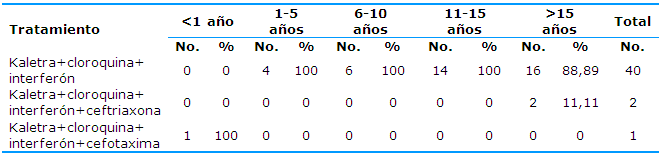
La Tabla 2 muestra que la totalidad de los pacientes fueron tratados con triple terapia (kaletra, cloroquina e interferón) según los protocolos establecidos en Cuba en ese momento para enfrentar esta pandemia. Solo en 3 pacientes fue necesario incluir antibioticoterapia con cefalosporina de tercera generación por cursar con infección sobreañadida; también se cumplieron con los protocolos establecidos.
DISCUSIÓN
El impacto de la infección por SARS-CoV-2 en niños es claramente diferente al que se observa en adultos. La Provincia de Villa Clara no se encuentra exenta de este comportamiento; en la investigación se evidencia un total de 43 niños enfermos con SARS-CoV-2 (los adolescentes y el sexo masculino fueron los más afectados).
Los casos notificados con la COVID-19 varían a escala mundial. En un estudio realizado en China, de un total de 44 672 casos confirmados con COVID-19, solo 416 se detectaron en niños de cero a 9 años (0,9%) y 549 en niños de 10 a 19 años (1,2%). En España los datos son superponibles: con 113 407 casos analizados 168 (0,1%) tenían menos de 2 años, 64 (0,1%) entre 2 y 4 años y 303 (0,3%) entre 5 y 14 años.10 La distribución por grupos de edad refleja una escasa incidencia en la población pediátrica (0,9%), con un cuadro clínico más leve.11
Chen y colaboradores12 contabilizaron mayor transmisión en los hombres, lo que coincide con los resultados de la presente serie. Tanto el informe del Centro Nacional de Epidemiología de España13 como una investigación llevada a cabo en China14 muestran coincidencias con lo expuesto en este estudio en lo relativo a la preponderancia de la enfermedad en el sexo masculino.
Los niños, en todas las investigaciones publicadas hasta la fecha, desarrollan un curso clínico mucho más leve. La clínica leve o la ausencia de síntomas en niños se observa, incluso, con carga viral alta y en presencia de alteraciones radiológicas importantes. En relación al tipo de manifestaciones clínicas de la población infantil con COVID-19 en una revisión sistemática que incluye 38 estudios con 1 117 pacientes se observan diferencias con las series de adultos; solamente un 47,5% presentaron fiebre y alrededor de la mitad fueron leves o asintomáticos. Estos coinciden con los datos de la investigación, en la que predominaron los niños asintomáticos y con síntomas leves.10
Entre los aspectos que se discuten como posibles factores que podrían hacer que la clínica en la población infantil sea más leve está la suposición de que la respuesta inmune en niños es diferente en adultos y que esta respuesta inmune sea parte de la patogenicidad observada en los mayores. Por el contrario, la mayor exposición de los niños a infecciones respiratorias durante el invierno podría hacer que esta población estuviera más protegida por tener mayores niveles de anticuerpos frente a virus que los adultos.10
Algunos síntomas son más específicos en la población infantil y adolescente, ejemplo la expresión de la enfermedad a nivel cutáneo, que es muy inespecífica y variada. Hasta el momento se han descrito las siguientes alteraciones con las siguientes características: exantema eritematoso/petequial/morbiliforme, de predominio troncular, escasamente pruriginoso, que puede aparecer antes o después del inicio de los síntomas respiratorios; este cuadro predominó en los pacientes en estudio.15
En la investigación predominaron las alteraciones de laboratorio relacionadas con los índices leucocitarios, algo que coincide con la literatura revisada.16,17 Al momento del ingreso predominaron los pacientes con leucograma normal, luego de 72 horas presentaron leucopenia ligera y, los menos, linfopenia ligera. En un estudio realizado en Wuhan, China, en el que se analizaron datos clínicos y de laboratorios de 989 pacientes, del 31 de enero al 21 de febrero de 2020, se plantea que el 95% de los pacientes positivos a la COVID-19 presentaron un número de leucocitos por debajo de 9,5x109/l, el 52,2% linfopenia por debajo de 1,1x109/l, el 74,7% eosinopenia inferior a 0,02x109/l y valores elevados de proteína C reactiva superiores a 4mg/l el 86,7% de los pacientes.16 Otro hallazgo de los datos de laboratorio fue el incremento de lactato deshidrogenasa (LDH) y la creatinina, al igual que en pacientes de otros estudios.12,17,18
La radiografía de tórax simple ofrece pocos signos anormales en las estructuras que conforman el aparato respiratorio, no así la tomografía axial computarizada que muestra, con mayor frecuencia, infiltrados irregulares en forma de cristal esmerilado sin que en algún caso aparezca derrame pleural, linfoadenopatías, colapso lobular, neumotórax o derrame en niños con COVID-19.19
En la actualidad no existe evidencia que permita determinar un tratamiento específico para la COVID-19. En Cuba se lleva a cabo el tratamiento según el protocolo de actuación nacional vigente para la COVID-19, acápite de Pediatría, que indica triple terapia con kaletra, cloroquina e interferón según dosis recomendadas y se han obtenido excelentes resultados en los pacientes estudiados.
El interferón recombinante, heberón alfa R líquido, está contraindicado en niños menores de tres años, especialmente en recién nacidos prematuros, debido a que utiliza alcohol bencílico como preservativo en su formulación. En pacientes menores de tres años solo puede emplearse la formulación liofilizada. Se debe administrar con precaución en pacientes con enfermedad cardíaca preexistente y con hemoglobinopatías. La presentación es en bulbos de 3 millones. No se usa en el paciente grave.
El fármaco conocido comercialmente como kaletra cuenta con las combinaciones de lopinavir-ritonavir. Se describe como un inhibidor de la proteasa del virus de inmunodeficiencia humana (VIH), que se metaboliza a través de la isoforma CYP3A del citocromo P450. Esta inhibición previene la escisión de la poliproteína gag-pol y da lugar a un virus más inmaduro no infeccioso. El lopinavir proporciona la actividad antiviral, mientras que el ritonavir actúa como un potenciador farmacocinético y aumenta la vida media en el plasma del primero.20,21
Su uso en pacientes positivos a SARS-Cov-2 se basó, inicialmente, en la actividad in vitro mostrada por esta combinación en varios estudios frente a los virus SARS-CoV y MERS-CoV.22
La seguridad de la kaletra se ha estudiado en más de 2 600 pacientes en los ensayos clínicos de fases II y IV; más de 700 recibieron una dosis de 800/200mg (6 cápsulas o 4 comprimidos) una vez al día. Las reacciones adversas más frecuentes durante los ensayos clínicos fueron diarreas, náuseas, vómitos, hipertrigliceridemia e hipercolesterolemia.20
La cloroquina es conocida por poseer acción antimalárica e inmunosupresora. Inhibe la quimiotaxis de eosinófilos y la migración de neutrófilos y disminuye las reacciones antígeno-anticuerpo dependientes del complemento. Diversos estudios han demostrado su eficacia in vitro frente al virus, atribuida a diferentes mecanismos, entre ellos el cese de la replicación viral mediante el aumento del pH endosomal que inactiva las enzimas indispensables para la misma. Entre ellas destaca la enzima convertidora de angiotensina-2 utilizada por el SARS-Cov-2 para su entrada a la célula.21
CONCLUSIONES
El diagnóstico clínico favoreció registrar una mayor incidencia de la enfermedad en los pacientes mayores de 15 años, predominaron los casos asintomáticos y los enfermos desarrollaron síntomas leves (fueron frecuentes las manifestaciones cutáneas y los síntomas respiratorios ligeros) y la mayoría presentó valores de laboratorio y Rx de tórax normales. El tratamiento se basó en la triple terapia según el protocolo de actuación vigente en Cuba en ese momento y se obtuvieron satisfactorios resultados; no se reportaron casos graves ni fallecidos hasta la fecha de culminada la investigación.